La medicina della riproduzione ha subito trasformazioni radicali negli ultimi due decenni, evolvendo verso protocolli sempre più personalizzati e tecnologicamente avanzati. Al centro di questo progresso si colloca lo studio e l’applicazione clinica del trasferimento di embrioni allo stadio di blastocisti. Comprendere questa fase biologica, che rappresenta l'apice dello sviluppo embrionale pre-impianto, è fondamentale per le coppie che si avvicinano a un percorso di procreazione medicalmente assistita (PMA).
Che cos'è la blastocisti umana
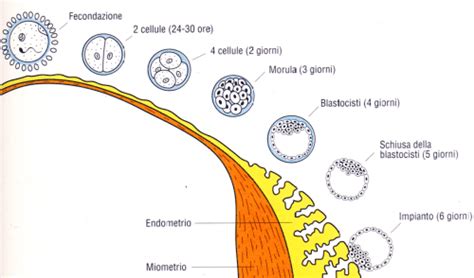
La blastocisti è lo stadio embrionale iniziale raggiunto intorno ai 5-6 giorni dal concepimento. Si tratta di una struttura biologica complessa, definita da una precisa architettura cellulare. Anatomicamente, una blastocisti umana è composta da tre elementi distinti:
- Blastocele: una cavità interna piena di liquido.
- Trofectoderma: lo strato cellulare esterno che darà origine alla placenta.
- Zona pellucida: l'involucro proteico che protegge l’embrione durante i primi stadi di sviluppo.
Fisiologicamente, è proprio allo stadio di blastocisti (cinque giorni dopo l’avvenuta fecondazione) che l’embrione transita naturalmente dalle tube all’utero. Il vantaggio di coltivare gli embrioni sino a questo stadio risiede nel fatto di ricreare il sincronismo fisiologico tra stadio di sviluppo embrionale e la sede anatomica del trasferimento, aumentando le possibilità che si realizzi l’impianto.
Il superamento del dogma del trasferimento precoce
In passato, la stragrande maggioranza dei centri di procreazione medicalmente assistita promuovevano l’embryo-transfer in 2°-3° giornata, scartando la possibilità di prolungare la coltura embrionaria. Si credeva inizialmente che trasferire in utero embrioni freschi fosse la scelta migliore sia per il successo della gravidanza sia per i rischi del nascituro.
Oggi, invece, si assiste allo scenario opposto, quasi un obbligo al trasferimento a blastocisti. Nelle tecniche di fecondazione assistita, che sia FIVET o ICSI, il momento finale della procedura è il trasferimento di embrioni. La materia è complessa, ma la differenza tra un transfer al 2°-3° giorno e uno a blastocisti (5°-6° giorno) risiede proprio nella capacità di selezione naturale. Non è infrequente che blastocisti di ottima qualità biologica (grado 1) non abbiano dato gravidanza e, al contrario, che in tentativi successivi un embrione in 3°/4° giornata si sia impiantato con successo; tuttavia, la coltura prolungata permette di identificare gli embrioni con il maggiore potenziale evolutivo.
Come nasce un embrione
Strategie di selezione: il transfer elettivo vs selettivo
Molti centri utilizzano la metodica del transfer selettivo di blastocisti, che consiste nell’arrivare a blastocisti solo se al giorno 3 si dispone di molti embrioni di ottima forma (tipo 1 o tipo A). Noi proponiamo un approccio differente: il trasferimento embrionale a blastocisti "elettivamente" e non "selettivamente".
Nei casi in cui si hanno pochi embrioni al giorno 3, occorre verificare se questi sono realmente in grado di raggiungere lo stadio di blastocisti, anche se presentano una morfologia non ottimale. È dunque questa la fase critica che si sceglie per eseguire un’indagine di preimpianto durante un percorso PMA. In un numero limitato di casi, la percentuale oscilla tra il 5% e il 10%, nessun embrione è in grado di svilupparsi sino allo stadio di blastocisti, vanificando il trasferimento embrionario, ma questa selezione è un passaggio cruciale per evitare insuccessi successivi.
La sicurezza e le performance del programma di blastocisti
La politica del centro è quella di effettuare, ove possibile, colture a blastocisti così da trasferire embrioni più maturi, mimando il più possibile l’impianto naturale. Contemporaneamente, mediante questa strategia, è possibile ridurre il numero di embrioni destinati al transfer minimizzando i rischi collegati all’insorgenza di una gravidanza gemellare. La decisione di non trasferire più di 2 blastocisti risiede nell’intento di evitare gravidanze plurime: poiché le blastocisti hanno una elevata capacità di attecchimento, trasferendone più di 2 in utero esiste una probabilità di ottenere gravidanze gemellari o trigemine, con una gravidanza maggiormente a rischio.
Scopri il nostro “PROGRAMMA DI BLASTOCISTI GARANTITE”: secondo le statistiche c’è la possibilità del 76,9% di gravidanza nel primo transfer e l’86,2% di opportunità di parto per ciclo. Quando si ottengono 3 o più blastocisti, una o al massimo 2 vengono trasferite e quelle soprannumerarie vengono crioconservate mediante vitrificazione.
Tecniche avanzate: vitrificazione e supporto uterino
La vitrificazione consiste in un congelamento rapidissimo in azoto liquido con temperature che si aggirano tra i -210°C e i -196°C. Dopo le modifiche apportate dalla sentenza della Corte Costituzionale, abbiamo scelto di crioconservare solo gli embrioni giunti allo stadio di blastocisti (5-6 giorni dalla fertilizzazione) e congelare quindi un numero molto ridotto di embrioni, a buona prognosi di poter portare ad una gravidanza dopo lo scongelamento.
Per le donne che hanno dovuto affrontare ripetuti fallimenti, la ricerca sta investendo sulla sperimentazione di plasma ricco in piastrine (PRP) da inserire direttamente in cavità uterina, in prossimità della fase di transfer dell’embrione. In pazienti che hanno già affrontato delle PMA infruttuose, vanno analizzati tutta una serie di dati, tra i quali lo scratching endometriale, l’analisi dei linfociti natural killer e l’evoluzione della coltura cellulare. Abbiamo inoltre esperienza nel trattamento di pazienti che hanno ricevuto da strutture estere blastocisti frutto di donazione dei gameti: in questo contesto, occupandoci della preparazione endometriale, abbiamo ottenuto un tasso di gravidanza del 42,86% per trasferimento di una singola blastocisti.
Analisi dei dati di efficacia
Al prelievo ovocitario vengono recuperati in media 6 ovociti, tuttavia tale numero varia notevolmente in base all’età della donna, la sua riserva ovarica e al protocollo di stimolazione. Trascorse circa 20 ore dalla inseminazione, si verifica che ogni singolo ovocita sia correttamente fertilizzato. Lo zigote va incontro, nei giorni seguenti, a divisioni cellulari.
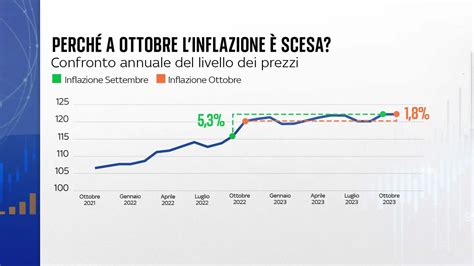
I dati storici indicano una crescita costante: nell’anno 2014 abbiamo ottenuto un tasso di successo del 24% (percentuale di gravidanze ottenute), in linea con quello della media nazionale che sfiora appena il 20%. Nel 2016 abbiamo implementato il numero di congelamenti ovocitari ed embrionali. Analizzando il quadro generale, su 32.556 cicli analizzati con 8.710 gravidanze cliniche in 22.671 coppie, si è osservata una percentuale cumulativa di gravidanza per coppia del 38,93%. Molte coppie abbandonano dopo uno o più cicli con esito negativo, ma i nostri dati indicano che le stesse coppie, se non abbandonassero, raggiungerebbero un tasso cumulativo del 52%.
Considerazioni sulla salute del nascituro
I dati di confronto con la popolazione generale e soprattutto con le gravidanze spontanee in coppie infertili, stratificate per età della coppia, non mostrano nella nostra esperienza un aumento della probabilità di anomalie congenite fetali e neonatali. La metodologia del trasferimento a blastocisti si configura quindi non solo come uno strumento di efficienza clinica per aumentare le probabilità di successo, ma anche come una pratica sicura sotto il profilo genetico e biologico. La selezione operata naturalmente in coltura esclude quegli embrioni che, pur avendo superato la terza giornata, non avrebbero avuto le caratteristiche metaboliche necessarie per proseguire lo sviluppo in utero.
tags: #icsi #embrioni #blastocisti