Il percorso che conduce alla scoperta di anomalie cromosomiche durante la gravidanza rappresenta una delle aree più complesse e in rapida evoluzione della medicina moderna. La comprensione del patrimonio genetico umano, costituito da 46 cromosomi organizzati in 23 coppie, è il prerequisito fondamentale per interpretare le variazioni numeriche e strutturali che possono interessare il feto. Le anomalie cromosomiche si verificano quando il numero o la struttura dei cromosomi presenta delle variazioni, influenzando lo sviluppo biologico dell'individuo.
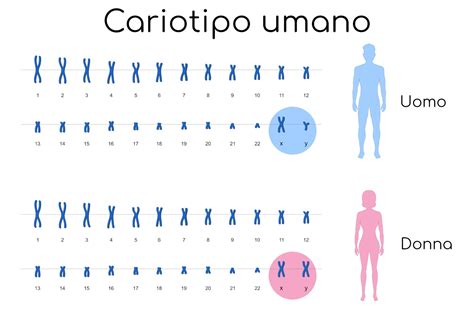
Il quadro genetico: trisomie e traslocazioni
La trisomia 21, comunemente nota come Sindrome di Down, è legata ad un cromosoma 21 in eccesso ed è la più comune trisomia alla nascita, con un’incidenza stimata pari ad 1/700 nati. L'eziologia è varia: nel 95% dei casi è causata da una non disgiunzione durante la meiosi, ma circa il 4% dei casi è dovuto a una traslocazione genetica. Le traslocazioni sono alterazioni della struttura dei cromosomi derivanti da uno scambio di porzioni di cromosomi non omologhi. Sebbene i portatori di riarrangiamenti bilanciati siano solitamente fenotipicamente normali, essi presentano un rischio aumentato di generare prole con squilibri genetici.
Le traslocazioni robertsoniane consistono nella fusione di due cromosomi acrocentrici (13, 14, 15, 21 e 22), con perdita delle braccia corte. Il tipo più comune coinvolge i cromosomi 13 e 14. Se un genitore è portatore di una traslocazione bilanciata, il rischio per la prole può essere significativo; ad esempio, nella traslocazione 21q21q, il rischio di avere un figlio con Sindrome di Down può raggiungere il 100% per la prole vitale.
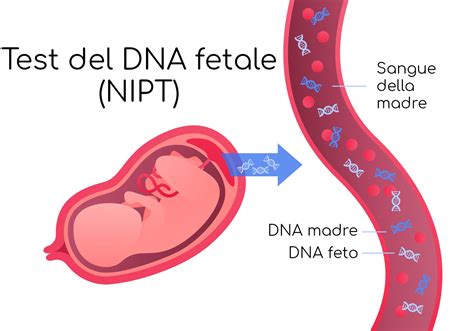
Strumenti di screening: il test NIPT
Il test del DNA fetale, o NIPT (Non Invasive Prenatal Testing), rappresenta un grande passo in avanti in materia di diagnosi prenatale. Si tratta di un test effettuato sul DNA fetale circolante nel sangue materno, basato sulla tecnica di sequenziamento NGS (Next Generation Sequencing). Il NIPT è un test di valutazione del rischio, non diagnostico, ed è indicato per definire la probabilità di aneuploidie dei cromosomi 21, 18, 13 e dei cromosomi sessuali.
Sebbene la sensibilità e la specificità per la trisomia 21 siano molto elevate (superiori al 99%), il valore predittivo positivo varia con il rischio pre-test. È fondamentale sottolineare che un risultato “ad alto rischio” al NIPT non è una diagnosi definitiva e richiede sempre la conferma tramite test invasivi come villocentesi o amniocentesi.
Differenze tra screening e test diagnostici
Le opzioni a disposizione delle gestanti si dividono in due categorie principali:
- Test di screening: stimano la probabilità statistica (es. bitest, NIPT).
- Test diagnostici: offrono una certezza (es. cariotipo su villi coriali o liquido amniotico).
L'approccio tradizionale prevede l'ecografia (translucenza nucale) combinata con marcatori biochimici materni (PAPP-A, β-hCG) tra l'11ª e la 13ª settimana. Il NIPT, invece, può essere effettuato già dalla 10ª settimana. È importante notare che, in casi specifici, le Regioni possono offrire il NIPT a tariffe agevolate in base al profilo di rischio calcolato tramite il test combinato.
Fattori di rischio e consulenza genetica
L’età materna avanzata è l’indicazione più frequente allo studio citogenetico. Sebbene le anomalie cromosomiche si verifichino nella prole di madri di ogni età, la frequenza aumenta in maniera esponenziale dopo i 35 anni. Oltre all'età, l'anamnesi familiare gioca un ruolo cruciale: in presenza di anomalie cromosomiche in un precedente figlio o in un genitore, è imperativo ricorrere a una consulenza genetica approfondita.
Infertilità di coppia: consulenza genetica - Dott. Sergio Carlucci
Gestione dei risultati e limiti biologici
Il NIPT, pur essendo rivoluzionario, presenta limiti biologici. Il mosaicismo cromosomico materno o la presenza di anomalie non compatibili con la vita possono creare risultati di difficile interpretazione. Offrire test "genome-wide" senza una corretta spiegazione clinica espone le famiglie a stress ingiustificati. Un centro di eccellenza deve saper integrare la competenza bioinformatica con un’adeguata consulenza genetica, accompagnando la coppia sia nella fase di screening che, eventualmente, in quella di conferma diagnostica tramite amniocentesi.

La ricerca del DNA fetale non deve mai sostituire le indagini ecografiche, che rimangono centrali per la valutazione delle malformazioni anatomiche e dello sviluppo fetale. L'integrazione tra l'analisi del cfDNA e l'ecografia morfologica di alta qualità costituisce oggi il pilastro per una diagnosi prenatale responsabile e informata.