Il corpo umano è un ecosistema biologico complesso, popolato fin dalle primissime fasi della vita da cellule staminali, entità che permangono nei nostri tessuti fino all’epoca adulta. La comprensione delle dinamiche cellulari rappresenta oggi una delle sfide scientifiche più ambiziose, spinta dalla speranza di tradurre la ricerca di base in strategie cliniche di successo. La sfida cruciale risiede nel determinare se e in quali condizioni queste cellule possano essere impiegate in strategie di trapianto per sostituire cellule perdute in seguito a lesioni o processi degenerativi.
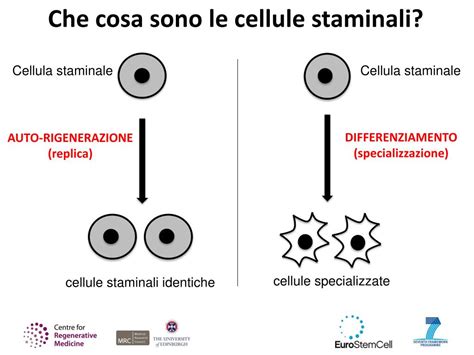
La classificazione delle cellule staminali: dalla biologia alla clinica
In base alla loro plasticità differenziativa, le staminali vengono classificate come totipotenti, pluripotenti o multipotenti. Le cellule totipotenti hanno la capacità di svilupparsi in un intero organismo e persino in tessuti extraembrionali. Le cellule pluripotenti, originate da quelle totipotenti, possiedono una versatilità straordinaria. Al gruppo delle pluripotenti appartengono le cellule staminali embrionali (ES), prelevate dalla blastocisti, che possono moltiplicarsi in modo pressoché illimitato, generando continue copie di sé stesse.
Accanto a queste, nel 2006, si sono aggiunte le cellule iPS (indotte pluripotenti). Per coloro che sono avversi alla ricerca sulle cellule staminali embrionali per motivi etici - ritenendo la distruzione della blastocisti in vitro, una struttura di circa 200 cellule, pari a un atto di interruzione della vita - le cellule iPS e la riprogrammazione rappresentano una soluzione alternativa. Tuttavia, le similitudini e le differenze tra cellule ES e iPS sono ancora oggetto di un serrato vaglio della ricerca.
Al gruppo delle multipotenti appartengono invece le cellule staminali adulte, in quanto capaci di generare, nella maggior parte dei casi, solamente le cellule specializzate del tessuto in cui risiedono. Infine, esistono le staminali unipotenti, in grado di differenziarsi in un unico tipo cellulare.
Le radici storiche: da Rita Levi-Montalcini alla visione moderna
Rita Levi-Montalcini, nata a Torino nel 1909, è stata fra i primi biologi al mondo a ipotizzare l’esistenza delle cellule staminali. Le ha incontrate per la prima volta fra gli anni Quaranta e Cinquanta, studiando il fattore di crescita delle cellule nervose (NGF), scoperta per la quale è stata insignita nel 1986 del Nobel per la medicina insieme a Stanley Cohen.
«Abbiamo scoperto le cellule staminali molto prima che diventassero primedonne», ha dichiarato nel 2009 la scienziata parlando a nome dei suoi collaboratori. «Le chiamavamo taniciti e avevamo notato che avevano la capacità di captare l’NGF ed erano molto ricettive nei confronti di questo fattore». L’NGF è una proteina della famiglia delle neurotrofine che stimola e regola la crescita delle cellule nervose. Sintetizzato nella corteccia cerebrale e nell’ippocampo di molti mammiferi, la sua carenza è correlata a fenomeni di degenerazione dei neuroni e all’invecchiamento cerebrale.
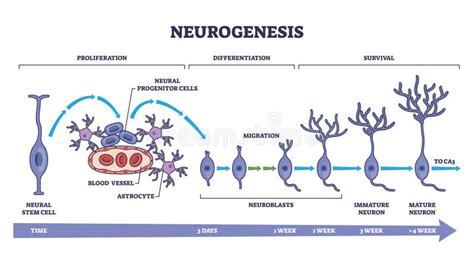
Il liquido amniotico: una risorsa biologica inaspettata
I ricercatori sanno da decenni che il liquido amniotico, che circonda e protegge il feto nell’utero, contiene cellule fetali. È il principio che guida, ad esempio, la pratica dell’amniocentesi, utilizzata per accertare la presenza di eventuali anomalie congenite. Tuttavia, la stragrande maggioranza di queste cellule, il 95% o più, sono cellule morte eliminate dal feto. Una frazione molto più piccola è rappresentata da cellule vive.
Una parte di queste è costituita da cellule progenitrici, un tipo di staminali “multipotenti”. Il team di ricerca italo-britannico, guidato dal professor Paolo De Coppi del Great Ormond Street Institute of Child Health (GOS ICH) dell’University College di Londra, ha utilizzato le cellule progenitrici del liquido amniotico ottenute da diverse gravidanze, prelevate in occasione di esami programmati senza alcun danno per il feto o la madre.
Queste cellule hanno dimostrato una versatilità notevole. Come spiega Anthony Atala, co-firmatario della ricerca e direttore dell'istituto di medicina rigenerativa alla Wake Forest University: «Sapevamo che nel liquido amniotico ci sono molti diversi tipi di cellule progenitrici derivanti dall'embrione in sviluppo, ma ci siamo chiesti se potevamo isolare vere cellule staminali. E la risposta è sì». Le staminali derivate dal liquido amniotico si isolano facilmente, si moltiplicano in fretta - raddoppiano in 36 ore - e sembrano versatili come quelle dell'embrione.
Organoidi: la frontiera del modello fetale
Una delle applicazioni più rivoluzionarie riguarda la creazione di organoidi, ovvero mini-organi riprodotti in una piastra da laboratorio a partire da cellule staminali. Questo metodo permette di studiare lo sviluppo del feto e l’insorgenza di difetti congeniti, che interessano circa 8 milioni di bambini ogni anno nel mondo.
In 4-6 settimane, i ricercatori possono generare l’organoide e testare farmaci o terapie personalizzate per curare le malattie del feto. Il team di De Coppi ha realizzato organoidi di polmone, intestino e rene. Un esempio significativo è la creazione di un modello di ernia diaframmatica congenita (CDH), un difetto caratterizzato dal mancato o incompleto sviluppo del diaframma. Il modello di CDH può aiutare a capire lo stato reale dei polmoni, se la terapia chirurgica è necessaria e se ha funzionato, permettendo di “accedere al feto senza toccare il feto”.
Prof. Arti Ahluwalia / Cellule coltivate in-vitro. Organoidi 3D interconnessi
Applicazioni neurologiche e neuro-protezione
Le potenzialità in campo neurologico sono oggetto di grande interesse. Le cellule staminali da liquido amniotico sono di due tipi: a forma affusolata (SS-hAFSCs) o tonda (RS-hAFSCs). Un lavoro riportato su Nature mostra che le cellule a forma affusolata hanno un’abilità neuro-protettiva specifica. Negli studi preclinici, le cellule nervose prodotte a partire da queste staminali, impiantate nel cervello di soggetti sperimentali, hanno ripopolato aree cerebrali degenerate.
Chris Sobey, responsabile di un progetto di ricerca, ha osservato: «In alcuni dei topi abbiamo riscontrato una guarigione più o meno completa dall'ictus nello spazio di circa due settimane». Secondo gli esperti, le staminali amniotiche presentano vantaggi unici quando vengono immesse nell’organismo per via endovenosa: una volta iniettate, si muovono spontaneamente verso l’area danneggiata senza scatenare reazioni immunitarie e, quindi, di rigetto.
Considerazioni etiche e il quadro normativo
Il progresso scientifico procede parallelamente alla riflessione etica. La legge 40 in Italia, ad esempio, vieta l’utilizzo di embrioni sovrannumerari ai fini della ricerca scientifica, preferendo la loro estinzione. In questo contesto, le cellule staminali da liquido amniotico rappresentano una via di ricerca promettente perché non richiedono la manipolazione di embrioni, risolvendo molte delle problematiche etiche che bloccano la ricerca sulle staminali embrionali.
Inoltre, l'uso di queste cellule permette di evitare la riprogrammazione genetica invasiva, riducendo il rischio di effetti collaterali gravi come lo sviluppo di tumori. Le cellule staminali prelevate dal liquido amniotico si trovano in uno stato biologico ideale: «È come se si trovassero a metà tra le cellule embrionali e quelle adulte», ha spiegato Pascale Guillot dell’Imperial College.
Le biobanche e il futuro dei trapianti
Le banche per la conservazione delle cellule staminali sono strutture nelle quali vengono trattate e conservate le unità di cellule prelevate, fino al momento dell'utilizzo. La legislazione che regolamenta l’attività delle biobanche varia da paese a paese. Alcune società private si stanno muovendo verso la creazione di banche del liquido amniotico per uso autogeno o trapianto allogenico.
Teoricamente, secondo le stime di Anthony Atala, una banca contenente 100.000 esemplari di queste staminali potrebbe supplire alle necessità di una vasta popolazione con una compatibilità genetica ottimale per il trapianto. Il percorso verso l'applicazione clinica richiede ancora cautela: sebbene le prospettive siano eccellenti, bisogna sempre tener presente che tali risultati sono stati osservati finora solo in sperimentazioni animali o in laboratorio. Come sottolineato da Paolo De Coppi, «È necessaria ancora molta ricerca, ma la strada è aperta e i primi test clinici potrebbero essere pronti entro quattro o cinque anni».
Il corpo umano e le sue potenzialità rigenerative continuano a essere oggetto di studio profondo, dove le culture scientifica e umanistica si incontrano nel tentativo di chiarire le questioni fondamentali della vita e di offrire risposte alle patologie neurodegenerative e congenite che oggi rimangono, per molte famiglie, una sfida ancora troppo difficile da vincere.