La procreazione medicalmente assistita (PMA) rappresenta un'area della medicina in continua evoluzione, volta ad aiutare le coppie che affrontano difficoltà nel concepimento. Tra le varie fasi che compongono i cicli di fecondazione in vitro (FIVET) e altre tecniche di riproduzione assistita, la stimolazione ovarica riveste un ruolo di primaria importanza. Questo processo mira a indurre lo sviluppo di un numero ottimale di follicoli ovarici, da cui verranno poi prelevati gli ovociti necessari per il successo del trattamento. Tuttavia, la risposta individuale ai farmaci utilizzati per la stimolazione è estremamente variabile. È qui che entra in gioco la farmacogenetica, un campo emergente che studia i fattori genetici ereditari responsabili delle differenze individuali nella risposta all’attività dei farmaci, offrendo la chiave per personalizzare i protocolli terapeutici e aumentarne significativamente l'efficacia.
Comprendere la Variabilità Individuale nella Stimolazione Ovarica
Nei cicli di fecondazione in vitro, le pazienti vengono sottoposte a stimolazione ovarica e per questo vengono somministrate gonadotropine. Questa famiglia di farmaci, che sono essenzialmente ormoni, è in grado di favorire la crescita dei follicoli delle ovaie. Nonostante l'utilizzo di dosi standardizzate, in molti pazienti la risposta a queste gonadotropine non è ottimale. Questa variabilità naturale nelle sequenze di DNA, espressa dai polimorfismi, spiega perché gli individui rispondono diversamente ai farmaci. La ricerca ha identificato che questi fattori genetici sono alla base delle differenze nella risposta ai farmaci tra i diversi individui.
Fino ad oggi, la scelta e la dose del farmaco ormonale da utilizzare per la stimolazione ovarica erano stabilite su base empirica e con criteri standardizzati, spesso basati su fasce d'età o su determinate condizioni cliniche. Questo approccio, sebbene abbia portato a successi, non teneva adeguatamente conto delle peculiarità genetiche di ciascuna paziente. La consapevolezza di questa variabilità ha spinto la ricerca verso strategie più mirate, in particolare per quelle pazienti che hanno dimostrato una bassa riserva ovarica o una risposta non ottimale nei precedenti cicli di fecondazione in vitro.
La Farmacogenetica: Un Ponte tra Geni e Farmaci
La Farmacogenetica è un nuovo settore della genetica che studia i fattori genetici ereditari responsabili delle differenze individuali nella risposta all’attività dei farmaci. In sostanza, analizza come il nostro DNA influenzi il modo in cui il nostro corpo metabolizza e risponde ai farmaci che assumiamo. Questa disciplina è particolarmente promettente nel campo della riproduzione assistita, dove la risposta ai farmaci iniettabili, come le gonadotropine, è cruciale per il successo del trattamento.
Nel Dipartimento di Genetica e Biologia Molecolare dell’Instituto Bernabeu, ad esempio, sono state identificate e caratterizzate varianti genetiche specifiche associate alla risposta alla stimolazione ovarica. Queste varianti genetiche corrispondono a cambiamenti nel codice genetico che alterano il comportamento del paziente nei confronti delle gonadotropine. Queste modifiche genetiche sono prodotte in geni importanti per la crescita e la maturazione degli ovociti, come i recettori per gli ormoni FSH (ormone follicolo-stimolante), i recettori per gli androgeni, i recettori per gli estrogeni e il gene che codifica per l’ormone anti-Mülleriano (AMH).
L'identificazione di questi polimorfismi genetici permette di prevedere, con maggiore affidabilità, come una paziente risponderà a determinati protocolli di stimolazione. Questo non solo ottimizza la scelta dei farmaci e dei loro dosaggi, ma può anche contribuire a ridurre i rischi associati a trattamenti non personalizzati. L'obiettivo è fornire una diagnosi precoce della predisposizione genetica individuale, offrendo così il trattamento più adeguato fin dall'inizio.
IBGenFIV: Un Test Diagnostico per Protocolli Personalizzati
Per sfruttare i benefici della farmacogenetica, sono stati sviluppati test diagnostici specifici. Un esempio è IBGenFIV, un test diagnostico eseguito dai pazienti prima di iniziare il ciclo di fecondazione in vitro. Questo test permette di conoscere il profilo genetico della paziente, su cui basare il disegno del miglior protocollo di stimolazione ovarica possibile.
Il processo coinvolge l'analisi di un campione biologico, come saliva o sangue, della paziente. Da questo campione, il laboratorio (ad esempio, IB BIOTECH) estrae il DNA sufficiente per studiare le varianti genetiche che permettono di conoscere la risposta ovarica della paziente prima ancora che inizi il suo trattamento. Questo approccio innovativo, basato su uno studio genetico della funzione ovarica, apporta informazioni cruciali per risolvere quei casi clinici di donne che desiderano essere madri ma presentano uno scarso numero di ovociti o hanno riscontrato inefficacia nei cicli precedenti.
IBGenFIV, in particolare, si configura come una strategia farmacogenetica particolarmente rilevante per quelle pazienti con una bassa riserva ovarica e/o che hanno avuto una risposta inadeguata nei precedenti cicli di fecondazione in vitro. Grazie a questo test, queste pazienti possono beneficiare della farmacogenetica per ottenere un maggior numero di ovociti maturi, aumentando così le possibilità di ottenere una gravidanza evolutiva.

L'Efficacia dei Trattamenti Personalizzati: Dati e Benefici
La ricerca condotta per sviluppare e validare questi test ha dimostrato benefici concreti. Un team scientifico, dopo più di quattro anni di ricerca, ha analizzato e identificato i geni implicati nella risposta ovarica. Le conclusioni di questi studi, presentate a congressi scientifici di rilievo e pubblicate su prestigiose riviste mediche, hanno permesso di conoscere in profondità la medicazione e il dosaggio più adeguato ad ogni genotipo.
Uno studio specifico ha analizzato i risultati della stimolazione ovarica in 228 pazienti che avevano precedentemente effettuato il test farmacogenetico. È stato verificato il risultato della stimolazione ovarica nei cicli precedenti e successivi alla realizzazione dell’analisi. Questo studio rappresenta il primo lavoro di ricerca a dimostrare che i test farmacogenetici possono effettivamente migliorare i risultati della stimolazione ovarica. Esiste quindi un beneficio importante derivante da queste analisi, teso alla personalizzazione dei trattamenti di stimolazione ovarica.
In generale, la farmacogenetica permette di conoscere la base genetica della variabilità nella risposta ai farmaci e, in questo modo, di modificare i trattamenti per renderli più effettivi. Nei trattamenti di riproduzione assistita, personalizzare la stimolazione ovarica significa ottimizzare la risposta delle ovaie, determinando con affidabilità la medicazione e il dosaggio più adeguati alla genetica specifica della paziente. Questo si traduce in un aumento dell’efficacia del trattamento di riproduzione assistita.
Can PGS, embryo genetic diagnosis, increase the IVF success rates?
Tecniche di Procreazione Medicalmente Assistita e Farmaci Coinvolti
Le tecniche di procreazione medicalmente assistita (PMA) si suddividono in diversi livelli, basati sulla complessità e sulla modalità di incontro tra ovocita e spermatozoo. Indipendentemente dalla tecnica specifica (inseminazione intrauterina o fecondazione in vitro), la stimolazione ovarica rimane una fase cruciale, specialmente per la FIVET.
I farmaci necessari in questa fase del programma vengono selezionati in base alle specifiche condizioni della coppia e alle esigenze del ciclo. Tra i farmaci più utilizzati per la stimolazione ovarica troviamo:
Gonadotropine (FSH e LH): Sono state una rivoluzione nelle possibilità terapeutiche, sia nell'induzione dell'ovulazione nelle pazienti anovulatorie, sia come terapia per la stimolazione della multi-ovulazione nelle procedure di procreazione assistita. Tra i vantaggi delle nuove molecole ricombinanti ci sono una maggiore omogeneità dei farmaci, una maggiore efficacia clinica e la possibilità di ricorrere a dosi inferiori di farmaco per gravidanza ottenuta. I dosaggi giornalieri variano generalmente da 75-100 UI in pazienti giovani con eccellente riserva ovarica, sottopeso e con tratto policistico, a un massimo di 450 UI/die, limite che non viene in genere superato perché ritenuto inefficace anche in pazienti con riserva ovarica compromessa. Il monitoraggio ecografico e ormonale ha lo scopo di definire la risposta e ridurre, per quanto possibile, la quantità di gonadotropine somministrate e il rischio di iperstimolazione ovarica.
Analoghi del GnRH (Ormone di rilascio delle gonadotropine): Possono essere utilizzati in formulazioni "deposito" (nelle pazienti in cui è attesa una normale risposta ovarica) o "giornaliere". Vengono impiegati nelle procedure che prevedono la soppressione dell'ipofisi prima di iniziare la stimolazione, per evitare un picco prematuro di LH e permettere uno sviluppo follicolare più controllato.
Antagonisti del GnRH: Possono essere proposti alla paziente che presenta una previsione di risposta ridotta o, al contrario, eccessiva alla terapia di somministrazione. Vengono associati a un estroprogestinico per la sincronizzazione del ciclo e generalmente rendono più breve il periodo di induzione della multi-ovulazione.
Antiestrogeni (es. Clomifene Citrato): Sebbene meno utilizzati nella FIVET moderna rispetto alle gonadotropine, possono essere impiegati in alcuni protocolli. La somministrazione è solitamente orale, in fase follicolare per circa 5 giorni. È possibile una risposta ridotta in caso di resistenza al farmaco.
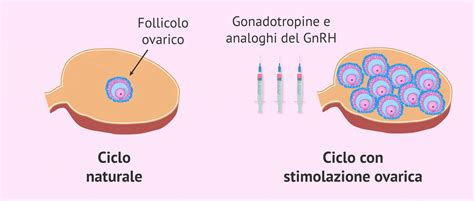
Gestione dei Rischi: Dalla Risposta Ottimale alla Sindrome da Iperstimolazione Ovarica
La risposta alla stimolazione e il controllo della terapia sono fondamentali per la buona riuscita del ciclo terapeutico. Tuttavia, è importante essere consapevoli dei potenziali rischi associati a questi trattamenti. I rischi più gravi sono sostanzialmente concentrati nella sindrome da iperstimolazione ovarica (Sindrome da Iperstimolazione Ovarica - SIO).
Questo fenomeno, descritto raramente anche in donne non sottoposte alle terapie di procreazione assistita, comporta un discreto aumento volumetrico delle ovaie, con produzione di liquido all’interno dell’addome (ascite) e comparsa di sintomi soggettivi a volte importanti: dolore, senso di peso, difficoltà alla respirazione, diminuzione della diuresi. I fattori di rischio per lo sviluppo di SIO includono età giovane, sindrome dell'ovaio policistico (PCOS), alti valori di estradiolo, numerosi piccoli follicoli e alcuni regimi di stimolazione specifici.
Il monitoraggio ecografico e ormonale è essenziale non solo per definire la risposta alla stimolazione, ma anche per ridurre per quanto possibile la quantità di gonadotropine somministrate e, di conseguenza, il rischio di iperstimolazione ovarica. Protocolli farmacogenetici personalizzati possono contribuire a minimizzare questo rischio, ottimizzando il dosaggio e la scelta dei farmaci in base al profilo genetico della paziente.
Esiste, inoltre, la possibilità che la terapia di induzione non produca la crescita di un numero adeguato di follicoli, oppure che il monitoraggio ormonale faccia ritenere di non poter prelevare ovociti maturi, portando a una risposta all'induzione per la crescita follicolare multipla assente o insufficiente. In tali casi, la decisione di procedere al prelievo o di sospendere il ciclo viene presa valutando attentamente il quadro clinico.
Prospettive Future e Ruolo della Genetica nell'Infertilità Inspiegata
L'infertilità inspiegata rappresenta una percentuale significativa (circa il 30%-40%) dei casi di infertilità totale. In queste situazioni, nonostante le indagini standard non rilevino anomalie evidenti, la gravidanza non avviene. Studi come quello condotto dal dottor Farquhar hanno analizzato l'impatto della stimolazione ovarica in combinazione con l'inseminazione intrauterina (IUI) in donne con infertilità inspiegata. Questo studio ha confrontato gruppi di donne, dimostrando che la stimolazione ovarica, in combinazione con l'IUI, aumenta notevolmente le possibilità di concepire. Tuttavia, è stato anche osservato un tasso più alto di aborti spontanei in uno dei gruppi trattati, evidenziando la complessità e la necessità di un approccio su misura.
Alcuni medici hanno quindi proposto di ampliare i normali test di valutazione della fertilità. Test genetici e immunologici, ad esempio, potrebbero aiutare a identificare eventuali anomalie sottostanti che non emergono con le indagini convenzionali. Bisogna però tenere conto che l'introduzione di questi test aumenterebbe anche i costi della fecondazione assistita, almeno nelle fasi iniziali.
Parallelamente, la ricerca si sta concentrando su altri marcatori biologici per migliorare l'esito dei trattamenti. Ad esempio, è stato recentemente dimostrato che la proteina endometriale SGK1 (Serum and Glucocorticoid regulated Kinase) riveste un ruolo fondamentale ai fini del buon esito dell’impianto embrionale in utero e dunque della gravidanza. Questa chinasi, scoperta da ricercatori britannici e definita “l’interruttore della fecondazione umana”, è oggetto di studi per stabilire il range di normalità dei suoi valori in grado di assicurare la formazione dell’impianto.
In sintesi, la farmacogenetica e l'avanzamento degli studi genetici offrono una prospettiva entusiasmante per la personalizzazione dei trattamenti di stimolazione ovarica. Passando da un approccio standardizzato a uno basato sul profilo genetico individuale, è possibile ottimizzare le risposte, migliorare l'efficacia dei cicli di riproduzione assistita, aumentare il numero di ovociti maturi ottenuti e, in ultima analisi, accrescere le probabilità di successo per le coppie che desiderano realizzare il sogno di una gravidanza.
tags: #stimolazione #ovarica #farmacogenetica #polimorfismo