Nel complesso e delicato percorso della procreazione assistita, l'ovodonazione emerge come una soluzione di grande speranza per molte coppie e donne che desiderano realizzare il sogno della genitorialità. Questa tecnica di fecondazione assistita eterologa, che prevede l'utilizzo di ovuli provenienti da una donatrice esterna alla coppia e gli spermatozoi del partner (o di un donatore), offre possibilità significative di successo laddove altre strade si siano rivelate inefficaci. Tuttavia, l'ovodonazione non è un percorso esente da domande e preoccupazioni, che spaziano dalla ricerca della somiglianza fisica ed emotiva con il futuro bambino, alla complessa interazione di fattori biologici che possono influenzare l'esito della gravidanza, come la compatibilità genetica e immunologica. In particolare, la presenza di condizioni quali il Lupus Anticoagulant (LAC) può aggiungere un ulteriore livello di complessità, richiedendo attenzioni e terapie specifiche per garantire l'attecchimento e il proseguimento della gestazione. L'obiettivo di questo articolo è esplorare in profondità questi aspetti, fornendo una panoramica chiara e dettagliata dell'ovodonazione, delle sue sfide e delle soluzioni che la medicina riproduttiva moderna è in grado di offrire.
L'Ovodonazione: Definizioni, Indicazioni e Percorso Clinico
L'ovodonazione è un trattamento di fertilità che si è affermato come una delle opzioni più efficaci per superare varie forme di infertilità femminile. È particolarmente consigliabile ricorrere all'ovodonazione in situazioni dove la riserva ovarica della donna è significativamente diminuita, o quando la qualità degli ovociti è compromessa, una condizione sempre più frequente per le donne che decidono di diventare madri dopo i 40 anni. In questo contesto, l'utilizzo di un ovulo di una donatrice diventa essenziale per ottenere una gravidanza.
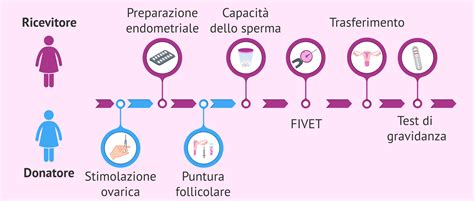
Il processo di ovodonazione si articola in diverse fasi, che coinvolgono sia la donatrice che la ricevente. Inizialmente, viene eseguita una valutazione dettagliata di entrambe le donne per verificare che siano idonee al trattamento. La donatrice di ovuli, selezionata secondo criteri rigorosi, inizia una stimolazione ovarica controllata, che dura tipicamente circa 10-12 giorni. Durante questo periodo, la sua risposta ai farmaci viene monitorata attentamente tramite ecografie e analisi del sangue. Una volta che i follicoli hanno raggiunto la dimensione adeguata, si procede con la puntura ovarica per il prelievo degli ovociti. Questa procedura viene eseguita sotto sedazione e consiste nell'aspirazione dei follicoli sviluppati all'interno delle ovaie stimolate, utilizzando una sonda ecografica transvaginale munita di un sottilissimo ago che attraversa la parete vaginale. Gli ovociti prelevati possono essere criocongelati per un utilizzo futuro o trattati a fresco, ovvero sottoposti immediatamente a fecondazione in vitro.
Parallelamente, la donna ricevente si sottopone a una terapia ormonale, generalmente per 20-30 giorni circa, il cui scopo è preparare l'endometrio, il rivestimento interno dell'utero, a ricevere l'embrione. Anche la ricevente viene monitorata tramite controlli ecografici per assicurarsi che l'utero sia pronto e ricettivo. Una volta che gli ovuli della donatrice sono stati fecondati con lo sperma del partner o di un donatore, gli embrioni che ne derivano vengono coltivati in laboratorio. Nella maggior parte dei centri specializzati, si tende a trasferire solo embrioni allo stadio di blastocisti, ovvero al 5° o 6° giorno di sviluppo. Questo approccio consente di selezionare l'embrione migliore, avendo monitorato il suo sviluppo per un periodo di tempo ragionevole e raccogliendo informazioni preziose sulla sua morfologia e altre caratteristiche.
Il trasferimento dell'embrione è una procedura relativamente semplice e indolore, spesso paragonabile a una visita ginecologica di routine, che generalmente non richiede anestesia. Attraverso un catetere sottile, che viene fatto passare dal canale cervicale uterino, gli embrioni vengono delicatamente depositati all'interno della cavità uterina, sotto guida ecografica. Questa fase si conclude con un breve periodo di riposo, considerato utile per ottimizzare le possibilità di impianto e di gravidanza. Circa 10 giorni dopo il trasferimento dell'embrione, sarà possibile eseguire un test di gravidanza sanguigno, noto come "beta" test, per controllare i livelli dell'ormone beta-hcg. I livelli di questo ormone, necessari per lo sviluppo della gravidanza, aumentano esponenzialmente con il passare dei giorni dopo il trasferimento dell'embrione, fornendo un'indicazione della vitalità della gravidanza.
I vantaggi dell'ovodonazione includono percentuali di successo notevolmente elevate, che possono superare il 72% al primo tentativo in cliniche specializzate e arrivare fino al 90% in donne con prognosi riproduttiva complicata, specialmente quelle di età superiore ai 40 anni. Centri di eccellenza, gestendo banche di gameti femminili estese, riescono a garantire l'assenza di liste di attesa per l'avvio del trattamento, permettendo così di intraprendere il percorso di ovodonazione immediatamente e con la garanzia di una veloce e efficace assegnazione degli ovociti più idonei.
Nonostante la sua sicurezza, l'ovodonazione può comportare alcuni effetti collaterali e rischi, sia per la donatrice che per la ricevente. Per la donatrice, il rischio principale è l'iperstimolazione ovarica, che in rari casi può portare a complicanze gravi come la rottura dell'ovaio. Tuttavia, l'impiego di protocolli farmacologici idonei e un monitoraggio ecografico costante riducono drasticamente questi pericoli. Possono verificarsi anche infezioni nel sito del prelievo o lievi sanguinamenti, gestibili con terapia antibiotica. Per la donna ricevente, la fase procedurale è più semplice, ma nel proseguo della gravidanza possono presentarsi rischi maggiori come la pre-eclampsia (ipertensione più proteinuria) e l'ipertensione gravidica. Questi rischi, pericolosi sia per la donna che per la gestazione, aumentano con l'età, suggerendo che l'età avanzata delle riceventi possa essere un fattore primario.
La Compatibilità nell'Ovodonazione: Dimensioni Multiple per un Successo Integrale
La scelta della donatrice di ovociti è un momento cruciale nel percorso di ovodonazione, poiché influenza non solo le probabilità di successo clinico, ma anche aspetti emotivi e psicologici profondamente sentiti dai futuri genitori. La "compatibilità" in questo contesto si rivela un concetto multidimensionale, che va ben oltre la mera disponibilità di ovociti e abbraccia criteri fenotipici, genetici e immunologici.
Compatibilità Fenotipica: L'Aspetto "Mi Assomiglierà?"
Una delle domande più comuni tra le donne che considerano l'ovodonazione è: "Mi assomiglierà?" o "Lo sentirò mio?". Questa preoccupazione per la somiglianza fisica è del tutto naturale. Per rispondere a questa esigenza, i team medici si impegnano in una valutazione approfondita della donatrice per trovare la massima compatibilità fenotipica. Questo processo di "matching" rispetta tratti come etnia, altezza, carnagione della pelle, colore di capelli e occhi, cercando di selezionare una donatrice le cui caratteristiche fisiche siano il più possibile allineate a quelle della ricevente. Sebbene la legge in molti paesi, come la Spagna, preveda che la donazione di ovuli sia anonima - il che significa che né la ricevente né la donatrice conosceranno l'identità dell'altra - l'attenzione alla compatibilità fenotipica è un passo importante per aiutare la futura madre a stabilire un legame con il bambino e a superare i dubbi iniziali.
Compatibilità Genetica: Proteggere il Futuro Bambino
La compatibilità genetica è un pilastro fondamentale per la sicurezza e la salute del futuro bambino. Nel processo di selezione delle donatrici di ovuli e dei donatori di sperma, vengono effettuati test genetici approfonditi per ridurre al minimo il rischio di trasmissione di malattie genetiche. Il "matching genetico" o "abbinamento genetico" è lo studio dei dati genetici tra donatore e ricevente al fine di garantire la compatibilità genetica ed evitare la trasmissione di malattie recessive.
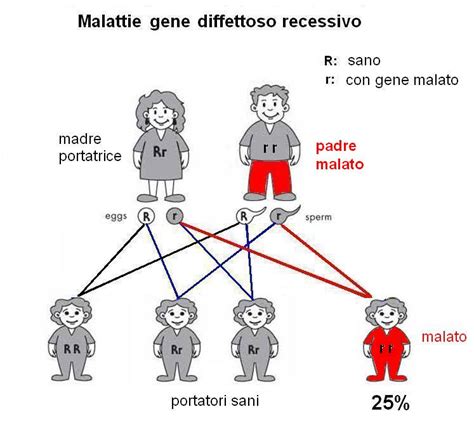
Le malattie ereditarie autosomiche recessive, sebbene abbiano una bassa prevalenza nella popolazione, sono spesso condizioni gravi. Per prevenire la loro trasmissione, in cliniche specializzate si esegue il Test di Compatibilità Genetica (GCT), uno studio genetico per identificare le mutazioni nei geni responsabili delle malattie recessive e X-linked. Nelle malattie recessive, una persona che ha una sola copia del gene mutato (portatore) non sviluppa la malattia, poiché è necessario che entrambe le copie del gene siano mutate perché la malattia si manifesti. Effettuando un'analisi genetica di donatori e riceventi, si evita che entrambi siano portatori della stessa mutazione, riducendo così in modo significativo il rischio di trasmissione di malattie ereditarie alla prole.
È importante notare che, sebbene estremamente utili, i test genetici possono essere costosi, il che può limitare l'accesso a queste tecnologie per alcune coppie. Inoltre, le informazioni genetiche, soprattutto se identificano mutazioni o rischi potenziali, possono creare ansia e stress per i futuri genitori. Tuttavia, la disponibilità di trattamenti come la Diagnosi Genetica Preimpianto (DGP) in concomitanza con la fecondazione in vitro può offrire soluzioni per coppie in cui entrambi i genitori sono portatori di mutazioni per una determinata malattia.
Compatibilità Immunologica: Il Ruolo Cruciale del Lupus Anticoagulant (LAC) e Altri Fattori
Oltre alla genetica, il sistema immunitario della madre gioca un ruolo fondamentale nell'attecchimento e nel mantenimento della gravidanza. L'embrione, infatti, è un "corpo estraneo" per la madre, poiché presenta antigeni che provengono dal padre o, nel caso dell'ovodonazione, dalla donatrice di ovuli. Se il sistema immunitario della madre lo rigetta, questo può essere una causa di fallimenti di impianto e aborti ricorrenti.
Un fattore immunitario particolarmente rilevante è la presenza del Lupus Anticoagulant (LAC) e di altri anticorpi antifosfolipidi (aPL). Questi anticorpi sono coinvolti in una condizione chiamata Sindrome da Anticorpi Antifosfolipidi (APS), che può avere gravi ripercussioni sulla gravidanza e sulla salute generale. Come osservato da specialisti, la presenza di questi anticorpi aumenta il rischio di provocare fenomeni coagulativi nelle vene e nelle arterie dell'organismo, in particolare nelle vene degli arti inferiori, dando luogo a fenomeni di trombosi venosa profonda. La trombosi, provocando spesso la formazione di emboli (in questo caso formati da coaguli di sangue), determina il blocco del flusso sanguigno e quindi, a seconda del settore colpito, può portare a ictus cerebrale, arresto cardiaco o embolia polmonare.
Il LAC può essere positivo in diversi stati patologici della coagulazione e in altre malattie, inclusi l'emofilia classica, alcuni stati infiammatori cronici, patologie del collageno e nel postpartum. È presente in circa il 10% dei pazienti affetti da Lupus Eritematoso Sistemico (LES) e con frequenza ancora maggiore in pazienti con altri processi autoimmuni e con positività degli anticorpi antinucleo. La presenza dei LAC insieme con gli anticorpi anti-fosfolipidi è considerato un fattore di rischio per le trombosi, sebbene la loro presenza non sempre si associ a manifestazioni cliniche. La prevalenza di anticorpi antifosfolipidi nella popolazione sana varia dall'uno al 5%. Si ritiene che il riscontro accidentale di anticorpi antifosfolipidi a basso titolo comporti un rischio minimo di trombosi, mentre le probabilità aumentano se tali anticorpi sono presenti a titolo elevato. È noto che nei soggetti positivi agli aPL che hanno avuto trombosi, il rischio di recidiva è superiore a quello dei soggetti negativi; lo stesso vale per gli aborti. La complicanza più frequente dell'APS in gravidanza è l'aborto precoce.
La patogenesi dell'APS in gravidanza non è completamente compresa, ma si pensa che coinvolga effetti procoagulanti degli aPL, l'attivazione delle piastrine e delle cellule endoteliali. Gli aPL sembrano anche avere un effetto diretto sulla funzione del trofoblasto umano placentare, diminuendone la vitalità, la sincizializzazione e la capacità di invasione, fattori cruciali per un impianto e uno sviluppo embrionale sani. In situazioni cliniche complesse, come nel caso di aborti interni ricorrenti o valori di beta-HCG molto bassi dopo un tentativo di ICSI, la ricerca di fattori come il LAC diventa fondamentale. Ad esempio, una paziente con FSH alto e un aborto interno alla 6/7 settimana dopo ICSI, in cui il test per il Lupus Antico