La medicina fetale, una disciplina che riconosce al feto la dignità di paziente, ha rivoluzionato l'approccio alle condizioni patologiche che si manifestano durante la gestazione. Questo approccio innovativo enfatizza la dignità del feto come paziente a tutti gli effetti, anche in condizioni patologiche ritenute fino a pochi anni fa incurabili. Partendo da questo punto di vista, la diagnosi prenatale assume una luce nuova, contrapponendosi alla visione che la vorrebbe finalizzata solamente all’eliminazione dei feti con anomalie congenite. Con la medicina fetale, la diagnosi prenatale diviene il punto di partenza per cercare soluzioni terapeutiche capaci di garantire vita e salute al nascituro. Questa filosofia è stata al centro del lavoro del professor Noia, uno dei fondatori della medicina fetale, il cui impegno ha dato vita a significative collaborazioni, come quella con l'Istituto di genetica MAGI, focalizzate sullo studio dell'Igroma Cistico e sul funzionamento, a scopi terapeutici, delle cellule staminali mesenchimali amniotiche e cordonali ematopoietiche.
In questo contesto di avanzamento scientifico e medico, due condizioni che richiedono particolare attenzione durante la gravidanza sono l'igroma cistico e l'ipotiroidismo, entrambe con implicazioni significative per lo sviluppo fetale e la salute materna. Esploreremo in dettaglio queste patologie, le loro diagnosi, le prognosi tradizionali e le nuove speranze offerte dalla ricerca contemporanea, sottolineando l'importanza di un approccio informato e di una gestione mirata.
L'Igroma Cistico: Una Malformazione Linfatica Complessa e le Sue Implicazioni
L'igroma cistico è una malformazione congenita del sistema linfatico, caratterizzata dalla presenza di strutture cistiche localizzate prevalentemente nella regione postero-laterale del collo. Questa anomalia si presenta come una sacca piena di liquido, principalmente nella zona del collo e della testa, ed è nota anche come linfangioma. Queste cisti sono spesso presenti alla nascita, ma possono anche svilupparsi più avanti nella vita. Sebbene benigna, la sua presenza può portare a notevoli problemi fisiologici ed estetici, a seconda delle dimensioni e della posizione delle cisti.
Definizione e Origine Embriologica dell'Igroma Cistico
L'igroma cistico si manifesta come un accumulo di liquidi dietro la nuca del feto che può raggiungere dimensioni ragguardevoli. Questo è dovuto ad un'alterazione del sistema linfatico durante l’embriogenesi, il processo di sviluppo dell’embrione dall’uovo fecondato o attivato, che consiste nell’ordinata sequenza dei fenomeni di accrescimento, di differenziamento e di organogenesi che conducono alla formazione di un individuo. Durante la vita embrionale, il sistema linfatico drena nel sacco linfatico giugulare, una struttura primitiva, bilaterale, che intorno ai 40 giorni di età gestazionale comunica con la vena giugulare. Se tale comunicazione si interrompe, vuoi per alterata linfoangiogenesi o per fenomeni ostruttivi, si ha come conseguenza la dilatazione dei sacchi linfatici laterocervicali e quindi la formazione dell'igroma. In pratica, si tratta di una difettosa connessione tra vasi linfatici e vene giugulari che fa accumulare liquido non drenato dentro una ciste.
Diagnosi Prenatale e Caratteristiche Ecografiche
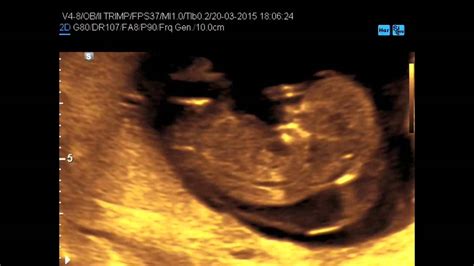
L'individuazione dell’igroma cistico avviene di solito nel corso della prima ecografia, tramite l’esame della Translucenza Nucale, tra 9 e 14 settimane di epoca gestazionale, dove si rileva la presenza di una formazione cistica localizzata nella regione postero-laterale del collo fetale. In genere, l'igroma cistico viene diagnosticato intorno alla 12a-14a settimana di epoca gestazionale. Può essere settato o non settato, indicando la presenza o assenza di setti interni all'interno della ciste, che possono influenzare la sua gestione. In presenza di anomalia, vengono poi prescritti altri esami per una valutazione più approfondita. L'ecografia, che può rivelare la presenza di strutture cistiche, è fondamentale per ottenere una diagnosi prenatale accurata.
Prognosi Tradizionale e Nuove Prospettive di Ricerca
Fino a poco tempo fa, si riteneva che tutte queste condizioni fossero foriere, nel 100% dei casi, di malattie genetiche o cromosomiche associate a un elevato tasso di cardiopatie. Questa convinzione spesso, quando diagnosticata durante la gestazione, induceva all’interruzione di gravidanza. La patologia comporta un elevato rischio di aborto spontaneo (63%); nei restanti casi, invece, si veniva, quasi sempre, indirizzati verso l’interruzione volontaria di gravidanza per la convinzione che questi bambini sarebbero nati gravemente malati.
Tuttavia, l'igroma cistico presenta un rischio di aneuploidia elevato, stimato tra il 35% e il 50%. Nei casi evidenziabili nel I trimestre, può associarsi a trisomia 21, 18, 13 e Sindrome di Turner. Nel II trimestre, l'aneuploidia associata più frequentemente è la monosomia X o sindrome di Turner. Anche il rischio sindromico è particolarmente elevato; le sindromi che più frequentemente possono associarsi all'igroma cistico sono la Sindrome di Noonan, la Sindrome di Fryns, la Sindrome di Neu-Laxova, la Multiple Pterygium Syndrome, la Sindrome di Escobar, la Sindrome di Klippel-Feil e la Sindrome di Zellweger. Le malformazioni associate hanno un'incidenza del 60%, e quelle più frequentemente riscontrate sono cardiopatie congenite, displasie scheletriche, anomalie del sistema nervoso centrale ed ernia diaframmatica.
Una delle ultime ricerche condotte dal professor Noia, che presto vedrà la pubblicazione, induce a rivedere queste convinzioni. Lo studio ha riguardato 220 gravidanze con diagnosi di Igroma Cistico, tutte donne che arrivavano presso il Centro Diagnosi Terapie Fetali del Gemelli con la diagnosi fatta in altra sede e un 'consiglio' di aborto volontario, ma che, invece, cercavano una speranza per non rassegnarsi. Si è capito che era necessario dar loro molte più informazioni sulla reale condizione del feto, pur nella consapevolezza che per molti casi si sarebbe verificato, come è poi avvenuto, un aborto spontaneo.
Le pazienti sono state sottoposte ad analisi cromosomica per verificare quali bimbi fossero affetti da altre condizioni genetiche patologiche oltre all’igroma. Dopo aver fatto l’amniocentesi, i cromosomi fetali erano normali nel 59% dei casi, un dato che offre una speranza significativa. Le ecocardiografie, effettuate per escludere patologia cardiaca, erano normali nel 70% dei casi. La regressione intrauterina è stata osservata nel 36% dei casi e la completa scomparsa dell’igroma nel 77% dei casi, specialmente nei casi non settati, che a volte possono costituire una "variante" della normalità. In questi casi, si ritiene che le connessioni veno-linfatiche del collo, che drenano sangue e linfa del distretto cefalico, non si siano ancora del tutto sviluppate o abbiano subito un'ostruzione transitoria.
Alla fine, sono nati 52 bambini sani, che altrimenti sarebbero stati condannati, per la diagnosi ricevuta, a non nascere. Di questi, 41 sono stati seguiti con follow up di lungo periodo, anche di 25 anni. Il dato più eclatante è che dopo una consulenza fondata sui dati internazionali e sul follow up effettuato dal gruppo del professor Noia (il più lungo esistente in letteratura mondiale), il 64% dei bambini è in braccio alle loro mamme. Insomma, non è vero che questi bimbi sono condannati; il 68% nasce ed è sano a un lungo follow up. In tal modo, utilizzando criteri di fortissima evidenza scientifica, si è compressa l'amplificazione del rischio stimato, si sono ridotti gli elementi di dubbio diagnostico, l’ansia e quindi il rifiuto, fornendo ai genitori una prospettiva più realistica e spesso più favorevole.
Cause dell'Igroma Cistico con Cariotipo Normale: Un Campo di Studio Aperto
Non sono ancora note le cause della comparsa dell’igroma cistico, né sono state riscontrate predisposizioni genetiche alla malattia, come evidenziato anche dalle esperienze di madri che hanno affrontato aborti terapeutici per igroma cistico con cariotipo fetale normale. Le cause esatte dell'igroma cistico restano elusive, ma sono stati identificati diversi fattori. Le anomalie genetiche, in particolare le anomalie cromosomiche come la sindrome di Turner e la sindrome di Down, sono state associate allo sviluppo di igromi cistici. Tuttavia, la persistenza di casi con cariotipo normale pone interrogativi importanti. Le cause dell’igroma cistico a cariotipo normale sono ancora in larga misura non note. Una parte dei casi è attribuibile alla sindrome di Noonan, che si caratterizza per specifiche mutazioni geniche senza alterazioni cromosomiche evidenti al cariotipo standard. La comprensione di queste cause è cruciale per poter pensare a delle terapie in grado di salvare la vita ad un numero maggiore di questi bambini.
MED2000ECO Igroma Cistico
Approcci Terapeutici e Gestione dell'Igroma Cistico
Nei casi in cui la gravidanza non si interrompe spontaneamente, è necessario studiare il cariotipo fetale mediante villocentesi o amniocentesi, una accurata valutazione ecografica dei vari organi ed apparati (specie apparato muscolo scheletrico ed apparato cardiovascolare mediante ecocardiografia fetale), e una consulenza genetica. Il management e la prognosi dell'igroma cistico dipendono in larga misura dalle sue dimensioni, dalla sua posizione e dalle complicazioni associate. Le cisti più piccole e isolate hanno generalmente un esito favorevole. Tuttavia, quelle collegate ad anomalie cromosomiche o a significative interruzioni anatomiche possono presentare maggiori sfide.
Il trattamento dell'igroma cistico mira a ridurre le dimensioni delle cisti e ad alleviare i sintomi associati. La terapia prenatale per questo tipo di patologia è motivata dalla necessità di anticipare la risoluzione della patologia e, soprattutto, impedirne l’evoluzione con eventuali complicanze come l’ostruzione delle vie aeree.
La chirurgia rimane la modalità di trattamento primaria per l'igroma cistico in fase postnatale. L'obiettivo è asportare completamente la cisti, anche se questo potrebbe non essere sempre fattibile a causa del coinvolgimento di strutture critiche. La scleroterapia consiste nell'iniettare uno sclerosante nella cisti, che nel tempo ne provoca il restringimento. Questo approccio meno invasivo è adatto ai pazienti che non sono candidati ideali per l'intervento chirurgico. La terapia laser è un'opzione di trattamento emergente, in particolare per le cisti superficiali, che utilizza energia luminosa focalizzata per ridurre le dimensioni dell'igroma. In scenari specifici, specialmente quando l'igroma cistico è piccolo e asintomatico, può essere adottato un approccio conservativo di osservazione.
Esperienze prenatali sono state fatte dal gruppo di Kuwwabara et al., inoculando una sorta di collante, OK-432, direttamente all’interno dell’igroma cistico con la sopravvivenza del 33% dei casi. Più recentemente, nella fase postnatale, alcuni autori hanno utilizzato un altro farmaco, il Sirolimus, un farmaco immunosoppressore utilizzato per prevenire il rigetto dei trapianti di organi. Un voluminoso igroma cistico (370 ml) è stato trattato per 15 mesi con Sirolimus, ottenendo una diminuzione del volume del 90%.
L’esperienza del gruppo del Gemelli (Chirurgia Pediatrica), ha visto il trattamento di 14 casi dal 1998 al 2013 utilizzando un approccio a doppio step di asportazione della malformazione vasculolinfatica postnatalmente e di iniezione dell’OK-432 all’interno della stessa, con una durata della procedura di circa 20 minuti. Attualmente, a causa dei campioni numericamente ancora esigui e della non omogeneità nelle casistiche legate alla malattia, la terapia è in fase sperimentale e non c’è ancora un protocollo terapeutico condiviso.
La gestione dell'igroma cistico pone diverse sfide. La vicinanza delle cisti alle strutture vitali può complicare gli interventi chirurgici e l'escissione completa potrebbe non essere sempre possibile. La recidiva è un problema comune, che richiede un follow-up continuo e, in alcuni casi, trattamenti multipli, rendendo essenziale una stretta collaborazione tra specialisti.
L'Ipotiroidismo in Gravidanza: Impatto sulla Salute Materna e sullo Sviluppo Fetale
Oltre alle malformazioni come l'igroma cistico, la gravidanza è di per sé causa di notevoli cambiamenti della concentrazione degli ormoni tiroidei anche in donne che non abbiano manifestato alterazioni tiroidee in precedenza. La diagnosi ed il trattamento delle alterazioni tiroidee in gravidanza richiedono particolare attenzione per diversi motivi: da una parte la gravidanza ed il puerperio si accompagnano ad una rilevante modificazione del funzionamento della ghiandola, dall’altra le malattie tiroidee in gravidanza possono influenzarne il corso e creare danno al feto oltre ad influenzare lo stato di salute nel periodo postparto.
La Funzione Tiroidea in Gravidanza: Cambiamenti e Importanza
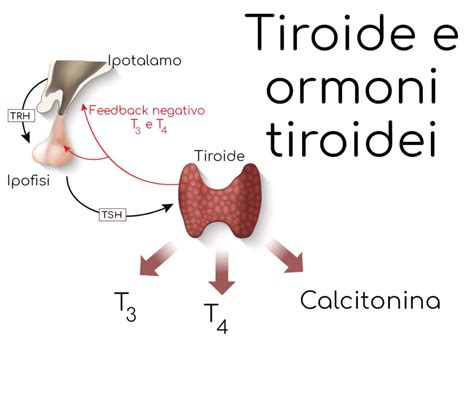
Durante la gravidanza, il fabbisogno di ormoni tiroidei aumenta in modo significativo per sostenere sia il metabolismo materno che lo sviluppo fetale. È importante, infatti, sapere che circa il 7% delle donne possono sviluppare un’alterazione tiroidea nel primo anno postparto, pur in assenza di precedenti malattie tiroidee. La tiroide produce ormoni essenziali per la regolazione di numerosi processi metabolici. Questi ormoni sono cruciali per lo sviluppo neurologico del feto, specialmente durante il primo trimestre, quando il feto dipende interamente dagli ormoni tiroidei della madre.
Definizione, Incidenza e Rischi dell'Ipotiroidismo Gestazionale
L’ipotiroidismo è una condizione in cui la donna in gravidanza ha troppo poco ormone tiroideo. Questa condizione, che si verifica nello 0,3-0,5% delle gravidanze (nel 2-3% se si include l’ipotiroidismo subclinico), è associata ad aumentato rischio di aborto spontaneo, parto pretermine, stress e morte fetale, ipertensione ed emorragia postparto. Inoltre, l’ipotiroidismo è associato anche a rischi legati allo sviluppo del feto. Infatti, durante il primo trimestre di gravidanza è la madre, con i propri ormoni tiroidei, a fornire al feto tutto l’ormone tiroideo di cui ha bisogno. Quindi, se una donna ha poco ormone tiroideo, anche il suo bambino può soffrire la mancanza di ormone in un momento critico in cui è in corso lo sviluppo del cervello. La carenza di ormoni tiroidei materni può compromettere gravemente la formazione delle strutture cerebrali fetali, con conseguenze a lungo termine sullo sviluppo cognitivo e neurologico del bambino.
MED2000ECO Igroma Cistico
Cause e Diagnosi dell'Ipotiroidismo in Gravidanza
La principale causa di ipotiroidismo in gravidanza è la tiroidite autoimmune (di Hashimoto), una malattia determinata dal sistema immunitario della donna che attacca e tende a distruggere la tiroide. La presenza nel sangue (rilevabile con un semplice prelievo) di anticorpi contro la tiroide segnala la presenza della malattia autoimmune tiroidea. La prima considerazione è che a causa dei gravi effetti dell’ipotiroidismo sul corso della gravidanza, è meglio essere consapevoli di soffrire di questa malattia prima di avviare una gravidanza. Le donne con una storia familiare di malattie della tiroide o altre malattie autoimmuni corrono un rischio maggiore di sviluppare ipotiroidismo. La presenza di sintomi suggestivi di ipotiroidismo deve subito suggerire al vostro medico di effettuare il dosaggio di TSH (ormone tireostimolante ipofisario che stimola la tiroide a produrre gli ormoni tiroidei) nel vostro sangue. Purtroppo, è possibile anche avere ipotiroidismo e non avvertire disturbi, cosicché la diagnosi viene posta quando la gravidanza è già in corso, rendendo lo screening precoce ancora più cruciale.
La Tiroidite Postpartum: Una Condizione da Monitorare
La tiroidite postpartum è un’infiammazione della ghiandola che colpisce il 7% di tutte le donne durante il primo anno dopo il parto. È caratterizzata da tre fasi o periodi: nel primo periodo vi è una fase di ipertiroidismo che può guarire spontaneamente nel giro di qualche settimana o mese e la funzione tiroidea ritorna alla norma. Tuttavia, in molti casi nella fase di ipertiroidismo si crea un danno alla ghiandola che causa la fase successiva di ipotiroidismo, richiedendo un attento monitoraggio e, se necessario, un intervento terapeutico.
Gestione e Trattamento dell'Ipotiroidismo: L'Importanza dell'Intervento Tempestivo
È bene ricordare che il trattamento tempestivo ed adeguato dell’ipotiroidismo azzera ogni rischio e “riporta” la donna ipotiroidea in trattamento alle stesse probabilità di complicanze delle gravide con funzione tiroidea normale. La terapia consiste nella somministrazione di levotiroxina, un ormone tiroideo sintetico, che integra la produzione insufficiente della tiroide materna. L'adeguamento della dose deve essere meticoloso e basato su regolari controlli dei livelli di TSH e ormoni tiroidei liberi, per assicurare che sia la madre che il feto ricevano un apporto ormonale ottimale. Questo approccio proattivo garantisce non solo la salute della madre, ma anche il corretto sviluppo del bambino, minimizzando i rischi associati a questa condizione.
Innovazione e Collaborazione: Il Ruolo delle Cellule Staminali e della Genetica nella Medicina Fetale
La volontà di combattere malattie come l'igroma cistico e l'ipotiroidismo, che rappresentano un terzo dei ricoveri pediatrici per il 50% del costo complessivo delle prestazioni, ha spinto verso una intensa collaborazione tra diverse realtà scientifiche. Se si riuscisse ad intervenire in età fetale, non solo si farebbe un grande passo per la vita, ma si darebbe anche un grande contributo al sistema sanitario, specialmente in questo periodo di crisi.
Il lavoro del professor Noia, unito a quello dell'Istituto di genetica MAGI, è un esempio brillante di questa sinergia, che si concentra sia sulla diagnosi che sulle terapie innovative, in particolare quelle basate sulle cellule staminali.
La Terapia Fetale con Cellule Staminali: Prospettive Future
Il professor Noia sta concentrando le sue ricerche sulle mesenchimali amniotiche, contenute nel liquido che circonda il bambino nella vita fetale, studiando - per ora solo su modelli animali - il loro uso come terapia fetale futura per malattie genetiche. Parallelamente, sta lavorando sulle staminali ematopoietiche del cordone ombelicale. L’obiettivo è trapiantare il feto quando ancora la sua reazione immunitaria è bassa o inesistente, quindi in un periodo molto precoce, per arrivare alla nascita di bimbi sani.
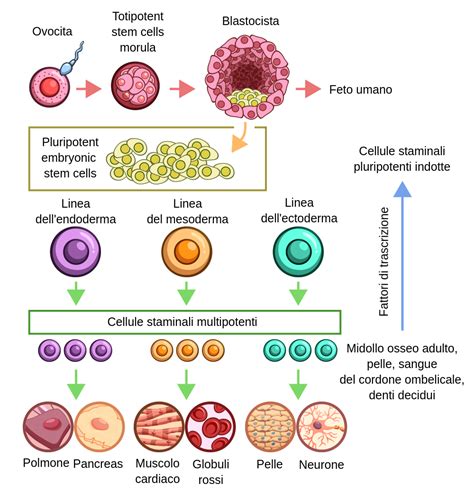
Questo approccio innovativo prevede il trapianto precoce delle cellule staminali, sfruttando la tolleranza immunologica del feto in via di sviluppo. Abbiamo provato a fare il trapianto inserendo le cellule staminali nella cavità celomatica tra 30 e 40 giorni di età gestazionale nelle pecore (corrispondente alla 11esima settimana nell’uomo). Gli studi hanno dimostrato che queste cellule hanno grande capacità di muoversi da una zona anatomica fuori dal ricevente (cavità celomatica) all’interno degli organi dello stesso (fegato, milza, midollo osseo e altri), dimostrando che c’è stato il 100% di attecchimento negli organi ematopoietici e in altri organi. Però, dopo circa un anno e mezzo, si verifica una forma di rigetto che fa diminuire la percentuale di attecchimento. Gli obiettivi dunque ora sono due: cercare di fare il trapianto ancora prima, sotto quel tempo che corrisponde alla decima settimana nell’uomo, e capire come indirizzare queste cellule verso i posti giusti. Il nostro obiettivo primario è l’anemia mediterranea (beta talassemia maior), ma questo approccio si potrebbe estendere anche ad altre patologie genetiche e metaboliche.
Il Contributo dell'Istituto MAGI nella Ricerca e Diagnosi
La collaborazione con l’Istituto di genetica MAGI è molto importante per entrambi i progetti di ricerca del professor Noia. Per l’Igroma Cistico, questa collaborazione consente di avere un laboratorio che esegue i test genetici necessari allo studio della patologia, sia sulle madri che sui bimbi, al fine di poter individuare un eventuale gene predisponente o fare consulenze per escludere le prognosi peggiori. Questo rappresenta un primo passo fondamentale per poter pensare poi a delle terapie in grado di salvare la vita ad un numero maggiore di questi bambini, andando oltre la semplice diagnosi per identificare cause specifiche e personalizzare gli interventi.

Per gli studi sulle staminali, invece, MAGI sta aiutando a individuare altre malattie genetiche da trattare prenatalmente. La combinazione delle competenze cliniche e di ricerca del professor Noia con le capacità diagnostiche e genetiche di MAGI apre nuove frontiere per la medicina fetale. Questa partnership si dedica a comprendere a fondo le basi genetiche delle malattie congenite e a sviluppare strategie terapeutiche innovative, con l'obiettivo ultimo di garantire una vita sana ai nascituri e ridurre l'impatto di queste condizioni sulla salute pubblica. La sinergia tra ricerca di base, clinica e genetica è fondamentale per trasformare le scoperte scientifiche in applicazioni concrete e salvare vite umane, offrendo una speranza tangibile dove prima c'era solo rassegnazione.
tags: #ipotiroidismo #e #igroma #cistico