La decisione di intraprendere un percorso di procreazione medicalmente assistita (PMA) rappresenta un momento significativo per molte coppie, finalizzata alla diagnosi e alla terapia dell'infertilità di coppia. All'interno di questo vasto campo, l'Iniezione Intracitoplasmatica di Spermatozoi, comunemente abbreviata in ICSI, si posiziona come una delle tecniche più avanzate e di frequente impiego nei centri di riproduzione assistita. Sebbene il termine ICSI sia spesso usato per riferirsi all'intero trattamento, esso si riferisce specificamente al metodo di fecondazione degli ovuli con lo sperma in laboratorio, distinguendosi dalla FIVET (Fecondazione In Vitro ed Embryo Transfer) convenzionale. La fase di preparazione ai trattamenti di fecondazione assistita è molto importante, poiché ogni passaggio, dalla prima visita alla preparazione dei gameti, contribuisce al successo dell'intero processo. Questo percorso, pur essendo impegnativo sia dal punto di vista medico-biologico che psicologico, è costellato di tappe ben definite e supportato da personale altamente specializzato, tecnologie innovative e ambienti confortevoli, come testimoniato dall'Ospedale Santa Maria, uno dei primi Centri in Italia ad applicare la tecnica ICSI.
L'Avvio del Percorso: Prima Visita e Valutazione della Coppia
Il primo incontro tra il medico e le coppie è fondamentale per pianificare l’intero percorso del programma. Questo colloquio preconcezionale permette allo specialista ginecologo di raccogliere tutte le informazioni necessarie sulla coppia, inclusi i fattori di rischio, l'età dei partner, gli eventuali esami già in possesso e i mesi di ricerca della prole. È un momento cruciale per esaminare tutta la documentazione medica pregressa, pianificare i tempi delle varie fasi e definire la necessità e le modalità di accesso ai trattamenti. Per questo è utile che siano presenti entrambi i partners ed è fondamentale portare con sé tutti gli accertamenti, le cartelle cliniche e, se del caso, i documenti relativi ai trattamenti eseguiti in altra sede. Questo approccio integrato consente di comprendere quali sono le sue fasi e di stabilire il protocollo più adatto.
Secondo le linee guida dell’Organizzazione Mondiale della Sanità (OMS), in caso di mancato concepimento, si può ricorrere alla Procreazione assistita dopo almeno 12/24 mesi di rapporti liberi e non protetti. Questo criterio definisce il momento in cui l'infertilità viene riconosciuta e si rende opportuno valutare interventi di medicina della riproduzione. Le procedure chirurgiche necessarie nel contesto della PMA, come vedremo, prevedono interventi minimamente invasivi e poco dolorosi e sono considerate a basso rischio chirurgico, con complicanze gravi molto rare. L'approccio moderno enfatizza la necessità per la donna di affrontare un ciclo di Procreazione medicalmente assistita in tutta serenità, motivo per cui gli specialisti consigliano sempre di condurre una vita normale prima, durante e anche dopo il trattamento, sfatando il mito che il riposo assoluto dopo il trasferimento embrionario abbia un valore nell'instaurarsi di una gravidanza.
La Preparazione dei Gameti Maschili: Dalla Raccolta alla Capacitazione
Una componente essenziale della fase preparatoria per l'ICSI è la gestione del campione di seme. Si consiglia di provvedere alla donazione del campione di seme dopo la prima visita, in modo da completare al meglio le analisi sull’infertilità della coppia. Per avere risultati ottimali, è meglio fornire il campione di seme dopo un periodo di astinenza sessuale di 3-5 giorni. Questo campione, ottenuto mediante masturbazione in una sala adibita a tale scopo, viene consegnato immediatamente al laboratorio della clinica che lo analizzerà.
La preparazione del campione seminale è un passaggio cruciale per ottimizzarne le caratteristiche e migliorarne le capacità di fecondazione ovocitaria. Il processo, chiamato capacitazione, prevede la rimozione del plasma seminale e la concentrazione degli spermatozoi di altissima qualità in un nuovo mezzo di coltura. Ci sono diverse tecniche per capacitare lo sperma, ma l'obiettivo comune è quello di ottenere un campione di sperma mobile progressivo (PMSC) di circa un milione per millilitro. In inviTRA, come spiega María de Las Heras Martínez, embriologa clinica, e Zaira Salvador, embriologa, questo processo è fondamentale.
Capacitazione e reazione acrosomiale | Fecondazione
In alcuni casi, specialmente in presenza di un fattore maschile grave, può essere necessario ottenere gli spermatozoi con metodi alternativi. Questo include una puntura testicolare o una biopsia, che possono essere impiegate quando gli spermatozoi non sono presenti nel liquido seminale o sono recuperati, pochi e scarsamente mobili o del tutto immobili, dall'epididimo o dal testicolo. Anche l’eiaculazione retrograda, in cui gli spermatozoi sono rinvenuti nell’urina, richiede l’ICSI. Nonostante queste sfide, anche se più complicato, l'ICSI può essere eseguito con successo, poiché per l'iniezione sono necessari solo tanti spermatozoi vivi quanti sono gli ovuli. È anche possibile l'impiego di un campione di seme congelato, sia del partner che di un donatore, a seconda del caso, che dovrà essere preparato in clinica circa 30 minuti prima dell'ora prevista per l'inseminazione. Con la fecondazione ICSI c’è inoltre un risparmio notevole di spermatozoi, in quanto ne basta solo uno per ogni ovocita, rendendo la tecnica adatta anche in presenza di campioni seminali molto limitati.
La Stimolazione Ovarica Controllata: Ottimizzare la Produzione di Ovociti
La fase di preparazione continua con la stimolazione ormonale della funzione ovarica, un passaggio fondamentale per ottenere un numero adeguato di ovociti maturi. Questo trattamento richiede l’assunzione di farmaci mirati, in particolare gonadotropine, per indurre una crescita follicolare multipla, a differenza del singolo ovocita che matura naturalmente ogni mese. La stimolazione ovarica controllata ha anche la funzione di regolare il ciclo mestruale della donna, impedendo l'ovulazione spontanea che potrebbe compromettere l'esito del ciclo FIV-ICSI.
Prima di iniziare la stimolazione ovarica, è comune prescrivere la pillola anticoncezionale alle pazienti per sincronizzare il ciclo mestruale. A seconda del protocollo personalizzato scelto per la paziente, la durata dell’intero ciclo di stimolazione ovarica può variare da 10 a 20 giorni. Esistono due protocolli di base:
- Protocollo lungo: inizia prima delle mestruazioni con farmaci agonisti di GnRH per rallentare l'ipofisi. Una volta arrivate le mestruazioni, si combinano con le gonadotropine per avviare lo sviluppo follicolare multiplo.
- Protocollo breve: il numero di punture è ridotto, poiché la stimolazione della gonadotropina inizia dopo l'arrivo delle mestruazioni, e si utilizzano antagonisti di GnRH per il freno ipofisario a partire dall'ottavo giorno.
Negli ultimi anni, come sottolinea il Dr. Gorka Barrenetxea, specialista in Ginecologia e Ostetricia, si è registrata una tendenza alla semplificazione dei protocolli di stimolazione ovarica controllata, con una durata media della fase di somministrazione delle gonadotropine (FSH) di circa 6-10 giorni. Durante questo periodo, la crescita follicolare viene seguita mediante monitoraggi ecografici seriali e dosaggi ormonali. Questi controlli consentono di modulare il dosaggio farmacologico in base alla risposta ottenuta e di stabilire il momento appropriato per procedere al recupero degli ovociti. Infatti, quando viene visualizzato un numero adeguato di follicoli con un diametro superiore a 17-18mm, viene indotta la maturazione finale degli ovociti contenuti nei follicoli e il loro distacco dalla parete follicolare mediante la somministrazione di hCG (gonadotropina corionica), circa 30-34 ore prima della puntura ovarica.

Il Prelievo Ovocitario (Pick-up): Un Intervento Minimamente Invasivo
La fase successiva alla stimolazione ovarica è il prelievo degli ovociti, noto anche come agoaspirazione follicolare o pick-up ovocitario. Per questo intervento, la paziente dovrà presentarsi a digiuno (almeno 6 ore senza bere/mangiare) e venire in clinica con circa 45 minuti di anticipo, senza trucco, profumo o gioielli. L'agoaspirazione follicolare è una procedura chirurgica di basso livello di invasività, eseguita in day hospital, che consiste nell'aspirazione del liquido contenuto nei follicoli ovarici per estrarre le uova mature attraverso una puntura vaginale guidata da ultrasuoni.
Per garantire che la procedura sia completamente indolore per la paziente, il medico eseguirà l’agoaspirazione follicolare sotto sedazione profonda. Questa è un procedimento mediante il quale l’anestesista somministra un farmaco con un’iniezione endovenosa che farà dormire la paziente per un breve periodo di tempo, solitamente tra i 10 e i 20 minuti. L'embriologa Maria De Las Heras afferma che "la puntura follicolare non è dolorosa, poiché la paziente viene sedata quando entra in sala operatoria". La procedura in sé dura all'incirca una decina di minuti, e il risveglio è immediato. Dopo l’agoaspirazione, la paziente rimarrà a riposo presso la Clinica Eugin o una struttura analoga per circa 2-3 ore. È importante notare che il numero degli ovociti prelevati non sempre corrisponde al numero dei follicoli e non sempre tutti gli ovociti prelevati sono maturi o idonei per la fecondazione. Una volta in laboratorio, il liquido follicolare deve essere esaminato in dettaglio sotto la lente d'ingrandimento per individuare le uova e trasferirle su una piastra con terreno di coltura.
L'Iniezione Intracitoplasmatica dello Spermatozoo (ICSI): Il Cuore della Tecnica
L'ICSI (Intracytoplasmic Sperm Injection) è una tecnica di fecondazione assistita (PMA) di secondo livello, che rappresenta un'evoluzione e un avanzamento della tecnica FIVET, proposta per la prima volta nel 1991. L'Ospedale Santa Maria è stato tra i primi centri in Italia ad applicarla, ottenendo da allora migliaia di gravidanze. L'ICSI è indicata in linea generale per coppie con un chiaro fattore di infertilità maschile, come la grave oligospermia (ridotto numero di spermatozoi), l'astenozoospermia (ridotta motilità) o l'oligoastenozoospermia severa. È anche cruciale per coppie che hanno avuto insuccessi mediante tecnica FIVET o inseminazione intrauterina, e in tutti i casi in cui il campione seminale non possieda i criteri necessari per una fecondazione convenzionale. L'ICSI è essenziale anche quando gli spermatozoi non sono presenti nel liquido seminale, ma sono recuperati, pochi e scarsamente mobili o del tutto immobili, dall'epididimo o dal testicolo, o in caso di eiaculazione retrograda.
La differenza fondamentale tra ICSI e FIVET risiede nel modo in cui avviene la fecondazione. Nella FIVET, gli ovuli prelevati e gli spermatozoi vengono fatti incontrare ponendoli a contatto in una piastra di coltura, con circa 100.000 spermatozoi per millilitro per ogni goccia di coltura. Al contrario, l'ICSI consiste nella microiniezione di un singolo spermatozoo direttamente all’interno del citoplasma della cellula uovo. Questa tecnica è molto accurata e permette di aumentare significativamente le possibilità di fecondazione degli ovuli, specie in presenza di gravi alterazioni del liquido seminale.
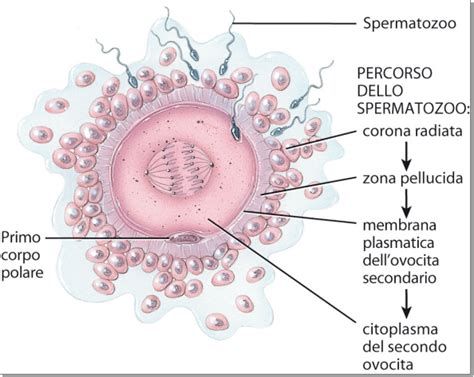
Un passaggio preliminare e distintivo per l'ICSI è il decumulo degli ovociti, noto anche come denudazione. Normalmente, l'ovocita è avvolto da una guaina mucinosa, detta zona pellucida, sulla cui superficie si trovano le cellule del cumulo ooforo. Per poter microiniettare gli ovociti, è necessario prima decumularli e valutare il loro grado di maturità cellulare. Il decumulo consiste nella rimozione di questo strato di cellule del cumulo, generalmente circa due ore dopo il prelievo. Ci sono due tecniche principali per la decumulazione degli ovociti:
- Decumulazione chimica: viene utilizzato un mezzo con ialuronidasi, un enzima che degrada l'acido ialuronico che lega le cellule granulose.
- Decumulo meccanico: l'uovo viene fatto passare attraverso pipette di diverso calibro, da diametri più grandi a diametri più piccoli, fino al completo distacco di tutte le cellule che lo circondano. In genere, i protocolli di laboratorio combinano entrambi i metodi.
Dopo il decumulo, è fondamentale controllare se le uova sono mature per l'ICSI. L'ovocita deve raggiungere la cosiddetta Metafase II, stadio in cui l'unione con lo spermatozoo consente la formazione di un embrione con corredo cromosomico diploide. Questo si verifica visibilizzando il corpuscolo polare nello spazio perivitellino degli ovuli.
La procedura di iniezione intracitoplasmatica richiede un apparato di micromanipolazione connesso a un microscopio rovesciato. Gli embriologi selezionano i migliori spermatozoi del partner o di un donatore e li iniettano uno ad uno direttamente all’interno di ciascun ovulo maturo. I passaggi chiave sono:
- Preparazione iniziale: Pipette di mantenimento e di microiniezione sono posizionate sul microscopio. Una piastra viene preparata con gocce di terreno di coltura per ovuli e spermatozoi.
- Selezione dello spermatozoo: Il campione di sperma viene osservato alla ricerca degli spermatozoi con la migliore qualità. Una volta selezionato, lo spermatozoo viene immobilizzato con un rapido movimento della pipetta ICSI per rompere la coda, quindi aspirato.
- Orientamento dell’ovulo: Per non danneggiare le strutture interne, l'ovulo viene posto con il suo corpuscolo polare verso l'alto e tenuto fermo da una pipetta di tenuta.
- Iniezione intracitoplasmatica: L'ago viene fatto passare attraverso la zona pellucida e inserito all'interno dell'ovocita. Una volta all'interno, un po' di citoplasma viene aspirato fino a quando non entra in contatto con lo sperma, che viene poi rilasciato delicatamente. Ciò consente un’interazione tra il contenuto dello spermatozoo e l’ambiente intracellulare dell’ovocita, essenziale per innescare la fecondazione.
- Valutazione finale: Si osserva il tipo di rottura dell'uovo, che può fornire informazioni sulla sua qualità, e le caratteristiche morfologiche complessive dell'ovocita.
In mani esperte, l’azione di microiniezione è rapida ed efficiente, richiedendo soltanto 1-2 minuti per ciascun ovocita. L’ICSI, in sintesi, bypassa le barriere (cellule follicolari e zona pellucida) che lo spermatozoo dovrebbe attraversare nel concepimento spontaneo o nella FIVET, rendendola un traguardo significativo nella storia della fecondazione assistita.

La Coltura e Lo Sviluppo Embrionario in Laboratorio
Dopo la fecondazione, gli ovociti fecondati, ora zigoti, vengono tenuti in coltura nel laboratorio di embriologia. Il monitoraggio della fecondazione avviene dopo circa 16-20 ore dall’iniezione per verificare l'avvenuta fecondazione. Questa si conferma con la comparsa dei due corpuscoli polari e dei due pronuclei. A volte la fecondazione può essere anomala e gli embrioni che ne conseguono vengono scartati. È necessario ancora un giorno per verificare la formazione o meno degli embrioni.
Gli embrioni ottenuti vengono coltivati in incubatori che simulano le condizioni fisiologiche dell’utero materno. Durante questo periodo, è fondamentale valutare le caratteristiche morfocinetiche degli embrioni per selezionare quelli di migliore qualità e con una maggiore probabilità di impianto. La coltura può durare da 2-3 giorni (fino allo stadio di 6-8 cellule) fino a 5-6 giorni (stadio di blastocisti), in base alla qualità degli embrioni e alla strategia clinica adottata.
Il monitoraggio include:
- Zigoti (circa 18 ore post-fecondazione): si valuta la presenza dei due corpuscoli polari e dei due pronuclei per confermare l'avvenuta fecondazione.
- Embrioni di 2-3 giorni: si valuta il numero di cellule (generalmente da 2 a 8), la loro simmetria, l'eventuale frammentazione cellulare, la multinucleazione e la presenza di vacuoli.
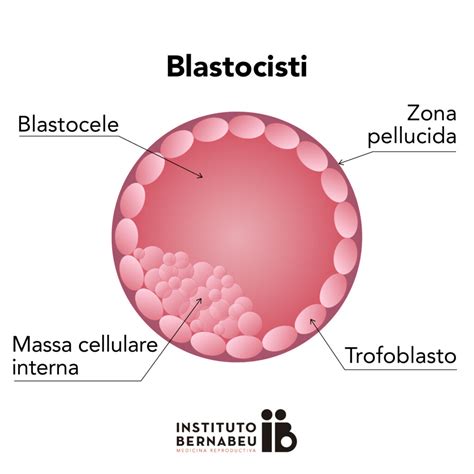
- Blastocisti (5-6 giorni): in questa fase più avanzata, l'embrione è costituito da una moltitudine di cellule che formano la massa cellulare interna (che darà origine al feto) e il trofoectoderma (che formerà la placenta). Si valuta anche il grado di espansione delle blastocisti e l'eventuale "hatching", cioè se hanno iniziato a uscire dalla zona pellucida.
In alcuni casi selezionati, può essere indicata la Diagnosi Genetica Preimpianto (PGT - Preimplantation Genetic Testing). Questa è una tecnica avanzata che permette di analizzare il patrimonio genetico degli embrioni prima del trasferimento per scoprire se soffrono di un'alterazione genetica. Questa biopsia cellulare viene normalmente effettuata 3 giorni dopo l'ICSI quando l'embrione ha circa 8 cellule. Tuttavia, è anche possibile fare la PGD con blastocisti, biopsiando diverse cellule del suo trofoectoderma, senza comprometterne la vitalità.
Il Trasferimento Embrionario: Il Momento Cruciale dell'Impianto
Il trasferimento di embrioni è la fase in cui uno o più embrioni selezionati, in base alla qualità e al quadro clinico della coppia, vengono inseriti nell'utero materno. Tenendo conto delle caratteristiche del trattamento e del numero di embrioni ottenuti, il trasferimento di embrioni può essere effettuato il giorno 3 o il giorno 5 (o raramente al giorno 4), cioè da 48 a 120 ore dopo il prelievo ovocitario.
Prima del trasferimento, la donna deve aver ricevuto estrogeni e progesterone per una preparazione endometriale ottimale, che renda l'utero ricettivo all'impianto. È molto importante che la paziente abbia la vescica piena al momento del trasferimento (sarà necessario bere 3-4 bicchieri d’acqua e non orinare 2-3 ore prima del transfer) per facilitare il controllo ecografico e visualizzare al meglio l'utero.
La procedura di trasferimento embrionale è generalmente rapida, indolore e non richiede l'anestesia. Il ginecologo inserisce lo speculum e deterge l’ambiente vaginale. Il catetere molto sottile e flessibile contenente gli embrioni viene poi inserito nella cavità uterina attraverso la cervice, usualmente sotto controllo ecografico, e gli embrioni vengono rilasciati nella parte inferiore dell'utero. Successivamente, il biologo verifica che nessun embrione sia rimasto all’interno del catetere impiegato per l’intervento. Se ciò dovesse verificarsi, viene ripetuto il transfer per inserire l'embrione o gli embrioni rimasti.
Nell’ottica di ridurre il rischio di gravidanza multipla, si consiglia di limitare il più possibile il numero di embrioni da trasferire. Sebbene la legislazione spagnola consenta il trasferimento di un massimo di 3 embrioni, c'è una crescente tendenza a trasferire un solo embrione invece di due o tre. Il motivo principale è quello di evitare la possibilità di una gravidanza multipla e i rischi che può comportare, sia per la madre che per i feti. Il trasferimento si definisce a "fresco" quando si utilizza l'embrione o la blastocisti ottenuta durante lo stesso ciclo della stimolazione ovarica e del prelievo follicolare. La paziente può alzarsi 15 minuti dopo il transfer e tornare subito alle sue occupazioni abituali, con l’eccezione di attività che comportano un eccessivo sforzo fisico. Mediamente si ottiene il 20-30% di gravidanza dopo il transfer.
Capacitazione e reazione acrosomiale | Fecondazione
La Crioconservazione: Custodire le Opportunità Future
Nella maggior parte dei cicli di FIVET/ICSI, è frequente che rimangano embrioni in eccesso dopo il trasferimento embrionario. La crioconservazione, o vitrificazione, offre la possibilità di conservare questi embrioni per un uso futuro. Per poter essere vitrificati, gli embrioni devono essere di buona o media qualità, in modo da garantire la loro sopravvivenza dopo la devitrificazione. Questa opzione è preziosa sia nel caso in cui il primo tentativo di trasferimento non abbia avuto successo, sia per avere un secondo figlio in futuro.
La tecnica ICSI rende possibile crioconservare sia gli ovociti che gli embrioni vitali in esubero per un ulteriore tentativo. Questo è particolarmente importante in contesti legislativi che non permettono di sopprimere embrioni vitali, come in Italia dove la legge non consente la distruzione degli embrioni. Un'altra opzione per gli embrioni in eccesso sarebbe quella di donarli ad altri pazienti o alla ricerca, qualora la coppia avesse firmato il consenso.
In aggiunta alla crioconservazione embrionaria, esiste anche la crioconservazione ovocitaria. Le pazienti accettate nel programma di crioconservazione degli ovuli vengono sottoposte a induzione farmacologica di una ovulazione multipla, monitorata attentamente con valutazioni ecografiche e ormonali. Al termine della stimolazione, si effettua il prelievo degli ovociti per via transvaginale, una procedura ambulatoriale eseguita in sedoanalgesia. La durata dell'intera procedura, dall'inizio della stimolazione al prelievo, varia a seconda della fase del ciclo in cui la paziente si trova, ma di massima non è superiore ai 14 giorni. Al momento del loro utilizzo, che può avvenire anche dopo molti anni, gli ovociti crioconservati potranno essere inseminati mediante la tecnica ICSI.
L'Attesa della Beta e la Verifica della Gravidanza
Dopo il trasferimento embrionario, inizia un periodo di attesa che, nel gergo dei centri di riproduzione assistita, viene chiamato "l'attesa della beta". La paziente dovrebbe aspettare circa 9-12 giorni prima di eseguire un test di gravidanza per verificare se il trattamento FIV-ICSI ha avuto successo. Questo test, che può essere eseguito sia sulle urine che sul sangue, misura la quantità di ormone beta hCG (gonadotropina corionica umana).
Se il test ematico dell'hCG risulta positivo, si consiglia di ripeterlo 2 giorni dopo. Se il valore del secondo dosaggio plasmatico dell’hCG è almeno raddoppiato rispetto a quello del primo, si esegue un’ecografia pelvica con sonda vaginale bidimensionale circa 2-3 settimane dopo il transfer. Con la sonda transvaginale, è possibile visualizzare la camera gestazionale già alla quarta settimana di amenorrea (assenza di mestruazioni). La localizzazione del sacco gestazionale all’interno dell’utero è di vitale importanza per escludere la presenza di una gravidanza ectopica o extrauterina, una condizione in cui l'embrione si impianta al di fuori dell'utero.
Durante questo periodo di attesa, la maggior parte degli specialisti raccomanda di continuare con la routine quotidiana e di evitare di focalizzare eccessivamente i pensieri sull'esito del trattamento. Affrontare questa fase con serenità è importante, ricordando che stare a letto giorni e giorni dopo il trattamento non ha alcun valore nell'instaurarsi o meno di una gravidanza.
tags: #icsi #fase #preparatoria