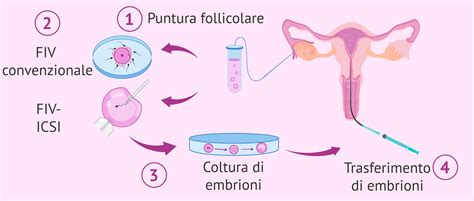
Il percorso verso la genitorialità tramite la fecondazione in vitro (FIVET) è un processo complesso che richiede una precisa sincronizzazione tra la biologia dei gameti e la tecnologia di laboratorio. Nella FIVET convenzionale, gli ovuli e gli spermatozoi vengono avvicinati tra loro affinché, in modo “naturale”, uno spermatozoo penetri all’interno dell’ovulo per fecondarlo. Si tratta di un processo alquanto fisiologico, ma non sempre è possibile realizzarlo, solitamente a causa di problemi legati alla qualità del seme o degli ovuli.
In questi casi, la medicina riproduttiva ricorre alla ICSI (iniezione intracitoplasmatica dello spermatozoo), che consiste nell’inserire uno spermatozoo previamente selezionato all’interno di un ovulo maturo mediante una micro-pipetta. Questo metodo viene scelto quando la qualità dei gameti non è quella desiderata, tuttavia, la realizzazione dei processi citati non garantisce la fecondazione in tutti i casi.
Anomalie nel processo di fecondazione
Anche quando il numero di ovuli prelevati è elevato, il risultato finale può essere frustrante. Possono verificarsi fecondazioni anomale, come quando si osserva la presenza di un solo pronucleo, oppure tre o più, anziché i due previsti (uno materno e uno paterno). Esistono inoltre casi, definiti "fallimento totale di fertilizzazione", in cui si giunge a ovuli non fecondati in cui non vi sono pronuclei visibili.
È fondamentale distinguere tra la quantità di follicoli prodotti e la qualità intrinseca dei gameti. La bassa risposta alla stimolazione ovarica, intesa come una scarsa raccolta di ovuli maturi dopo la puntura follicolare, è un problema che si verifica nel 7-24% delle pazienti. Tuttavia, il problema opposto - una buona produzione di follicoli che tuttavia non si fecondano - solleva quesiti differenti che spaziano dalla genetica alla dinamica di laboratorio.
Il ruolo della maturazione ovocitaria
Ottenere un ovocito maturo per la fecondazione è un passo necessario per l’inizio del processo riproduttivo. Normalmente, l’85% degli ovociti recuperati dopo un ciclo di stimolazione ovarica sono maturi e idonei al trattamento ICSI. Il restante 15% è immaturo e solitamente viene scartato, a meno che il centro non offra la tecnica IVM (maturazione in vitro).
Le cause della presenza di ovuli immaturi possono essere varie:
- Risposta non ottimale al picco di ormone luteinizzante (LH), fondamentale per il completamento della maturazione nucleare.
- Protocolli di stimolazione non adeguati al profilo endocrino della paziente.
- Età biologica, che influisce sulla competenza citoplasmatica dell'ovulo.
Un ovulo immaturo non è adatto alla fecondazione perché la sua dotazione cromosomica non è ancora pronta, rendendo necessaria una valutazione attenta del timing del prelievo (pick-up).
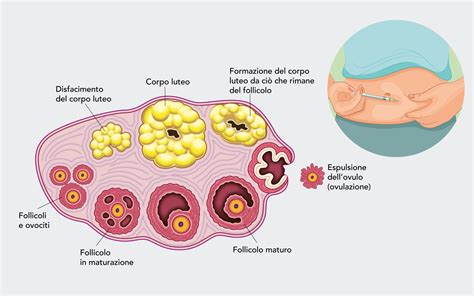
Follicologenesi - processo di maturazione dei follicoli (A cura di Prof.C.Manna)
Fattori predittivi e diagnosi della riserva ovarica
Per comprendere perché un ciclo non produca embrioni nonostante un numero apparentemente adeguato di ovociti, i medici valutano diversi biomarcatori:
- Ormone Antimulleriano (AMH): Livelli inferiori a 1 ng/ml indicano una riserva ridotta.
- FSH Basale: Valori superiori a 10 mUI/ml non solo prevedono una risposta quantitativamente bassa, ma suggeriscono spesso una qualità ovocitaria inferiore, che diminuisce il tasso di gravidanza.
- Ecografia transvaginale: Il conteggio dei follicoli antrali (AFC) permette di osservare quanti follicoli sono disponibili all'inizio del ciclo.
È importante chiarire che "riserva ovarica bassa" e "risposta ovarica bassa" non sono la stessa cosa. La riserva si riferisce al potenziale totale di ovuli disponibili in quel momento, mentre la risposta indica come l'ovaio reagisce effettivamente alla stimolazione farmacologica.
Strategie per superare il mancato sviluppo embrionale
Quando una coppia si trova di fronte a un ciclo con mancata fecondazione, lo shock emotivo è significativo. Le cliniche tendono a consigliare un approccio personalizzato:
- Accumulo di ovociti (Vitrificazione): Invece di tentare la fecondazione con un numero limitato di ovociti prodotti in un unico ciclo, si procede al congelamento degli ovuli ottenuti in più cicli successivi, aumentandone la disponibilità numerica per una singola procedura di inseminazione.
- Modifica del protocollo di stimolazione: Il protocollo "flare-up" con agonisti del GnRH, ad esempio, evita la soppressione ovarica profonda e può migliorare la qualità di reclutamento in soggetti che rispondono poco o in modo disomogeneo.
- Approfondimenti sul fattore maschile: Anche se lo spermiogramma appare normale, possono esserci danni nel DNA spermatico (frammentazione) che impediscono la corretta attivazione dell'ovulo dopo l'iniezione.
L'impatto della qualità ovocitaria e dei protocolli
Non esistono misure dirette che una donna possa adottare per migliorare istantaneamente il tasso di maturazione degli ovociti, poiché la maggior parte del processo è guidato dall'equilibrio ormonale esogeno ed endogeno. Tuttavia, l'uso di farmaci adiuvanti come il clomifene citrato può, in casi selezionati, favorire una crescita follicolare più stabile e progressiva, riducendo la necessità di dosaggi massicci di gonadotropine.
Per le donne che hanno superato i 40-42 anni, la qualità ovocitaria è il fattore limitante principale. La donazione di ovuli diventa, in molti contesti clinici, l'alternativa con il tasso di successo più elevato, poiché permette di utilizzare il potenziale genetico di donatrici giovani in cui il tasso di fecondazione e la qualità embrionale sono statisticamente ottimali.
È essenziale che le pazienti comprendano che il fallimento di un ciclo, anche con un numero elevato di ovociti, non è sempre indicativo di una sterilità irreversibile. Spesso, il passaggio da protocolli standardizzati a protocolli di stimolazione altamente personalizzati, o l'analisi dei tempi di maturazione, permette di identificare le criticità che hanno impedito il corretto sviluppo embrionale nel tentativo precedente.