Introduzione: Il Viaggio della Vita e il Ruolo della Genetica
Il miracolo della vita ha inizio con la fusione di due cellule specializzate, l'ovulo e lo spermatozoo, che portano con sé il progetto ereditario di un nuovo individuo. I geni sono manuali di istruzioni che si trovano all’interno delle nostre cellule: sono costituiti da DNA e disposti in lunghe strutture chiamate cromosomi. Ogni cellula del nostro corpo ha 46 cromosomi, tranne gli ovuli e gli spermatozoi, che ne hanno 23. Quindi, quando si uniscono per dare vita a un nuovo essere, viene creata una prima cellula contenente 46 cromosomi: 23 ereditati dalla madre e 23, dal padre. Le informazioni genetiche che ereditiamo dai nostri genitori determinano alcune delle nostre caratteristiche fisiche, come il colore degli occhi, della pelle e l'altezza, ma le informazioni contenute nei geni ci permettono anche di svolgere funzioni essenziali per il corretto sviluppo e funzionamento del nostro organismo. Per questo motivo, qualsiasi anomalia genetica può causare problemi di salute o funzionali, sia fisici che mentali.
Le indagini prenatali permettono di individuare precocemente malattie che possono essere causate da anomalie del DNA, da alterazioni dei cromosomi, da malattie infettive contratte in gravidanza, come la rosolia o la toxoplasmosi, dall’assunzione di farmaci che possono indurre malformazioni fetali e da altre cause, tra cui alcune curabili in utero prima della nascita. I principali obiettivi della diagnosi prenatale consistono nel fornire informazioni a tutte le coppie e, in caso di rischio elevato di malattie congenite, nell’informarle dell’esistenza di un test mirato per l’accertamento della presenza di specifiche anomalie. Consente, inoltre, di identificare alcune malattie che interessano il feto e, quando possibile, di instaurare una cura farmacologica o chirurgica prima della nascita. Tutte le indagini prenatali disponibili, che includono ecografie, test non invasivi e test invasivi, permettono di identificare solo alcune malattie o condizioni patologiche ed è importante che ogni coppia scelga con consapevolezza se sottoporvisi, o meno. Offrire alla coppia un colloquio con un genetista che permetta loro di effettuare una scelta informata e consapevole è parte integrante della diagnosi prenatale, configurandosi come una fondamentale consulenza genetica. È, inoltre, essenziale instaurare un rapporto medico-paziente trasparente ed etico, garantendo che non ci sia alcun obbligo di ricorrere a tali tecniche diagnostiche se non lo si desidera.
L'Età Materna Avanzata: Un Fattore Predominante nel Rischio di Anomalie Cromosomiche
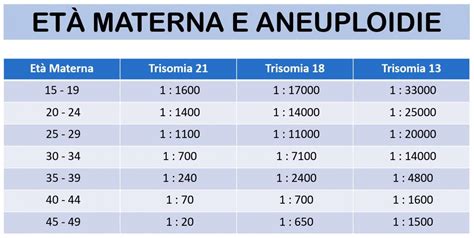
Una delle cause più frequenti di anomalie genetiche è il ritardo della maternità. Con il passare degli anni, infatti, gli ovuli perdono qualità e possono presentare alterazioni genetiche, rendendo più probabile che durante il processo di divisione cellulare e sviluppo dell’embrione si verifichino errori. L’età materna avanzata è l’indicazione più frequente allo studio citogenetico prenatale. Anche se le anomalie cromosomiche si verificano nella prole di madri di ogni età, la frequenza di figli affetti da trisomia aumenta con l’età, e in maniera esponenziale dopo i 35 anni. Questa correlazione è ben documentata e rappresenta un punto cruciale nella valutazione del rischio in gravidanza. Per esempio, la sindrome di Down è un evento casuale che può verificarsi nella gravidanza di ogni donna, ma esiste in ogni caso un rischio generico legato all'età della madre: tanto più avanzata è l'età materna quanto maggiore è il rischio di concepire un bambino affetto da sindrome di Down.
La prevalenza delle anomalie cromosomiche è del 30% più alta nei feti a 16-18 settimane di gestazione, riferita all'età mestruale, rispetto ai bambini nati vivi. Questo dato è da ricondurre all'elevata incidenza di aborti spontanei, che spesso eliminano embrioni e feti con gravi anomalie cromosomiche incompatibili con la vita. In base a questa semplice osservazione, già dal 1972 si iniziò a proporre l'analisi del cariotipo fetale alle donne di età superiore a 35 anni, ritenute arbitrariamente “a rischio”, poiché i primi dati sul reale rischio di sindrome di Down in base all'età materna vennero pubblicati solo alla fine del 1984. È stato poi osservato che le gravide di età superiore a 35 anni costituiscono solo il 6-8% della popolazione ostetrica generale e partoriscono non più del 25-30% dei bambini con sindrome di Down. Questo indica che, sebbene l'età sia un fattore importante, non è l'unico parametro e la maggior parte dei bambini con sindrome di Down nasce da madri più giovani. Per questo motivo, la diagnosi prenatale deve essere offerta a tutte le donne che avranno 35 anni di età al momento del parto, garantendo un approccio universale al rischio.
Comprendere i Fondamenti: Geni, Cromosomi e le Loro Anomalie
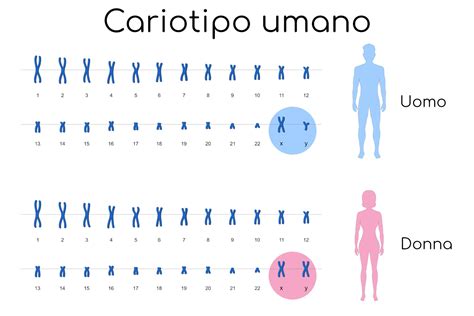
Per comprendere appieno le implicazioni dell'età materna avanzata, è fondamentale conoscere cosa sono i cromosomi e come le loro alterazioni possono manifestarsi. I cromosomi sono strutture filiformi presenti nel nucleo delle cellule, responsabili della trasmissione dei caratteri ereditari e del controllo della crescita e della differenziazione dell'organismo. Il corredo cromosomico di un individuo è l'insieme dei cromosomi presente nelle cellule.
Le anomalie cromosomiche rappresentano una delle principali preoccupazioni durante la gravidanza, poiché possono influire significativamente sulla salute e sullo sviluppo del feto. Le anomalie cromosomiche si dividono in due principali categorie: anomalie numeriche e anomalie strutturali.
Anomalie Numeriche: Le Aneuploidie
Le anomalie numeriche si verificano quando c’è un numero anomalo di cromosomi rispetto al corredo cromosomico normale, che nell'uomo è di 46. CHE COSA SONO LE ANEUPLOIDIE? Le aneuploidie sono alterazioni del numero di cromosomi, caratterizzate dalla presenza di un cromosoma in più o in meno rispetto al corredo cromosomico normale (invece di due copie per ogni coppia di cromosomi omologhi). Le più comuni sono la monosomia e la trisomia completa. Possono anche esserci alterazioni numeriche che riguardano la copia di singoli segmenti di cromosoma.
Tra le aneuploidie più note troviamo:
- Sindrome di Down (Trisomia 21): È uno degli esempi più noti e la più comune anomalia cromosomica numerica, causata dalla presenza di una copia extra del cromosoma 21. Cioè, invece di due come sarebbe corretto (uno dal padre e uno dalla madre), ce ne sono tre. Per questo motivo, questa alterazione viene chiamata trisomia.
- Sindrome di Edwards (Trisomia 18): Una grave condizione dovuta a un cromosoma 18 in più. I neonati affetti presentano gravi ritardi nello sviluppo mentale e fisico e spesso malformazioni congenite multiple. Si associa ad una elevata abortività.
- Sindrome di Patau (Trisomia 13): Causata da un cromosoma 13 in più, comporta gravi disabilità fisiche e mentali, inclusi difetti cardiaci, anomalie cerebrali e malformazioni facciali. Si associa anch'essa ad elevata abortività.
Esistono anche anomalie che coinvolgono i cromosomi sessuali (X e Y):
- Sindrome di Turner (Monosomia X): Colpisce solo le femmine ed è dovuta all’assenza parziale o totale di uno dei due cromosomi X, risultando in un corredo 45,X. La monosomia del cromosoma X è associata alla sindrome di Turner.
- Sindrome di Klinefelter (Trisomia XXY): Colpisce i maschi che possiedono un cromosoma X extra, con un corredo 47,XXY.
- Trisomia X (Sindrome della tripla X): Le femmine con Trisomia X hanno un cromosoma X in più (47,XXX).
- Sindrome di Jacobs: I maschi con Sindrome di Jacobs hanno un cromosoma Y in più (47,XYY). Questa condizione è generalmente meno evidente rispetto ad altre anomalie cromosomiche e molti individui vivono senza sintomi evidenti.
Anomalie Strutturali
Oltre alle alterazioni numeriche, piccoli segmenti di uno o più cromosomi possono essere cancellati (delezioni), duplicati (duplicazioni), invertiti (inversioni), scambiati con parte di un altro cromosoma (traslocazioni) oppure la loro posizione normale può essere alterata. Queste anomalie strutturali coinvolgono cambiamenti nella struttura di uno o più cromosomi. Si verificano quando il materiale genetico viene scambiato tra i cromosomi senza perdita o guadagno di informazioni genetiche, oppure quando si verificano perdite o guadagni netti. Le anomalie strutturali possono essere ulteriormente suddivise in bilanciate e non bilanciate.
I riarrangiamenti bilanciati parentali includono le traslocazioni (robertsoniane o reciproche) e le inversioni (paracentriche o pericentriche). Le persone con un riarrangiamento cromosomico bilanciato sono, di solito, fenotipicamente normali, poiché non vi è una perdita o un guadagno netto di materiale genetico. Tuttavia, esse possono avere una più alta probabilità di generare figli affetti da patologie cromosomiche. Le traslocazioni sono alterazioni della struttura dei cromosomi derivanti da uno scambio di porzioni di cromosomi non omologhi. La traslocazione è detta bilanciata se lo scambio non comporta la perdita o il guadagno di materiale genetico.
Un tipo specifico e clinicamente rilevante è la Traslocazione Robertsoniana. Una traslocazione robertsoniana consiste nella fusione di due cromosomi acrocentrici, ovvero cromosomi in cui il centromero è situato molto vicino alla parte terminale del cromosoma. Questi due cromosomi si rompono ambedue in corrispondenza del centromero, ma su lati opposti. Per unione dei frammenti rotti si forma un nuovo cromosoma costituito dalle braccia lunghe dei due elementi originali, e un piccolo cromosoma costituito dalle due braccia corte, che di solito viene perduto. In seguito a questa anomalia, che non ha conseguenze fenotipiche probabilmente perché il materiale perduto è geneticamente inerte, il corredo cromosomico dell’individuo viene ridotto di un’unità (45 cromosomi anziché 46). Le traslocazioni robertsoniane possono coinvolgere tutte le combinazioni possibili di cromosomi acrocentrici (nell’uomo, sono i cromosomi 13, 14, 15, 21 e 22), ma il tipo più comune coinvolge i cromosomi 13 e 14, e viene rilevata con una frequenza di circa 1 su 1300 nati. Come per le altre traslocazioni, i portatori di una traslocazione robertsoniana possiedono un fenotipo normale, ma hanno una più alta probabilità di generare figli affetti da patologie cromosomiche, spesso correlate a trisomie specifiche, come la Sindrome di Down da traslocazione.
Oltre l'Età Materna: Altri Fattori di Rischio e Implicazioni Genetiche
Le anomalie cromosomiche non sono esclusivamente legate all'età materna avanzata, ma possono essere influenzate da una varietà di fattori genetici e ambientali. Queste alterazioni cromosomiche si possono verificare spontaneamente quando si forma un nuovo feto, oppure possono essere ereditate e trasmesse dai genitori alla prole.
Fattori Genetici Ereditari
In alcuni casi, le anomalie cromosomiche possono essere ereditate. Un’anomalia cromosomica nei genitori aumenta il rischio di avere un bambino con anomalie cromosomiche. Le persone con un riarrangiamento cromosomico bilanciato, come traslocazioni o inversioni, sono di solito fenotipicamente normali. Tuttavia, la presenza di tali anomalie nei genitori deve portare a una consulenza genetica e si deve prendere in considerazione lo studio prenatale, data l'aumentata probabilità di concepire un figlio con un riarrangiamento sbilanciato. Teoricamente, il 50% dei figli di un genitore con aneuploidia è aneuploide. Ad esempio, un terzo dei figli di donne affette da una trisomia 21 è trisomico, anche se gli uomini con trisomia 21 sono sterili. La trisomia di un cromosoma sessuale, come la 47,XXY, è più comune, ma è frequentemente associata a una riduzione della fertilità; pochissimi figli di genitori con trisomia dei cromosomi sessuali sono aneuploidi.
Le anomalie cromosomiche in un precedente figlio sono un'indicazione alla diagnosi prenatale nelle gravidanze successive. Se una coppia ha avuto un figlio nato vivo affetto da trisomia 21 e la donna avrà meno di 30 anni al momento del parto, il rischio di avere un altro figlio trisomico è di circa l’1%. Queste cifre presuppongono che i genitori non siano portatori di una traslocazione robertsoniana. Per le altre trisomie le informazioni sono limitate, ma il rischio di avere un altro figlio con anomalie cromosomiche sembra essere aumentato a circa l’1%.
Problemi di Fertilità e Aborti Ricorrenti
Le alterazioni cromosomiche possono anche causare problemi di fertilità, dato che la natura stessa, quando rileva l’errore, a volte impedisce o interrompe lo sviluppo di una gravidanza. Per questo motivo, il fatto di subire diversi aborti spontanei - chiamati aborti di ripetizione - o di accumulare diversi tentativi falliti di trattamenti di riproduzione assistita, può essere un motivo di sospetto, sia nel caso delle donne che degli uomini, o di entrambi. In questi casi, si raccomanda ai genitori di fare un cariotipo per identificare eventuali anomalie cromosomiche che potrebbero essere alla base dei problemi riproduttivi. Le traslocazioni, in particolare, costituiscono uno dei più frequenti riscontri nei pazienti con difficoltà riproduttiva.
Gli aborti spontanei ricorrenti possono indicare un’anomalia cromosomica. Se l’aborto iniziale è causato da un’aneuploidia, gli aborti successivi sono con più facilità causati anch’essi da una aneuploidia, sebbene non necessariamente dello stesso cromosoma. Una trisomia, ad esempio la trisomia 16, in una gravidanza può essere letale e causare un aborto, ma nelle gravidanze successive un’altra trisomia, come la trisomia 18, può causare la nascita di un feto vivo con anomalie cromosomiche e fenotipiche. Tuttavia, non è del tutto chiaro se l’aneuploidia in un feto abortito spontaneamente aumenti significativamente il rischio di avere un futuro bambino nato vivo con aneuploidia.
Fattori Ambientali e Mutazioni Geniche
Oltre ai fattori genetici ereditari, l'esposizione a sostanze tossiche, come radiazioni, sostanze chimiche o infezioni durante la gravidanza, possono aumentare il rischio di anomalie cromosomiche o genetiche. Queste possono essere classificate come anomalie infettive, iatrogene (causate da farmaci o trattamenti medici) o ambientali.
Esistono anche malattie causate da mutazioni nei geni, come nel caso delle cosiddette “malattie autosomiche recessive”. Queste malattie sono così chiamate perché si manifestano solo quando il padre e la madre presentano una mutazione nello stesso gene ed entrambi la trasmettono ai figli. Per questo motivo, nei trattamenti di riproduzione assistita, a tutte le persone che devono ricorrere alla donazione di ovuli o di sperma viene consigliato di sottoporsi a un test genetico preconcepimento. L’obiettivo è scoprire se sono portatrici di qualche alterazione genetica, in modo da selezionare un donatore o una donatrice geneticamente “compatibile” con loro per ridurre il rischio di trasmettere questo tipo di malattia alla loro prole. Presso centri specializzati, sono disponibili test specifici per questo scopo, come il qCarrier, che è in grado di individuare circa 300 malattie ereditarie associate ad alterazioni genetiche.
La Diagnosi Prenatale: Un Percorso di Informazione e Scelta Consapevole
La diagnosi prenatale rappresenta un insieme di procedure e test volti a monitorare la salute del feto durante la gravidanza, identificando precocemente la presenza di anomalie cromosomiche, genetiche o malformazioni. È un percorso che richiede una profonda riflessione e una scelta consapevole da parte della coppia. I principali obiettivi della diagnosi prenatale consistono nel fornire informazioni a tutte le coppie e, in caso di rischio elevato di malattie congenite, nell’informarle dell’esistenza di un test mirato per l’accertamento della presenza di specifiche anomalie. Inoltre, essa consente di identificare alcune malattie che interessano il feto e, quando possibile, di instaurare una cura farmacologica o chirurgica prima della nascita.
La diagnosi prenatale permette di individuare la presenza del genoma di agenti infettivi, come Rubeovirus o HIV, e offre la possibilità di accertamenti citogenetici e la presenza di alcune delle patologie del feto, siano esse di origine cromosomica, genetica, infettiva, iatrogena o ambientale. È fondamentale sottolineare che tutte le indagini prenatali disponibili, comprese ecografie, test non invasivi e test invasivi, permettono di identificare solo alcune malattie o condizioni patologiche. Per questo motivo, è di vitale importanza che ogni coppia scelga con consapevolezza se sottoporsi, o meno, a tali test. La consulenza genetica, che include un colloquio approfondito con uno specialista, è parte integrante di questo processo decisionale, permettendo alla coppia di effettuare una scelta informata e consapevole.
Indicazioni per la Diagnosi Prenatale
Oltre all'età materna avanzata, che rimane l’indicazione più frequente allo studio citogenetico prenatale e per cui la diagnosi prenatale deve essere offerta a tutte le donne che avranno 35 anni di età al momento del parto, esistono altre condizioni che possono indicare la necessità di un'indagine approfondita:
- Anomalie cromosomiche in un precedente figlio: La nascita di un figlio con un'anomalia cromosomica rappresenta un fattore di rischio significativo per le gravidanze successive, come discusso in precedenza. Anche la presenza di un'anomalia cromosomica nei genitori o in uno dei parenti stretti costituisce un'indicazione.
- Risultati anomali dei test di screening: Se i test di screening non invasivi, come il test combinato o il NIPT, indicano un rischio elevato di anomalie cromosomiche, viene solitamente raccomandato un test diagnostico invasivo per conferma.
- Presenza di fattori di rischio parentali: I genitori portatori di riarrangiamenti cromosomici bilanciati, come traslocazioni robertsoniane o reciproche, hanno un rischio aumentato di concepire feti con anomalie cromosomiche sbilanciate.
- Anomalie riscontrate all'ecografia: La scoperta di malformazioni o marcatori di rischio ecografici durante gli esami di routine può indirizzare verso ulteriori accertamenti.
Le Metodologie di Screening Non Invasive: Sicurezza e Valutazione del Rischio
I test di screening non invasivi sono una parte fondamentale della diagnosi prenatale. Sono sicuri al 100% per il feto oltre che per la donna, ma forniscono solo una stima del rischio della presenza di alcune anomalie cromosomiche, in particolare la trisomia 21 (sindrome di Down), la 13 o la 18 e, eventualmente, anomalie dei cromosomi sessuali. Non sono diagnostici, ma selezionano le gravidanze a rischio elevato che potrebbero beneficiare di test invasivi.
Ecografia
L'ecografia è una tecnica fondamentale che permette di controllare e seguire lo sviluppo dell’embrione e del feto. È la tecnica più usata perché si basa sugli ultrasuoni che, ad oggi, non hanno dimostrato effetti nocivi sul feto. Viene impiegata per valutare l’anatomia del feto ed escludere malformazioni identificabili mediante questo esame. Inoltre, è impiegata per guidare i prelievi eseguiti durante le indagini prenatali invasive. L'Ecocardiografia fetale è un esame ecografico eseguito specificamente al fine di esaminare il cuore del feto per escludere la presenza di una patologia o di una malformazione congenita. Le ecografie e le analisi biochimiche del sangue materno (es. test combinato) sono offerte gratuitamente dal Servizio Sanitario Nazionale.
Plica Nucale (Translucenza Nucale) e Test Combinato
La plica nucale si effettua tramite ecografia e consta nella misurazione dello spessore esistente tra il piano muscolare e la cute del collo del feto, che risulta ispessita nel 70-80% dei bambini Down. Il test combinato prevede anche l’esecuzione di una ecografia per valutare lo spessore della cosiddetta plica retro-nucale del feto che, insieme ai risultati dell’esame del sangue, permette di stimare il rischio di alcune anomalie cromosomiche. Il Test Combinato include quindi un’ecografia per misurare la translucenza nucale del feto e un esame del sangue materno (spesso chiamato Bi-test) per analizzare i livelli di specifiche proteine e ormoni (betaHCG, PAPP-A) che risultano alterate nell'80% dei bambini Down.
Da un paio di anni si sta cercando di mettere a punto uno screening di tipo ecografico più raffinato, applicabile però al primo trimestre di gravidanza. L'idea è nata dopo che nel 1989 Rottem aveva riportato di un feto con trisomia 21 che a 11 settimane di gravidanza presentava un igroma nucale cistico, risoltosi poi a 15 settimane. Da allora, numerosi studi ecografici hanno dimostrato un'elevata associazione tra anomalie cromosomiche ed il riscontro nel primo trimestre di gravidanza di un accumulo di fluido a livello della nuca del feto, tra il piano muscolare e la cute. È importante sottolineare che una plica nucale di spessore aumentato, generalmente non evolve verso un edema nucale o un igroma cistico nel secondo trimestre, ma solitamente si risolve, rendendosi così non più valutabile nel 2° e 3° trimestre di gravidanza. In base ad alcuni studi anatomopatologici sembra che la causa principale della comparsa della plica nucale sia imputabile ad anomalie cardiache, in particolare a difetti del setto atrioventricolare o della parte perimembranosa del setto interventricolare, che spesso si risolvono in utero o durante il primo anno di vita. In letteratura sono ormai stati pubblicati numerosi studi sulla valutazione dello spessore della plica nucale nel 1° trimestre di gravidanza e l'associazione con le cromosomopatie. Attualmente sono pochi i centri specializzati nel campo della diagnosi prenatale che possono disporre di casistiche sufficientemente ampie da poter proporre e applicare clinicamente questa metodica; in molti altri centri invece lo screening è proposto e applicato in via sperimentale. L'obiettivo di questi protocolli è identificare i feti che mostrando una plica nucale superiore a un certo cut-off (ad esempio, 3 mm), vengono ritenuti genericamente a rischio, anche se non si possono ancora calcolare dati sufficienti per ogni gravida il rischio specifico per cromosomopatia.
Non-Invasive Prenatal Test (NIPT) o Test del DNA Fetale Libero
Il test prenatale non invasivo, o NIPT, si basa sulla scoperta scientifica di D. Lo che nel 1997 individuò, per la prima volta, la presenza del DNA di origine fetale libero nel plasma materno. Il NIPT è un test di screening non invasivo che analizza frammenti di DNA fetale presenti nel sangue materno. Fornisce informazioni su possibili anomalie cromosomiche ed offre la possibilità di analizzare il DNA libero del feto, presente nel sangue materno già dalla 10° settimana di gravidanza. Questa metodologia rappresenta un progresso significativo, offrendo un'elevata sensibilità e specificità per le trisomie più comuni.
Tri-Test e Test Integrato
Nel secondo trimestre di gravidanza, tra la 15° e la 18° settimana, si può effettuare un altro test di screening che si chiama tri-test. Questo consiste in un prelievo di sangue materno per la misurazione di tre sostanze di origine placentare: HCG, estriolo non coniugato e alfafetoproteina. Attualmente il metodo di screening più utilizzato è di tipo biochimico: un prelievo di sangue materno viene effettuato a 15-18 settimane di gravidanza e si analizzano tre ormoni prodotti dall'unità feto-placentare. In base a calcoli statistici, che tengono conto anche dell'età, del peso e della razza materni, viene stabilito per ogni donna il rischio specifico per quella gravidanza di avere un bambino affetto da sindrome di Down. Le gravide che hanno un rischio elevato possono accedere all'indagine citogenetica, indipendentemente dalla loro età.
Tutti e tre i test di screening (duo-test, tri-test, NIPT) sono stati messi a punto in modo tale da avere un tasso di falsi positivi contenuto. Il tritest serve a conoscere la probabilità che il bambino sia affetto da trisomia 21. Se il numero è compreso tra 1/1 e 1/250, la probabilità che il bambino sia affetto da Trisomia 21 è considerata elevata. Se il numero è superiore a 250, la probabilità è considerata bassa. Come si interpreta il risultato del tritest? Un risultato di bassa probabilità non esclude completamente la trisomia 21 e le malformazioni fetali; alcuni casi non sono evidenziati, poiché un test di probabilità non può mai fare una diagnosi. Allo stesso modo, un risultato di alta probabilità non significa che il bambino è affetto da trisomia 21 o da malformazioni, ma indica la necessità di ulteriori accertamenti. Quali sono gli esami ulteriori da eseguire? Se la probabilità per la trisomia 21 è elevata, l'esame diagnostico indicato è l'amniocentesi. Poiché considerando l'età materna come unico fattore di rischio si riesce a individuare solo il 30% dei feti Down, si è posta l'esigenza di identificare dei tests di screening a cui sottoporre la popolazione ostetrica generale, capaci di evidenziare un gruppo di gravide “a rischio”, da poter così indirizzare verso la diagnosi prenatale invasiva.
Screening prenatale delle malattie cromosomiche, i parametri ecografici
Le Metodologie Diagnostiche Invasive: Accertamento e Rischi Connessi
A differenza dei test di screening, i test invasivi permettono di accertare la presenza di anomalie legate al DNA e ai cromosomi e per questo sono detti test diagnostici. L'unico modo per escludere con certezza un'anomalia cromosomica è quello di sottoporsi a esami invasivi, come la villocentesi o l'amniocentesi, che comportano, tuttavia, un rischio di aborto. L'unico mezzo diagnostico disponibile è l'analisi del cariotipo fetale, che si esegue su cellule fetali che possono provenire da liquido amniotico, tessuto placentare e sangue fetale. Le tecniche di prelievo di tali materiali (rispettivamente amniocentesi, villocentesi e cordocentesi) sono ovviamente invasive e comportano un rischio di perdita fetale che varia dall'1 al 3% a seconda della metodica impiegata e dall'esperienza dell'operatore.
Villocentesi
La Villocentesi è una procedura invasiva che consiste nel prelievo di un piccolo campione di villi coriali, ovvero tessuto placentare. Viene eseguita tra la 10° e la 13° settimana di gravidanza. Le principali indicazioni per la villocentesi includono l'età materna avanzata (generalmente considerata superiore ai 35 anni al momento dell’indagine invasiva) e la presenza di anomalie cromosomiche in un precedente figlio, o se i genitori o uno dei parenti stretti ne è affetto.
Amniocentesi
L’Amniocentesi è una procedura che implica il prelievo di una piccola quantità di liquido amniotico, il fluido che circonda il feto nell'utero. Viene eseguita tra la 14° e la 20° settimana di gravidanza. È l'esame diagnostico raccomandato se la probabilità per la trisomia 21 è elevata a seguito dei test di screening. Anche in questo caso, le indicazioni sono simili a quelle della villocentesi, focalizzate sulla necessità di una diagnosi certa in presenza di rischio elevato.
Cordocentesi
La Cordocentesi è una tecnica di prelievo di sangue fetale direttamente dal cordone ombelicale. È una procedura più rara e viene generalmente riservata a casi specifici, spesso quando è necessario ottenere informazioni più rapidamente o quando altre metodiche non sono state conclusive o non erano applicabili. Le informazioni ottenute dalla cordocentesi possono includere un cariotipo, analisi di infezioni o condizioni ematologiche fetali.
Distinguere le Anomalie: Cromosomiche, Congenite e Multifattoriali
È importante distinguere tra anomalie cromosomiche, anomalie congenite e disturbi multifattoriali, poiché le loro cause, i rischi e le implicazioni possono variare. Le anomalie cromosomiche sono quelle direttamente legate a un'alterazione nel numero o nella struttura dei cromosomi. Le anomalie congenite, invece, si intendono come malattie o disordini presenti fin dalla nascita e possono avere diverse origini.
Anomalie Congenite e l'Età Materna: Un Recente Studio
Secondo un recente studio, se la gravidanza inizia dopo i 35 anni, il bambino ha un rischio minore di sviluppare anomalie congenite ma non cromosomiche. Gli esperti hanno sempre sostenuto che più una gravidanza è tardiva, maggiori sono i rischi di malattie e anomalie a carico del feto. Ora un nuovo studio sembra ribaltare queste convinzioni, almeno in parte. Secondo un gruppo di ricercatori americani, della Washington University in St. Louis School of Medicine, infatti, le donne che diventano mamme dopo i 35 anni hanno meno probabilità di avere figli con malformazioni congenite maggiori.
Alla base delle anomalie congenite possono esserci alterazioni genetiche, ma non necessariamente. Anche l’esposizione ad agenti fisici e chimici, il consumo di alcol e droghe, errori durante il processo di sviluppo dell’embrione o di crescita del feto, malattie materne e problemi nelle fasi finali del parto possono avere un ruolo importante. Lo studio negli Stati Uniti ha riguardato 76 mila donne americane nel secondo trimestre di gravidanza. Tutte sono state invitate a rispondere a dei questionari sulla gestazione, in particolare sull’età in cui sono rimaste incinta. Inoltre, tutte sono state sottoposte ad alcuni esami per verificare lo stato di salute dei feti. Incrociando i dati, è emersa un’associazione fra rischio di anomalie del feto ed età della mamma al momento della gravidanza. In particolare, si è visto che le donne con più di 35 anni avevano il 40% in meno di probabilità di avere bimbi affetti da importanti malformazioni congenite, soprattutto del cervello, dei reni e delle pareti addominali.
Tuttavia, è fondamentale ribadire che resta alto il rischio per le anomalie cromosomiche. Gli autori hanno spiegato che l’età materna avanzata comporta un maggior rischio di anomalie cromosomiche a carico del bambino, come quelle responsabili della sindrome di Down. Ad oggi non era dimostrato, invece, se vi fosse un’associazione fra gravidanza tardiva e malformazioni congenite. Ebbene, questo studio esclude una qualsiasi correlazione. Anzi, più la donna aspetta e più i figli sembrano protetti da questo punto di vista per quanto riguarda le malformazioni congenite non cromosomiche. Questo può rassicurare tutte quelle donne che aspirano a diventare mamme quando hanno più di 35 anni, pur mantenendo l'attenzione sul rischio cromosomico.
Disturbi Poligenici o Multifattoriali
I disturbi poligenici o multifattoriali, più frequentemente identificati prima della nascita, sono i difetti della cresta neurale; negli USA la loro incidenza è di 1-2 casi ogni 1000 nascite. La maggior parte dei difetti del tubo neurale, come la spina bifida o l'anencefalia, viene ereditata come affezioni poligeniche/multifattoriali. Alcuni possono essere conseguenza dell’alterazione di un singolo gene, di anomalie cromosomiche o di agenti teratogeni (es., l’acido valproico). Quando il soggetto valutato ha un difetto del tubo neurale, il rischio per i figli dei parenti di primo grado (germani, genitori, figli) è pari all’1%-2%. Per i figli dei parenti di secondo grado (zii, nipoti) il rischio è inferiore all’1%. Per i figli dei parenti di terzo grado il rischio è solo leggermente superiore a quello della popolazione generale. Il rischio nelle gravidanze successive può essere ridotto con la somministrazione di folati, 4 mg/die per 1 mese prima e fino al 3˚ mese dopo il concepimento.
Per altre anomalie, come i difetti cardiaci congeniti, la schisi labiale e del palato, la stenosi pilorica, o la lussazione congenita dell’anca, il rischio di ricorrenza si accorda con l’ereditarietà poligenica/multifattoriale. La diagnosi prenatale può essere disponibile in alcuni casi, in particolare con l’ecografia ad alta risoluzione, rendendo ottimale il trattamento prima del parto e possibile l’immediata cura neonatale.
Approcci e Opzioni in Caso di Rischio o Diagnosi Accertata
Se viene confermato che c’è effettivamente un problema di origine genetica che può influire sulla salute del futuro bambino o causare problemi di fertilità, esistono diverse strade da percorrere. È fondamentale chiedere una consulenza personalizzata a uno specialista di genetica, in modo che possa valutare quale sia l’opzione migliore per la coppia.
In caso di gravidanza spontanea e un rischio elevato o una diagnosi preliminare di anomalie, è consigliabile effettuare un test di diagnosi prenatale mediante biopsia corionica o amniocentesi, per confermare o escludere la presenza di alterazioni genetiche nel bebè. Queste procedure forniscono una diagnosi certa, essenziale per la pianificazione futura.
Un'altra opzione, specialmente per le coppie con problemi di fertilità o con un rischio genetico noto, è optare per la fecondazione in vitro (Fivet) e applicare la tecnica della Diagnosi Genetica Preimpianto (DGP). Questa tecnica permette di studiare le caratteristiche genetiche degli embrioni prima del loro trasferimento nell’utero della madre, per selezionare solo quelli sani e non portatori di alterazioni. La DGP offre la possibilità di ridurre significativamente il rischio di trasmettere malattie genetiche note alla prole.
In situazioni in cui entrambi i partner sono portatori di alterazioni genetiche significative o di determinate malattie autosomiche recessive, un’altra opzione sarebbe quella di ricorrere alla riproduzione assistita utilizzando lo sperma di un donatore o gli ovuli di una donatrice che non siano portatori della stessa alterazione del/la paziente. Come si può notare, disporre di questi test e degli specialisti di genetica è essenziale in qualsiasi centro specializzato in ginecologia, ostetricia e riproduzione assistita, sia per offrire consulenze genetiche che per individuare questo tipo di anomalie.