Nel campo della riproduzione assistita, l'iniezione intracitoplasmatica di spermatozoi (ICSI) rappresenta una tecnica avanzata e spesso fondamentale, specialmente quando si affrontano problemi di infertilità maschile. È possibile che, nel caso in cui ci sia un problema di infertilità maschile nella coppia, nella clinica di riproduzione assistita si sentirà parlare di questa tecnica. L'ICSI è una delle fasi di un trattamento di fecondazione in vitro (FIVET), sebbene molte persone spesso usino il termine ICSI o FIV-ICSI per riferirsi all'intero processo di trattamento della fertilità. Questa metodologia ha trasformato le prospettive per molte coppie che, altrimenti, avrebbero incontrato significative difficoltà nel concepire.
Cos'è e Come Funziona l'ICSI: La Specificità della Microiniezione
La tecnica ICSI, abbreviazione di Iniezione Intracitoplasmatica di Spermatozoi, è una procedura di laboratorio che consente l'inserimento di un singolo spermatozoo all'interno dell'ovocita maturo. Grazie a questa tecnica, si riesce ad inseminare un ovulo attraverso una microiniezione di uno spermatozoide. Questa capacità è di fondamentale importanza nei casi in cui il campione seminale non possieda i criteri necessari per effettuare una FIVET convenzionale. La differenza sostanziale tra la FIVET normale e l'ICSI risiede proprio nel meccanismo di fecondazione. Per realizzare una FIVET convenzionale, infatti, sono necessari tra 50.000 e 100.000 spermatozoi che circondano l'ovulo, lasciando che uno di essi penetri spontaneamente. Con l'ICSI, invece, è sufficiente solo uno spermatozoide per ovulo, poiché questo viene iniettato direttamente nel citoplasma dell'ovocita, forzandone quindi l'entrata e agevolandone la fecondazione.
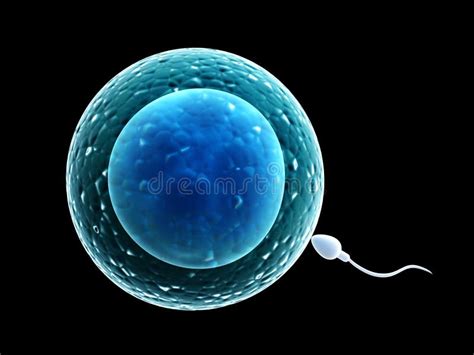
La procedura di ICSI è intrinsecamente legata all'uso di strumentazioni di alta precisione. Per l'esecuzione dell'ICSI, l'operatore si avvale di un apparato di micromanipolazione connesso a un microscopio. Questo microscopio, con un potere di ingrandimento che può arrivare a 8.000 volte - come se fosse 20 volte più potente di quelli solitamente utilizzati per eseguire ICSI (400 volte) - permette di osservare gli spermatozoi e gli ovuli con una chiarezza eccezionale. L'operatore può così far compiere ad appositi microstrumenti minimi movimenti aventi un'escursione di pochi micron o decine di micron, necessari per le operazioni di micromanipolazione.
L'iniezione intracitoplasmatica di spermatozoi è una tecnica di riproduzione assistita che viene spesso utilizzata nei trattamenti di fecondazione in vitro. Sebbene l'ICSI sia più complessa e tecnica, consente tassi di successo più elevati nei casi di infertilità maschile grave, rendendola un'opzione ideale per molti pazienti che affrontano gravi problemi di fertilità, soprattutto quando la qualità del liquido seminale è un fattore determinante.
Quando si Ricorre all'ICSI? Indicazioni Specifiche della Tecnica
L'ICSI è consigliata in una varietà di situazioni, principalmente legate a fattori di infertilità maschile, ma anche in altri contesti clinici. In molti centri di riproduzione assistita, si è osservata una tendenza ad eseguire sempre la tecnica ICSI in tutti i trattamenti di fertilità, indipendentemente dalla causa, per aumentare i tassi di successo e offrire un controllo ottimale sulla procedura di fecondazione, adattandosi alle caratteristiche specifiche di ogni campione di seme e ovulo.
Le principali indicazioni per l'ICSI includono:
- Azoospermia: Questa condizione si riferisce all'assenza di spermatozoi nel liquido seminale. In questi casi, l'ICSI consente di utilizzare spermatozoi ottenuti direttamente dal testicolo mediante tecniche come la puntura testicolare o la biopsia testicolare, anche se recuperati in numero esiguo o con scarsa mobilità. L'ICSI è essenziale anche nel caso in cui gli spermatozoi non siano presenti nel liquido seminale, ma siano recuperati, pochi e scarsamente mobili o del tutto immobili, dall'epididimo o dal testicolo.
- Oligozoospermia: Caratterizzata da una bassa concentrazione di spermatozoi. Se gli spermatozoi sono di qualità accettabile, l'ICSI consente di introdurre un solo spermatozoo in ogni ovulo, massimizzando le possibilità di fecondazione anche con un numero limitato di gameti maschili.
- Astenozoospermia: Questo disturbo comporta una ridotta motilità degli spermatozoi. In questo caso, l'ICSI facilita la fecondazione, anche quando gli spermatozoi non si muovono correttamente, poiché il movimento non è un prerequisito per l'iniezione diretta.
- Teratozoospermia: Si riferisce alla presenza di spermatozoi con morfologie anomale. L'ICSI consente di selezionare spermatozoi di buona qualità, anche se il campione generale presenta alterazioni morfologiche significative. L'operatore può scegliere lo spermatozoo con la morfologia più normale tra quelli disponibili.
- Combinazione di alterazioni nel liquido seminale: Nei casi in cui sono presenti alterazioni multiple nel liquido seminale, come l'oligoastenoteratozoospermia (una combinazione di bassa concentrazione, scarsa motilità e morfologia anomala), l'ICSI è spesso l'opzione più efficace per superare tutte queste barriere contemporaneamente.
- Fallimento di precedenti cicli di FIV convenzionale: Se una coppia ha avuto insuccessi di fecondazione con la FIV convenzionale, l'ICSI può essere adottata per aumentare le probabilità di successo.
- Uomini sottoposti a vasectomia: Anche in uomini che hanno subito una vasectomia, dove gli spermatozoi possono essere recuperati chirurgicamente ma in quantità limitate e talvolta con mobilità ridotta, l'ICSI è l'opzione preferibile.
- Malattie infettive: Nei casi di uomini con malattie infettive (come l'HIV o l'epatite) che richiedono procedure speciali di lavaggio dello sperma, l'ICSI può essere indicata.
- Trattamento oncologico pregresso: Quando è stato effettuato un trattamento oncologico (chemioterapia o radioterapia) e il liquido seminale è stato precedentemente congelato, l'ICSI è spesso utilizzata per ottimizzare l'uso del campione spermatico prezioso.
- Eiaculazione retrograda: Questa condizione, in cui gli spermatozoi sono rinvenuti nell'urina, richiede l'ICSI per utilizzare gli spermatozoi recuperati.
- Diagnosi Genetica Preimpianto (PGT): Se è prevista una diagnosi genetica preimpianto (DGP), l'ICSI è preferibile per evitare la contaminazione dell'embrione con spermatozoi estranei, che potrebbe interferire con l'analisi genetica.
Tecnica #ICSI
Il Processo ICSI: Una Guida Passo-Passo Attraverso il Trattamento
La procedura ICSI si articola in più fasi successive, che richiedono una stretta collaborazione tra ginecologo, embriologo e biologo della riproduzione. Le fasi del trattamento FIV-ICSI hanno procedure che sono completamente identiche alle parti del processo convenzionale di FIVET, con la differenza principale nel modo in cui avviene la fecondazione una volta che gli ovuli e lo sperma sono stati ottenuti in laboratorio.
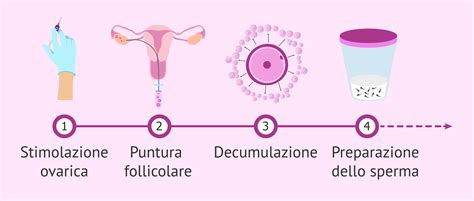
1. Stimolazione Ovarica Controllata
La stimolazione ovarica controllata è il punto di partenza del ciclo di FIV-ICSI e consiste nella somministrazione di farmaci ormonali. L'obiettivo primario di questa fase è promuovere la crescita di più follicoli ovarici in modo che diversi possano maturare contemporaneamente. In questo modo sarà possibile ottenere un numero maggiore di ovuli per fecondarli in laboratorio e aumentare le possibilità di gravidanza, diversamente da un ciclo naturale che produce generalmente un solo ovulo maturo.
Inoltre, grazie alla stimolazione ovarica, il ciclo mestruale della donna viene controllato e viene impedita l'ovulazione spontanea, che causerebbe il fallimento del ciclo FIV-ICSI. Prima di iniziare la stimolazione ovarica, è comune prescrivere la pillola anticoncezionale alle pazienti per sincronizzare il ciclo mestruale, permettendo al team medico di pianificare al meglio l'intero processo.
A seconda della durata e delle modalità di somministrazione dei farmaci, ci sono due protocolli di base nelle pazienti in FIVET:
- Protocollo Lungo: Inizia prima delle mestruazioni con gli "scatti" dei farmaci agonisti di GnRH. Questi servono a rallentare l'ipofisi e a prevenire la secrezione endogena di ormoni che potrebbero innescare un'ovulazione precoce. Una volta arrivato il ciclo mestruale (il "regolo"), le punture anteriori vengono combinate con le punture di gonadotropina per avviare lo sviluppo follicolare multiplo desiderato. Questo protocollo è stato storicamente molto utilizzato per la sua efficacia nel prevenire l'ovulazione prematura.
- Protocollo Breve: In questo protocollo, il numero di punture è ridotto. La stimolazione della gonadotropina inizia dopo l'arrivo delle mestruazioni. L'ottavo giorno del ciclo, le punture vengono avviate con gli antagonisti di GnRH per "frenare" l'ipofisi e prevenire un picco di LH (ormone luteinizzante) che potrebbe causare l'ovulazione spontanea. Negli ultimi anni si è registrata una tendenza alla semplificazione dei protocolli di stimolazione ovarica controllata dalla moltitudine di vantaggi che offre, come tempi di trattamento più brevi e un carico farmacologico minore per la paziente. Come dice il Dr. Gorka Barrenetxea, specialista in Ginecologia e Ostetricia: "Per 10-15 anni abbiamo usato altri farmaci coadiuvanti, antagonisti dello GnRH, per cui ora il processo di stimolazione richiede circa 10 giorni."
La fase di somministrazione delle gonadotropine (FSH) dura di solito circa 6-10 giorni. Durante questo tempo, la paziente dovrà sottoporsi a controlli ecografici circa 2 o 3 volte per monitorare la crescita follicolare e i livelli ormonali, permettendo al medico di aggiustare la dose dei farmaci. Circa 30-34 ore prima della puntura ovarica, la paziente deve essere sottoposta ad un'iniezione dell'ormone hCG (gonadotropina corionica umana) per innescare l'ovulazione e indurre la maturazione finale delle uova, preparandole per il prelievo.
2. Puntura Follicolare e Prelievo Ovocitario
La puntura follicolare, nota anche come pick-up ovocitario, consiste nell'aspirazione del liquido contenuto nei follicoli ovarici per estrarre le uova mature. Si tratta di una procedura semplice e rapida, che dura circa 30 minuti e che viene eseguita in sala operatoria. La paziente viene posta in sedazione profonda, in anestesia, in modo che non senta dolore, come confermato dall'embriologa Maria De Las Heras: "La puntura follicolare non è dolorosa, poiché la paziente viene sedata quando entra in sala operatoria."
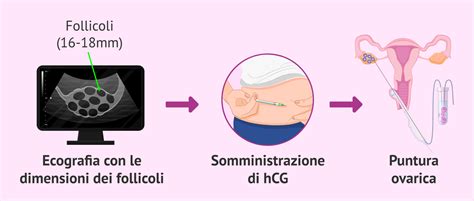
L'operazione viene eseguita attraverso una puntura vaginale guidata da ultrasuoni. Una sonda ecografica viene inserita nella vagina per visualizzare le ovaie e i follicoli. Successivamente, un ago sottile, guidato dall'ecografia, viene inserito attraverso la parete vaginale fino a raggiungere i follicoli. Il liquido follicolare, contenente gli ovociti, viene aspirato delicatamente e raccolto in provette. Una volta in laboratorio, il liquido follicolare deve essere esaminato in dettaglio sotto la lente d'ingrandimento per individuare le uova e trasferirle su una piastra con terreno di coltura appropriato.
3. Decumulo degli Ovociti
Questa fase del processo FIV-ICSI, nota anche come denudazione, consiste nella rimozione dello strato di cellule del cumulo ooforo (strato di granulosio) che circonda l'uovo maturo. Per effettuare la decumulazione degli ovociti è necessario attendere qualche ora dopo la puntura follicolare, poiché l'uovo subisce la maturazione finale durante questo tempo di riposo, raggiungendo lo stadio di metafase II, l'unico stadio in cui può essere fecondato con successo.
Ci sono due tecniche principali per la decumulazione degli ovociti:
- Decumulazione Chimica: Viene utilizzato un mezzo con ialuronidasi, un enzima che degrada l'acido ialuronico che lega le cellule granulose tra loro e all'ovulo. Nella fecondazione naturale, la ialuronidasi viene secreta dallo sperma per facilitare la penetrazione nell'ovulo.
- Decumulazione Meccanica: Dopo il trattamento enzimatico, l'uovo viene fatto passare attraverso pipette di diverso calibro, da diametri più grandi a diametri più piccoli, fino al completo distacco di tutte le cellule che lo circondano.
In genere, i protocolli di laboratorio FIVET combinano entrambi i metodi per decumulare le uova in modo più efficace e delicato. Gli ovociti così liberati dalle cellule follicolari e rivestiti dalla sola zona pellucida (una sorta di guscio proteico) sono pronti per la microiniezione. Dopo la decumulazione, è fondamentale controllare se le uova sono mature per poter eseguire l'ICSI. Per fare questo, è necessario visualizzare il corpuscolo polare nello spazio perivitellino degli ovuli, un indicatore chiave della maturità ovocitaria. La presenza di un solo corpuscolo polare indica che l'ovulo ha completato la sua prima divisione meiotica ed è pronto per la fecondazione.
4. Raccolta e Preparazione degli Spermatozoi
Mentre la donna si sottopone alla puntura follicolare, l'uomo deve lasciare un campione di sperma in laboratorio, generalmente raccolto tramite masturbazione. In alternativa, si può utilizzare sperma congelato precedentemente o sperma di un donatore. Nei casi di azoospermia o grave oligozoospermia, gli spermatozoi possono essere ottenuti chirurgicamente attraverso una puntura testicolare o una biopsia, tecniche che consentono il recupero diretto dal testicolo o dall'epididimo.
Per la preparazione del campione seminale, è necessaria la capacitazione degli spermatozoi. Questo processo di laboratorio è cruciale per isolare e concentrare gli spermatozoi di migliore qualità. Il plasma seminale viene rimosso e lo sperma di altissima qualità viene concentrato in un nuovo mezzo di coltura. L'obiettivo è quello di ottenere un campione di sperma mobile progressivo (PMSC) di circa un milione per millilitro, poiché se ci fossero più spermatozoi sarebbe difficile selezionarli al microscopio. D'altra parte, in caso di fattore maschile grave, è possibile ottenere un numero inferiore di spermatozoi di qualità inferiore. Infatti, a volte è necessario ottenere lo sperma con una puntura testicolare o una biopsia per fare l'ICSI. Nonostante ciò, anche se è più complicato, l'ICSI può essere fatto anche in queste condizioni, poiché per l'iniezione sono necessari solo tanti spermatozoi vivi quanti sono gli ovuli.
5. La Microiniezione Intracitoplasmatica (ICSI)
Questo è il cuore della tecnica e ciò che differenzia la ICSI dalla FIV convenzionale. Come suggerisce il nome, l'ICSI prevede l'iniezione di sperma direttamente nel citoplasma dell'ovulo. Questo processo viene eseguito con estrema precisione in un ambiente controllato, utilizzando un micromanipolatore e un microscopio ad alta potenza.
Per fare ciò, si seguono attentamente i seguenti passi:
- Preparazione iniziale: Le pipette di mantenimento (holding pipette) e di microiniezione (ICSI pipette) sono posizionate su un microscopio rovesciato. La piastra ICSI viene quindi preparata con gocce di terreno di coltura: in una goccia vengono posti gli ovuli denudati e in un'altra gli spermatozoi capacitati e selezionati.
- Selezione dello spermatozoo: Il campione di sperma viene osservato attentamente alla ricerca dello spermatozoo con la migliore qualità, in termini di morfologia e, se possibile, motilità. Una volta selezionato, lo spermatozoo deve essere immobilizzato con un rapido e delicato movimento della pipetta ICSI per rompere la coda. Questa rottura è cruciale perché permette agli enzimi presenti nella testa dello spermatozoo di essere rilasciati, facilitando l'attivazione dell'ovulo dopo l'iniezione. Lo sperma viene poi aspirato con questa stessa pipetta. Lo spermatozoo prescelto viene inizialmente manipolato in modo da rompere delicatamente la membrana cellulare e facilitare il rilascio del suo contenuto nell’ambiente ovocitario dopo la microiniezione.
- Orientamento dell’ovulo: Per non danneggiare le strutture interne dell'uovo con l'iniezione, l'ovulo viene accuratamente posizionato. Viene posto con il suo corpuscolo polare rivolto verso l'alto (alle ore 12 o 6), e viene tenuto fermo dalla pipetta di tenuta (holding pipette) per evitare qualsiasi movimento durante l'iniezione. Questo orientamento è fondamentale per evitare di iniettare lo spermatozoo vicino ai cromosomi dell'ovulo, che si trovano appunto sotto il corpuscolo polare.
- Iniezione intracitoplasmatica dello sperma: L'ago di microiniezione, contenente lo spermatozoo immobilizzato, viene delicatamente premuto contro la zona pellucida (il guscio esterno dell'ovulo) e poi attraverso la membrana interna dell'ovulo (oolemma). Una volta che la punta dell'ago è all'interno del citoplasma dell'ovulo, un po' di citoplasma viene delicatamente aspirato fino a quando non entra in contatto con lo sperma. Successivamente, lo spermatozoo viene delicatamente introdotto all'interno dell'ovulo. Questa azione consente un’interazione tra contenuto dello spermatozoo e ambiente intracellulare dell’ovocita, che è essenziale per innescare la fecondazione, senza che lo spermatozoo debba superare le barriere (cellule follicolari e zona pellucida) che intervengono nel concepimento spontaneo o nella FIVET. In mani esperte, l’azione di microiniezione è rapida ed efficiente, richiedendo soltanto 1-2 minuti per ciascun ovocita.
- Valutazione finale: Dopo l'iniezione, il tipo di rottura dell'uovo fornisce informazioni sulla qualità dell'uovo e può condizionarne l'ulteriore sviluppo. Pertanto, è necessario valutare il tipo di rottura, che può essere per pressione o per aspirazione. Una volta completato l'intero processo ICSI, è importante notare anche le caratteristiche morfologiche delle uova: corpuscolo polare, citoplasma, spazio perivitellino, zona pellucida, ecc.
Infine, le uova iniettate vengono conservate in piastre di coltura nell'incubatrice, in attesa di valutare se la fecondazione si è verificata. Questo avviene dopo circa 16-20 ore dall’iniezione.
6. Coltura Embrionaria
Dopo aver verificato l'avvenuta fecondazione, gli embrioni ottenuti vengono coltivati in incubatori che simulano le condizioni fisiologiche dell’utero materno. Durante tutto lo sviluppo embrionale, è necessario valutare le caratteristiche morfocinetiche degli embrioni con l'obiettivo di trasferire quelli di migliore qualità e con una maggiore possibilità di impianto. La coltura può durare da 2-3 giorni (fino allo stadio di 6-8 cellule) fino a 5-6 giorni (stadio di blastocisti), in base alla qualità degli embrioni e alla strategia clinica adottata.
A seconda dello stadio di sviluppo in cui si trova l'embrione, alcuni parametri specifici vengono valutati:
- Zigoti (circa 18 ore dopo la fecondazione): Vengono valutati per vedere se sono apparsi i due corpuscoli polari e i due pronuclei (uno maschile e uno femminile), il che indica che la fecondazione ha avuto successo e che l'embrione è diventato uno zigote.
- Embrioni di 2-3 giorni: A questo stadio, l'embrione si è già diviso in 4-8 cellule (blastomeri). Si valuta il numero di cellule, la loro simmetria (cioè se hanno dimensioni simili), la frammentazione citoplasmatica (presenza di piccole porzioni di citoplasma staccatesi dalle cellule), la multinucleazione (presenza di più nuclei in una singola cellula) e la presenza di vacuoli. Questi parametri sono indicatori della qualità e del potenziale di sviluppo dell'embrione.
- Blastocisti (5-6 giorni): In questa fase, l'embrione è già costituito da una moltitudine di cellule che formano due strutture distinte: la massa cellulare interna (ICM), che darà origine al feto, e il trofoectoderma (TE), che formerà la placenta. Si valuta anche il grado di espansione delle blastocisti e se hanno iniziato ad uscire dalla zona pellucida, un processo noto come hatching (schiusa), che è necessario per l'impianto nell'utero.
In alcuni casi selezionati, può essere indicata la diagnosi genetica preimpianto (PGT - Preimplantation Genetic Testing), una tecnica avanzata che permette di analizzare il patrimonio genetico degli embrioni prima del trasferimento. Questa biopsia cellulare viene normalmente effettuata 3 giorni dopo l'ICSI quando l'embrione ha circa 8 cellule. Tuttavia, è anche possibile fare la PGD con blastocisti, biopsiando diverse cellule del suo trofoectoderma, senza comprometterne la vitalità.
7. Trasferimento Embrionario
Il trasferimento di embrioni è la fase in cui gli embrioni di migliore qualità vengono collocati nell'utero materno. Tenendo conto delle caratteristiche del trattamento e del numero di embrioni ottenuti, il trasferimento può essere effettuato il giorno 3 o il giorno 5 di coltura, a seconda della strategia clinica e della valutazione embriologica. L'embrione o gli embrioni della migliore qualità saranno selezionati in base ai parametri discussi durante la coltura.
Prima del trasferimento dell'embrione, la donna deve aver ricevuto estrogeni e progesterone per una preparazione endometriale ottimale. Questi ormoni aiutano a rendere l'endometrio (il rivestimento interno dell'utero) ricettivo all'impianto embrionario.
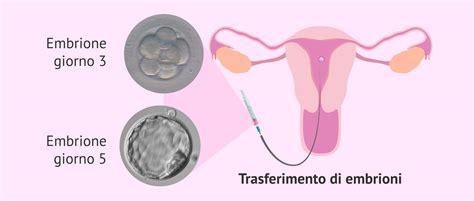
La procedura di trasferimento embrionale è molto semplice e solitamente non richiede l'anestesia. L'embrione selezionato viene dapprima prelevato con un sottile e flessibile catetere. Questo catetere viene poi introdotto nell'utero attraverso la vagina della donna, passando attraverso la cervice uterina. Grazie all'ecografia che viene eseguita contemporaneamente, è possibile vedere come l'embrione viene lasciato nella parte inferiore dell'utero in modo che l'impianto possa avvenire. Una volta che l'embrione è depositato nell'utero della donna, il personale del laboratorio controllerà la cannula al microscopio per assicurarsi che non siano rimasti embrioni al suo interno.
8. Congelamento degli Embrioni in Eccesso
Nella maggior parte dei cicli di FIVET, rimarranno embrioni in eccesso dopo il trasferimento di embrioni. Questo accade perché, ad esempio, la legislazione spagnola consente il trasferimento di un massimo di 3 embrioni, sebbene ci sia una crescente tendenza a trasferire un solo embrione invece di due o tre. Il motivo principale è quello di evitare la possibilità di una gravidanza multipla e i rischi che può comportare, sia per la madre che per i feti.
Di conseguenza, gli embrioni che non vengono trasferiti al primo tentativo vengono vitrificati per un uso futuro. La vitrificazione è una tecnica di congelamento ultra-rapido che consente una conservazione ottimale degli embrioni. Questi embrioni possono essere utilizzati in un tentativo successivo, sia perché il primo trasferimento non ha avuto successo, sia per avere un secondo figlio in futuro. Per poter vitrificare gli embrioni, essi devono essere di buona o media qualità, in modo da garantire la sopravvivenza degli embrioni dopo la devitrificazione (scongelamento). Un'altra opzione per gli embrioni in eccesso, a seconda delle normative e delle scelte della coppia, sarebbe quella di donarli ad altri pazienti o alla ricerca scientifica.
9. Il Test di Gravidanza
Dopo il trasferimento embrionario, inizia un periodo di attesa che può essere emotivamente intenso per la coppia. La paziente dovrebbe aspettare circa 9-12 giorni per fare un test di gravidanza per vedere se la FIV-ICSI ha avuto successo. Questo periodo di tempo tra il trasferimento di embrioni e il test di gravidanza è comunemente chiamato "L'attesa della beta", riferendosi all'ormone beta-hCG. Questo test può essere eseguito sia sulle urine (un test di gravidanza casalingo) che sul sangue (un prelievo ematico) e misura la quantità dell'ormone beta hCG (gonadotropina corionica umana), che viene prodotto solo durante la gravidanza. Un valore positivo, in aumento nel tempo, indica una gravidanza in corso. La maggior parte degli specialisti raccomanda di continuare con la routine quotidiana e di evitare di focalizzarsi eccessivamente sul risultato durante l'intero periodo di attesa della beta, al fine di ridurre lo stress.
Differenze Chiave tra FIV Convenzionale e ICSI
Entrambe le tecniche, la FIV (Fecondazione In Vitro) convenzionale e l'ICSI, fanno parte della più ampia categoria delle tecniche di riproduzione assistita, ma differiscono principalmente nel modo in cui viene effettuata la fecondazione.
- FIV Convenzionale: In questa procedura, un numero significativo di spermatozoi (tra 50.000 e 100.000) viene posto in una piastra di coltura con l'ovulo. Lo spermatozoo deve quindi attraversare le barriere naturali dell'ovulo (il cumulo ooforo e la zona pellucida) per fecondarlo in modo "naturale", imitando ciò che accadrebbe in vivo nella tuba di Falloppio. Questo approccio è generalmente utilizzato quando la qualità e la quantità del seme maschile sono nella norma e non ci sono ostacoli noti alla fecondazione spontanea. L'intero cumulo ooforo, costituito dall’ovocita e dalle cellule follicolari ad esso associate, è posto in un mezzo di coltura contenente ialuronidasi, un enzima che digerisce la matrice viscoelastica. In tal modo, gran parte delle cellule sono rilasciate nel mezzo di coltura, mentre quelle più tenacemente legate all’ovocita sono eliminate meccanicamente facendo passare l’oocita stesso attraverso un capillare di adeguato calibro. Gli ovociti così liberati dalle cellule follicolari e rivestiti dalla sola zona pellucida (una sorta di guscio proteico) sono pronti per la microiniezione.
- ICSI: Con l'ICSI, uno spermatozoo viene selezionato e iniettato direttamente nell’ovulo tramite un microago, bypassando così tutte le barriere esterne dell'ovulo. Questa tecnica è stata sviluppata specificamente per superare i problemi di infertilità maschile grave, dove gli spermatozoi potrebbero non essere in grado di raggiungere o penetrare l'ovulo da soli. In questo caso, le cellule follicolari e la matrice viscoelastica che le tiene insieme rappresentato più un ostacolo che un ausilio per la fecondazione. In laboratorio, le cellule follicolari sono rimosse dall’ovocita in maniera semplice e veloce per permettere l'iniezione diretta.
Sebbene l'ICSI sia più complessa e tecnica, e richieda l'uso di apparecchiature sofisticate come il micromanipolatore, consente tassi di successo più elevati nei casi di infertilità maschile grave o in altre situazioni specifiche, come il fallimento di fecondazione in precedenti cicli FIV.
Tecnica #ICSI
Tassi di Successo e Fattori Influenzanti
I tassi di successo dell’ICSI sono tra i più elevati nell'ambito della riproduzione assistita e variano a seconda di diversi fattori, tra cui l'età della donna e la qualità del liquido seminale. La percentuale di successo è un dato dinamico e può differire tra le diverse cliniche, ma esistono statistiche generali che forniscono un'indicazione.
Secondo le statistiche più recenti, i tassi di gravidanza per trasferimento di ovuli propri sono i seguenti:
- Donne con meno di 35 anni: circa il 43,7% di successo.
- Donne tra 35 e 39 anni: circa il 35% di successo.
- Donne tra 40 e 42 anni: circa il 21,2% di successo.
Questi tassi di successo possono variare a seconda della clinica e dei fattori individuali di ciascuna coppia, come la causa specifica dell'infertilità, la riserva ovarica, la qualità degli ovuli e degli spermatozoi, e la presenza di altre condizioni mediche. L'esperienza degli embriologi e la tecnologia utilizzata nel laboratorio giocano un ruolo fondamentale nel massimizzare le probabilità di successo.
È importante notare che la percentuale di successo si riferisce alla probabilità di ottenere una gravidanza per ogni ciclo di trattamento avviato. Spesso, sono necessari più cicli per raggiungere l'obiettivo della gravidanza.
Aspetti Economici del Trattamento ICSI
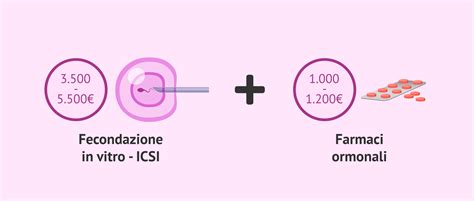
Il costo di un trattamento con ICSI è un fattore importante da considerare per le coppie che intraprendono questo percorso. Essendo parte della fecondazione in vitro, il costo di un trattamento con ICSI varia solitamente tra 3.500 € e 5.500 €. Questo prezzo può fluttuare a seconda di diversi fattori quali la clinica prescelta, il protocollo di stimolazione ovarica utilizzato, l'inclusione di servizi aggiuntivi (come la Diagnosi Genetica Preimpianto, la coltura a blastocisti, o il congelamento di embrioni extra) e la regione geografica in cui viene effettuato il trattamento.
È importante sottolineare che questo costo base non sempre include i farmaci necessari per la stimolazione ovarica controllata. Le spese per i farmaci ormonali possono costare tra 1.000 € e 1.200 €, a seconda del protocollo utilizzato e della dose necessaria per la paziente. Pertanto, è fondamentale richiedere un preventivo dettagliato che specifichi tutti i costi inclusi ed esclusi, per avere un quadro economico completo e trasparente.
Domande Frequenti sull'ICSI
L'ICSI, come ogni procedura medica complessa, solleva diverse domande. Approfondiamo alcune delle più comuni.
È possibile effettuare un'iniezione intracitoplasmatica lenta di sperma?
Sì, la cosa più importante nel fare un'ICSI è assicurarsi che gli spermatozoi siano vivi. Nei campioni di sperma astenozoospermico con ridotta motilità spermatica, la selezione degli spermatozoi è ancora più critica. Si cercherà di selezionare spermatozoi che, sebbene con mobilità ridotta o assente, presentino i migliori criteri morfologici e la certezza della vitalità. In alcuni casi, tecniche come la cosiddetta "piccola vibrazione" o l'uso di specifici media possono aiutare a identificare spermatozoi vitali anche se immobili. La microiniezione stessa avviene con una manipolazione attenta e, una volta che lo spermatozoo è nel citoplasma dell'ovulo, la sua mobilità non è più un fattore determinante per la fecondazione.
Quando si fa la DGP (Diagnosi Genetica Preimpianto) dopo l'ICSI?
La diagnosi genetica preimpianto o DGP (PGT, Preimplantation Genetic Testing) consiste nell'analisi genetica di una cellula o di alcune cellule dell'embrione per scoprire se soffre di un'alterazione genetica specifica o di anomalie cromosomiche. Questa biopsia cellulare viene normalmente effettuata in momenti specifici dello sviluppo embrionale.
Tradizionalmente, la biopsia veniva eseguita 3 giorni dopo l'ICSI, quando l'embrione si trova allo stadio di divisione e ha circa 8 cellule (stadio di blastomero). In questa fase, viene prelevata una singola cellula. Tuttavia, è anche possibile fare la PGD con blastocisti, biopsiando diverse cellule del suo trofoectoderma (lo strato esterno che darà origine alla placenta) al giorno 5 o 6 di sviluppo embrionale. La biopsia allo stadio di blastocisti è preferita in molti centri perché si ritiene meno invasiva per lo sviluppo futuro dell'embrione e fornisce un maggior numero di cellule per l'analisi, migliorando l'accuratezza diagnostica. Indipendentemente dal momento della biopsia, l'ICSI è spesso preferita nei cicli con PGT per minimizzare il rischio di contaminazione da parte di spermatozoi estranei che potrebbero aderire alla zona pellucida dell'ovulo dopo la FIV convenzionale, potenzialmente falsando i risultati dell'analisi genetica.
tags: #descrivi #brevemente #la #tecnica #icsi