L'avanzamento delle tecnologie di editing genomico, in particolare il sistema CRISPR/Cas9, sta aprendo scenari rivoluzionari nel campo della biologia e della medicina. La possibilità di modificare il DNA con precisione millimetrica offre speranze concrete per il trattamento di malattie genetiche, ma solleva anche interrogativi etici e normativi complessi, specialmente quando si tratta di applicazioni sugli embrioni umani. In Italia, il dibattito sull'utilizzo di queste tecniche in ambito embrionale è particolarmente acceso, con implicazioni che vanno dalla ricerca scientifica alla procreazione assistita.
Le Forbici Molecolari CRISPR/Cas9: Uno Strumento di Precisione Rivoluzionario
Il sistema CRISPR/Cas9, acronimo di Clustered Regularly Interspaced Short Palindromic Repeats, è una tecnologia di ingegneria genetica che agisce come un meccanismo di difesa naturale, adattato per modificare il DNA. In termini semplici, si compone di una sequenza di RNA (acido ribonucleico) costruita in laboratorio, programmata per individuare una regione specifica del genoma, e dell'enzima Cas9, una proteina capace di tagliare il DNA in quel punto preciso. Questo permette ai ricercatori di "editare" il codice genetico, eliminando, correggendo o sostituendo determinate sequenze di DNA. La precisione di questo strumento è tale da poter individuare e correggere errori anche a livello di singole basi azotate, ripristinando la sequenza "selvatica", ovvero quella originale e sana.
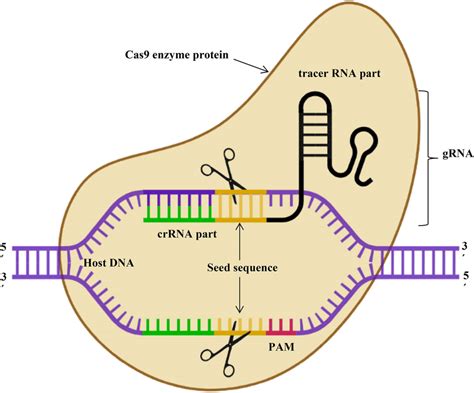
Questa capacità di intervento mirato ha aperto le porte a nuove frontiere nella ricerca medica. Ad esempio, studi come quello condotto nel Regno Unito e illustrato sulla rivista Nature, hanno utilizzato CRISPR/Cas9 per indagare le prime fasi dello sviluppo embrionale umano. L'obiettivo era comprendere meglio i meccanismi che regolano la differenziazione delle cellule embrionali e identificare le cause di aborti precoci ricorrenti.
Studio sulla Differenziazione Cellulare Embrionale e il Ruolo della Proteina OCT4
Uno degli esperimenti più significativi ha riguardato lo studio del ruolo della proteina OCT4 nelle primissime fasi dello sviluppo embrionale. Kathy Niakan, la biologa a capo dello studio, ha richiesto l'autorizzazione per condurre ricerche su 37 embrioni umani a singola cellula (zigoti), donati da coppie sottoposte a trattamenti di fecondazione in vitro. L'obiettivo era analizzare il processo che, nell'arco di sette giorni, porta dalla cellula uovo fecondata alla formazione della blastocisti, la fase embrionale più avanzata prima dell'impianto nell'utero.
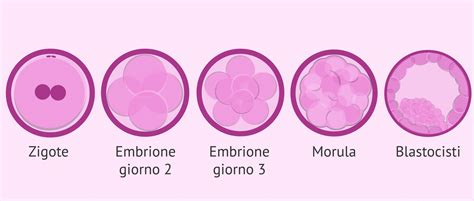
In particolare, l'attenzione si è concentrata sulla proteina OCT4, un marcatore essenziale per lo sviluppo di cellule pluripotenti, ovvero cellule in grado di differenziarsi in tutti i tipi di tessuto del corpo umano. Nei topi, la disattivazione dei geni che codificano per OCT4 porta alla formazione esclusiva di cellule placentari, senza lo sviluppo del feto. Nell'esperimento sugli embrioni umani, l'assenza di questo marcatore ha impedito la formazione non solo del feto, ma anche della placenta e del sacco vitellino, quest'ultimo fondamentale per il nutrimento dell'embrione. Questi risultati suggeriscono che OCT4 riveste un ruolo ancora più determinante nella diversificazione delle cellule embrionali umane rispetto a quanto osservato nei modelli murini.
Sfide Tecnologiche: Sicurezza, Specificità e Sistemi di Delivery
Nonostante le potenzialità, l'applicazione clinica di CRISPR/Cas9 presenta ancora sfide significative. Una delle preoccupazioni maggiori riguarda l'attività "off-target", ovvero la possibilità che l'enzima Cas9 possa tagliare il DNA in regioni non desiderate, simili a quelle bersaglio. Questa eventualità potrebbe portare a effetti indesiderati e imprevedibili, rendendo la tecnologia non sicura per il trattamento di pazienti.
Per affrontare questo problema, ricercatori come quelli di Alia Therapeutics, una startup italiana fondata da scienziati del CIBIO dell'Università di Trento, stanno lavorando allo sviluppo di versioni modificate della proteina Cas9, definite "mutanti ad alta fedeltà". L'obiettivo è ottimizzare la tecnologia, rendendola più sicura e applicabile in ambito clinico, con una specificità senza precedenti.
Un'altra sfida cruciale è rappresentata dai sistemi di "delivery", ovvero i metodi per trasportare in modo efficiente e sicuro gli strumenti molecolari di editing genetico all'interno delle cellule bersaglio. La ricerca in questo campo esplora diverse frontiere, tra cui nanoparticelle polimeriche, liposomi e nanotubi di carbonio. Alia Therapeutics ha sviluppato due approcci innovativi:
- Vettore Lentivirale con Circuito Autolimitante: Questo sistema agisce come un "interruttore di autospegnimento", permettendo l'espressione della nucleasi (Cas9) solo per un periodo di tempo molto breve. Ciò minimizza il rischio di attività off-target e migliora il profilo di sicurezza e specificità dell'editing.
- Vescicole Prodotte da Linee Cellulari Specifiche: Queste vescicole, opportunamente caricate durante la produzione, sono in grado di consegnare il carico proteico (Cas9) nelle cellule bersaglio in modo efficiente e "senza lasciare traccia".
Questi sistemi di delivery, sviluppati in collaborazione con il laboratorio della Prof.ssa Anna Cereseto, hanno dimostrato la loro validità e migliorano significativamente le prestazioni dell'editing genetico, anche con la versione classica di Cas9. Alia Therapeutics ha brevettato queste piattaforme tecnologiche (evoCas9, lentiSLICES e VEsiCas), creando un sistema coerente di tecnologie unico in Italia e raro a livello internazionale, che coniuga lo sviluppo di nuovi strumenti di editing con sistemi di delivery avanzati.
Il Contesto Normativo Italiano e il Dibattito Etico
La regolamentazione dell'editing genetico sugli embrioni umani varia significativamente da paese a paese. In Italia, l'applicazione di queste tecniche sugli embrioni è attualmente vietata. Questo divieto pone un freno alla ricerca scientifica in questo specifico ambito, nonostante le potenzialità terapeutiche.
La Corte Europea di Giustizia, nel luglio 2018, ha stabilito che le piante migliorate geneticamente tramite intervento umano cosciente sono da considerarsi Organismi Geneticamente Modificati (OGM). Tuttavia, le nuove tecniche di editing genomico come CRISPR permettono di correggere il DNA senza spostare geni tra organismi diversi, generando varianti naturali.
Il dibattito sull'ingegneria genetica e le implicazioni etiche della modifica del DNA risale agli anni '70. La comparsa di tecniche precise, relativamente facili da usare e a costi contenuti, ha portato all'uso dei termini "gene editing" o "genome editing". Queste tecniche sollevano questioni fondamentali sulla manipolazione della vita, sull'identità umana e sul potenziale per creare disuguaglianze genetiche.
Che cos'è l'editing genetico
Organizzazioni come l'Associazione Luca Coscioni, fondata per promuovere le libertà civili e i diritti umani, inclusi il diritto alla scienza, si battono per una maggiore libertà di ricerca. L'associazione supporta temi come la ricerca sugli embrioni, l'accesso alla procreazione medicalmente assistita e il monitoraggio delle leggi in materia di scienza e autodeterminazione. La libertà di ricerca scientifica è stata al centro di discussioni in occasione di congressi mondiali, che hanno affrontato temi come genoma, staminali, biotecnologie e le implicazioni etiche dell'intelligenza artificiale.
Prospettive Future e Applicazioni Cliniche
Nonostante i divieti attuali in Italia sull'uso di CRISPR sugli embrioni, la ricerca continua a progredire in altri ambiti e con altri obiettivi. La Dott.ssa Rita Vassena, direttrice scientifica della Clinica Eugin e membro del comitato esecutivo della Società Europea di Riproduzione Assistita ed Embriologia (ESHRE), sottolinea come CRISPR/Cas9 abbia il potenziale per correggere mutazioni genetiche e risolvere una vasta percentuale di casi che oggi non possono essere prevenuti con le attuali tecniche di diagnosi genetica preimpianto o preconcezionale.
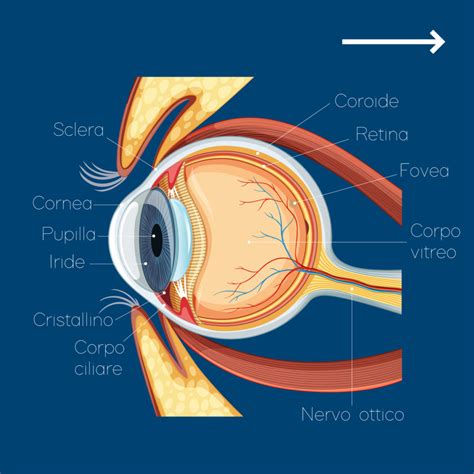
L'obiettivo immediato della ricerca in questo campo è garantire i più alti standard di efficacia e sicurezza per gli interventi sulla catena genetica umana. Alia Therapeutics, ad esempio, sta collaborando con il laboratorio di Anna Cereseto e il Tigem (Telethon Institute of Genetics and Medicine) per sperimentare nuovi strumenti di editing genetico in ambito oftalmologico, con il potenziale di trattare alcune forme di degenerazione retinica.
La strada verso l'applicazione clinica diffusa di CRISPR/Cas9, specialmente in aree sensibili come la riproduzione umana, è ancora lunga e richiederà un dialogo continuo tra scienziati, eticisti, legislatori e la società nel suo complesso. La promessa di curare malattie genetiche incurabili è immensa, ma deve essere bilanciata con un'attenta considerazione delle implicazioni etiche e sociali. La ricerca in Italia, pur affrontando restrizioni normative sull'uso di embrioni, continua a contribuire allo sviluppo di tecnologie più sicure ed efficaci, aprendo la strada a future terapie innovative.