Se ti è stato comunicato che è difficile avere un bambino con una bassa riserva ovarica, e ti è stato anche detto che la situazione è complessa, perché dal numero di ovociti (uova) dipende la probabilità di un risultato positivo delle tecniche di fecondazione assistita, è naturale provare dubbi e preoccupazioni. La risoluzione del problema delle poche uova è un argomento che affascina da anni gli specialisti della fertilità, portando allo sviluppo di apposite esperienze in questi casi. Purtroppo, non si riesce in tutti i casi, perché la riduzione del numero di uova è un problema serio. È fondamentale poter contare su un laboratorio di fecondazione in provetta con ottima esperienza. In questo articolo potrai trovare utili notizie su come riconoscere questa condizione, quali sono gli esami per diagnosticarla e cosa fare per avere un bambino, o almeno, per provarci in un modo corretto e seguendo un approccio di qualità.
Cos'è la riserva ovarica e come viene valutata
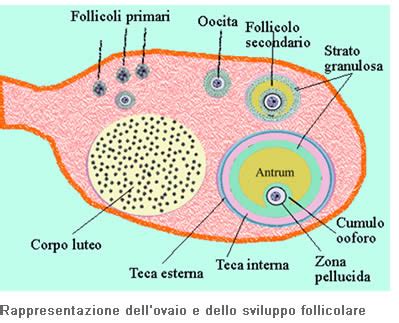
La riserva ovarica è la capacità dell'ovaio di rispondere alla stimolazione. In un ciclo spontaneo, l'ovaio dà inizio allo sviluppo di diversi follicoli (contenenti ovuli al loro interno). Uno di questi, il follicolo dominante, crescerà maggiormente e si romperà durante l'ovulazione, rilasciando un ovulo che verrà fecondato da uno spermatozoo. Quando si verifica l'ovulazione, il follicolo che si è rotto diventa il corpo luteo e produce progesterone. Se non c'è una gravidanza, dopo 15 giorni le ovaie rilevano che l'embrione non si è impiantato e smettono di produrre progesterone. Questo perché prima della nascita le donne hanno già tutti gli ovuli, e nel corso della vita questi ovuli diminuiscono a causa di un processo di distruzione chiamato apoptosi.
La diagnosi di ridotta riserva ovarica prevede un'ecografia transvaginale per la determinazione della riserva ovarica. È importante precisare che l'ecografia per la valutazione della riserva ovarica non è una normale ecografia ginecologica. Essa non si limita a vedere la forma, le dimensioni, l'ecostruttura dell'utero. L'ecografia di riserva ovarica si concentra sul numero di follicoli antrali (piccoli follicoli di 3-5 millimetri di diametro) presenti nelle ovaie. Per effettuare lo studio dei follicoli antrali, si esegue un'ecografia all'inizio del ciclo e si valuta il numero di follicoli con dimensioni comprese tra 2 e 8 mm presenti nelle ovaie. Questo valore ci indica indirettamente il numero di follicoli che possono essere reclutati durante la stimolazione ovarica. Il loro numero si riduce con l'aumentare dell'età della donna. La conta dei follicoli antrali è un test di riserva ovarica molto utile, ma di non facile esecuzione. Occorre un macchinario ecografico di grande qualità, che ha costi elevati che in genere il ginecologo di base non può affrontare. Una donna con buona riserva ovarica deve possedere almeno 6 follicoli per ovaio, meglio se sono di più.
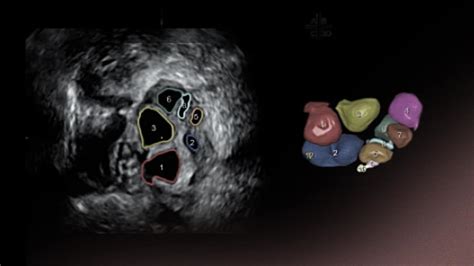
Parametri ormonali per la diagnosi di riserva ovarica
La riserva ovarica viene diagnosticata con il dosaggio dell'ormone antimulleriano (AMH), che normalmente dovrebbe essere maggiore di 1-1.5 ng/mL, e valutando la conta di follicoli antrali (AFC), che normalmente dovrebbe essere superiore a 7-10.
L'ormone antimulleriano (AMH) è un ormone prodotto nello strato esterno dei piccoli follicoli. Quando il follicolo cresce, smette di produrre AMH. L'AMH è prodotto dai piccoli follicoli nelle ovaie di una donna ed è uno dei marcatori più affidabili della riserva ovarica, che rappresenta il numero di ovociti rimanenti nelle ovaie. A differenza di altri ormoni riproduttivi, l'AMH è secreto localmente dalle cellule della granulosa dei follicoli preantrali e antrali. La sua produzione non dipende dal cervello o dai circuiti di feedback ormonali che regolano il ciclo mestruale. Ciò contrasta con altri ormoni della fertilità come FSH, LH ed estradiolo, che fanno parte dell'asse ipotalamo-ipofisi-ovaio (HPO). Questi ormoni sono influenzati da un complesso sistema di feedback. Ad esempio, quando l'attività ovarica diminuisce e un minor numero di follicoli produce estrogeni e inibina B, i livelli di FSH aumentano per compensare. Poiché l'AMH riflette l'attività ovarica direttamente, anziché attraverso meccanismi di feedback, offre una misura più chiara e oggettiva della riserva ovarica. Valori di AMH più elevati di solito suggeriscono una coorte più ampia di follicoli e una risposta più forte alla stimolazione ovarica. Al contrario, livelli di AMH molto bassi o non rilevabili indicano una ridotta riserva ovarica. Tuttavia, è importante ricordare che l'AMH riflette quantità di uova, non loro qualità. Tra i vantaggi della misurazione dell'ormone antimulleriano, invece, si annovera l'indipendenza dei suoi livelli rispetto alla fase del ciclo mestruale: può essere misurato in qualunque giorno del ciclo. L'ormone antimulleriano agisce in modo simile all'inibina B, regolando l'attività del FSH per reclutare un singolo follicolo (diminuisce il numero di follicoli che possono essere reclutati in un ciclo e diminuisce la sensibilità dei follicoli al FSH).
L'FSH (ormone follicolo stimolante) è un ormone prodotto dalla ghiandola pituitaria che stimola lo sviluppo dei follicoli nelle ovaie. Per valutare la riserva follicolare, i livelli di FSH vengono misurati all'inizio del ciclo (tra il 2° e il 4° giorno del ciclo). Alti livelli di FSH indicano che l'ipofisi deve fare uno sforzo importante per iniziare un ciclo naturale, che di solito è correlato a una bassa riserva ovarica. Durante i cicli naturali i valori di FSH possono oscillare. Anche se alcuni aspettano che i valori di FSH siano bassi per iniziare la stimolazione, a nostro avviso il valore prognostico è determinato dal valore più alto. Pertanto, una volta che il valore è alto, aspettare valori più bassi per cercare di ottenere più ovuli non è una buona opzione.
L'inibina B è un ormone prodotto nella prima metà del ciclo dalle cellule dello strato esterno dei piccoli follicoli. L'inibina B provoca una diminuzione dei livelli di FSH che facilita la selezione del follicolo dominante, ovvero il follicolo che ovulerà in quel mese.
Cause e conseguenze della ridotta riserva ovarica
Nessun sintomo è evidente nelle sue fasi iniziali, una riserva ovarica bassa è asintomatica. Nelle fasi avanzate causa invece irregolarità nel ciclo. Inizialmente cicli più frequenti ("dottore, ho sempre avuto il ciclo di 28 giorni, ora lo ho di 24") e poi cicli che si allungano, di 40-60 giorni.
Ci sono cause note quali interventi chirurgici sull'ovaio, endometriosi, trattamenti di radio o chemioterapia, familiarità e genetica. Spesso è sempre più frequente vedere pazienti, anche molto giovani, con bassa riserva ovarica, cioè con un basso AMH (ormone antimulleriano) o una bassa conta dei follicoli antrali (AFC).
In alcuni casi, purtroppo, ti sarà comunicato che l'ovaio è completamente esaurito per la POI (una volta definita POF) cioè la Premature Ovarian Insufficiency. Questa condizione si diagnostica quando il numero di follicoli residui nelle ovaie è esaurito e hai meno di 40 anni. Se però sei oltre i 35 anni di età, è normale che i follicoli ovarici siano un po' ridotti, condizione che diventa sempre più severa man mano che l'età avanza. La menopausa è la cessazione della funzione ovarica, le ovaie non ovulano e smettono di produrre ormoni.
Le conseguenze di una bassa riserva ovarica sono una riduzione delle chance di gravidanza spontanea. Ovviamente determina l'impossibilità di una gravidanza: molte pazienti del nostro centro di PMA che avevano una bassa riserva ovarica hanno concepito, ma ovviamente le chance di pazienti della loro stessa età a riserva ovarica alta sono nettamente migliori. Inoltre, si verifica una riduzione delle chance di gravidanza da PMA. Questo accade perché più ovociti recuperiamo con una tecnica di FIVET/ICSI, più embrioni avremo e più chance di gravidanza avremo. Quindi un basso recupero purtroppo "pesa" sull'esito della PMA. Infine, si può avere un'età della menopausa un po' più precoce rispetto alla media italiana (50 anni).
Approccio alla stimolazione ovarica con AMH basso e pillola anticoncezionale
La riserva ovarica indica indirettamente le possibilità di gravidanza che si hanno quando si effettua un ciclo di riproduzione assistita con i propri ovuli. Il trattamento da scegliere dipende dai risultati degli esami effettuati, dall'età e dalla storia clinica della coppia. Il consiglio è comunque di rivolgersi a persone esperte di questa materia, perché la stimolazione ovarica si presenterà piuttosto complessa e necessita di un medico con lunga esperienza in questa materia.
La bassa riserva ovarica purtroppo influenza una FIVET. Però la FIVET è anche l'unica terapia possibile. Nel senso che, non potendo aumentare la riserva ovarica, l'unica soluzione è rivolta a ottimizzare la risposta ovarica (otteniamo il massimo numero possibile di ovociti) mettendoli nelle migliori condizioni possibili (limino alcun variabili, per esempio il fattore tubarico, la motilità e il numero degli spermatozoi, ecc.). Premesso che nulla esclude una gravidanza spontanea, l'unica "mossa" da fare è procedere prima possibile con una tecnica di PMA ad alta efficienza, cioè una FIVET, perché "non c'è tempo da perdere".
Riserva Ovarica, AMH,AFC, La lezione- Prof. Manna di Biofertility agli specializzandi ginecologia
In questi casi, meno follicoli si hanno, più sarà difficile se non impossibile ottenere una stimolazione ovarica e procedere al tentativo di ottenere un bambino geneticamente materno: si dovrà ricorrere alla fecondazione eterologa femminile detta anche ovodonazione. Nella maggior parte dei casi, per fortuna, l'ovaio avrà semplicemente una riduzione della riserva ovarica.
I cicli di stimolazione ovarica con bassa riserva ovarica hanno risultati in genere scadenti se l'età supera i 35 anni: si tratta di percentuali di successo che non superano numeri ad una cifra. Se i valori di AMH sono molto bassi (molto vicini a zero), e il valore di FSH al 3° giorno del ciclo è superiore a 16, la stimolazione non sarà attuabile, così come non consigliabile sarà la ICSI su ciclo spontaneo o naturale.
Tuttavia, ci sono pazienti con bassa riserva ovarica che rispondono meno alla stimolazione ovarica, ma producono ovociti di buona qualità (questo è tanto più vero quanto più giovane è la paziente).
Strategie di stimolazione ovarica e ottimizzazione
Il fatto che spesso le donne si presentano in età avanzata, dopo i 37 anni, comporta di dover gestire situazioni con AMH basso, bassa conta dei follicoli antrali, ripetuti fallimenti.
Una strategia utile è la doppia stimolazione in due cicli successivi, che può portare a un aumento ovocitario soprattutto nel secondo ciclo. Questo perché agli ovociti servono 2-3 mesi per essere sensibili all'azione dell'FSH nel ciclo successivo e possono avere più chance di arrivare a maturazione.
Un'altra alternativa è la doppia stimolazione, per cui le pazienti vengono stimolate con alte dosi di gonadotropine. Dopo aver indotto l'ovulazione con l'analogo del GNRH sfruttando l'effetto flare-up, 2-3 giorni dopo viene iniziata la stimolazione.
Può essere utile anche l'utilizzo di clomifene associato alle gonadotropine. Un protocollo molto utilizzato è l'FSH sincronizzato, che ha l'obiettivo di sincronizzare la crescita follicolare. Spesso, infatti, le pazienti poor responder in cui viene iniziata la stimolazione dal 2° - 3° giorno del ciclo hanno un'ovulazione prematura in 7° - 8° giornata e un'ecografia in 2° giornata mostrerà almeno un follicolo a 10-11 mm. Quindi, nel momento in cui si inizia la stimolazione ovarica ci sarà un follicolo pronto già dopo 3-4 giorni e gli altri che arrancheranno. Quindi si utilizza o una pillola anticoncezionale nel ciclo precedente o dell'estradiolo valerato a partire dal giorno 2-3 fino al primo giorno del ciclo successivo, con l'obiettivo di limitare e abbassare i livelli di FSH nella fase premestruale cercando di sincronizzare il più possibile la crescita follicolare.
Esistono anche protocolli sperimentali che non hanno percentuali di successo dimostrabili. Ad esempio, l'utilizzo del DEA, il deidroepiandrosterone solfato che, essendo un androgeno, pare riattivi una percentuale di ovociti nascosti. Oppure, può essere utile utilizzare del testosterone in gel 5 microgrammi per due mesi prima dell'inizio della stimolazione. Si tratta di protocolli non ancora consolidati perciò non danno alcuna certezza.
Tecniche avanzate e approcci innovativi
Nell'ambito della riproduzione assistita, i progressi stanno aprendo nuove porte alle donne che desiderano preservare o ripristinare la propria capacità riproduttiva, soprattutto in presenza di una riserva ovarica ridotta.
Terapia con plasma ricco di piastrine (PRP) ovarico
La terapia con plasma ricco di piastrine (PRP) ovarico è una tecnica emergente che prevede l'iniezione del plasma della paziente, arricchito con fattori di crescita, direttamente nelle ovaie. L'obiettivo è stimolare i follicoli primordiali dormienti e potenzialmente riavviare il processo di sviluppo dell'ovulo. In alcuni protocolli, il PRP viene combinato con gli esosomi, piccole vescicole extracellulari derivate da cellule staminali che svolgono un ruolo nella comunicazione intercellulare. Gli esosomi trasportano proteine, lipidi e acidi nucleici che possono migliorare il microambiente ovarico, ridurre lo stress ossidativo e migliorare le condizioni per la follicologenesi (Mojadadi et al., 2021). Tuttavia, il potenziale successo della terapia ovarica con PRP dipende dalla presenza o meno di follicoli residui. Un livello rilevabile di ormone antimulleriano (AMH) è generalmente considerato essenziale, poiché livelli non rilevabili di AMH riflettono tipicamente l'assenza di follicoli vitali e quindi una mancanza di substrato biologico su cui il PRP possa agire (Polyzos e Devroey, 2011). Nelle donne con attività ovarica bassa ma misurabile, il PRP può contribuire a migliorare il reclutamento follicolare naturale e ad aumentare le possibilità di recupero degli ovociti nei successivi cicli di fecondazione in vitro.
Conservazione degli ovociti
La conservazione degli ovociti non è una novità nella riproduzione assistita, ma viene spesso trascurata come metodo altamente efficace per migliorare i risultati della fecondazione in vitro. Quando una donna si sottopone a stimolazione ovarica controllata, il numero di ovociti maturi recuperati può essere limitato, in particolare nelle donne di età superiore ai 35 anni o in quelle con riserva ovarica ridotta. Con un numero limitato di ovociti, la probabilità di sviluppare una blastocisti sana è bassa. Questo non solo a causa della quantità, ma anche perché la qualità degli ovociti diminuisce con l'età. La conservazione degli ovociti affronta questo problema consentendo alle pazienti di sottoporsi a più di una stimolazione e prelievo di ovociti prima di tentare la fecondazione e il trasferimento. Raccogliendo gli ovociti di più cicli, si aumenta il numero totale disponibile per la fecondazione, aumentando le probabilità di creare uno o più embrioni sani. Questo approccio è particolarmente utile per le donne quarantenni, per le quali potrebbe essere necessario un numero maggiore di ovociti per ottenere almeno un embrione cromosomicamente normale (Goldman et al., 2017). In pratica, questa strategia può fare la differenza tra ripetute delusioni e una gravidanza di successo. Accettando che un singolo ciclo potrebbe non essere sufficiente e investendo in più di un ciclo di stimolazione, le pazienti si assicurano le migliori possibilità di produrre embrioni adatti al trasferimento.
Terapia sostitutiva mitocondriale (MRT)
Per molte donne in età riproduttiva avanzata, la sfida principale non è il numero di ovociti disponibili, ma la loro qualità. Gli embrioni potrebbero non svilupparsi normalmente o potrebbero presentare anomalie cromosomiche (aneuploidie), strettamente legate alla disfunzione mitocondriale legata all'età. La terapia sostitutiva mitocondriale (MRT) cerca di superare questo problema introducendo mitocondri sani provenienti da un ovocita donato nell'ovulo della paziente, preservandone al contempo il DNA nucleare. Questo approccio ripristina efficacemente l'apporto energetico dell'ovulo e può ripristinarne la capacità di sviluppo. Questa tecnologia avanzata viene applicata in casi accuratamente selezionati in cui le donne producono ovociti ma subiscono ripetuti fallimenti della fecondazione in vitro a causa di uno scarso sviluppo embrionale o di aneuploidie ricorrenti.
Ciclo di fecondazione in vitro tandem
Un ciclo di fecondazione in vitro tandem consente l'utilizzo di ovuli della paziente insieme a ovuli di una donatrice all'interno dello stesso ciclo di trattamento. Lo scopo non è quello di sostituire il potenziale riproduttivo della paziente, ma di salvaguardarlo. Questo approccio può essere particolarmente conveniente ed emotivamente rassicurante, poiché evita la necessità di più cicli di fecondazione in vitro nel caso in cui gli ovociti della paziente non producano embrioni adatti al trasferimento. Invece di affrontare la delusione di un trasferimento annullato o il ritardo di un ciclo completamente nuovo, le pazienti hanno la possibilità di procedere immediatamente con embrioni derivati da donatrice. I cicli tandem sono particolarmente rilevanti per le donne con riserva ovarica ridotta o qualità ovocitaria borderline che desiderano comunque tentare il trattamento con i propri ovociti ma non vogliono rischiare un ciclo vuoto. Mentre le donne in età riproduttiva avanzata o con scarsa risposta hanno spesso bassi tassi di successo con i propri ovociti, l'uso di ovociti di donatrice aumenta significativamente la probabilità di un parto vivo (Sunkara et al., 2011; Kushnir et al., 2015). Il trattamento della fertilità non è più un'unica soluzione. È fondamentale personalizzare gli approcci di ringiovanimento in base alla biologia e agli obiettivi della paziente.
tags: #stimolazione #ovarica #pillola #anticoncezionale #amh #basso