Nel percorso complesso della diagnosi prenatale, i risultati dei test genetici possono a volte presentare scenari articolati, in particolare quando si evidenzia una condizione di mosaicismo. Questo fenomeno, caratterizzato dalla presenza di cellule con un patrimonio genetico diverso all'interno della stessa persona, assume una rilevanza critica quando coinvolge anomalie cromosomiche come la trisomia, e la sua interpretazione richiede un'analisi approfondita e multidisciplinare. Comprendere il significato di una trisomia a mosaico, specialmente per cromosomi rari come il cromosoma 1, è fondamentale per una gestione informata della gravidanza.
Il Fenomeno del Mosaicismo: Una Panoramica Generale e la Sua Base Biologica
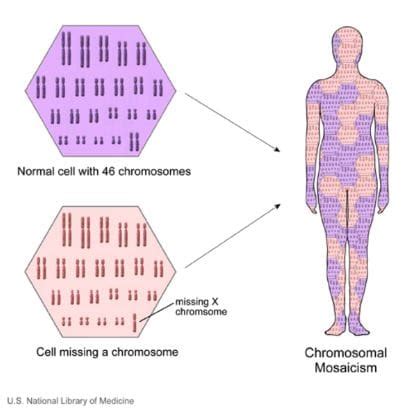
Si parla di mosaicismo quando una stessa persona ha dentro di sé cellule con un patrimonio genetico diverso. Questa condizione implica che una parte delle cellule può essere sana, mentre un'altra parte può essere affetta da un'anomalia cromosomica. Alla base del mosaicismo c’è un errore nella divisione cellulare che si verifica durante lo sviluppo embrionale, specificamente un errore mitotico post-zigotico precoce in un embrione inizialmente diploide normale, con comparsa di una linea cellulare anomala durante le prime divisioni cellulari. Un altro fenomeno che può portare al mosaicismo è il trisomy rescue, ovvero la ricostituzione della disomia normale a partire da un concepimento inizialmente trisomico: una delle tre copie del cromosoma viene “eliminata” per ripristinare il numero corretto.
Gli effetti di questa condizione variano molto in base alla gravità e alle cellule interessate. Se le cellule affette dall’anomalia sono poche, è possibile che gli effetti sull’individuo siano limitati. Qualora fossero la maggioranza, diventa molto più probabile che si manifestino delle patologie. In generale, è difficile prevedere con sicurezza gli effetti di una condizione del genere, poiché la penetranza e l'espressione fenotipica dipendono dalla percentuale di cellule anomale e dalla loro distribuzione nei vari tessuti. Un’anomalia cromosomica presente nella maggior parte delle cellule è quasi equivalente a un’anomalia presente nel 100% delle cellule. D'altra parte, una bassa percentuale di cellule anomale può non avere conseguenze sull’individuo, ma può potenzialmente avere ripercussioni sulla sua prole, a seconda che le cellule germinali siano coinvolte.
I cromosomi più frequentemente coinvolti nel mosaicismo, con oltre 25 casi nelle grandi casistiche, sono il 2, 7, 8, 13, 18 e 21. I cromosomi 3, 9, 15, 16 e 20 mostrano un coinvolgimento intermedio. È importante sottolineare che le trisomie dei cromosomi 1, 4, 5, 6, 10, 11, 12, 14, 17, 19 e 22 sono le più rare.
La Trisomia a Mosaico del Cromosoma 1: Un Caso di Rara Occorrenza e le Sue Implicazioni Potenziali
Come evidenziato, le trisomie dei cromosomi 1, insieme ad altri cromosomi come 4, 5, 6, 10, 11, 12, 14, 17, 19 e 22, sono le più rare tra le anomalie cromosomiche in stato di mosaicismo. La rarità di un tale evento, come una trisomia a mosaico del cromosoma 1, aggiunge un ulteriore livello di complessità alla sua interpretazione clinica e alla previsione degli effetti fenotipici.
La gestione di un caso di trisomia a mosaico, anche quando riguarda un cromosoma meno comune come il cromosoma 1, è intrinsecamente difficile a causa della variabilità intrinseca della condizione. Un esempio di questa complessità può essere illustrato da situazioni simili che coinvolgono altri cromosomi. Ad esempio, in un contesto clinico in cui un test del DNA fetale ha restituito un risultato dubbio relativamente al cromosoma 18, seguito da un'amniocentesi che ha mostrato 9/61 nuclei positivi per trisomia 18 alla FISH, mentre il cariotipo standard e l'array CGH risultano nella norma, si evidenzia la necessità di un'ulteriore valutazione. La ripetizione della FISH da un altro operatore, che evidenzia 5/100 nuclei con 3 segnali per cromosoma 18, con una morfologica di II livello nella norma, suggerisce la presenza di un mosaicismo costituzionale molto diluito per un'aneuploidia del cromosoma 18. In tali circostanze, è impossibile definire una correlazione precisa con il fenotipo dato che non è possibile stabilire l’origine dell’aneuploidia e la sua distribuzione nei diversi tessuti. Questo principio di incertezza fenotipica, legato alla diluizione del mosaicismo e all'impossibilità di tracciare la distribuzione tissutale dell'anomalia, si applica in modo analogo alle trisomie a mosaico rare, inclusa quella del cromosoma 1.
Il Percorso Diagnostico Prenatale: Dallo Screening ai Test Invasivi
L'unico metodo per avere una diagnosi sicura del mosaicismo sono i test genetici e i test di screening prenatale. Si analizzano le cellule del feto e si verifica l’eventuale presenza di cellule con anomalie cromosomiche. In caso di esito positivo, si prosegue con ulteriori test genetici.
Il Test del DNA Fetale (NIPT) e il Mosaicismo Confinato alla Placenta (CPM)
Il NIPT è un test di screening, non diagnostico. Analizza frammenti di DNA libero circolante (cfDNA) nel sangue materno, che provengono prevalentemente dalla placenta, non direttamente dalle cellule fetali. Per capire perché il CPM possa influenzare il NIPT, è utile chiarire un aspetto spesso frainteso: il DNA circolante nel sangue materno analizzato con il NIPT non proviene direttamente dalle cellule del feto, ma dall’apoptosi, cioè dalla normale morte cellulare delle cellule del trofoblasto placentare. In pratica, il test “legge” la placenta, non il feto. Pertanto, il mosaicismo fetale e placentare e il mosaicismo confinato alla placenta possono influenzare il risultato del test del DNA fetale.
La causa più comune di falso positivo al NIPT è proprio il mosaicismo confinato alla placenta (CPM). Si parla di mosaicismo confinato alla placenta (CPM) quando una linea cellulare cromosomicamente anomala è presente esclusivamente nella placenta, mentre il corredo cromosomico del feto è normale. Il mosaicismo feto-placentare, di cui il CPM è un sottotipo, si riscontra nel 2-3% delle gravidanze. È importante sottolineare che anche quando il mosaicismo rimane confinato alla placenta e il feto è cromosomicamente normale, il CPM non è privo di conseguenze. Pur essendo nella maggior parte dei casi associato a esiti fetali normali, il CPM è stato correlato in alcuni casi a restrizione della crescita intrauterina, perdita della gravidanza o morte perinatale. Non vi è ancora una sufficiente conoscenza di quale sia la correlazione tra mosaicismo placentare (CPM) e sviluppo di ritardo di crescita intrauterino (IUGR) e/o preeclampsia (PE).
Il NIPT sembra essere più sensibile della villocentesi nel rilevare il CPM, poiché l’intero trofoblasto placentare rilascia DNA in circolo, consentendo di intercettare anche cellule anomale presenti in aree non raggiunte dal prelievo. Tuttavia, in Italia, la Società Italiana di Genetica Umana (SIGU) sottolinea che un NIPT positivo non significa che il feto sia affetto; significa che è necessario approfondire. La presenza di un gemello non vitale (vanishing twin), anche se riassorbito precocemente, può rilasciare cfDNA anomalo in circolo per settimane, alterando il risultato del NIPT.
Capire il NIPT - La tua guida per uno screening in gravidanza più sicuro
La Villocentesi e la Necessità di Conferma
Quando si esegue una villocentesi, il laboratorio analizza due componenti distinte del villo coriale: il citotrofoblasto, esaminato con il metodo diretto, e la componente mesenchimale, analizzata attraverso la coltura cellulare. Questa distinzione non è solo accademica. Un mosaicismo rilevato nel citotrofoblasto ma non nel nucleo mesenchimale del villo è generalmente un CPM; se invece è presente nel mesenchima, potrebbe essere sia confinato alla placenta che generalizzato.
Il mosaicismo cromosomico nei villi coriali viene rilevato in circa l’1-2% dei casi. Quando si riscontra questa condizione è necessario un cariotipo di conferma su amniociti per distinguere un CPM da un vero mosaicismo fetale. I dati della letteratura offrono una risposta concreta: in una grande casistica di oltre 15.000 CVS, la linea cellulare anomala si è estesa al feto nel 12,8% dei casi in cui era stato rilevato mosaicismo ai villi. Quando la villocentesi rileva un mosaicismo, è indicata un’amniocentesi nel secondo trimestre per analizzare il corredo genetico degli amniociti, che contengono cellule di origine fetale.
L'Amniocentesi: Una Finestra Diretta sul Corredo Genetico Fetale
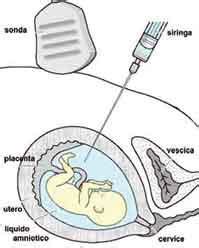
Con il termine Amniocentesi si intende il prelievo di liquido amniotico che viene effettuato, per via transaddominale, con un sottile ago sotto controllo ecografico. Tale liquido contiene in sospensione alcune cellule fetali ed alla fine degli anni '60 fu dimostrata la possibilità di coltivarle, cioè di farle crescere in vitro e poterle, quindi, studiare. Le cellule ottenute dall’amniocentesi originano dall’epiblasto della massa cellulare interna, e sono quindi più direttamente rappresentative dell’embrione rispetto a quelle della villocentesi. L’amniocentesi analizza gli amniociti, cellule di origine fetale presenti nel liquido amniotico. Nel liquido amniotico sono inoltre presenti alcune sostanze che possono essere dosate ed analizzate per particolari indicazioni.
Indicazioni all'Amniocentesi
L'amniocentesi è consigliata in diverse situazioni, tra cui:
- Alle donne che abbiano avuto un risultato positivo al test di screening prenatale (test combinato, bi test, tri test).
- Alle donne che abbiano avuto figli con malattie cromosomiche o difetti del tubo neurale, come la spina bifida.
- Alle donne con una età superiore ai 35 anni che non si siano sottoposte ai test di screening del primo trimestre. L’incidenza di anomalie dei cromosomi aumenta in parallelo con l’età materna, ma anche nelle donne giovani si possono avere casi di anomalie. Ad esempio se la madre ha 20 anni le probabilità che nasca un bimbo Down sono di 1 : 1.105, se ha 30 anni 1 : 723, se ne ha 40 1 : 92. Il rischio complessivo per tutte le anomalie dei cromosomi è invece all’incirca il doppio.
- In caso di familiari (storia familiare) con specifiche malattie genetiche o pregressa aneuploidia fetale.
- In caso di risultati dell'ecografia che facciano sospettare la presenza di anomalie fetali.
- Alterazioni cromosomiche nei genitori.
- Ricerca di agenti infettivi.Nel terzo trimestre, fra la 32a e la 39a settimana di gravidanza, l'amniocentesi può essere utilizzata anche per valutare la maturazione dei polmoni del feto nelle donne in cui si consideri di anticipare il parto prima del termine della gravidanza. A prescindere dalle indicazioni mediche, la donna e il partner sono liberi di decidere se effettuare o non effettuare il test, dopo averne parlato con il medico.
Esecuzione e Tempistiche
Il prelievo di liquido amniotico viene effettuato per via transaddominale. Viene eseguito preliminarmente un esame ecografico per confermare l’epoca gestazionale, il numero dei feti, la vitalità e la morfologia di questi, la quantità di liquido amniotico e la localizzazione placentare. Tutta la procedura viene eseguita sotto controllo ecografico per diminuire i rischi di fallimento della procedura o di danni occasionali al feto che in questo modo sono rarissimi. Una volta giunti in cavità si aspirano 15 cc di liquido amniotico che vengono inviati al laboratorio con le indicazioni del caso. Nelle gravidanze gemellari, in presenza di due diversi sacchi amniotici, la procedura è sostanzialmente la stessa, ma l’operatore esperto è generalmente in grado di eseguire entrambi i prelievi con un’unica inserzione attraversando le membrane che dividono i gemelli. Ciò naturalmente riduce il rischio di aborto perché si effettua una sola puntura dell’utero. Il liquido amniotico è formato prevalentemente da urina fetale e viene, quindi, nuovamente reintegrato in tempi rapidi. L’esame dura circa un minuto ed è praticamente indolore se eseguito da mani esperte.
L’esame viene generalmente eseguito a partire dalla 15° settimana di gestazione. Si ritiene che questo sia il periodo ideale, sia per la presenza di una quantità ottimale di liquido amniotico, che per il riscontro di minori fallimenti colturali dovuti all’elevato numero di cellule fetali presenti nel liquido in quest’epoca. L’amniocentesi può comunque essere eseguita sino al termine della gravidanza.
Rischi e Precauzioni
Il rischio di aborto viene generalmente quantificato nello 0,5-1%, cioè un caso ogni 100-200 procedure. Il rischio è legato soprattutto alla rottura delle membrane che può occorrere entro 2-3 giorni dall’esame. Tale rottura appare legata principalmente ad una intrinseca fragilità delle membrane oppure ad infezioni latenti che si riaccendono con il trauma del prelievo. Qualora il primo tentativo di prelievo non avesse successo è possibile introdurre nuovamente l’ago ma ciò naturalmente aumenta i rischi. Altre possibili complicanze sono le infezioni (amniotiti), lo scolo intermittente di liquido ed i danni fetali (eccezionali). Nonostante l’apparente semplicità dell’esame l’incidenza di aborto e complicanze è strettamente legata alla capacità ed all’esperienza dell’operatore ed il rischio può tranquillamente essere ridotto od aumentato in modo significativo.
Per minimizzare i rischi, si consiglia di assumere, dal giorno precedente l’esame, un antispastico per ridurre l’eventuale insorgenza di contrazioni uterine, e di rimanere a riposo a casa per 2-3 giorni. È sconsigliabile praticare l’esame in presenza di episodi febbrili della madre ed in caso di minaccia di aborto in corso. Nel caso di madre Rh negativa è opportuno eseguire dopo l’amniocentesi l’immunoprofilassi anti-D per prevenire la possibile formazione di anticorpi anti Rh.
Analisi Citogenetica e Molecolare del Liquido Amniotico
L’indicazione principale all’amniocentesi è rappresentata dallo studio dei cromosomi fetali. Questi sono presenti nelle cellule del nostro organismo nel numero di 46 o, per meglio dire, di 23 coppie di cromosomi omologhi che derivano in parti uguali dal padre e dalla madre. I cromosomi possono presentare delle anomalie di numero o struttura, vi possono essere quindi cromosomi in più o in meno (aneuploidia), oppure con anomalie della loro struttura. Il caso più frequente e conosciuto è la Sindrome di Down o Mongolismo che è causato dalla presenza di 47 cromosomi con un 21 in eccesso, infatti viene anche definita Trisomia 21. Altre aneuploidie sono la Trisomia 18 (S. di Edwards), la Trisomia 13 (S. di Patau), la Monosomia X (S. di Turner), etc. I risultati consentono, nel 99% dei casi, di escludere o accertare (diagnosticare) numerose malattie genetiche, anche se non possono identificarle tutte.
La diagnosi può essere fatta attraverso la coltura delle cellule fetali presenti nel liquido amniotico e l’osservazione al microscopio dei cromosomi (tecnica tradizionale). Per la determinazione del cariotipo fetale con tecnica tradizionale è necessaria la coltura delle cellule ricavate dal liquido amniotico e la successiva valutazione dell’assetto cromosomico attraverso l’analisi al microscopio. Le colture cellulari richiedono tempi di attesa di circa 15-18 giorni, a volte anche di più perché le cellule si moltiplicano con lentezza o è addirittura possibile che non crescano adeguatamente, il che richiede la ripetizione del prelievo per allestire una nuova coltura. Questa evenienza, estremamente rara e quantificabile all’incirca nello 0,5% dei casi, accade circa una volta ogni 100-150 prelievi.
Più recentemente, si utilizzano metodiche di biologia molecolare per un'analisi più rapida e dettagliata:
- QF-PCR (Quantitative Fluorescent Polymerase Chain Reaction): Questa è una tecnica molecolare rapida che consente di ottenere in sole 48 ore una valutazione estremamente attendibile relativa alle principali aneuploidie (es. cromosomi 13, 18, 21, X, Y). Per ridurre i disagi derivanti dalla lunga attesa, questa tecnica è spesso eseguita di routine per fornire un esito preliminare rapido, con un’attendibilità del 95% circa.
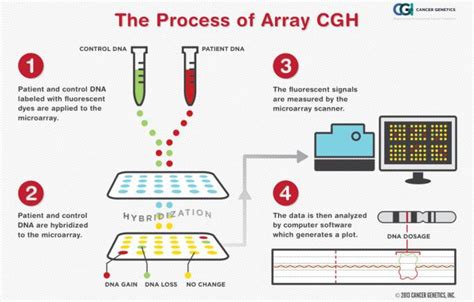
- Microarray-Comparative Genomic Hybridization (CMA o cariotipo molecolare): L’introduzione della tecnica microarray CGH, basata sulla biologia molecolare, consente di effettuare un approfondimento diagnostico di secondo livello che si esegue per integrare l’esame tradizionale. Con questa tecnica non è necessaria la coltura cellulare, e quindi i tempi diagnostici sono più brevi (3-5 giorni), consentendo una risposta più veloce anche in epoca gestazionale avanzata e annullando il rischio di fallimento della coltura cellulare. L’analisi con microarray consente di identificare, oltre alle tradizionali aneuploidie, alcune patologie derivanti da alterazioni cromosomiche submicroscopiche (ad esempio la Sindrome di DiGeorge, la cri-du-chat, la Prader-Willi, etc.) non evidenziabili con il cariotipo tradizionale. È particolarmente indicata in feti con severo ritardo di crescita, malformazioni, Traslucenza Nucale molto elevata ed a supporto dello studio citogenetico tradizionale. L’American College of Obstetricians and Gynecologists ha suggerito che l’uso dell’analisi con microarray è in grado di identificare quasi tutte le anomalie individuate dallo studio tradizionale del cariotipo fetale ed anche altre, ma non tutte, specifiche malattie genetiche. Questo test potrebbe individuare casi di consanguineità fra i genitori o di non-paternità. Possono essere diagnosticate malattie la cui gravità ed epoca di insorgenza sono molto variabili e non è possibile prevederle per il caso singolo. L’impiego dell’analisi con microarray richiede, quindi, una attenta consulenza genetica prima e dopo l’esame.
Si possono inoltre valutare sostanze presenti nel liquido che consentono la diagnosi di alcune malattie come i difetti del tubo neurale (tramite il dosaggio dell’alfa-fetoproteina che è un ottimo marcatore diagnostico), le anomalie del metabolismo, etc. Tramite tecniche di biologia molecolare (PCR), può inoltre essere eseguita l’analisi diretta di frammenti di DNA per la diagnosi di svariate malattie genetiche quali la talassemia, la fibrosi cistica, la Sindrome del Cromosoma X fragile, la Sordità Congenita, la Distrofia Muscolare di Duchenne-Becker, etc., i deficit metabolici e ricercare la presenza di frammenti di DNA di agenti infettivi, segno di possibile infezione fetale nei casi di Toxoplasmosi, Virus Citomegalico, Rosolia, etc. Per ricercare agenti infettivi, malattie genetiche o metaboliche, il tempo necessario per la diagnosi è compreso fra i 10 ed i 15 giorni.
Interpretazione dei Risultati dell'Amniocentesi: Il Dilemma del Mosaicismo
Anche quando l'amniocentesi analizza gli amniociti, cellule di origine fetale presenti nel liquido amniotico, non tutti i risultati che sembrano indicare un mosaicismo hanno lo stesso significato clinico. La diagnosi di mosaicismo su amniociti si classifica in base alla sua estensione:
- Livello I: viene osservata una singola cellula anomala. I dati provenienti da grandi casistiche sono chiari: nelle amniocentesi eseguite prevalentemente per età materna avanzata, circa il 3,73% dei casi presenta pseudomosaicismo a cellula singola (livello I).
- Livello II: due o più cellule anomale con la stessa anomalia cromosomica compaiono in una singola coltura o in una singola colonia, ma non in colture indipendenti. Circa lo 0,76% dei casi presenta pseudomosaicismo a cellule multiple (livello II).
- Livello III: cellule anomale con la stessa anomalia cromosomica sono presenti in due o più colture indipendenti. Solo lo 0,2% dei casi mostra un vero mosaicismo (livello III).
Lo pseudomosaicismo è uno dei limiti tecnici riconosciuti dell’analisi citogenetica prenatale. Non riflette la reale costituzione cromosomica del feto, ma può originare da errori nella divisione cellulare durante la coltura in laboratorio, o in alcuni casi dalla presenza di cellule di origine placentare o materna nel campione. Quando si rileva un livello III, o quando un livello II suscita dubbi clinici, la diagnosi non si ferma al cariotipo classico. Il vero mosaicismo fetale è raro: come visto nelle sezioni precedenti, si riscontra nello 0,1-0,2% delle amniocentesi. Riguarda più frequentemente anomalie dei cromosomi sessuali o trisomie dei cromosomi 21, 18 e 13. È importante ricordare che nella maggior parte dei casi il mosaicismo è confinato alla placenta e l’esito fetale è normale.
Discordanze e Complessità Interpretative nel Percorso Diagnostico Integrato
Nel percorso della diagnosi prenatale esistono condizioni biologiche complesse che possono rendere l’interpretazione dei risultati più articolata. Il sospetto di mosaicismo può emergere in diversi momenti:
- Discordanza tra NIPT ed ecografia: Uno dei dilemmi clinici più frequenti si presenta quando il NIPT risulta ad alto rischio ma l’ecografia è normale. In questi casi il mosaicismo, soprattutto confinato alla placenta, è una delle spiegazioni biologiche più plausibili. L'utilizzo dei test prenatali non invasivi (NIPT) con sequenziamento MPS ha determinato come conseguenza la possibilità di avere un risultato positivo per anomalie diverse dalle comuni trisomie (13, 18 e 21). Molte di queste aberrazioni non sono compatibili con la vita extrauterina.
- Discordanza tra villocentesi e amniocentesi: La villocentesi esamina le cellule del citotrofoblasto e del sinciziotrofoblasto placentare, mentre l’amniocentesi analizza gli amniociti di origine fetale. Queste due indagini possono dare risultati discordanti proprio in presenza di mosaicismo feto-placentare.
- Presenza di linee cellulari anomale a bassa percentuale: Quanto più basso è il rapporto di mosaicismo rilevato al NIPT, tanto maggiore è la probabilità che il risultato sia discordante rispetto all’esito del test diagnostico invasivo.
- Alterazioni biochimiche con esito ecografico normale: Un dato meno noto ma clinicamente rilevante è che valori anomali di marcatori biochimici del primo trimestre (come PAPP-A ridotta) in presenza di un NIPT rassicurante e un’ecografia apparentemente normale possono talvolta essere un segnale indiretto di mosaicismo.
Le condizioni di discordanza tra test di screening e test diagnostico rappresentano una minoranza dei casi. In un contesto biologico complesso come quello del mosaicismo fetale o placentare, la qualità del laboratorio e dell’interpretazione dei dati assume un ruolo centrale. L’interpretazione del DNA fetale circolante richiede familiarità con le possibili cause biologiche di discordanza, come mosaicismo confinato alla placenta, vanishing twin o anomalie cromosomiche a bassa percentuale. L’analisi del cfDNA prevede algoritmi statistici complessi che stimano la frazione fetale, la distribuzione delle sequenze cromosomiche e il rischio di aneuploidia.
L'Importanza Cruciale della Consulenza Genetica
Di fronte alla complessità dei risultati che possono emergere, soprattutto in presenza di mosaicismo, la consulenza genetica rappresenta un passaggio chiave e irrinunciabile. In presenza di condizioni come il mosaicismo, la comunicazione corretta è parte integrante della qualità del test. Il consulente genetico ha il compito di illustrare ai futuri genitori il significato dei risultati ottenuti, le possibili implicazioni cliniche, le incertezze diagnostiche e le opzioni disponibili per ulteriori approfondimenti o per la gestione della gravidanza. Questa figura professionale guida la coppia attraverso un processo decisionale informato, fornendo tutte le informazioni necessarie in un linguaggio comprensibile e sensibile. La donna e il partner sono liberi di decidere se effettuare o non effettuare il test, dopo averne parlato con il medico.
È fondamentale ribadire che un NIPT positivo non significa che il feto sia affetto; significa che è necessario approfondire. Ricordiamo che PrenatalSafe è un test di screening prenatale non invasivo e, come tale, non sostituisce la diagnosi invasiva quando indicata. La qualità del laboratorio e dell’interpretazione dei dati assume un ruolo centrale per affrontare queste condizioni.