La medicina prenatale ha compiuto passi da gigante negli ultimi decenni, passando dalla semplice osservazione morfologica a una comprensione molecolare sempre più raffinata. Al centro di questo progresso si colloca l'integrazione tra tecniche di prelievo invasivo, come la villocentesi, e metodiche di analisi genetica avanzata, quali l’Array-CGH. Questi strumenti permettono oggi di indagare con una precisione senza precedenti le basi molecolari di patologie complesse come l'epilessia, i disturbi dello spettro autistico e le disabilità intellettive.
Evoluzione storica della diagnostica prenatale: dalla villocentesi alle tecniche molecolari
Il percorso che ha condotto alle moderne tecniche di indagine genetica ha radici profonde. La villocentesi, in particolare, ha una storia che inizia nel 1966, quando Alvarez la eseguì per la prima volta per via transaddominale per la diagnosi di mola idatiforme. Solo nel 1968, Hahnemann utilizzò il prelievo dei villi coriali per la diagnosi prenatale, aprendo la strada a una nuova era. Successivamente, Rhine tentò il lavaggio della porzione inferiore della cavità uterina per ottenere cellule trofoblastiche, ma le mappe cromosomiche ottenute avevano un tasso di successo limitato (49%).
Già in quegli anni, la sfida principale risiedeva nella contaminazione del tessuto fetale con cellule materne. L'introduzione negli anni '80 della guida ultrasonica per il prelievo transcervicale rappresentò un punto di svolta, sebbene il rischio di infezioni intrauterine rimanesse una preoccupazione. Le cellule trofoblastiche sono particolarmente preziose poiché possiedono un alto indice di crescita mitotica, permettendo colture "long-term" rapide (5-7 giorni), decisamente più veloci rispetto a quelle degli amniociti.
Rischi, precauzioni e evoluzione delle tecniche di prelievo
Per molto tempo si è stimata una maggiore pericolosità del prelievo dei villi coriali rispetto all'amniocentesi. Questo dato è certo se il prelievo viene effettuato per via transcervicale, mentre per il prelievo transaddominale le differenze sembrano essere molto ridotte. Una problematica storica è la discrepanza tra il cariotipo delle cellule dei villi coriali ed il cariotipo fetale: recenti studi hanno mostrato una discordanza del 2,1%, di cui l'1,2% costituito da mosaicismi. Mentre nelle preparazioni dirette si studia il citotrofoblasto (che presenta spesso aneuploidie), nelle colture a lungo termine si esamina il cariotipo dei fibroblasti, che rispecchia più fedelmente quello fetale.
Un capitolo doloroso della storia clinica riguarda le procedure eseguite in epoche troppo precoci. La prima segnalazione di eventi malformativi, come l'ipoplasia oro-mandibolare e la focomelia, risale al 1991 (Radcliffe Maternity Hospital) in casi eseguiti tra il 50° e il 66° giorno di gravidanza. Anche Mastroiacovo, in uno studio multicentrico, segnalò un aumento della percentuale di anomalie degli arti. Sebbene tale associazione non sia stata confermata in numerosi altri studi, la prudenza resta fondamentale: ad oggi, appare prudente astenersi dalla villocentesi prima della 10^ settimana di gestazione.
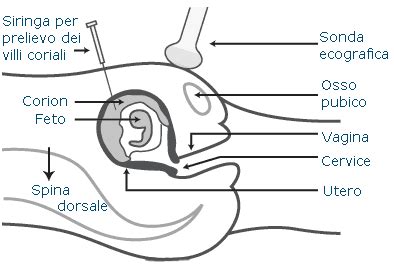
L'ecografia precedente al prelievo è l'unico strumento capace di stabilire se convenga operare o attendere. La villocentesi deve essere eseguita da mani esperte per ridurre i rischi, che mediamente si attestano tra lo 0,5% e l'1%. La tecnica di prelievo oggi adottata da centri specializzati permette, tramite l'aspirazione sotto guida ecografica, di rendere l'esame pressocché indolore e di breve durata.
L'Array-CGH: un salto di qualità nel cariotipo molecolare
La tecnica di Ibridazione genomica comparativa su microarray, meglio nota come Array-CGH, ha rivoluzionato l'approccio diagnostico negli ultimi dieci anni. La citogenetica convenzionale, pur utile, è limitata dal potere di risoluzione del microscopio: non è generalmente in grado di evidenziare alterazioni cromosomiche di dimensioni inferiori a circa 5-10 Mb. L'Array-CGH, con una risoluzione circa 100 volte superiore, permette di individuare queste micro-anomalie.
Il principio dell'Array-CGH si basa sulla comparazione quantitativa del DNA fetale (test) e di un DNA di riferimento proveniente da un soggetto sano. I due DNA, marcati con fluorocromi diversi (solitamente rosso per il test e verde per il riferimento), vengono ibridati su un supporto di vetro coperto da migliaia di sonde di DNA. L'analisi del segnale risultante permette di identificare:
- Aneuploidie: variazioni nel numero totale dei cromosomi.
- Microdelezioni e Microduplicazioni (CNV): alterazioni strutturali inferiori al limite visibile al microscopio.
What is an Array CGH?
Queste variazioni del numero di copie (CNVs), pur essendo presenti anche in individui sani, possono essere la causa diretta di patologie quando alterano l'espressione genica o interrompono sequenze regolatorie. In diagnosi prenatale, la scoperta di una CNV può portare a incertezza prognostica, rendendo indispensabile una consulenza genetica esperta.
Epilessia e disordini dello sviluppo: l'impatto clinico
L'integrazione dell'Array-CGH è diventata cruciale nello studio di fenotipi complessi. Mutazioni o riarrangiamenti nei geni deputati allo sviluppo della corteccia cerebrale possono avere gravi conseguenze, quali epilessia, comportamenti autistici, ritardo mentale e disturbi dell'apprendimento.
Studi recenti condotti su migliaia di pazienti hanno evidenziato che una percentuale significativa (intorno al 15,8%) di individui affetti da disabilità intellettive o anomalie congenite è portatrice di un'anomalia patologica identificabile tramite microarray. La ricerca si è concentrata su geni specifici e loci cromosomici correlati, tra cui:
- Il gene CDKL5, coinvolto in encefalopatie epilettiche a esordio precoce.
- Il locus 7q11.23 (associato alla sindrome di Williams-Beuren) e le relative duplicazioni.
- Le delezioni a carico del cromosoma 2q23.1.
- Le mutazioni del gene FLNA, responsabili di eterotopie nodulari periventricolari.
- Le alterazioni del gene GLUT1, causa rara di epilessia generalizzata idiopatica.
La possibilità di diagnosticare queste condizioni prima della nascita offre ai genitori informazioni preziose per le necessità future del bambino, consentendo l'accesso precoce a servizi di supporto e definendo con chiarezza il rischio di ricorrenza in gravidanze future.
Applicazioni pratiche: villocentesi come porta d'accesso
L'utilizzo dell'Array-CGH in villocentesi rappresenta oggi il "gold standard" per l'approfondimento diagnostico in presenza di segni ecografici suggestivi di patologia cromosomica, anche quando il cariotipo standard risulta normale. La procedura prevede l'estrazione del DNA fetale direttamente dai villi coriali, senza la necessità di coltura cellulare prolungata, permettendo di ottenere risposte in tempi rapidissimi (3-5 giorni).
I vantaggi di questa sinergia sono molteplici:
- Rapidità: l'esclusione della coltura cellulare riduce l'ansia del paziente e il rischio di fallimenti diagnostici.
- Sensibilità: l'individuazione di alterazioni submicroscopiche altrimenti invisibili.
- Prognosi: una migliore definizione del quadro clinico permettendo, laddove possibile, approcci terapeutici mirati (come nel caso delle encefalopatie metaboliche o genetiche).
L'esperienza dei genetisti rimane tuttavia il fattore determinante nell'interpretazione dei dati. La corretta distinzione tra varianti patologiche e varianti di incerto significato clinico (VOUS) è ciò che separa una diagnosi vaga da una guida clinica efficace. Il futuro della diagnostica prenatale risiede proprio in questa convergenza: un prelievo tempestivo, sicuro e guidato dall'ecografia, seguito da un'analisi genomica in grado di leggere il codice della vita con una risoluzione sempre più nitida.
tags: #villocentesi #array #vede #epilessia