La riproduzione umana è un processo intrinsecamente complesso, dove un delicato equilibrio di fattori genetici, ormonali e cellulari deve armonizzarsi per consentire il concepimento e lo sviluppo di una nuova vita. Quando questo equilibrio viene alterato, possono emergere difficoltà significative nel percorso verso la genitorialità. Tra le varie cause di infertilità, le anomalie cromosomiche rappresentano una sfida importante, spesso silenziosa e profonda. Una di queste è la traslocazione cromosomica, in particolare quella che coinvolge i cromosomi 14 e 21, nota come traslocazione robertsoniana 14;21. Questa condizione genetica può avere un impatto diretto sulla qualità degli ovuli e sulla loro capacità di essere fecondati o di dare origine a un embrione sano, influenzando drasticamente le prospettive di gravidanza e la salute della prole. Comprendere le meccaniche di tali anomalie e le loro conseguenze sulla maturazione ovocitaria e sullo sviluppo embrionale è fondamentale per delineare percorsi diagnostici e terapeutici adeguati nell'ambito della procreazione medicalmente assistita.
Le Traslocazioni Cromosomiche: Un Alterato Riarrangiamento del Genoma
Le traslocazioni cromosomiche sono anomalie strutturali in cui una parte di un cromosoma si stacca e si attacca a un altro cromosoma. Queste possono essere bilanciate, quando non c'è perdita o aggiunta netta di materiale genetico, o sbilanciate, quando vi è un guadagno o una perdita di materiale. Sebbene un individuo portatore di una traslocazione bilanciata sia solitamente sano, la sua riproduzione può essere compromessa a causa della produzione di gameti (spermatozoi o ovuli) con assetti cromosomici sbilanciati.
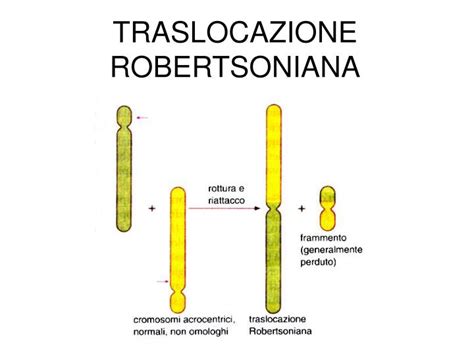
La traslocazione robertsoniana 14;21 è una forma specifica di traslocazione in cui i bracci lunghi del cromosoma 14 e del cromosoma 21 si fondono, formando un unico cromosoma derivativo. I bracci corti di questi cromosomi, che contengono scarso materiale genetico essenziale, vengono generalmente persi. Un individuo portatore di questa traslocazione bilanciata avrà un numero totale di cromosomi di 45 anziché 46, ma avrà comunque tutto il materiale genetico necessario, fuso in un unico cromosoma. Tuttavia, durante la meiosi, il processo di divisione cellulare che produce gli ovuli e gli spermatozoi, il portatore di una traslocazione 14;21 può produrre gameti con un numero anomalo di cromosomi.
I possibili esiti della meiosi in un portatore di traslocazione robertsoniana 14;21 includono:
- Gameti normali: Con un assetto cromosomico completo e senza la traslocazione.
- Gameti portatori bilanciati: Contengono il cromosoma traslocato, ma con un corredo genetico completo e bilanciato.
- Gameti con monosomia 14 o 21: Mancanza di un cromosoma essenziale, spesso letale per l'embrione.
- Gameti con trisomia 14 o 21: Presenza di un cromosoma in eccesso. La trisomia 21 è nota come sindrome di Down.
La produzione di gameti aneuploidi, ovvero con un numero anomalo di cromosomi, è la principale causa di ovuli non fecondabili o di embrioni con scarse probabilità di impianto e di sviluppo sano. La traslocazione 14;21, in particolare, è una delle traslocazioni robertsoniane più comuni e porta a un rischio significativamente aumentato di avere figli con sindrome di Down dovuta a traslocazione, nonché un aumentato rischio di aborti spontanei ricorrenti dovuti ad altre aneuploidie letali.
L'Impatto delle Anomalie Cromosomiche Sull'Ovocita e la Fecondazione
Quando si parla di ovuli non fecondabili a causa di anomalie genetiche come la traslocazione 14;21, il problema non è necessariamente legato alla maturazione nucleare dell'ovocita, che potrebbe apparire morfologicamente maturo (stadio MII), ma piuttosto alla sua "dotazione cromosomica non corretta". Un ovulo con un'anomalia cromosomica significativa è intrinsecamente compromesso nella sua capacità di supportare le prime fasi dello sviluppo embrionale, rendendolo, di fatto, non adatto alla fecondazione efficace o a un successivo impianto.
Il processo di formazione degli ovociti è complesso, a partire dalle prime fasi dello sviluppo embrionale, gli ovociti attraversano diverse fasi durante la vita prenatale e infine arrestano temporaneamente il loro sviluppo fino all’inizio della pubertà. La qualità di un ovocita, che si può definire come la sua capacità di produrre un embrione, supportare le prime fasi di sviluppo dello stesso per poi generare una gravidanza, concorre in tre eventi biologici fondamentali: la maturazione epigenetica, la maturazione citoplasmatica e la maturazione nucleare. Ad oggi, con la sola osservazione morfologica, si può esclusivamente valutare il grado di maturazione nucleare, per cui si definisce un ovocita come GV, MI o MII. Tuttavia, una traslocazione cromosomica come la 14;21 va oltre la maturazione nucleare visibile, compromettendo la vera qualità genetica dell'ovulo. Anche se l'ovocita raggiunge lo stadio di maturazione MII (metafase II), un'alterazione cromosomica al suo interno può impedirne una corretta fecondazione o uno sviluppo embrionale vitale. Questo significa che, anche se l'ovocita può essere inseminato, l'embrione risultante sarà aneuploide e avrà scarse probabilità di impianto o di un esito positivo della gravidanza. Nella maggior parte dei laboratori di FIV, gli ovociti immaturi vengono solitamente scartati, ma un ovulo geneticamente anormale, anche se maturo, presenta sfide ancora più complesse. Non esistono misure in sé che una donna possa adottare per migliorare il tasso di maturazione degli ovociti da un punto di vista genetico; in questi casi, la soluzione risiede nella selezione degli embrioni geneticamente sani.
Aneuploidie ed anomalie cromosomiche
La Riserva Ovarica: Un Indicatore Cruciale, ma Non Assoluto, della Fertilità
La riserva ovarica, pur non misurando direttamente la qualità degli ovociti e dei follicoli, è un indicatore della potenziale fertilità della donna. Essa quantifica la quantità dei follicoli presenti nelle ovaie e tende a diminuire con l’avanzare dell’età, in particolar modo dopo i 35 anni, quando si riduce anche la qualità dei follicoli. La contemporanea riduzione della quantità e della qualità determina una diminuzione delle possibilità di ottenere una gravidanza anche con le tecniche di riproduzione assistita.
La riserva ovarica di ogni bambina, circa 7 milioni di follicoli, si costituisce prima di nascere, alla 20a settimana di gestazione materna. Subito dopo, però, inizia a diminuire per fenomeni di atresia (morte) cellulare, tant'è che alla nascita la stessa bambina avrà solo 2 milioni di follicoli. La scomparsa dei follicoli continuerà negli anni successivi.Nei casi invece in cui si verifica una prematura o precoce riduzione della riserva ovarica prima dei 35 anni, la riduzione quantitativa dei follicoli e degli ovociti non sempre si associa a una riduzione qualitativa degli stessi, data la giovane età della donna. Tuttavia, anche in queste circostanze, fattori genetici come la traslocazione 14;21 possono compromettere la qualità ovocitaria indipendentemente dalla quantità disponibile, rendendo la questione della qualità ancora più preminente.
È difficile accorgersi della progressiva riduzione della riserva ovarica perché non si manifesta con sintomi evidenti; i cicli sono regolari, solo raramente si riscontra una riduzione dell’intervallo fra un ciclo ed un altro e una lieve riduzione del flusso mestruale. I test più specifici e sensibili per misurare la riserva ovarica sono il conteggio dei follicoli antrali (AFC), eseguito con ecografia transvaginale, e il dosaggio ematico dell’ormone antimulleriano (AMH), prodotto dai follicoli pre-antrali.Il conteggio dei follicoli antrali si esegue tra il terzo e il quinto giorno del ciclo. Se ecograficamente nelle ovaie si rilevano più di 10 follicoli antrali (sommando i follicoli di entrambi le ovaie), vuol dire che la riserva ovarica è corretta; se, al contrario, ce ne sono meno di 7, la riserva ovarica è bassa. Con una conta follicolare bassa, la possibilità di una gravidanza naturale o dopo fecondazione in vitro è ridotta.
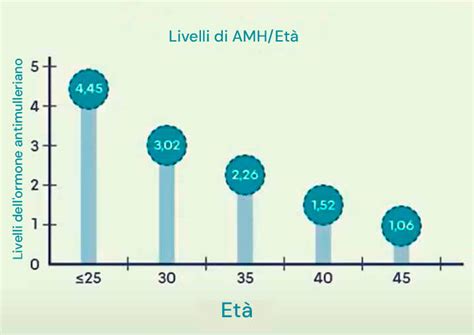
L’ormone anti-Mülleriano (AMH) può essere misurato sul siero in qualsiasi giorno del ciclo. Viene prodotto dai follicoli pre-antrali e ha la funzione di inibire la maturazione dei follicoli primordiali in antrali; infatti, in assenza di AMH, la crescita follicolare aumenta causando l’esaurimento precoce della riserva ovarica. Un valore alto (superiore a 3,1 ng/ml) è indicativo di una riserva ovarica alta. Un valore basso (meno di 1 ng/ml) è indicativo di una riserva ovarica diminuita, di una vita fertile più breve e di una possibile menopausa precoce. I medici possono anche misurare i livelli di ormone follicolo-stimolante (FSH) e di estrogeni nel sangue in un determinato momento durante il ciclo mestruale. Livelli innalzati di ormone follicolo-stimolante e livelli inferiori di estrogeni all’inizio del ciclo mestruale suggeriscono un problema degli ovuli.
Le conseguenze di una bassa riserva ovarica sono una riduzione delle chance di gravidanza spontanea e una riduzione delle chance di gravidanza da PMA, poiché più ovociti recuperiamo con una tecnica di FIVET/ICSI, più embrioni avremo e più chance di gravidanza avremo. Quindi, un basso recupero purtroppo "pesa" sull’esito della PMA. Inoltre, può determinare un’età della menopausa un po’ più precoce rispetto alla media italiana (50 anni). Le cause note di una riserva ovarica ridotta includono interventi chirurgici sull’ovaio, endometriosi, trattamenti di radio o chemioterapia, familiarità e genetica. Tuttavia, è essenziale ricordare che il miglior indicatore della fertilità di una donna è la sua stessa età, in quanto la riserva ovarica è influenzata dall’età biologica, condizionata dal processo d’invecchiamento.
La Maturazione Ovocitaria e la Sua Valutazione nei Trattamenti di Riproduzione Assistita
Ottenere un ovocita maturo per la fecondazione è un passo necessario per l’inizio del processo riproduttivo. Normalmente, l’85% degli ovociti recuperati dopo un ciclo di stimolazione ovarica sono ovociti maturi e sono quindi adatti al trattamento con la tecnica ICSI. Il restante 15% degli ovociti è immaturo e nella maggior parte dei laboratori di FIV solitamente viene scartato, purché la risposta ovarica rientri nei risultati di recupero di un numero di ovociti considerato normale. Questo non dovrebbe ridurre la possibilità di gestazione.
Nei trattamenti di riproduzione assistita, non esiste un follicolo dominante, ma i follicoli presenti vengono prelevati per recuperare gli ovociti prima che vengano rilasciati. Questi ovociti recuperati a volte non sono maturi e richiedono una maturazione in vitro. Una delle possibili cause può essere una risposta non ottimale al picco di ormone luteinizzante (LH), che è l’ormone responsabile della maturazione degli ovociti. Ciò può essere dovuto a vari fattori, come l’età. L'ovulo immaturo non è adatto alla fecondazione perché la sua dotazione cromosomica non è corretta.
La “qualità” di un ovocita è una caratteristica multifattoriale. A definirla concorrono, come detto, tre eventi biologici fondamentali: la maturazione epigenetica, la maturazione citoplasmatica e la maturazione nucleare. Ad oggi, con la sola osservazione morfologica, i biologi possono esclusivamente valutare il grado di maturazione nucleare, classificando un ovocita come GV (vescicola germinativa), MI (metafase I) o MII (metafase II). La fase MII è lo stadio ottimale per la fecondazione. Tuttavia, essere in stadio MII è un dato grezzo che non fornisce ulteriori informazioni circa le potenzialità specifiche dell'ovocita, in particolare sulla sua integrità genetica o sulla sua maturazione citoplasmatica ed epigenetica. Le anomalie cromosomiche, come una traslocazione 14;21, non sono rilevabili tramite la semplice osservazione morfologica.
Non esistono esami che chiariscano totalmente quelle che sono le potenzialità di un ovocita al di là della sua maturazione nucleare. La comunità scientifica è al lavoro quotidianamente per delucidare quanto più possibile questi aspetti complessi. Pertanto, un ovocita che appare perfettamente maturo dal punto di vista nucleare potrebbe comunque presentare difetti a livello citoplasmatico, epigenetico o, più criticamente, cromosomico, rendendolo incapace di sostenere lo sviluppo di un embrione sano. Questa complessità spiega perché, a volte, anche con un numero elevato di ovociti maturi, la qualità degli embrioni ottenuti possa essere scarsa o il tasso di impianto basso, come nel caso di coppie portatrici di traslocazioni.
Risposta Ovarica alla Stimolazione e Impatto sul Successo della FIVET/ICSI
Il processo di fecondazione in vitro (FIVET) include quasi sempre il trattamento di stimolazione ovarica. Lo scopo è quello di favorire la maturazione di più di un uovo, che è ciò che avviene naturalmente, per ottenere un numero maggiore di ovuli e aumentare le probabilità di gravidanza. La risposta a questa stimolazione varia da una donna all'altra a seconda delle qualità individuali, del programma di cura indicato, dello stato di fertilità della donna, ecc.
Si possono distinguere tre tipi di donne in base alla loro risposta alla stimolazione ovarica:
- Low responders: Donne da cui è stato possibile ottenere solo un massimo di 3-5 ovuli dopo la puntura follicolare. In questo gruppo si trovano donne con una bassa riserva ovarica, generalmente dovuta all'età, e anche quelle con alcune patologie che impediscono di ottenere un numero maggiore di ovuli.
- Normoresponders: La maggior parte delle donne rientra in questo gruppo, con un numero di ovuli ottenuto compreso tra 6-7 e 9-10 per ciclo.
- Hyperresponders: Donne da cui si possono ottenere in media 20 ovociti per ciclo, spesso giovani donne senza problemi di fertilità (ad esempio, le donatrici di ovuli).
È molto importante che, durante il periodo di stimolazione ovarica, la donna sia sottoposta a ecografie e controlli analitici da parte di uno specialista. In questo modo, il ginecologo potrà valutare la risposta dell'ovaio al farmaco ormonale somministrato e aggiustare la dose se necessario. Questo significa anche monitorare la dimensione follicolare (quando un follicolo è lungo circa 16-18 mm, si stabilisce che si è sviluppato a sufficienza per contenere un ovocita maturo) e la concentrazione di estradiolo nel sangue (ogni follicolo maturo corrisponde a circa 200-300 pg/ml di estradiolo) per programmare la puntura follicolare al momento giusto.
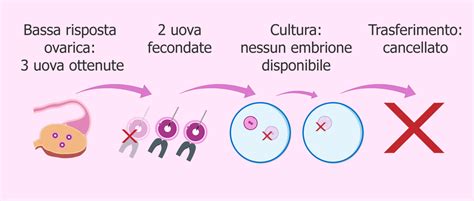
Tuttavia, il numero di ovociti recuperati dopo la puntura ovarica può essere inferiore al numero di follicoli visti nelle ecografie, poiché non tutti i follicoli contengono un ovocita o alcuni ovociti ottenuti possono essere immaturi.La questione fondamentale, però, non è solo la quantità, ma la qualità degli ovuli. Sebbene un maggior numero di ovuli aumenti le probabilità di creare embrioni vitali, se gli ovuli ottenuti non sono di buona qualità, sarà più difficile ottenere il concepimento, anche se ne sono stati estratti molti. Al contrario, con meno ovuli, ma di alta qualità, è probabile che si ottenga almeno un embrione in grado di impiantarsi. Questo è particolarmente vero per i portatori di traslocazioni cromosomiche: un'elevata quantità di ovociti può essere ottenuta, ma una percentuale significativa di questi potrebbe essere geneticamente anormale, rendendoli di fatto di "scarsa qualità" ai fini riproduttivi.
È importante anche notare che il numero di ovuli non sempre corrisponde al numero di embrioni. Degli ovociti maturi ottenuti, non tutti si fecondano correttamente e, tra quelli fecondati, alcuni si bloccano durante lo sviluppo embrionale. Questo sottolinea l'importanza di ottenere un buon numero di ovuli di qualità per avere un maggior numero di embrioni vitali, che possano essere vitrificati e trasferiti in cicli successivi.
Strategie e Trattamenti per le Difficoltà Riproduttive: Dalla PMA alla Diagnosi Genetica Preimpianto
Di fronte a una riserva ovarica ridotta o a problemi di qualità ovocitaria, come quelli che possono derivare da una traslocazione cromosomica 14;21, i percorsi terapeutici devono essere attentamente personalizzati. Se si desidera una gravidanza e la riserva ovarica è ridotta, si consiglia come prima cosa di controllare l’ovulazione, utilizzando i kit che prevedono l’ovulazione o di iniziare un monitoraggio ecografico del follicolo al fine di individuare il momento migliore per concepire. Se nonostante ciò non avviene il concepimento, è necessario l’aiuto di un medico esperto in sterilità che può consigliare le migliori tecniche disponibili per aumentare le possibilità di concepimento.
I trattamenti di procreazione medicalmente assistita (PMA) rappresentano spesso l'unica via per queste coppie. L'obiettivo dei trattamenti di stimolazione ovarica è quello di ottenere lo sviluppo di molteplici follicoli invece di soltanto uno o due, come avviene naturalmente in un ciclo mestruale. Nella fecondazione in vitro (FIVET), questi trattamenti servono a ottenere un numero sufficiente di ovociti da poter fecondare e ottenere almeno un embrione che possa essere trasferito. Trattamenti come la fecondazione in vitro o l’utilizzazione di ovuli donati possono essere suggeriti. Se invece si desidera procrastinare la gravidanza, si può prendere in considerazione la possibilità di sottoporsi a una procedura di preservazione della fertilità.
Per le donne con una bassa risposta alla stimolazione ormonale, una delle situazioni più complesse nel mondo della riproduzione assistita, esistono diverse opzioni. Queste includono trattamenti con androgeni, inseminazione artificiale, protocolli specifici di stimolazione o l'accumulo di ovociti mediante cicli di vitrificazione. Quest'ultima è un'opzione che può aiutare a ottenere un numero ottimale di ovuli da utilizzare in un singolo tentativo di FIVET.
Tuttavia, quando la causa principale risiede in un'anomalia cromosomica come la traslocazione 14;21, la strategia più efficace e spesso raccomandata è la Diagnosi Genetica Preimpianto (PGT). In particolare, si utilizza il PGT per riarrangiamenti strutturali (PGT-SR). Questa tecnica analizza gli embrioni ottenuti tramite fecondazione in vitro per individuare quelli con alterazioni genetiche e cromosomiche, consentendo di selezionare per il trasferimento solo gli embrioni geneticamente normali o, nel caso di traslocazioni, quelli con un assetto cromosomico bilanciato. Questo approccio aumenta significativamente le probabilità di successo dell'impianto, riduce il rischio di aborti spontanei e, crucialmente, minimizza il rischio di gravidanze con feti affetti da sindromi cromosomiche come la sindrome di Down dovuta a traslocazione.
Presso centri specializzati, come Equipo Juana Crespo, l'approccio è quello di fornire una visita diagnostica iniziale per la fertilità più completa, dalla quale viene elaborata l'intera strategia per raggiungere la gravidanza. Questo include non solo la valutazione della riserva ovarica e della maturazione ovocitaria, ma anche uno studio approfondito di eventuali fattori genetici, maschili (poiché il fattore maschile è direttamente coinvolto nel 47% dei casi di sterilità e nel 30% dei casi di infertilità) o uterini (l'utero è una delle principali cause di infertilità, tra cui i fallimenti dell'impianto e gli aborti spontanei ricorrenti). Possono essere considerati trattamenti innovativi come il plasma ricco di fattori di crescita per ottenere i migliori risultati e favorire una gravidanza sana e senza complicazioni, e stimolazioni altamente personalizzate, adattate ai profili ormonali di ciascun paziente.
È fondamentale che le pazienti, specialmente quelle con storie di insuccessi ripetuti o con fattori di rischio genetici noti, discutano apertamente con i loro medici e gli embriologi. La comprensione della qualità ovocitaria e embrionale, per quanto complessa sia la sua valutazione completa, è cruciale. Sebbene non vi siano esami di routine per valutare aspetti come la maturazione epigenetica o citoplasmatica, la conoscenza approfondita del proprio caso, inclusa l'eventuale presenza di anomalie cromosomiche strutturali, è la chiave per un percorso terapeutico informato e mirato.
tags: #traslocazione #14 #21 #ovuli #non #fecondabili