La ricerca scientifica sugli embrioni umani, in particolare quella che coinvolge le cellule staminali embrionali (CSE), rappresenta una delle aree più complesse e dibattute della bioetica contemporanea. Mentre le cellule staminali embrionali offrono la speranza per nuove terapie capaci di rivoluzionare la medicina, il loro utilizzo nella ricerca suscita un acceso dibattito che coinvolge scienziati, eticisti, legislatori e il pubblico. Molti paesi hanno scelto di regolare la ricerca sulle cellule staminali embrionali in modi molto diversi, riflettendo la profonda divergenza di opinioni che emerge non appena l'argomento viene introdotto in pubblico.
Al centro di questa discussione vi è una questione fondamentale: quali sono esattamente i temi etici e perché è così difficile trovare un accordo? Quali sono i punti più controversi? Per comprenderlo, è necessario addentrarsi nella natura stessa dell'embrione umano e nelle implicazioni delle sue manipolazioni scientifiche, esplorando le diverse prospettive che animano il confronto e le rapide evoluzioni tecnologiche che continuano a sfidare i confini del possibile e dell'accettabile.
Le Cellule Staminali Embrionali: Promesse Terapeutiche e Dilemmi Fondamentali
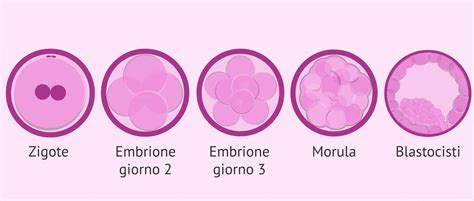
Le cellule staminali embrionali (CSE) sono un tipo di cellule primariamente composte da quelle presenti nella blastula umana, uno dei primi stadi della vita. Una blastula è una struttura formata da circa 100 cellule che si sviluppa da un ovulo fecondato e può sopravvivere per un tempo limitato prima di impiantarsi nell'utero. Le CSE possiedono una straordinaria capacità di differenziarsi in qualsiasi tipo di cellula del corpo, rendendole un potenziale strumento inestimabile per la medicina rigenerativa, la comprensione delle malattie e lo sviluppo di nuove terapie.
In genere, le blastule utilizzate nella ricerca vengono estratte, purificate ed espanse in laboratori o in cliniche dove viene praticata la fecondazione artificiale. Un aspetto cruciale di questo dibattito è che ogni anno le cliniche specializzate nella fecondazione artificiale creano molte blastule che vengono poi distrutte, perché generate in soprannumero. I sostenitori della ricerca sulle CSE, in generale, ritengono che sia di gran lunga preferibile utilizzare le cellule tratte da queste blastule in soprannumero per la ricerca e lo sviluppo di trattamenti medici in grado di, potenzialmente, salvare delle vite, piuttosto che buttarle via. Questa argomentazione sottolinea un principio etico di utilità, ovvero massimizzare i benefici per il maggior numero di persone.
Tuttavia, il dibattito è animato da una profonda tensione. Le parti contrapposte sono mosse entrambe dal desiderio di proteggere la vita umana, ma le loro opinioni divergono drasticamente. Il nodo cruciale risiede in come si considera la blastula umana. Da una parte, la distruzione di una blastula per ottenerne le cellule viene considerata equivalente all’uccisione di un bambino non ancora nato. Questa tesi è avversata da chi invece ritiene che la blastula non sia tecnicamente da considerarsi un bambino, perché, in assenza di annidamento nella parete dell’utero, non avrà mai la possibilità di svilupparsi in feto. Questa prospettiva evidenzia che lo sviluppo dell'embrione è contingente a condizioni esterne e che, in assenza di tali condizioni, il suo potenziale non si realizza.
È qui che parlarne diventa importante. I dibattiti e i confronti sulle problematiche morali ed etiche che ruotano intorno alle CSE aiutano a stabilire quali norme e regole dovrebbero governare la ricerca scientifica e lo sviluppo di trattamenti medici con cellule staminali. È fondamentale rendersi conto che, sebbene le idee su cosa sia "meglio" per la società siano molto sentite da entrambe le parti del dibattito, il desiderio di tutti rimane quello di proteggere e salvaguardare la vita umana. Comprendere questo può favorire il rispetto delle opinioni diverse e l’impegno per trovare un terreno comune.
Il Dilemma Etico dello Stato Morale dell'Embrione
La ricerca sulle cellule staminali embrionali pone una questione etica intrinseca e complessa, costringendoci a scegliere tra due principi morali profondamente radicati: il dovere di prevenire o alleviare la sofferenza e il dovere di rispettare il valore della vita umana. Nel caso della ricerca sulle cellule staminali embrionali, è impossibile rispettare entrambi questi principi contemporaneamente. Per ottenere le cellule staminali embrionali, l'embrione stesso deve essere distrutto. Ciò significa distruggere una potenziale vita umana, ma al contempo, la ricerca sulle cellule staminali embrionali potrebbe condurre alla scoperta di nuovi trattamenti che allevino la sofferenza di molte persone affette da malattie gravi e debilitanti.
La domanda cruciale diventa quindi: quale principio morale dovrebbe prevalere in questa situazione? La risposta a questa domanda si trova fondamentalmente in come noi concepiamo e valutiamo un embrione. Può essere già considerato una persona, con tutti i diritti e la dignità che ne conseguono? O il suo status morale è diverso nelle fasi iniziali del suo sviluppo? Lo stato morale di un embrione è una questione complessa e altamente controversa, con diverse posizioni che cercano di definire quando e in che misura un embrione acquisisca uno status di protezione equivalente a quello di un essere umano nato.
Le principali opinioni sullo stato morale dell'embrione sono molteplici e profondamente radicate in visioni filosofiche, religiose e scientifiche:
1. L'embrione ha pieno stato morale dal momento della fecondazione
Questa prospettiva sostiene che l'embrione debba essere visto come una persona già durante la sua fase embrionale, o almeno come una potenziale persona il cui sviluppo è un processo continuo e ininterrotto. I criteri per definire una "persona" sono notoriamente poco chiari, e ogni individuo può definire in modo diverso cosa ci rende persone.
- Opinioni a favore: Lo sviluppo da ovulo fecondato a bambino è un processo continuo e ogni tentativo di stabilire un punto arbitrario per l'inizio della persona è intrinsecamente fallace. Un embrione umano è un essere umano allo stato embrionale, proprio come un neonato è un essere umano allo stato neonatale. Anche se un embrione non ne ha attualmente le caratteristiche cognitive o fisiche che associamo a una persona, presto diventerà una persona e merita lo stesso rispetto e la dignità. La sua unicità genetica e la sua traiettoria di sviluppo lo qualificano come un individuo con un potenziale intrinseco che deve essere protetto fin dal suo concepimento.
- Opinioni contrarie: Un embrione allo stadio iniziale, che non si è ancora impiantato nell'utero, non possiede le caratteristiche psicologiche, emotive e fisiche che associamo all'essere una persona. Non ha per tale motivo alcun interesse a essere protetto e, in questa fase, può essere utilizzato per il bene dei pazienti, i quali SONO persone con bisogni e sofferenze attuali. Inoltre, l'embrione non può svilupparsi in un bambino se non viene trasferito nell'utero di una donna; ha quindi bisogno di un aiuto esterno per svilupparsi. Anche in queste condizioni, le probabilità che un embrione usato per la fecondazione artificiale si sviluppi in una gravidanza riuscita sono basse. Qualcosa che può diventare una persona non dovrebbe essere trattato come se lo fosse già. Ad esempio, un candidato alla presidenza è un potenziale presidente, eppure non ha ancora i diritti di un presidente e non dovrebbe essere trattato come tale. Il potenziale, per quanto significativo, non equivale alla realtà dello stato attuale.
2. C'è un punto limite dopo 14 giorni dalla fecondazione
Questa posizione suggerisce che un embrione umano meriti una protezione speciale dopo circa 14 giorni dalla fecondazione. Questo limite temporale non è arbitrario, ma si basa su specifici cambiamenti biologici nello sviluppo embrionale.
- Motivazioni principali: Dopo 14 giorni, l'embrione non può più dividersi per formare dei gemelli. Prima di questo momento, l'embrione è ancora in grado di dividersi per diventare due o più bambini, o può smettere di svilupparsi del tutto. Questa incapacità di gemellazione è vista da alcuni come il momento in cui l'embrione diventa un "individuo" biologicamente definito. Inoltre, prima dei 14 giorni, l'embrione è privo di sistema nervoso centrale e, di conseguenza, non ha sensi né capacità di percepire dolore o sensazioni. Se è socialmente e medicalmente accettato prelevare organi da pazienti dichiarati cerebralmente morti per usarli nei trapianti, allora, per analogia, si potrebbe considerare eticamente accettabile usare embrioni costituiti da un centinaio di cellule e privi di sistema nervoso per scopi di ricerca che possono salvare vite. Infine, la fecondazione è essa stessa un processo, non un "momento" singolo e discreto. Un embrione allo stadio iniziale non è chiaramente definibile come individuo in senso stretto.
Storicamente, questa soglia dei 14 giorni ha avuto un impatto significativo sulla regolamentazione. Già nel 1984, la Human Fertilisation and Embryology Authority (HFEA) inglese ha raccomandato un limite di 14 giorni dalla fecondazione per la ricerca sugli embrioni. Questa restrizione temporale, apparsa per la prima volta in un documento nel 1979, è diventata legge nel 1990 nel Regno Unito e successivamente adottata da altri Paesi. Anche l’International Society for Stem Cell Research (ISSCR) ha adottato questo limite nelle sue linee guida, mantenendolo fino al 2021, quando ha proposto di allentare la restrizione in alcune circostanze. Questa proposta è stata una risposta alla nuova capacità dei ricercatori di far crescere gli embrioni oltre tale limite in laboratorio e alla consapevolezza delle informazioni potenzialmente utili che si potrebbero ottenere superandolo, riflettendo la dinamicità e l'adattabilità delle linee guida etiche di fronte al progresso scientifico.
ABORTO: fra morale, scienza e legge
3. Lo stato morale dell'embrione cresce con il suo sviluppo
Questa prospettiva progressiva suggerisce che l'embrione merita una protezione dal momento in cui lo sperma feconda l'ovulo, ma il suo stato morale aumenta gradualmente con il suo svilupparsi in una figura umana riconoscibile e funzionale.
- Opinioni a favore: Ci sono diverse fasi dello sviluppo che potrebbero godere di un maggiore stato morale. Tra queste, l'impianto dell'embrione nella parete uterina dopo circa sei giorni dalla fecondazione, momento in cui si stabilisce una connessione biologica più profonda con la madre. Un'altra fase significativa è la comparsa della stria primitiva, le origini del sistema nervoso, dopo circa 14 giorni. Si può anche considerare la fase in cui il bambino potrebbe sopravvivere se nato prematuro, o infine, la nascita stessa. Tendiamo ad avere una considerazione diversa della perdita della vita a seconda della fase in cui si trovava; un ovulo fecondato prima dell'impianto nell'utero potrebbe ricevere meno rispetto di un feto umano o di un bambino nato. Un ulteriore argomento è che più della metà degli ovuli fecondati vengono persi per cause naturali. Se anche il processo naturale implica queste perdite significative, allora l'uso di alcuni embrioni in soprannumero nella ricerca scientifica non dovrebbe preoccuparci eccessivamente, in quanto la ricerca potrebbe compensare queste perdite naturali con benefici terapeutici.
- Opinioni contrarie: Se giudichiamo lo stato morale di un embrione dalla sua età o dal suo grado di sviluppo, corriamo il rischio di effettuare delle decisioni arbitrarie sulla vita umana. Per esempio, anche ammettendo che la formazione del sistema nervoso segni l'inizio della persona, non penseremmo mai che un paziente che abbia perso alcune cellule nervose a causa di un ictus sia meno umano o meno degno di protezione (tuttavia, è importante notare che esiste una differenza fondamentale tra perdere alcune cellule nervose e perdere l’intero sistema nervoso, o non averne mai avuto uno). Inoltre, proteggiamo la vita e gli interessi di una persona non perché essi abbiano un valore dal punto di vista dell'universo, ma perché sono importanti per la persona in questione. Qualunque stato morale abbia per noi l'embrione umano, la sua vita ha un valore intrinseco per l'embrione stesso e per il suo potenziale di realizzazione. Infine, se non siamo sicuri che un ovulo fertilizzato vada considerato un essere umano, allora non dovremmo distruggerlo. Questo principio di cautela è spesso paragonato all'atteggiamento di un cacciatore che non spara se non è assolutamente sicuro se il suo obiettivo sia un cervo o un uomo.
4. L'embrione non ha alcuno stato morale
Questa posizione radicale considera l'embrione come materiale organico, attribuendogli lo stesso stato di altre parti del corpo umano, almeno nelle sue primissime fasi di sviluppo.
- Opinioni a favore: Ovuli fecondati, in questa visione, non sono altro che una parte del corpo umano finché non siano sviluppati in modo da poter sopravvivere indipendentemente. L'unico rispetto dovuto alle blastocisti è quello dovuto a qualsiasi proprietà di altre persone, come le cellule o i tessuti da cui sono derivate. Se distruggiamo una blastocisti prima dell'impianto nell'utero, non la danneggiamo perché, non avendo pensieri, desideri, aspettative, intenzioni o propositi, non ha la capacità di essere danneggiata in un senso moralmente rilevante.
- Opinioni contrarie: Prelevando cellule staminali da un embrione, si impedisce a quest'ultimo di svilupparsi come potrebbe. Ciò significa che gli si impedisce di diventare ciò per cui è biologicamente e geneticamente programmato: un essere umano. Questa interruzione di un processo naturale di sviluppo è vista come un atto che priva l'embrione della sua intrinseca finalità.
Ricerca sulle Cellule Staminali Embrionali e Prospettive Religiose
Le considerazioni sullo stato di un embrione umano in fase iniziale sono profondamente influenzate anche dalle diverse dottrine religiose, che offrono prospettive variegate e spesso contrastanti sull'argomento. Queste visioni contribuiscono in modo significativo alla complessità del dibattito pubblico e alla difficoltà di raggiungere un consenso.
- Cristianesimo (Cattolicesimo, Ortodossia, Protestantesimo conservatore): Queste tradizioni religiose credono fermamente che l'embrione acquisisca lo stato di essere umano dal momento del concepimento. Questa posizione si basa sulla convinzione che la vita umana inizi con la fecondazione, quando si forma un nuovo e unico codice genetico. Di conseguenza, non ammettono alcun tipo di ricerca distruttiva sugli embrioni, ritenendo che ogni embrione abbia una dignità intrinseca e il diritto inalienabile alla vita fin dal suo inizio. Per queste fedi, la potenziale vita è già vita e merita protezione assoluta.
- Ebraismo e Islam: Al contrario, l'Ebraismo e l'Islam tendono a sottolineare l'importanza di aiutare gli altri e ritengono che l'embrione non raggiunga il pieno stato di essere umano prima di un certo periodo, spesso indicato intorno ai 40 giorni dal concepimento. Questa distinzione temporale consente quindi alcune ricerche sugli embrioni, purché queste siano condotte con scopi terapeutici e rispettino specifici principi etici e legali. Queste religioni spesso bilanciano il valore della vita potenziale con il dovere di alleviare la sofferenza e promuovere la salute della comunità esistente.
- Altre religioni: Altre tradizioni religiose e sistemi di credenze presentano posizioni diverse, che possono variare ampiamente a seconda delle interpretazioni teologiche e delle pratiche culturali. Alcune potrebbero adottare una visione più pragmatica, mentre altre potrebbero enfatizzare il principio di non nuocere o il rispetto per tutte le forme di vita.
La varietà di queste posizioni religiose evidenzia come il dibattito sulla sperimentazione sugli embrioni umani non sia solo una questione scientifica o filosofica, ma anche un profondo confronto culturale e spirituale che richiede sensibilità e comprensione delle diverse visioni del mondo.
Gli Organoidi: Mini-Organi, Grandi Questioni Etiche
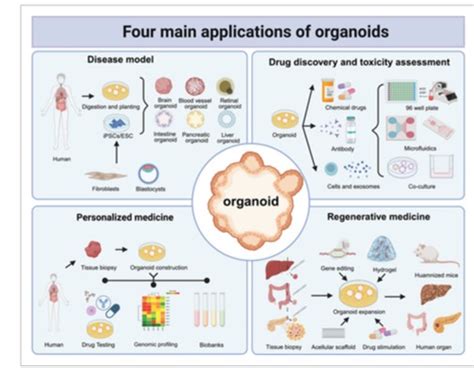
Lo sviluppo delle tecniche di manipolazione delle cellule staminali e di tecnologie di ultima generazione, come la stampa 3D, hanno consentito la realizzazione di innovazioni straordinarie, tra cui gli "organoidi". Gli organoidi sono aggregati di cellule dalla conformazione tridimensionale creati in laboratorio a partire da cellule staminali, che emulano gli organi o i tessuti umani in dimensioni ridotte. In altre parole, sono colture tridimensionali di cellule staminali che replicano la struttura e le funzioni degli organi. I ricercatori, già a partire dagli anni ’80 del secolo scorso, hanno iniziato a riprodurre in laboratorio gli organi umani; solamente in tempi più recenti, però, la ricerca ha ottenuto risultati promettenti, portando alla creazione di diversi modelli di organi umani, tra i quali fegato, intestino, reni, pancreas, cuore, ovaio, retina, pelle e anche cervello.
Oggi, gli organoidi rappresentano una delle nuove frontiere per lo studio della biologia dello sviluppo e nel campo della bioingegneria. Vengono utilizzati, ad esempio, nella ricerca oncologica e farmacologica, per la scoperta di nuove terapie, permettendo di testare l'efficacia dei farmaci in un contesto più realistico rispetto alle tradizionali colture cellulari bidimensionali. Durante l’emergenza pandemica, sono stati impiegati per lo studio del coronavirus Sars-Cov-2, per svolgere test preliminari su potenziali farmaci e per studiare l’effetto del virus su specifici organi, offrendo un modello unico per comprendere la patogenesi e l'interazione ospite-patogeno. In futuro, i mini-organi potrebbero essere utilizzati come strutture di partenza per la rigenerazione di un organo danneggiato o, addirittura, come fonte alternativa di organi da destinare ai trapianti, alleviando la cronica carenza di donatori. Inoltre, gli organoidi potrebbero essere una valida alternativa alle sperimentazioni sugli animali, riducendo l'uso di modelli viventi e migliorando la pertinenza dei risultati per la fisiologia umana.
Tuttavia, queste straordinarie potenzialità scientifiche sollevano nuove e complesse questioni etiche. Un articolo dal titolo "Organoid Ethical Typology: varieties of three-dimensional stem cell constructs and the many issues they raise in bioethics" di Gaillard, Pence & Botbol-Baum (pubblicato in un orizzonte temporale recente), si interroga proprio su questo aspetto. Secondo gli autori, se la ricerca sugli organoidi è un’espansione della ricerca sulle cellule staminali, allora l’etica degli organoidi dovrebbe essere considerata come un’espansione dell’etica della ricerca sulle cellule staminali. Poiché gli organoidi sono prodotti da cellule staminali (anche se le cellule staminali potrebbero non essere più presenti negli organoidi, poiché si sarebbero differenziate in tessuti specifici), dovrebbe essere considerato un requisito minimo per lo sviluppo etico degli organoidi il rispetto dei principi etici legati all’approvvigionamento delle cellule e alla conduzione responsabile della ricerca sulle cellule staminali.
L’approvvigionamento di cellule staminali solleva questioni diverse a seconda della fonte delle cellule e del tipo di biomateriale utilizzato. La problematica riguarda, in particolare, l’uso di embrioni in eccesso derivanti dalla fecondazione in vitro a fini di ricerca, riproponendo i dilemmi già discussi in merito alle cellule staminali embrionali. L’articolo, così come le considerazioni di Mollaki in "Ethical challenges in organoid use", distinguono vari “tipi” di organoidi in base alle loro proprietà emergenti e alle implicazioni etiche specifiche:
- Organoidi “classici”: Sono strutture tridimensionali derivate da cellule staminali che replicano, in scala ridotta, l’architettura e le funzionalità di organi specifici (ad esempio, organoidi intestinali, epatici, renali o cerebrali). Le loro implicazioni etiche riguardano principalmente la provenienza delle cellule e la gestione dei tessuti.
- “Tumoroidi”: Creati a partire da campioni tumorali (ad esempio, da biopsie), sono utilizzati per comprendere la patogenesi del cancro e per testare l’efficacia di terapie personalizzate. Le sfide etiche qui si concentrano sul consenso informato del paziente donatore e sulla gestione dei campioni tumorali.
- Organoidi cerebrali: Questi modelli che riproducono aspetti della struttura e funzione del cervello sollevano particolari e profonde preoccupazioni etiche. La principale preoccupazione è il rischio che possano sviluppare forme di attività cosciente, anche rudimentali, portando a domande sul loro status morale e sui limiti sperimentali. Se un organoide cerebrale potesse provare sensazioni o autoconsapevolezza, la sua manipolazione solleverebbe dilemmi senza precedenti.
- Organoidi delle gonadi: Sebbene lo scopo primario della ricerca di base su questi organoidi sia la comprensione dell’infertilità e dei suoi meccanismi, essi sollevano la questione del loro potenziale uso per la riproduzione. Un tale impiego avrebbe un impatto significativo sul futuro dell’umanità. L’uso di organoidi per la riproduzione equivarrebbe a un cambiamento nel loro status, da modelli sperimentali a componenti reali della vita. Tale cambiamento dovrebbe essere valutato attentamente, non solo in termini di sicurezza della procedura, ma soprattutto per le conseguenze future sull’umanità e sulla definizione stessa di riproduzione.
Vi sono anche sfide etiche che coinvolgono trasversalmente tutte le tipologie di organoidi. Queste includono il rispetto della dignità dell’essere umano da cui provengono le cellule, i rischi di commercializzazione degli stessi organoidi o delle cellule da cui sono derivati (con la possibilità che le cellule donate diventino merce di scambio commerciale), e le questioni relative alla loro conservazione presso biobanche. In particolare, per gli organoidi cerebrali, si sottolinea il pericolo di un possibile sviluppo di coscienza o sensibilità e, pertanto, si presentano domande sul loro status morale e sui limiti sperimentali. Un'altra preoccupazione riguarda il rischio dell’umanizzazione degli animali: gli organoidi umani (spesso cerebrali) potrebbero essere trapiantati in animali, creando "chimere" e sollevando interrogativi sulla natura di tali esseri e sui loro diritti. Per gli organi bioartificiali (destinati al trapianto), il passaggio dalla sperimentazione preclinica a quella clinica richiederebbe una rigorosa valutazione dei rischi per il paziente, inclusi possibili effetti imprevisti dopo il trapianto.
A preoccupare in tale prospettiva è il possibile futuro uso dei cosiddetti “embrioidi” umani, ovvero modelli embrionali creati da cellule staminali, come alternativa all’uso di embrioni umani per lo studio delle prime fasi dello sviluppo umano. Il loro status morale è incerto, e questa è una questione urgente per i ricercatori di laboratorio e i legislatori. Un aspetto critico è che i modelli embrionali, non essendo embrioni fecondati, non avrebbero tutela dalle leggi che regolano la ricerca sugli embrioni. Se potessimo creare embrioni da cellule staminali, quali sarebbero le conseguenze per l’umanità? Basterebbe come limite il divieto della clonazione e l’attuale divieto di editing ereditario del genoma per evitare la creazione di tali embrioni “sintetici” con implicazioni potenzialmente destabilizzanti per la società? Questi rischi etici evidenziano la necessità di un approccio prudenziale nella ricerca, nel rispetto della dignità del corpo umano, anche dell’embrione. Rimane, in ogni caso, un principio generale e comune a tutti i modelli: il rispetto della dignità umana.
L'Editing del Genoma Umano: Dalla "Bambina in Provetta" alle Modifiche Ereditabili
La scienza della manipolazione embrionale e genetica ha compiuto passi da gigante negli ultimi decenni, portando a scoperte che hanno radicalmente trasformato il nostro approccio alla vita e alla malattia. Facendo un salto indietro di quasi 50 anni, si può tornare al momento in cui - il 25 luglio 1978 - nacque Louise Brown: la prima bambina “in provetta”, cioè concepita in vitro. Il risultato fu possibile grazie al lavoro del biologo Robert Edwards e del ginecologo Patrick Steptoe; Edwards fu successivamente premiato con il Nobel per la Medicina nel 2010, mentre Steptoe morì nel 1994. Quello fu un momento importante nella storia della medicina in generale, e dell’embriologia in particolare, che nel giro di poco tempo ha cambiato la percezione e la gestione dei problemi legati all’infertilità, offrendo speranza a milioni di coppie.
La scienza ha poi fatto dei passi ulteriori e oggi è possibile far nascere bambini sani da coppie portatrici di malattie genetiche ereditarie, come la fibrosi cistica o l’emofilia, grazie alla diagnosi preimpianto (PGD). Questa tecnica permette di selezionare embrioni privi delle mutazioni genetiche indesiderate prima dell'impianto in utero, prevenendo la trasmissione di gravi patologie. Sebbene i benefici siano evidenti e abbiano portato a una drastica riduzione della sofferenza in molte famiglie, non sono mai mancati - né mancano tuttora - i dibattiti sull’argomento, in particolare sull'uso e il destino degli embrioni sovrannumerari.
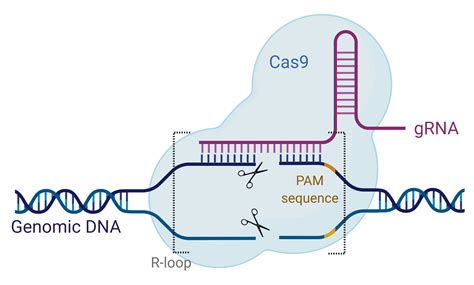
Il progresso più recente e dirompente è l'editing del genoma, in particolare con l'avvento della tecnologia CRISPR-Cas9, spesso definita "forbici molecolari". Questa tecnica offre la speranza di correggere mutazioni del DNA, anche in più punti e a livello di una singola lettera, rappresentando una potenziale cura per innumerevoli malattie. Il suo uso è stato autorizzato per alcune patologie rare ma che interessano milioni di persone nel mondo, come l'anemia falciforme e la beta-talassemia (due malattie del sangue), o l'atrofia muscolare spinale (una patologia neuromuscolare). Più di recente, è stato applicato per terapie geniche personalizzate, cioè progettate appositamente per la sequenza genetica di un paziente e non valide per nessun altro, segnando un'era di medicina di precisione.
Questo rapido avanzamento ha, tuttavia, già generato scandali e profonde preoccupazioni etiche. Alla fine del 2018, He Jiankui, un genetista cinese, ha gettato un’ombra sul mondo scientifico dichiarando di aver modificato con CRISPR i genomi di tre embrioni umani con l'obiettivo di renderli resistenti all'infezione da HIV. Tre bambini in carne e ossa sono stati i primi in cui un gene è stato ritoccato dalle ormai famose forbici molecolari, e questa azione è costata al ricercatore cinese altrettanti anni di carcere per aver violato la legge, oltre a essere stato aspramente criticato dalla comunità scientifica internazionale. In seguito si è saputo che i primi esseri umani nati già con DNA geneticamente modificato per la decisione sconsiderata dello scienziato non erano due, ma tre (una terza bimba sarebbe stata partorita qualche mese dopo le gemelle) e che l'editing del genoma apportato da Jiankui aveva dato esiti incerti e potenzialmente non controllabili. Parallelamente al ritorno di He Jiankui sulla scena scientifica a fine 2024, affermando di essere pronto a riprendere la ricerca sull'editing genetico della linea germinale umana, un'altra notizia ha attirato l'attenzione. Recenti notizie, riportate da quotidiani statunitensi, segnalano che una startup californiana, la Preventive, avrebbe lavorato in segreto alla creazione di un embrione geneticamente modificato per far nascere un bambino già protetto da una malattia ereditaria. Sebbene la Preventive abbia definito "completamente false" le accuse di aver già scelto la coppia candidata, ha ammesso di essere concentrata su ricerche per provare "la sicurezza dell'editing dell'embrione", prima che questa tecnologia possa essere attuata. L'interesse dimostrato dalla Preventive non è comunque un caso isolato, e l'obiettivo è lavorare a una prossima generazione di bambini più protetti da malattie ereditarie, ma anche con potenziali modifiche per caratteristiche come intelligenza o riduzione dell'ansia, aprendo scenari futuri ancora più complessi.
Il settore dell'editing genomico sta accelerando. A inizio anno, un editoriale di Nature, dal titolo “C’è bisogno di parlare di editing del genoma umano”, ha sottolineato la necessità di iniziare a discutere di cosa potrebbe accadere se le tecnologie di editing genomico più complesse diventassero disponibili, cosa che - stando alle previsioni - potrebbe accadere in pochi decenni. Infatti, è stato pubblicato uno studio secondo cui l’editing poligenico - cioè la modifica di più varianti genetiche in contemporanea - nel genoma di embrioni umani e cellule germinali dovrebbe essere realizzabile entro 30 anni.
Il banco di prova delle terapie geniche sono state le malattie monogeniche, cioè quelle legate all’effetto di un unico gene difettoso. Questo perché, agendo sulla specifica mutazione o inserendo una copia funzionale del gene nelle cellule target, la malattia può essere corretta. Ovviamente il passaggio dalla teoria alla pratica non è scontato, e questo è dimostrato dal fatto che non abbiamo una terapia genica per ogni malattia monogenica esistente. Le terapie avanzate approvate sono ancora poche e per un limitato numero di condizioni, ma l’obiettivo è quello di ampliare sempre di più le applicazioni, specialmente verso patologie che colpiscono molte persone nel mondo.
Tutti noi abbiamo varianti genetiche e - anche se la maggior parte di esse ha effetti limitati, se prese singolarmente - la loro combinazione può influenzare in modo significativo la predisposizione a determinate patologie. Questo ha fatto sì che la ricerca volgesse il suo sguardo verso la possibilità di modificare più varianti contemporaneamente, nella speranza di migliorare la qualità di vita di chi soffre di queste malattie. Diabete, malattia di Alzheimer, patologie coronariche, schizofrenia e molte altre malattie multifattoriali con componente genetica variabile potrebbero beneficiare di questi trattamenti. Un recente studio, pubblicato su Nature, affronta la questione dell’editing poligenico nell’essere umano e della vicinanza temporale che pare esserci con il raggiungimento di un nuovo traguardo. Le speranze di riuscirci e le capacità tecnico-scientifiche ci sono - e sono descritte da un complesso modello matematico descritto dagli autori dello studio - ma sono accompagnate da diverse preoccupazioni etiche.
Dilemmi Etici e Regolatori nell'Era del Progresso Scientifico Accelerato
La velocità a cui si muove la scienza è sostenuta da un'innovazione incessante, ma la normativa è spesso statica e lenta a cambiare, creando un divario sempre più ampio tra ciò che è tecnicamente possibile e ciò che è eticamente e legalmente permesso. Questa lentezza normativa potrebbe limitare lo sviluppo scientifico anche in caso di eventuali grandi benefici per l'umanità. D'altra parte, essa potrebbe imporre un inevitabile lasso di tempo extra per valutare le tecnologie che tanto velocemente si fanno spazio nei laboratori di ricerca di tutto il mondo, garantendo una maggiore riflessione e cautela.
Le preoccupazioni etiche più note e presenti nel dibattito pubblico fin dai primi studi sull’editing genomico riguardano il rischio di un ritorno all’eugenetica, l’alterazione non voluta di altri geni (i cosiddetti effetti off-target, che potrebbero avere conseguenze imprevedibili e dannose), e il potenziale aumento delle disuguaglianze sociali. Infatti, uno degli ostacoli principali riguarda l’accesso alle terapie avanzate, editing genomico incluso. In questo caso, se si pensa ad esempio a un ipotetico editing di embrioni, è necessario procedere con la fecondazione assistita, e questo limiterebbe le possibili applicazioni a causa dei costi elevati della procedura, rendendola accessibile solo a pochi privilegiati e accentuando le disparità nella salute.
ABORTO: fra morale, scienza e legge
Il caso di He Jiankui nel 2018 ha suscitato preoccupazione e indignazione a livello mondiale, ma ha anche evidenziato la necessità urgente di un quadro normativo chiaro e robusto, in grado di stare al passo con la scienza. Organizzazioni come l'International Society for Stem Cell Research (ISSCR) e l’Organizzazione Mondiale della Sanità (OMS) sconsigliano l’utilizzo dell’editing genomico per alterare il DNA negli embrioni umani - dato che le modifiche sarebbero ereditabili - almeno fino a quando non saranno chiariti tutti i dubbi sulla sicurezza e gli effetti a lungo termine. Al recente Terzo Summit Internazionale sull’editing del genoma umano, svoltosi a Londra, sono stati presentati i risultati di diversi studi su embrioni e altri sull’editing, segnale che la ricerca in questi ambiti è estremamente attiva e prolific.
La storia della scienza ha dimostrato che le innovazioni tecnologiche avanzano spesso più velocemente delle discussioni etiche e regolamentari. Esattamente 50 anni fa, ad Asilomar, in California, si è tenuta la famosissima conferenza sul DNA ricombinante: 140 scienziati provenienti da tutto il mondo hanno discusso su come regolamentare l’ingegneria genetica, che proprio in quegli anni scriveva i suoi primi capitoli, incuriosendo e impaurendo ricercatori e cittadini. Il tema di come la scienza si intreccia con la società, nelle sue diverse sfaccettature, resta attualissimo, a maggior ragione quando ci si ritrova - di nuovo - a parlare di etica e regolamentazione, di frenare un certo tipo di ricerche o di lasciare totale libertà.
Una delle proposte che emergono dal dibattito è quella di chiedere un’opinione a chi potrebbe trarre beneficio da queste innovazioni: i pazienti dovrebbero essere consultati, anche se inevitabilmente la loro percezione dei rischi sarà influenzata dalla gravità della patologia di cui soffrono. Un confronto tra regolatorio e opinione pubblica è anch’esso fondamentale per costruire una governance robusta e condivisa. E poi, è davvero così problematico avere un processo deliberativo lento di fronte a tecnologie con implicazioni così profonde e irreversibili? Un approccio prudenziale e riflessivo potrebbe essere l'unica strada percorribile per garantire che il progresso scientifico sia al servizio dell'umanità nel rispetto della sua dignità.
Recenti sviluppi, come l'aggiornamento delle linee guida per la ricerca sanitaria in Sudafrica a fine 2024, indicano una direzione verso una regolamentazione più attenta. Secondo le nuove direttive sudafricane, l’editing del genoma ereditabile dovrà avere "una chiara e convincente giustificazione scientifica e medica, incentrata sulla prevenzione di gravi disordini genetici e sull'immunità contro malattie gravi". Dovrà essere trasparente, sottoposto a rigorosa supervisione etica e garantire che i benefici superino chiaramente i rischi. Tuttavia, rimangono molte incertezze e la complessità di questa sfida richiede un dialogo continuo e una collaborazione stretta tra governi, ricercatori e società civile per stabilire limiti chiari e garantire che l’editing genomico venga utilizzato in modo responsabile ed etico.
tags: #sperimentazione #su #embrioni #umani