La sindrome da trasfusione feto-fetale (TTTS, dall'inglese Twin to Twin Transfusion Syndrome) rappresenta una delle complicanze più severe e complesse della medicina materno-fetale. Questa patologia è una condizione peculiare delle gravidanze gemellari monocoriali, ovvero quelle in cui i due feti condividono un'unica placenta. La sua insorgenza è legata a una dinamica emodinamica alterata che mette in comunicazione i sistemi circolatori dei due gemelli, portando a esiti clinici che, senza un intervento mirato, possono compromettere gravemente la sopravvivenza e lo sviluppo neurologico dei feti.
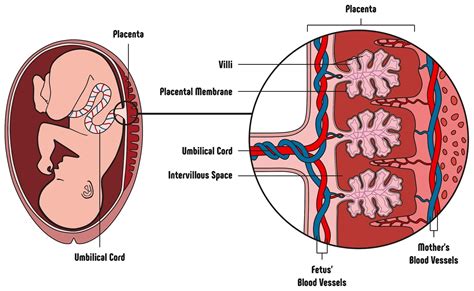
L'architettura vascolare della placenta monocoriale
Per comprendere la TTTS, è fondamentale analizzare la struttura della placenta in una gravidanza gemellare monocoriale. In questa configurazione, i due feti sono nutriti da un unico organo placentare. Sulla superficie della placenta esiste una zona, spesso definita "equatore vascolare", dove i vasi sanguigni appartenenti al territorio di un gemello entrano in comunicazione con quelli dell'altro attraverso dei collegamenti specifici chiamati anastomosi.
In condizioni fisiologiche, questo scambio di sangue avviene in modo bilanciato e bidirezionale, garantendo a entrambi i feti un apporto nutriente e un'ossigenazione adeguati. Tuttavia, quando il delicato equilibrio tra i vasi sanguigni dei due gemelli viene meno, si verifica la malattia. La sindrome TTTS è caratterizzata dal passaggio anomalo di sangue e di sostanze vasoattive attraverso le anastomosi da un gemello, definito "donatore", all'altro, definito "ricevente". Questa condizione colpisce il 10-15% delle gravidanze gemellari monocoriali e si associa ad elevata mortalità e morbilità perinatali.
Meccanismi emodinamici e squilibri fisiologici
Lo squilibrio emodinamico che ne deriva comporta conseguenze sistemiche profonde per entrambi i feti. Il gemello ricevente subisce un aumento del volume di liquidi, che si traduce in un sovraccarico cardiocircolatorio. Questo aumento del precarico è dimostrato da un flusso venoso ombelicale più elevato, che provoca un aumento di volume delle camere cardiache con il rilascio del peptide natriuretico atriale e cerebrale. Tale dinamica innesca un aumento della diuresi e, di conseguenza, il polidramnios, ovvero un eccesso di liquido nel sacco amniotico.
Parallelamente, nel gemello ricevente aumenta la produzione di endotelina, un potente vasocostrittore, con conseguente ipertensione, ipertrofia cardiaca e rigurgito valvolare. Le variazioni emodinamiche caratteristiche della TTTS possono portare alla malattia cardiaca sia funzionale che strutturale per ciascun feto. Cambiamenti nella funzione cardiaca del ricevente possono essere osservati prima dello sviluppo di TTTS conclamata e possono includere ingrossamento cardiaco, ipertrofia biventricolare, ridotta contrattilità e anomalie del tratto di efflusso del ventricolo destro.
Di converso, nel gemello donatore si verifica ipovolemia e, successivamente, una ridotta produzione di urina, il che conduce a un quadro di oligoidramnios o anidramnios, con riempimento vescicale minimo o assente. In risposta a tale carenza di perfusione, il donatore sperimenta un rallentamento della crescita, poiché il sistema circolatorio compensa dirigendo il poco sangue a disposizione verso gli organi vitali, come il cervello, a scapito di quelli secondari come i reni. Questa sovraregolazione del sistema renina-angiotensina può amplificare ulteriormente l'ipertensione e la cardiomiopatia nel gemello ricevente, attraverso la circolazione condivisa.
Lezione 20 - Fisiologia della gravidanza, fecondazione, placenta e circolazione
Diagnosi ecografica e stadiazione della patologia
La diagnosi di sindrome da trasfusione feto-fetale è esclusivamente ecografica. La valutazione ecografica dovrebbe comprendere la biometria fetale, la visualizzazione del riempimento vescicale in entrambi i feti, la misurazione del liquido amniotico (falda massima) e la valutazione della flussimetria Doppler. La diagnosi si effettua durante il secondo trimestre di gravidanza (tipicamente tra la 16a e la 24a settimana) per l'associazione di polidramnios nel gemello ricevente (falda massima > 8 cm prima della 20a settimana e > 10 cm in epoche più avanzate) e oligoidramnios o anidramnios nel donatore (falda massima < 2 cm).
Per definire lo stadio di evoluzione della patologia, si utilizza la classificazione di Quintero, che distingue la malattia in cinque stadi:
- Stadio 1: polidramnios nel ricevente e oligoidramnios nel donatore, con vescica visibile nel donatore.
- Stadio 2: polidramnios e oligoidramnios con vescica non visibile nel donatore.
- Stadio 3: polidramnios e oligoidramnios con alterazioni flussimetriche critiche (inversione o assenza del flusso).
- Stadio 4: presenza di idrope (eccesso di liquido nei tessuti) in uno o entrambi i gemelli.
- Stadio 5: morte di uno o di entrambi i feti.
Il controllo delle gravidanze monocoriali per la precoce individuazione di TTTS deve essere condotto con un'ecografia attorno alle 16 settimane di gestazione e, a seguire, le ecografie di screening devono essere ripetute ogni due settimane.
Strategie terapeutiche: il ruolo della chirurgia fetale
Fino a pochi decenni fa, le prospettive per le gravidanze colpite da TTTS erano estremamente limitate. Oggi, il trattamento di prima scelta è rappresentato dalla coagulazione laser endoscopica delle anastomosi vascolari placentari in fetoscopia. Il razionale di questo intervento è quello di interrompere lo scambio anomalo instauratosi a livello dei vasi sanguigni placentari, "bruciando" le connessioni vascolari che determinano lo scompenso e ristabilendo, di fatto, una separazione circolatoria adeguata per entrambi i gemelli.

L'intervento viene eseguito in anestesia locale materna e sedazione, in regime di ricovero. Attraverso una sottile telecamera inserita nell'utero, i chirurghi individuano i vasi "colpevoli" e, mediante una fibra laser, procedono alla coagulazione del cosiddetto equatore vascolare. Questa procedura, sebbene delicata, ha migliorato sensibilmente la prognosi: in caso di diagnosi tempestiva e trattamento adeguato, la sopravvivenza di entrambi i gemelli è possibile nel 60-70% dei casi, mentre la sopravvivenza di almeno uno dei due raggiunge l'80-90%.
Le forme precoci (prima della 28° settimana) sono quelle che traggono il maggior beneficio dalla laser-ablazione. Dopo l'intervento, è previsto un rigoroso follow-up: controllo ecografico con Doppler ogni settimana fino alla risoluzione dei segni della TTTS e normalizzazione dei valori; successivamente, i controlli vengono cadenzati ogni due settimane, prestando particolare attenzione a segni di danno cerebrale, recidiva di TTTS o sviluppo della TAPS (sindrome da anemia-policitemia gemello-gemello).
Gestione clinica e complicazioni correlate
Oltre all'intervento laser, in casi selezionati dove la fetoscopia sia impraticabile, possono essere valutate opzioni come l'amniodecompressione, ovvero il drenaggio del liquido amniotico in eccesso per ridurre la pressione intrauterina, sebbene quest'ultima non agisca sulla causa emodinamica primaria quanto la laser-terapia. È essenziale sottolineare che le gravidanze complicate da TTTS presentano un maggior rischio di rottura prematura delle membrane (pPROM) e parto pretermine, complicanze che possono associarsi alla stessa procedura chirurgica in utero.
Il monitoraggio deve essere gestito da centri altamente specializzati, dotati delle competenze necessarie per la gestione della chirurgia fetale. L'impatto della patologia sui piccoli non si esaurisce con la nascita; il follow-up postnatale è cruciale per monitorare l'evoluzione di eventuali cardiopatie o residui neurologici. La frequenza e la gravità delle complicazioni, incluse le necessità di re-intervento, devono essere discusse chiaramente con i genitori durante il percorso di consenso informato, garantendo una piena consapevolezza riguardo ai rischi e alle potenzialità del trattamento intrapreso.
tags: #sindrome #da #trasfusione #fetale #cronica