Il processo riproduttivo umano, una delle più complesse e affascinanti manifestazioni della biologia, dipende in larga misura dalla qualità e dalla maturità delle cellule germinali. Tra queste, l'ovocita femminile svolge un ruolo insostituibile, essendo la cellula riproduttiva di maggiori dimensioni dell'organismo, con una dimensione di circa 100 micrometri, ovvero un decimo di millimetro. La sua maturazione è un percorso meticoloso che, attraverso diverse fasi di sviluppo e divisione, lo prepara al momento cruciale della fecondazione. La comprensione approfondita di questo viaggio, in particolare della sua fase terminale, la seconda metafase ovocitaria, è fondamentale non solo per la ricerca biologica ma anche per l'avanzamento delle tecniche di Procreazione Medicalmente Assistita (PMA).
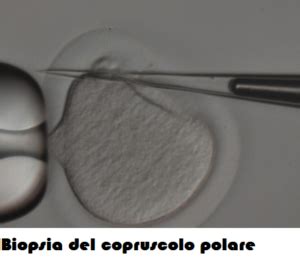
La PMA comprende l’insieme di quelle tecniche che tendono ad aiutare o favorire il processo riproduttivo, offrendo nuove possibilità per superare le sfide legate a diverse patologie femminili, maschili o di coppia. Il successo di queste tecniche è strettamente correlato alla capacità di identificare e selezionare gli ovociti con il più alto potenziale di sviluppo.
L'Ovocita: Dalla Nascita all'Ovulazione
Le cellule riproduttive femminili, gli ovociti, si formano prima della nascita, durante lo sviluppo degli organi genitali. Questo processo, noto come ovogenesi (o oogenesi o gametogenesi femminile), avviene nelle ovaie, la gonade femminile. Esso si ripete con andamento ciclico per tutta la durata della fase di fertilità della femmina, che ha inizio con il menarca e termina con la menopausa. Inizialmente, le cellule germinali primordiali dell'epiblasto invadono il sacco vitellino nella terza settimana di sviluppo embrionale per proliferare per mitosi e, nella settima settimana, si spostano e invadono le ovaie differenziandosi in ovogoni. Il loro numero aumenta per mitosi, raggiungendo il massimo al settimo mese con un totale di 7 milioni di ovogoni, ma molti inizieranno a degenerare e ad atrofizzarsi.
Quelli che sopravvivono si differenziano in ovociti primari (o ovociti I), che formano i follicoli primordiali. In questi follicoli, gli ovociti I inizieranno la prima meiosi. Tuttavia, le cellule follicolari rilasciano fattori inibitori della meiosi che bloccano questo processo nella profase I. Gli ovociti I prodotti resteranno congelati in questo stato, con una struttura nucleare chiamata vescicola germinale (VG), fino al momento della maturità sessuale. Al momento della nascita, una donna nasce con 1 o 2 milioni di ovociti. Alla pubertà, questa "riserva ovarica" si è ridotta a circa 500.000 ovociti. L'entità della vascolarizzazione follicolare può rappresentare un importante parametro clinico di selezione follicolo-ovocitaria. Durante la vita riproduttiva, il sistema riproduttivo femminile dipende dal ciclico reclutamento follicolare, dalla selezione di un unico follicolo dominante e dall’ovulazione. Solo circa 400-500 ovociti saranno ovulati fino alla menopausa.
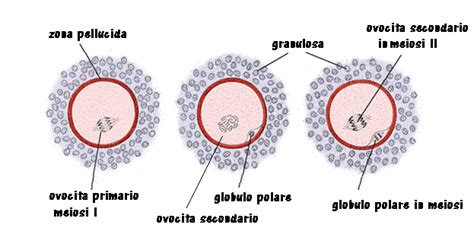
Al raggiungimento della maturità sessuale, grazie all’azione di alcune glicoproteine, chiamate gonadotropine e prodotte dalla ghiandola ipofisaria, l’ovocita primario, circondato da cellule dette follicolari, riprende il processo maturativo. La prima divisione meiotica, detta di carattere riduzionale, porta alla formazione di una cellula aploide più grande, l'ovocita secondario (o ovocita II), e una più piccola, inerte, chiamata globulo polare primario. Il globulo polare primario, pur avendo un corredo cromosomico aploide formato da cromosomi fratelli, non è in grado di proseguire la meiosi e quindi di dividersi ulteriormente.
La Seconda Metafase Ovocitaria: Il Punto di Arresto Chiave
L'ovocita secondario, generato dalla prima divisione meiotica, entra immediatamente nella seconda divisione meiotica, che è di carattere equazionale. Tuttavia, questo processo si arresta in un punto cruciale: la metafase II (MII). Questo ovulo, se non viene fecondato, è espulso con la mestruazione. L'ovocita si presenta in questo stadio quando viene ovulato naturalmente o recuperato tramite agoaspirazione follicolare ecoguidata in cicli di PMA.
Un ovocita ideale da sottoporre ad ICSI (Iniezione Intracitoplasmatica di Spermatozoo) è un ovocita allo stadio di MII, in cui è avvenuto il completamento della metafase II. Questo stadio è caratterizzato dalla presenza del primo globulo polare e dalla disposizione dei cromosomi sul piano equatoriale della cellula, pronti per essere separati nella successiva anafase II. La metafase II rappresenta quindi il momento di maturazione ottimale per la fecondazione, come evidenziato da Lindner et al. (1974).
FASI DI UN TRATTAMENTO FIVET (Fecondazione In Vitro). Coltura embrionale
Al momento del prelievo ovocitario in PMA, la maggior parte degli ovociti si trova ad uno stadio di maturazione ottimale per la fecondazione, ovvero proprio la Metafase II. Tuttavia, una percentuale compresa tra il 30 e il 70% degli ovociti che si trovano allo stadio di Metafase I può maturare in-vitro e raggiungere lo stadio di Metafase II in alcune ore. Questi ovociti maturati in-vitro hanno ridotte percentuali di fecondazione ma simile qualità embrionaria rispetto agli ovociti Metafase II prelevati direttamente (Coetzee et al., 2001; Nagy et al., 1996).
La seconda divisione meiotica, se l'ovocita viene fecondato, si completa, producendo un ovotidio e un secondo globulo polare. A questo punto, i due pronuclei (contenenti ciascuno solo 23 cromosomi) dell’ovocita e dello spermatozoo, congiungendosi, ricostituiscono il corretto numero di cromosomi della cellula.
Criteri di Valutazione e Selezione degli Ovociti in PMA
Nella Procreazione Medicalmente Assistita, la possibilità di ottenere la gravidanza parte dall’applicazione di protocolli di stimolazione alla donna, necessari per la produzione di un numero variabile di ovociti da utilizzare in laboratorio per la FIVET classica o per la ICSI. La selezione degli ovociti recuperati è un passaggio cruciale.
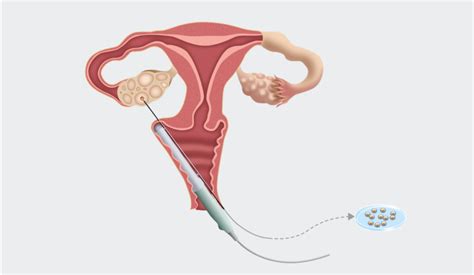
Una prima valutazione può essere effettuata in corso di stimolazione mediante i valori di estradiolo sierico: maggiori sono i valori plasmatici, tanto più elevato è il numero di ovociti maturi (Frydman et al., 2000). Successivamente, gli ovociti recuperati tramite agoaspirazione follicolare ecoguidata vengono studiati in base alle loro caratteristiche morfologiche e al loro stato di maturità nucleare.
I principali criteri di selezione ovocitaria sono:
- Valutazione dell’aspetto del complesso cumulo-corona ovocita: Il cumulo ooforo e la corona radiata sono strati di cellule che circondano l'ovocita. Sebbene l’aspetto delle cellule della corona radiata e del cumulo sia poco significativo nel predire la maturità ovocitaria (Veeck, 1990), gli ovociti maturi presentano un elevato grado di espansione delle cellule del cumulo dovuto alla loro attiva secrezione di acido ialuronico, che si interpone tra gli strati cellulari separandoli e conferendo al complesso cumulo-corona radiata un aspetto filante. L’aspetto del cumulo viene considerato come preovulatorio, mentre un cumulo meno espanso indicherebbe un ovocita di maturità intermedia.
- Valutazione della maturità nucleare ovocitaria: Questa è fondamentale per identificare l'ovocita in MII. L'introduzione della ICSI ha consentito di osservare le caratteristiche morfologiche ovocitarie dopo la rimozione delle cellule del cumulo, e si è osservato che l’aspetto del complesso cumulo-corona non è strettamente legato alla maturità nucleare degli ovociti decumulati.
- Valutazione della morfologia ovocitaria: Questo include l'aspetto del citoplasma, della zona pellucida e del primo globulo polare.
Classificazione degli Ovociti in Base alla Morfologia
Sulla base della presenza e morfologia del globulo polare e dello stato della corona radiata, è possibile distinguere quattro tipi di ovociti (Veeck, 1990; Ubaldi et al., 2000):
- Ovociti immaturi (GV - Vescicola Germinale): Il cumulo ooforo appare ammassato, la corona radiata è compatta ed addossata alla zona pellucida. Il globulo polare è assente. Questi ovociti sono bloccati in profase I della meiosi e non sono idonei alla fecondazione.
- Ovociti immaturi (MI - Metafase I): Caratterizzati da un fuso meiotico formato ma senza il primo globulo polare, hanno ancora un set diploide di cromosomi. Questi possono a volte maturare in vitro.
- Ovociti maturi (MII - Metafase II): Il cumulo ooforo appare espanso, filante, e la corona radiata ha cellule estese. È visibile il globulo polare primario (o primo corpo polare). Questi sono gli ovociti ottimali per la fecondazione.
- Ovociti post-maturi: Il cumulo ooforo appare disperso, granulare, con cellule ammassate e la corona radiata, anche se espansa, spesso è separata dalla zona pellucida. Il globulo polare è presente. Questi ovociti potrebbero avere una ridotta qualità.
- Ovociti ipermaturi o luteinizzati: Il cumulo ooforo appare scuro ed ammassato e la corona radiata è addensata e scura. Il globulo polare è presente ma spesso frammentato. Questi ovociti hanno una probabilità molto bassa di successo.
Ai differenti tipi di ovociti corrisponde una diversa percentuale di fertilizzazione, esclusi ovviamente quelli immaturi, e conseguentemente una diversa implantation rate.
Il Ruolo del Complesso Cumulo-Ooforo
Nonostante l'aspetto del complesso cumulo-corona-ovocita non rappresenti un elemento sufficiente a valutare la maturità e le competenze ovocitarie, studi recenti hanno evidenziato l’importanza del rapporto metabolico tra cellule del cumulo e ovocita. La presenza delle cellule del cumulo può migliorare il metabolismo degli embrioni sia stimolando l’espressione di determinati geni coinvolti nei processi metabolici, sia riducendo gli effetti dello stress ossidativo che possono verificarsi durante la coltura in vitro (Ubaldi et al., 2000).
Inoltre, la rimozione parziale delle cellule del cumulo prima della ICSI incide positivamente sullo sviluppo embrionale (Nagy et al., 1996). La pratica di laboratorio, con l’introduzione della ICSI, ha dato meno importanza all'aspetto del complesso cumulo-corona radiata proprio perché l'aspetto non è strettamente legato alla maturità nucleare degli ovociti decumulati.
L'Importanza della Morfologia Citoplasmatica e del Fuso Meiotico
Oltre alla valutazione dello stato meiotico, è importante andare a valutare l’aspetto morfologico del citoplasma ovocitario, in quanto spesso circa la metà degli ovociti prelevati presentano almeno un’anomalia morfologica (Veeck, 1990). Queste anomalie possono essere distinte in citoplasmatiche ed extracitoplasmatiche. Tra le anomalie citoplasmatiche, le più comuni includono la presenza di granulazioni, vacuoli, aggregazioni del reticolo endoplasmatico o "refractile bodies" (Cornet et al., 2000). Sebbene la loro esatta implicazione non sia sempre chiara, alcune di queste dismorfie possono influenzare negativamente la competenza ovocitaria (Van Blerkom e Henry, 1992).
Un elemento di fondamentale importanza per una normale fecondazione e un corretto sviluppo embrionario è l’integrità del fuso mitotico o meiotico. Questo apparato cellulare permette la divisione dei cromosomi nel corso della mitosi e della meiosi. La divisione cellulare si verifica a causa della bipolarità del fuso, costituito da due gruppi di polarità opposta, disposti intorno ai cromosomi. Il fuso meiotico negli ovociti in Metafase II è di fondamentale importanza.
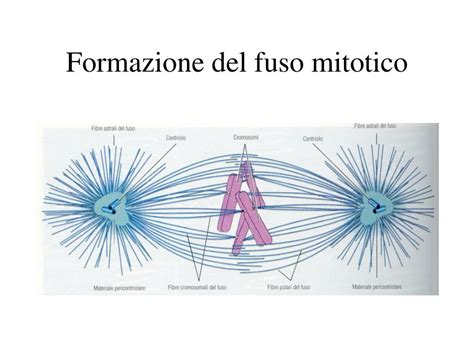
I limiti dell'utilizzo del fuso meiotico come criterio di selezione sono insiti nella sua struttura, che risulta essere altamente sensibile a modificazioni chimico-fisiche che si possono verificare durante la manipolazione ovocitaria (Serhal et al., 1997). Recentemente, la possibilità della valutazione del fuso meiotico, sfruttando la sua birifrangenza e la sua localizzazione alla periferia ovocitaria, ha offerto un altro criterio di selezione ovocitaria (Rienzi et al., 2004). Tuttavia, la sua valutazione non può essere effettuata su ovociti in cui né la vescicola germinale né il primo globulo polare sono visibili (Ebner et al., 2003).
Le anomalie del fuso meiotico sono state correlate a problemi nella segregazione cromosomica e alla formazione di embrioni aneuploidi (Battaglia et al., 1996; Bernard e Fuller, 1996), sottolineando ulteriormente la sua importanza nella potenziale qualità dell'ovocita.
Il Primo Globulo Polare e la Diagnosi Genetica Preimpianto (PGT-P)
Quando l'ovocita primario completa la sua prima divisione meiotica, i cromosomi si suddividono in modo uniforme ma questo non avviene con il citoplasma, che si concentra per la maggior parte in una delle due cellule figlie (chiamata ovocita secondario) e rimane in piccole quantità nell’altra che viene chiamata corpo polare (o globulo polare primario). Il corpo polare non è un ovocita funzionale, ma degenera e muore.
La tecnica di selezione ovocitaria basata sull’analisi cromosomica del primo corpo polare si basa sul principio secondo il quale tale corpo costituisce un'immagine speculare dell'ovocita (Verlinsky et al., 1990). Una volta prelevato, il primo corpo polare viene trattato specificamente per poterne analizzare il materiale genetico. L'analisi genetica del primo corpo polare, se confrontata con quella eseguita sull'embrione, ha il vantaggio di consentire la selezione degli ovociti prima della fecondazione. Ad esempio, se si riscontra la mancanza di un cromosoma nel primo globulo polare, l'ovocita darà origine a un embrione monosomico per il cromosoma in questione. Al contrario, se si riscontra un cromosoma in più, si avrà la formazione di un embrione trisomico per il cromosoma analizzato. Questa tecnica non comporta la selezione di embrioni che presentino anomalie cromosomiche ma permette di selezionare a priori gli ovociti sani.
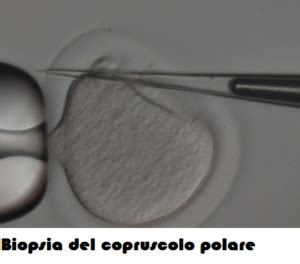
L’analisi del primo globulo polare consente la diagnosi di aneuploidie comuni come quelle dei cromosomi 13, 16, 18, 21, 22, X e Y (Munné et al., 2002; Verlinsky et al., 1993, 1997, 1998; Benadiva et al., 1996; Dailey et al., 1996). Sebbene il testing del primo globulo polare sia tecnicamente più complesso di quello dei blastomeri, e i costi siano maggiori, presenta alcuni vantaggi etici e religiosi significativi, in quanto consente la selezione prima della fecondazione (Munné, 2002; Magli et al., 2004).
Fattori Che Influenzano la Qualità Ovocitaria e i Tassi di Successo
La qualità dell'ovocita, e di conseguenza i tassi di gravidanza, sono influenzati da diversi fattori, sia legati alla paziente che alle procedure di laboratorio.
Vascolarizzazione Follicolare
La possibilità di identificare i follicoli maggiormente vascolarizzati da cui prelevare gli ovociti permetterebbe di ridurre il numero di embrioni da trasferire, riducendo al massimo il rischio di gravidanze multiple senza diminuire i tassi di gravidanza (Van Blerkom et al., 1997; Van Blerkom, 1998). Da un punto di vista clinico sono incoraggianti i risultati riportati dalla ricerca sulla correlazione tra vascolarizzazione del follicolo e potenziale di sviluppo dell'ovocita corrispondente: follicoli maggiormente vascolarizzati conterrebbero ovociti con maggiore potenziale di fecondazione e di sviluppo embrionario. I follicoli che mostrano un flusso ematico perfollicolare persistente e una velocità di picco massima superiore a 10 cm/sec hanno una maggiore probabilità di contenere ovociti competenti (Blerkom and Henry, 1992; Van Blerkom et al., 1997).
Protocolli di Stimolazione Ovarica
I protocolli di stimolazione ovarica controllata sono essenziali per la PMA. L'obiettivo è recuperare un numero adeguato di ovociti maturi. La tipologia di gonadotropine utilizzate può influenzare la qualità ovocitaria. Esistono due principali tipi di preparati:
- FSH urinario (uFSH) o HMG (Menotropina): Derivato dall'urina di donne in menopausa, contiene FSH e a volte LH. L'utilizzo di HMG o FSH urinario o con la combinazione FSH-LH urinario (HMG) è stato ampiamente studiato (Hughes et al., 1992; Jacob et al., 1998; Weissman et al., 1999).
- FSH ricombinante (rFSH): Prodotto con tecnologia del DNA ricombinante, è più puro e consistente. Alcuni studi hanno suggerito che l'FSH ricombinante potrebbe indurre un numero maggiore di ovociti recuperati e un minor tasso di aborto rispetto all'FSH urinario (Huang et al., 2004).
Età Materna
L'età materna avanzata è un fattore ben noto che incide negativamente sulla qualità ovocitaria e sulla probabilità di aneuploidie (Battaglia et al., 1996; Benadiva et al., 1996; Verlinsky et al., 2002). L'analisi del primo globulo polare, ad esempio, ha rivelato un aumento significativo delle anomalie cromosomiche negli ovociti di donne anziane (Verlinsky et al., 2002).
La Normativa e i Criteri di Selezione: Un Contesto in Evoluzione
L’introduzione in Italia della Legge 19 febbraio 2004, n. ha avuto un impatto significativo sulle pratiche di PMA. Secondo questa legge, la selezione ovocitaria doveva essere limitata a un massimo di tre ovociti da inseminare, basandosi esclusivamente su criteri clinici e morfologici, la cui correlazione con gli esiti clinici era ancora da dimostrare. Questa limitazione aveva lo scopo di ridurre il rischio di gravidanze multiple, ma poneva sfide nella selezione degli ovociti con il miglior potenziale. La legge specificava che gli ovociti da trasferire, comunque non superiori a tre, dovevano avere la massima potenzialità di impianto.
Questo quadro normativo ha stimolato la ricerca di criteri di selezione ovocitaria sempre più affidabili e non invasivi, che potessero essere applicati prima della fecondazione. Tuttavia, la non univocità di risultati riportati in letteratura sulla reale efficacia di alcuni di questi criteri ha mantenuto aperto il dibattito.
Prospettive Future e Nuovi Orizzonti nella Selezione Ovocitaria
La ricerca continua a esplorare nuovi biomarcatori e tecniche per migliorare la selezione ovocitaria, con l'obiettivo di aumentare i tassi di successo della PMA e ridurre i rischi associati. Nuovi criteri di selezione ovocitaria, come la valutazione dettagliata del fuso meiotico in rapporto al primo corpo polare, potrebbero affiancarsi ai metodi tradizionali. Ad esempio, l'orientamento del fuso meiotico rispetto al primo globulo polare, se supera i 90°, è stato suggerito come possibile indicatore di qualità (Ebner et al., 2003).
La possibilità di identificare i follicoli maggiormente vascolarizzati, che conterrebbero ovociti con maggiore potenziale di fecondazione e di sviluppo embrionario, resta un'area promettente. Parallelamente, si approfondiscono gli studi sul ruolo di alterazioni morfologiche citoplasmatiche ed extracitoplasmatiche, cercando di comprendere meglio la loro influenza sulla competenza ovocitaria. Il futuro della PMA dipenderà in gran parte dalla capacità di sviluppare e validare questi nuovi criteri, garantendo che i criteri verranno confermati o identificati, portando a una selezione degli ovociti che possa massimizzare le probabilità di una gravidanza sana.