L'infertilità rappresenta una sfida significativa per la salute riproduttiva umana, affliggendo circa il 15% delle coppie a livello globale. Le cause possono essere molteplici e interconnesse, spesso radicate in disturbi dello sviluppo sessuale o endocrini che esordiscono in età precoce. L'infertilità maschile, in particolare, contribuisce per circa la metà a questi casi e si manifesta con alterazioni quantitative e qualitative dello sperma: azoospermia o oligozoospermia (riduzione del numero di spermatozoi), astenozoospermia (diminuita motilità) e teratozoospermia (aumento di spermatozoi morfologicamente anomali).
La valutazione di questi parametri avviene tramite lo spermiogramma, un'analisi dettagliata del liquido seminale che segue le raccomandazioni del manuale di laboratorio dell'OMS. L'obiettivo è caratterizzare il potenziale riproduttivo maschile, integrando i risultati con indagini cliniche ed endocrine per definire le strategie terapeutiche più appropriate. La qualità dello sperma è intrinsecamente legata a influenze endocrine ed esterne, che necessitano di essere identificate e, ove possibile, gestite.
Comprendere la Morfologia Spermatica: Definizione e Parametri di Normalità
La teratozoospermia, o teratospermia, è una condizione definita da una morfologia anomala degli spermatozoi. Secondo l'Organizzazione Mondiale della Sanità (OMS), per definire uno spermatozoo come morfologicamente normale, esso deve possedere specifiche caratteristiche:
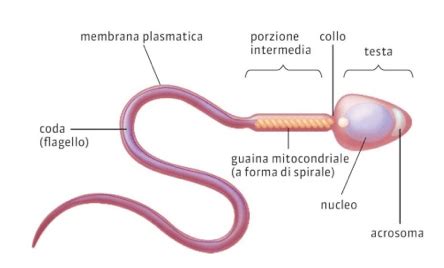
- Testa: Ovalare, con una regione acrosomica ben definita nella porzione apicale. Eventuali vacuoli non devono superare il 20% della superficie della testa.
- Collo: Attaccato assialmente alla testa (di fronte all'acrosoma) e con una lunghezza circa 1,5 volte quella della testa.
- Coda: Lunga approssimativamente 45-50 micron e più sottile del resto dello spermatozoo.
- Lunghezza Totale: Circa 50-60 micron.
Gli spermatozoi che non rientrano in questi parametri sono classificati come amorfi o anormali. In generale, la percentuale di spermatozoi con morfologia normale in un campione di eiaculato sano varia tra il 4% e il 14%. Una teratozoospermia significativa, definita dall'OMS come meno del 4% di spermatozoi morfologicamente normali, può rappresentare una causa di infertilità maschile, rendendo più difficile il concepimento naturale.
Tipi di Deformità Spermatica: Un'Analisi Dettagliata
Le anomalie morfologiche possono interessare diverse parti dello spermatozoo, compromettendo la sua capacità di fecondare l'ovulo. Queste deformità possono essere categorizzate come segue:
Deformità della Testa
Le anomalie più comuni riguardano la testa dello spermatozoo e includono:
- Dimensioni: Testa eccessivamente grande o piccola.
- Forma: Testa circolare, piriforme (a pera), o vacuolata (con vacuoli che occupano più del 20% del volume).
- Acrosoma: Area acrosomica ridotta (inferiore al 40% della testa) o assente, come nel caso della globozoospermia, dove la testa è sferica e manca l'acrosoma, essenziale per penetrare la zona pellucida dell'ovulo.
- Teste doppie: Presenza di due teste su un singolo spermatozoo, condizione che rende impossibile la fecondazione di un embrione sano a causa del raddoppio del carico genetico, portando a embrioni triploidi destinati all'arresto dello sviluppo.
- Pinhead: Una condizione in cui la testa è poco differenziata dal collo, spesso dovuta a fallimenti di adesione tra acrosoma e nucleo, con conseguente assorbimento delle teste e permanenza delle sole code nel seme. Questi spermatozoi sono privi di contenuto genetico e non possono fecondare.
Deformità del Collo (o Parte Centrale)
Alterazioni della parte intermedia dello spermatozoo, responsabile dell'apporto energetico necessario al movimento, includono:
- Angolazione: Collo piegato, formando un angolo maggiore di 90° rispetto all'asse longitudinale della testa.
- Inserzione: Inserimento asimmetrico del collo nella testa.
- Spessore: Collo eccessivamente spesso o irregolare.
- Assenza di Mitocondri: Fondamentali per la produzione di energia, la loro mancanza compromette gravemente la motilità.
Deformità della Coda
Difetti nella coda dello spermatozoo influenzano direttamente la sua capacità di movimento:
- Lunghezza: Coda troppo corta o troppo lunga.
- Struttura: Coda doppia o multipla, biforcuta, spezzata, arricciata o di spessore irregolare.
- Angolazione: Coda piegata con un angolo maggiore di 90°.
Queste anomalie, sebbene non sempre impediscano la fecondazione, possono causare problemi di infertilità noti come oligo-asteno-teratozoospermia (OAT), poiché spermatozoi con queste caratteristiche presentano una ridotta capacità di movimento e progressione verso l'ovulo.
Indice di Teratozoospermia (TZI) e Valutazione della Gravità
Per quantificare l'impatto della teratozoospermia sulla fertilità, viene calcolato l'Indice di Teratozoospermia (TZI). Questo parametro indica il numero di anomalie morfologiche presenti in ogni singolo spermatozoo. Un TZI elevato suggerisce che gli spermatozoi presentano difetti multipli (es. testa e coda anomale), aumentando la gravità della condizione. La formula per il calcolo è:
TZI = (c + p + q) / x
dove:
c= numero di alterazioni della testap= numero di disturbi del colloq= numero di disturbi della codax= numero totale di spermatozoi anormali
Il valore del TZI varia da 1 a 3. Un valore più vicino a 1 indica che la maggior parte degli spermatozoi presenta un'unica anomalia, mentre un valore più alto (fino a 3) indica spermatozoi con difetti multipli in testa, collo e coda, correlati a una maggiore gravità dell'infertilità.
Cause della Teratozoospermia e Fattori Influenzanti
Le cause della teratozoospermia sono molteplici e spesso interconnesse, riflettendo la complessità del processo di spermatogenesi. Tra i fattori eziologici principali si annoverano:
- Fattori Genetici: Anomalie cromosomiche o mutazioni genetiche possono compromettere la corretta formazione degli spermatozoi. La perdita di funzione di specifici geni, come osservato in studi su modelli murini, può portare a difetti morfologici.
- Stress Ossidativo: Uno squilibrio tra specie reattive dell'ossigeno (ROS) e capacità antiossidante nel plasma seminale è una causa frequente di danno spermatico. I ROS possono danneggiare le membrane degli spermatozoi attraverso la perossidazione lipidica, influenzando motilità, reazione acrosomiale e aumentando la frammentazione del DNA.
- Infezioni: Infezioni delle ghiandole accessorie possono aumentare la produzione di ROS e causare danno al DNA spermatico. Alcuni agenti patogeni, come l'antigene dell'Epatite B e alcuni tipi di papillomavirus umano (HPV), sono stati associati a un aumento della frammentazione del DNA spermatico e a una riduzione della motilità.
- Fattori Ambientali ed Esposizioni:
- Tossine: L'esposizione a pesticidi, metalli pesanti e inquinanti chimici industriali può avere effetti negativi sulla qualità dello sperma. L'esposizione occupazionale a sostanze chimiche è stata correlata a modifiche dell'integrità del DNA nelle cellule germinali maschili.
- Calore: L'esposizione prolungata ad alte temperature, sia a livello occupazionale che da fonti come l'uso eccessivo di dispositivi elettronici (cellulari), può compromettere la spermatogenesi, aumentare i ROS e la frammentazione del DNA.
- Radiazioni Elettromagnetiche: Le radiazioni a radiofrequenza emesse dai telefoni cellulari sono state associate a un aumento della produzione di ROS mitocondriali e della frammentazione del DNA.
- Stile di Vita e Abitudini:
- Alcol e Droghe: Il consumo cronico di alcol e l'uso di oppiacei o marijuana sono stati associati a stress ossidativo, aumento della frammentazione del DNA, riduzione della motilità e alterazioni della spermatogenesi.
- Fumo: Sostanze nocive presenti nel tabacco producono specie reattive dell'ossigeno e dell'azoto, compromettendo la qualità e la quantità dello sperma, l'integrità del DNA e l'attività antiossidante. Il fumo può interferire con il processo di protaminazione della cromatina spermatica.
- Obesità: L'obesità maschile è considerata un fattore di rischio per l'infertilità, associata a una diminuzione della motilità e a un aumento del danno al DNA spermatico, probabilmente a causa di squilibri ormonali e stress ossidativo.
- Farmaci: L'assunzione regolare di farmaci può influenzare l'asse ipotalamo-ipofisi-gonadi e la qualità dello sperma.
- Caffeina: Un elevato consumo di caffeina (tre o più tazze al giorno) è stato associato a un aumento del danno al DNA degli spermatozoi.
- Condizioni Mediche:
- Infezioni Febbrili Acute: Possono compromettere temporaneamente la spermatogenesi, con un recupero della qualità dello sperma solitamente entro 3-6 mesi.
- Diabete: Può avere effetti dannosi sul potenziale di fertilità e sull'integrità del DNA spermatico.
- Varicocele: La correlazione tra varicocele e teratozoospermia è dibattuta, ma la presenza di varicocele palpabile è spesso associata a un aumento della percentuale di spermatozoi con DNA anomalo e cromatina immatura, portando a una ridotta condensazione della cromatina e potenziale infertilità. La varicocelectomia può migliorare la qualità dello sperma e aumentare i livelli di testosterone in uomini ipogonadici.
- Problemi Ormonali: L'ipogonadismo, una disfunzione delle gonadi, può causare bassi livelli di testosterone, influenzando la produzione e la funzione degli spermatozoi.
Impatto dello Sviluppo Embrionale e Tecniche di Riproduzione Assistita
La qualità della cromatina spermatica e l'integrità del DNA sono cruciali non solo per la fecondazione, ma anche per il normale sviluppo embrionale. Danni al DNA spermatico possono influenzare negativamente la qualità dell'embrione fin dalle prime fasi di sviluppo, riducendo la capacità di impianto e le probabilità di gravidanza. Sebbene l'ovocita possieda meccanismi di riparazione del DNA, danni eccessivi o specifici potrebbero non essere riparabili, portando a un basso sviluppo embrionale, difetti fetali e un aumentato rischio di aborti precoci, anche dopo tecniche di fecondazione in vitro (FIV).
la fecondazione e impianto
In presenza di teratozoospermia, la fecondazione naturale può essere compromessa. Tuttavia, esistono diverse tecniche di riproduzione assistita (ART) che possono aumentare le probabilità di concepimento:
- Iniezione Intracitoplasmatica di Spermatozoi (ICSI): Questa tecnica, una variante della FIV, prevede l'iniezione diretta di uno spermatozoo selezionato in un ovulo. L'ICSI è particolarmente utile nei casi di teratozoospermia severa, poiché permette di bypassare le problematiche legate alla morfologia e alla motilità dello sperma, selezionando spermatozoi con caratteristiche apparentemente normali per la microiniezione. È l'unica tecnica efficace per la globozoospermia e la pinhead.
- Fecondazione In Vitro (FIV) Convenzionale: Sebbene non risolva direttamente il problema morfologico, la FIV può essere utilizzata in combinazione con altre tecniche o in casi di lieve teratozoospermia.
- Selezione Avanzata degli Spermatozoi: Tecniche come la selezione microfluidica o la valutazione della frammentazione del DNA spermatico possono aiutare a selezionare spermatozoi con migliore morfologia e minore danno al DNA da utilizzare nelle procedure ART.
- Diagnosi Genetica Preimpianto (PGD): Nei casi di teratozoospermia grave o in presenza di altre anomalie genetiche, la PGD può essere impiegata per analizzare gli embrioni alla ricerca di anomalie genetiche prima dell'impianto.
Trattamenti e Gestione della Teratozoospermia
Il trattamento della teratozoospermia mira a correggere le cause sottostanti e a migliorare i parametri spermatici. Le opzioni terapeutiche includono:
- Terapie Farmacologiche e Integratori:
- FSH (Ormone Follicolo-Stimolante): La somministrazione di FSH ricombinante (recFSH) o umano purificato (hpFSH) può essere considerata in uomini normogonadotropi con oligozoospermia idiopatica o OAT, sebbene l'evidenza a supporto sia limitata.
- Antiestrogeni: Farmaci come tamoxifene e clomifene sono stati utilizzati con successo per aumentare la concentrazione e la motilità degli spermatozoi in casi di infertilità maschile idiopatica.
- Antiossidanti: La supplementazione con antiossidanti (vitamine C ed E, glutatione, coenzima Q10, selenio, zinco) può migliorare i parametri spermatici e i tassi di gravidanza, specialmente in coppie sottoposte a tecniche ART, sebbene le prove di alta qualità siano ancora limitate.
- Inibitori dell'Aromatasi: Farmaci come letrozolo o anastrozolo sono stati raccomandati in uomini con bassi rapporti testosterone/estrogeni e parametri spermatici alterati, mostrando risultati promettenti in piccoli studi. Tuttavia, il loro uso generale non è ancora raccomandato a causa della limitatezza delle evidenze.
- Interventi Chirurgici: La chirurgia può essere indicata per rimuovere cause ostruttive o compromettenti della spermatogenesi, come nel caso del varicocele, o per correggere disturbi dello svuotamento del tratto seminale.
- Cambiamenti dello Stile di Vita: Sebbene le prove dirette dell'efficacia dei cambiamenti dello stile di vita sul miglioramento della fertilità maschile siano ancora in fase di studio, è ampiamente riconosciuto che l'adozione di abitudini sane - dieta equilibrata, esercizio fisico regolare, mantenimento di un peso corporeo sano, astensione dal fumo e dalla consumo eccessivo di alcol, riduzione dello stress - possa contribuire a migliorare la salute riproduttiva generale. Un periodo di astinenza sessuale da 2 a 5 giorni prima dell'analisi dello sperma è generalmente raccomandato per ottimizzare i risultati dello spermiogramma.

Prospettive Future e Ricerca
La ricerca continua a esplorare le basi genetiche e molecolari della teratozoospermia, cercando biomarcatori predittivi e nuove strategie terapeutiche. La comprensione del ruolo dei meccanismi epigenetici, che trasferiscono informazioni sullo stato di salute paterno e sull'ambiente vissuto, sta ampliando la prospettiva sull'influenza paterna nella salute riproduttiva e nello sviluppo embrionale. La valutazione dell'integrità del DNA spermatico, attraverso test specifici, sta diventando uno strumento sempre più importante per integrare l'analisi dello spermiogramma standard e valutare la reale funzionalità dello spermatozoo. La consulenza preconcezionale dovrebbe idealmente includere una valutazione completa della salute paterna, riconoscendo lo spermatozoo non solo come vettore genetico, ma anche come "diario" della storia biologica del padre.