Nel campo in continua evoluzione della procreazione medicalmente assistita (PMA), l'obiettivo primario è quello di ottenere una gravidanza, cercando in tutti i modi di massimizzare l'efficacia di ogni ciclo di trattamento. Questo approccio mira a evitare insuccessi ripetuti, continue stimolazioni e demoralizzazioni da parte della coppia. Le tecniche di fecondazione in vitro (FIVET o ICSI) ricreano artificialmente le condizioni ideali per l'incontro dei gameti e la formazione dell'embrione, con l'obiettivo finale di portare a termine la gravidanza con la nascita di un bambino sano. In questo contesto, il trasferimento di blastocisti rappresenta una strategia fondamentale, i cui tassi di successo sono oggetto di costante studio e miglioramento. La fecondazione in vitro aiuta anche da questo punto di vista, grazie a sempre nuove ed efficaci procedure e tecnologie.
La Blastocisti: Fondamenti Biologici e Sviluppo Embrionale
La comprensione di cosa sia una blastocisti è essenziale per apprezzarne il ruolo nella PMA. La blastocisti è un embrione che si è sviluppato fino a 5-6 giorni dopo il concepimento, o dal concepimento. Fisiologicamente, infatti, è proprio allo stadio di Blastocisti (cinque giorni dopo l’avvenuta fecondazione) che l’embrione transita dalle tube all’utero. Questo stadio embrionale iniziale è raggiunto intorno ai 5-6 giorni dalla fecondazione.
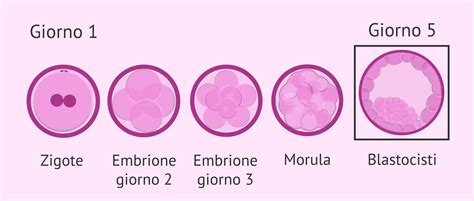
In questa fase, si distinguono due gruppi di cellule, che daranno a loro volta origine alle strutture annesse, come la placenta. La blastocisti è caratterizzata da un altissimo numero di cellule e da una maggiore predisposizione all’impianto in utero. Si tratta di un embrione che presenta una cavità interna piena di liquido, detta blastocele, e uno strato esterno di cellule chiamato trofectoderma, che darà origine alla placenta. La blastocisti umana è, in sintesi, l'embrione che raggiunge 5-6 giorni di sviluppo. Un aspetto importante è la "zona pellucida", il guscio proteico che protegge l'embrione nelle prime fasi di sviluppo. Quando si parla di blastocisti espansa, si ha a che fare con un embrione che, attorno al quinto o sesto giorno di sviluppo, appare gonfio per via dell’accumulo di liquidi al suo interno. Visto l’aumento del volume, l’embrione esce dal suo guscio proteico, noto come “zona pellucida”, e ha la possibilità di impiantarsi finalmente nell’utero, se ci sono le condizioni adatte. L’impianto, che consente alla blastocisti di trarre nutrimento dall’utero materno, dura una settimana e comprende rispettivamente le fasi di apposizione, adesione e invasione. In questo periodo sia l’embrione che l’endometrio esercitano un ruolo attivo.
Qual è l’embrione con più chance di ottenere una gravidanza?
È in questa fase, inoltre, che è possibile - laddove necessario - eseguire un’indagine di preimpianto. Qualora fosse necessario, nella fecondazione in vitro, si può realizzare un’analisi genetica pre-impianto della blastocisti, detta anche diagnosi PDG, che permette di escludere gli embrioni che presentano mutazioni genetiche o alterazioni cromosomiche. Se si esegue un’indagine genetica preimpianto e si selezionano solo le blastocisti cromosomicamente sane il tasso può salire anche fino all’70%, con un unico impianto.
Il Vantaggio del Trasferimento a Blastocisti nella PMA
La coltura degli embrioni allo stadio di blastocisti è una tecnica terapeutica diffusa, utilizzata nella fecondazione assistita, che può migliorare le probabilità di ottenere una gravidanza. Il vantaggio di coltivare gli embrioni sino allo stadio di Blastocisti risiede, dunque, nel fatto di ricreare il sincronismo fisiologico tra stadio di sviluppo embrionale e la sede anatomica del trasferimento, aumentando le possibilità che si realizzi l’impianto. Questo offre una migliore sincronizzazione con l'endometrio, il che aumenta le probabilità di impianto.
Un altro beneficio significativo è la migliore selezione embrionale. Non tutti gli embrioni che vengono formati (sia in vitro che fisiologicamente) riescono a superare le prime fasi di sviluppo e a raggiungere lo stadio di blastocisti; solo il 35% circa vi riesce. Per cui è facile comprendere che lungo questo percorso avviene una selezione naturale in favore degli embrioni più forti. Ciò permette di effettuare una migliore selezione embrionale, poiché si ottengono maggiori informazioni sullo sviluppo e solo i migliori sono in grado di raggiungere questo stadio. In un numero limitato di casi, la percentuale oscilla tra il 5% e il 10%, nessun embrione è in grado di svilupparsi sino allo stadio di blastocisti, vanificando il trasferimento embrionario.
Contemporaneamente, mediante questa strategia, è possibile ridurre il numero di embrioni destinati al transfer, minimizzando i rischi collegati all’insorgenza di una gravidanza gemellare. Ciò offre la possibilità di fare più trasferimenti di un singolo embrione per evitare gravidanze multiple senza compromettere le probabilità di successo. La decisione di non trasferire più di 2 blastocisti risiede nell’intento di evitare gravidanze plurime: poiché le blastocisti hanno una elevata capacità di attecchimento, trasferendone più di 2 in utero esiste una probabilità di ottenere gravidanze gemellari o trigemine, con una gravidanza maggiormente a rischio. Questi motivi permettono un aumento delle percentuali di successo di gravidanza, evidenziato anche dalla letteratura scientifica, che salgono al 56% contro il 30-35% rispetto ad embrioni di 2 o 3 giorni.
Blastocisti Fresche vs. Crioconservate: Un Confronto Approfondito
Tradizionalmente, i risultati con il trasferimento di embrioni a fresco erano considerati migliori rispetto a quelli con embrioni congelati. Inizialmente si credeva che trasferire in utero embrioni freschi fosse la scelta migliore sia per il successo della gravidanza sia per i rischi del nascituro. Tuttavia, oggigiorno, grazie ai progressi nel campo della riproduzione assistita e alle moderne tecnologie, sappiamo che non è più così. I risultati in termini di efficacia sono sovrapponibili tra le due metodiche, e la crioconservazione o vitrificazione può essere preferibile in alcuni casi.
La crioconservazione è particolarmente indicata per le donne sottoposte a cure mediche, che potrebbero rappresentare un problema per la fertilità e durante la gestazione. I dati scientifici dimostrano che le percentuali di gravidanza da embrioni scongelati sono più alte rispetto ai casi in cui si impiegano ovuli crioconservati. Per quanto riguarda le probabilità di attecchimento di una blastocisti, il transfer di blastocisti congelate potrebbe avere un maggiore tasso di successo rispetto al transfer di embrioni a fresco. La sopravvivenza degli embrioni criocongelati corrisponde a una percentuale alta (pari al 95%), anche se non è sempre così.
La tecnica utilizzata per crioconservare gli embrioni è la vitrificazione, un metodo di congelamento ultrarapido che evita la formazione di cristalli. La vitrificazione consiste in un congelamento rapidissimo in azoto liquido con temperature che si aggirano tra i -210°C e i -196°C. Attraverso questa procedura, si ottengono tassi di sopravvivenza molto elevati (90-95%) poiché si minimizzano i danni che gli embrioni subiscono nel processo di congelamento. Questo raffreddamento ultrarapido previene la formazione di cristalli di ghiaccio all’interno delle cellule, trasformandole in uno stato simile al vetro. Pertanto, questi progressi nella crioconservazione consentono di vitrificare gli embrioni senza compromettere i tassi di successo, anzi migliorandoli. La risposta breve alla domanda se il congelamento diminuisca la probabilità che l'embrione si impianti è no; di fatto, in molti casi, la migliora. Grazie alla tecnica della vitrificazione (congelamento ultrarapido), il tasso di sopravvivenza delle blastocisti allo scongelamento è piuttosto elevato.
Un beneficio cruciale della crioconservazione deriva dalla fisiologia del ciclo di PMA. Durante una procedura di PMA, la stimolazione per il recupero degli ovociti innalza i livelli di estrogeni e progesterone, disturbando la recettività endometriale. Sebbene in questo modo si aumentino le probabilità di successo di queste tecniche, la stimolazione ha anche effetti dannosi sull'endometrio (lo strato che ricopre la superficie della cavità uterina), influenzando negativamente l'impianto embrionale nei cicli a fresco. Pertanto, l'endometrio è più ricettivo nei trasferimenti di embrioni congelati rispetto ai cicli a fresco, poiché ha avuto un intero ciclo mestruale per riprendersi dagli effetti della stimolazione ormonale. Crioconservare gli embrioni e posticipare il trasferimento in un ciclo preparato “ad hoc” al fine di ottimizzare la recettività endometriale può quindi aumentare il tasso di successo della fecondazione assistita. Nelle donne ad alto rischio di iperstimolazione ovarica o con endometrio non idoneo, il trasferimento a fresco è da evitare.
I dati più recenti supportano la superiorità o almeno la parità del transfer di embrioni congelati. Secondo l’ultimo Registro Nazionale di Attività della Società Spagnola di Fertilità (SEF) relativo all’anno 2023, i risultati sono i seguenti: il tasso di gravidanza per trasferimento di embrioni congelati (specialmente quando è stato eseguito un test genetico preimpianto o PGT) è del 53,2%, mentre con embrioni a fresco si aggira intorno al 45,8%. Per quanto riguarda il tasso di parto (neonato vivo a casa), le cifre relative all’anno 2023 sono del 37,5% con embrioni a fresco e del 41,8% con embrioni vitrificati. Nel nostro “PROGRAMMA DI BLASTOCISTI GARANTITE“, secondo le statistiche c’è la possibilità del 76,9% di gravidanza nel primo transfer e l’86,2% di opportunità di parto per ciclo. È importante notare che, per contro, un embrione scongelato potrebbe in qualche caso risentire della tecnica di vitrificazione e scongelamento e dare un risultato inferiore, sebbene questo sia meno comune con le tecniche attuali.
È necessaria una preparazione endometriale per il trasferimento di embrioni congelati? I trasferimenti di embrioni congelati possono essere eseguiti sia in un ciclo naturale che in un ciclo sostituito. Nel caso del ciclo naturale, si sfruttano gli ormoni naturali del ciclo mestruale della paziente e si controlla mediante ecografia l’evoluzione del follicolo e dell’endometrio, senza somministrare alcun farmaco. Una volta avvenuta l’ovulazione (rilascio dell’ovulo maturo), si inizia un trattamento con progesterone. Nei cicli sostituiti, si somministrano estrogeni per preparare l’endometrio, sotto forma di cerotti o pillole. Quando si osserva tramite ecografia che l’endometrio è pronto, si somministra progesterone. Si procederà in un modo o nell’altro a seconda delle caratteristiche di ciascuna paziente: se ha un ciclo mestruale, i risultati dei cicli precedenti. Inoltre, possono esserci anche variazioni in queste linee guida di trattamento, come la somministrazione di analoghi del GnRH, per esempio. Un embrione che è stato scongelato può essere congelato di nuovo? Sì, a condizione che la vetrificazione e lo scongelamento (devetrificazione) vengano eseguiti correttamente, un embrione può sopravvivere a diversi cicli di congelamento senza che la sua vitalità venga compromessa ed essere in grado di impiantarsi. I sintomi del trasferimento di blastocisti congelate sono gli stessi di quelle a fresco? Sì, poiché non ci sono differenze tra i due trasferimenti, la procedura è la stessa. L’unica cosa che può variare è che nel trasferimento a fresco potrebbero rimanere dei sintomi dovuti alla stimolazione ormonale.
Qual è l’embrione con più chance di ottenere una gravidanza?
Fattori Che Influenzano il Tasso di Successo nella PMA
Per comprendere quali siano le percentuali di successo nei trattamenti di Procreazione Medicalmente Assistita, è innanzitutto importante ricordare che rimanere incinta non è semplice come sembra, poiché la specie umana ha una bassa efficienza del sistema riproduttivo: la probabilità di rimanere incinta al primo tentativo per una giovane coppia presumibilmente fertile, dopo un mese di rapporti sessuali mirati e non protetti, non supera infatti il 20%. Le procedure di fecondazione assistita hanno l’obiettivo di superare le difficoltà di concepimento e, più in generale, di creare le condizioni per iniziare e portare a termine la gravidanza con la nascita di un bambino sano. La FIVET ha una percentuale di successo al primo tentativo del 38,2%, che aumenta fino a quasi l’80% al terzo tentativo, a parità di condizioni, nella specie umana.
Ci sono però alcuni fattori che influenzano negativamente il tasso di successo della PMA. I principali sono: la qualità/quantità dei gameti (maschili e femminili) prodotti e la recettività endometriale e uterina, che è strettamente correlata alla fisiopatologia della donna. Gli embrioni possono essere trasferiti in utero sia in questa fase evolutiva che prima, dopo 2 o 3 giorni dalla fecondazione. Preferire un transfer piuttosto che un altro dipende dal singolo caso, caratterizzato da numerosi fattori come le cause dell’infertilità, il numero di embrioni realizzati e la loro qualità, l’età materna ed eventuali altri percorsi di PMA falliti in precedenza.
L’età della donna è uno dei fattori più rilevanti nell’influenzare il tasso di gravidanza nei trattamenti di Procreazione Medicalmente Assistita (PMA). Dopo i 35 anni, la fertilità femminile subisce infatti un calo significativo e fisiologico, legato alla progressiva riduzione sia del numero sia della qualità degli ovociti disponibili. Questo declino incide direttamente sulle percentuali di successo della fecondazione assistita, rendendo più complesso ottenere una gravidanza, anche con tecniche avanzate come la FIVET o l’ICSI. Per questo motivo, si propone la tecnica di crioconservazione degli ovociti che consente di preservare la fertilità nel momento di massima efficienza riproduttiva. Non sempre i gameti (ovociti e spermatozoi) sono disponibili in quantità/qualità sufficienti. Questa è la prima condizione di scelta tra una tecnica di fecondazione assistita omologa (con gameti appartenenti ai partner della coppia) o di tipo eterologo (gameti provenienti da donatori esterni alla coppia).
L’infertilità maschile è un problema assai più comune di quanto si pensi ed è spesso sottovalutato, poiché di frequente erroneamente confuso con la “potenza sessuale” ovvero la capacità di avere rapporti. Solo dopo l’analisi del liquido seminale (spermiogramma) l’uomo scopre eventualmente di avere una compromissione della qualità degli spermatozoi: riduzione del numero (Oligozoospermia), riduzione della motilità (Astenozoospermia), morfologia alterata (Teratozoospermia). Talvolta ci si trova di fronte a una situazione di drastica riduzione del numero degli spermatozoi prodotti (Criptozoospermia) o addirittura di totale assenza di produzione spermatica (Azoospermia). Lo stile di vita (alcool, fumo, stress), l’inquinamento ambientale e l’esposizione a fattori di rischio lavorativi hanno sicuramente un peso determinante sulla qualità degli spermatozoi.
Secondo il Registro Nazionale della Procreazione Medicalmente Assistita in Italia, il 16,2% delle coppie che si sottopongono a tecniche di PMA soffre di infertilità inspiegata (o idiopatica). In generale, sono molteplici le condizioni che durante il percorso terapeutico concorrono a determinare l’esito favorevole della procedura di Procreazione Medicalmente Assistita, ossia l’ottenimento della gravidanza. Tra le più importanti ricordiamo: il corretto inquadramento clinico e conseguentemente la scelta della tecnica più appropriata; la personalizzazione della stimolazione ovarica, al fine di massimizzare il recupero ovocitario e/o ottimizzare la preparazione dell’endometrio alla ricezione dell’embrione; la presenza di attrezzature e tecnologie all’avanguardia nel laboratorio IVF, per garantire che gli embrioni si sviluppino e siano selezionati in condizioni ottimali.
Nell’approcciarsi ai trattamenti di PMA, è di fondamentale importanza comprendere che le possibilità di ottenere una gravidanza aumentano ad ogni tentativo: è il concetto di probabilità cumulativa di gravidanza. Tutti gli studi effettuati in tal senso mostrano che la probabilità di successo aumenta effettuando più tentativi, ovvero più trasferimenti embrionari. In un ciclo di fecondazione in vitro possono prodursi più embrioni di quelli necessari ad un singolo trasferimento. Questi embrioni in “sovrannumero” vengono crioconservati e sono disponibili per transfer successivi.
Monitoraggio e Innovazioni nel Percorso PMA
Dopo il transfer a blastocisti, quando si può fare il test di gravidanza? Se si consulta una tabella dei valori beta post transfer blastocisti, è possibile notare che i valori sotto il 10 dosati dopo circa 5-6 giorni possono già preannunciare una gravidanza. L’ottenimento della gravidanza viene valutato tipicamente a due livelli: il test di gravidanza positivo (beta-hCG +) è il primo segnale di una gravidanza, riflesso del risultato del trattamento, e indica l’avvenuto impianto dell’embrione nell’utero, solitamente 14 giorni dopo il transfer.
Per le donne che hanno dovuto affrontare ripetuti fallimenti, la ricerca sta investendo sulla sperimentazione di plasma ricco in piastrine (PRP) da inserire direttamente in cavità uterina, in prossimità della fase di transfer dell’embrione. Queste innovazioni contribuiscono a massimizzare il tasso di successo della fecondazione assistita. La fecondazione in vitro (FIVET) prevede di ricreare in vitro tutti i processi che portano all’unione dei gameti. Di conseguenza, è necessario avere in laboratorio sia l’ovocita sia lo spermatozoo ed eseguire la fertilizzazione in provetta. FIVET e ICSI sono tecniche con un tasso di fecondazione leggermente diverso: mediamente 65% per FIVET e 75% per ICSI.
Un esempio tangibile dell'impatto della tecnologia e della competenza si riscontra nel racconto di una paziente: “Venivo da una serie di stimolazioni non riuscite e da quattro ICSI andate tutte male. Un medico, non so se definirlo tale, mi aveva detto che se volevo dei figli l’unica possibilità era l’ovodonazione. Mi sono rivolta a lui quando ancora non ero sposata, mi ha fatto fare delle cure pesantissime, punture e tutto, per farmi arrivare la mestruazione solo perché avevo l’ovaio micropolicistico e un ciclo non ovulatorio. Poi sono stata in Svizzera, dove ho fatto l’ICSI e due transfer a distanza di qualche mese, ma non è andata. Allora ho deciso di cambiare, ho cercato un’altra clinica vicino casa, ma anche lì, nonostante il prelievo ovocitario andasse bene, la coltura non andava oltre le 4 cellule. Ho fatto due volte il prelievo, due volte l’impianto e per due volte non è andata bene. A quel punto ho detto: basta, non faccio più niente, non ne voglio più sapere. Ero demoralizzata al massimo. Poi, viste le insistenze di mio suocero sono venuta a [nome clinica, omesso dal testo originale] dove ho deciso di riprovare. Ho fatto la visita con il Prof. Cerusico e la prima cosa che mi ha detto è stata «qui tu diventi mamma», questa è stata la sua prima parola." Questo sottolinea l'importanza di affidarsi ad un centro per la fertilità qualificato.
Nel contesto della fecondazione eterologa, specialmente con donazione di ovociti, si osservano numeri promettenti. I programmi si basano principalmente sull’importazione di cellule crioconservate da banche estere, dato il numero molto ridotto di donatrici di ovociti in Italia. L’estrema efficacia e sicurezza della tecnica di vitrificazione ovocitaria, quella che oggi usiamo per congelare gli ovociti, permette l’utilizzo di uova crioconservate con risultati pressoché paragonabili a quelli ottenuti con ovociti freschi. Un programma di fecondazione eterologa con ovociti donati crioconservati richiede che venga aumentato il numero di ovociti da assegnare ad ogni coppia, per ridurre al minimo il rischio di degenerazione dopo lo scongelamento e soprattutto per massimizzare i risultati clinici. Dall’analisi dei dati è emerso che il 57% degli ovociti che si fecondano correttamente dopo scongelamento e inseminazione mediante tecnica ICSI è in grado di raggiungere gli stadi più avanzati della coltura embrionale (cioè lo stadio di blastocisti). In media, a partire da 8 ovociti scongelati si ottengono 3.3 blastocisti. Ebbene, il 95,6% dei nostri cicli di scongelamento ovocitario si conclude con l’ottenimento di almeno una blastocisti da trasferire e nel 79,3% dei casi si ottengono blastocisti sovrannumerarie che possono essere crioconservate per futuri tentativi. I programmi di fecondazione assistita si basano sempre sul trasferimento di un singolo embrione allo stadio di blastocisti, per minimizzare il rischio di insorgenza di gravidanze multiple. Il tasso cumulativo di gravidanza a termine (ossia il numero totale di parti ottenuti dai cicli di scongelamento ovocitario e dagli eventuali successivi trasferimenti di embrioni crioconservati) per ciclo iniziato è pari al 50%. C’è da sottolineare, infine, che non è sempre necessario scongelare l’intero lotto di ovociti, ma che al fine di minimizzare il numero di embrioni sovrannumerari si può procedere con lo scongelamento di una parte di ovociti, mantenendo riservata alla coppia la restante parte.
Approcci al Trasferimento: Selettivo o Elettivo?
Il trasferimento può essere svolto durante la seconda o terza giornata dall’inseminazione oppure direttamente allo stadio di blastocisti, che corrisponde alla quinta/sesta giornata dalla fecondazione. In passato, la stragrande maggioranza dei centri di procreazione medicalmente assistita (PMA) promuovevano l’embryo-transfer in 2°-3° giornata scartando la possibilità di prolungare la coltura embrionaria. Mentre in passato si guardava alla coltura a blastocisti con molti timori, oggi si assiste allo scenario opposto, quasi un obbligo al trasferimento a blastocisti.
Molti utilizzano la metodica del transfer selettivo di blastocisti, che vuol dire arrivare a blastocisti solo se al giorno 3 si hanno molti embrioni di ottima forma (tipo 1 o tipo A). Tuttavia, si pensa invece che proprio nei casi in cui si hanno pochi embrioni al giorno 3 occorra verificare se questi sono in grado di raggiungere lo stadio di blastocisti, e soprattutto se sono di qualità inferiore. In tali circostanze, si propone il trasferimento embrionale a blastocisti “elettivamente” e non “selettivamente”.
Il trasferimento embrionale a blastocisti è particolarmente indicato in diverse situazioni: per poliabortività, come accennato in precedenza, la coltura a blastocisti è anche un metodo per selezionare naturalmente gli embrioni. Un'altra indicazione sono i pregressi fallimenti di fecondazione in vitro: in pazienti che hanno già affrontato delle PMA infruttuose, vanno analizzati tutta una serie di dati, tra i quali scratching e analisi dei linfociti natural killer ed evoluzione della coltura cellulare. Non è infrequente nell’esperienza clinica che blastocisti di ottima qualità biologica (grado 1) non abbiano dato gravidanza e invece, nel tentativo successivo, un embrione in 3°/4° giornata si sia impiantato con successo. Questo evidenzia la complessità e la variabilità individuale nel percorso PMA. Ottenute delle blastocisti in coltura, si può procedere all’embryo-transfer e/o alla crioconservazione. Ciò avviene quando si ottengono 3 o più blastocisti e quindi una o al massimo 2 vengono trasferite e quelle soprannumerarie vengono crioconservate mediante vitrificazione.
tags: #possibilita #di #successo #trafert #blastocisti