Introduzione: La Nausea e il Vomito in Gravidanza: Un Fenomeno Diffuso
La gravidanza, un periodo di profonde trasformazioni, è spesso accompagnata da sintomi che, sebbene comuni, possono influenzare significativamente la qualità della vita delle future madri. Più del 50% delle donne gravide presenta nausea e vomito, un disagio che si manifesta soprattutto nelle fasi precoci della gravidanza. Questa condizione, definita spesso "mattutina", in realtà, nella maggior parte delle gestanti si manifesta anche in altri momenti della giornata. La nausea è uno dei sintomi più frequenti nelle prime settimane di gravidanza; interessa 3 donne su 4 e tende a scomparire verso il terzo-quinto mese. Nel 50% circa dei casi è accompagnata da episodi più o meno frequenti di vomito.
La cura della maggior parte delle donne è gestita in maniera conservativa, attraverso semplici accorgimenti di natura alimentare, quali mangiare poco e spesso, preferire cibi solidi ad elevato contenuto di zuccheri e poveri di grassi, e bere a piccoli sorsi, evitando le bevande gasate. Queste misure dietetiche, in genere, migliorano e/o risolvono il problema. Tuttavia, dal 10% al 15% di queste donne con nausea e vomito riceve un trattamento farmacologico. In casi più gravi, l'iperemesi gravidica, che colpisce lo 0,3-2% delle gestanti, ne rappresenta la forma più severa ed è caratterizzata da sintomi persistenti che, se non corretti per tempo, possono dar luogo a complicanze come disidratazione, chetosi e alterazioni idroelettrolitiche. Le cause di questi disturbi non sono note con certezza, ma probabilmente vanno individuate nell'aumento dei livelli plasmatici di gonadotropina corionica umana, estrogeni e progesterone. Quando le misure dietetiche non sono sufficienti e la nausea risulta particolarmente disturbante, può essere necessario ricorrere al trattamento farmacologico.
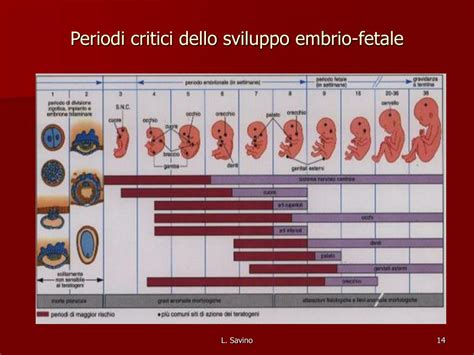
Il primo trimestre di gravidanza è il periodo in cui avviene l'organogenesi ed è quello più a rischio per il nascituro. Tradizionalmente, la metoclopramide viene spesso raccomandata quando il trattamento con antistaminici o con vitamina B6 fallisce. Nel nostro paese, l'unico farmaco registrato per il trattamento della nausea in gravidanza è la piridossina (vitamina B6), associata a tiamina e riboflavina nella specialità Biochetasi. Dai pochi dati disponibili, la sola piridossina, al dosaggio di 25 mg ogni 8 ore, sembra possedere qualche utilità nel controllo della nausea, mentre è inefficace contro il vomito. Tuttavia, quando queste opzioni non bastano, si ricorre a farmaci di seconda linea, tra cui la metoclopramide. La domanda chiave per le future mamme è: è efficace e sicura in gravidanza?

La Metoclopramide (Plasil): Meccanismo d'Azione e Indicazioni Terapeutiche
Il Plasil, il cui principio attivo è la metoclopramide, appartiene alla classe dei farmaci per i disturbi funzionali gastrointestinali e associa all'attività procinetica intestinale spiccate proprietà antiemetiche. La metoclopramide è un antagonista dopaminergico D2 con attività procinetica sul tratto gastrointestinale superiore e blanda azione antagonista 5-HT3 ad alte dosi. Questo meccanismo d'azione la rende efficace nel trattamento e nella prevenzione di nausea e vomito.
Le indicazioni terapeutiche di Plasil nella popolazione adulta sono molteplici:
- Prevenzione di nausea e vomito ritardati indotti da chemioterapia (CINV).
- Prevenzione di nausea e vomito indotti da radioterapia (RINV).
- Trattamento sintomatico di nausea e vomito, inclusi nausea e vomito indotti da emicrania acuta.La metoclopramide può essere utilizzata in associazione con analgesici orali per migliorare l'assorbimento degli analgesici nell'emicrania acuta.
Nonostante la metoclopramide sia uno dei farmaci più comunemente prescritti in gravidanza, le principali società scientifiche (ACOG, RCOG) inseriscono la metoclopramide in gravidanza tra le opzioni di seconda linea quando le misure non farmacologiche e i farmaci di prima scelta non sono sufficienti. È considerata una buona opzione con un buon profilo di efficacia come monoterapia o in combinazione, e la necessità di un'opzione parenterale (per esempio, in caso di vomito incoercibile) la rende particolarmente utile in contesti clinici come il pronto soccorso o il ricovero.
Sicurezza della Metoclopramide in Gravidanza: L'Evidenza dagli Studi
Il punto più sensibile e cruciale riguardo l'uso della metoclopramide è la sua sicurezza in gravidanza, specie nel primo trimestre, periodo fondamentale per l'organogenesi. Gli unici dati disponibili riguardanti la sicurezza dei farmaci in gravidanza provengono, di fatto, da serie di casi e da studi di coorte.
Ampiezza e Limiti degli Studi Precedenti
Gli studi pubblicati finora, che includono cinque studi di coorte con un totale di 4261 donne esposte in gravidanza e uno studio caso-controllo con un totale di 15 casi esposti alla metoclopramide di malformazioni congenite, non hanno trovato un incremento significativo del rischio di eventi maggiori in gravidanza, e di esiti fetali. Numerosi case reports e gli studi di coorte, retrospettivi e prospettici, disegnati con l'obiettivo di valutare la sicurezza della metoclopramide durante il primo trimestre di gravidanza non hanno evidenziato effetti dannosi sullo sviluppo embrio-fetale.
Sebbene questi risultati siano genericamente rassicuranti ed indichino che la metoclopramide non aumenta il rischio di malformazioni congenite, quando questi esiti sono valutati in aggregato, le malformazioni congenite sono un gruppo eterogeneo di disordini che andrebbero studiati singolarmente. Inoltre, nessuno studio con sufficiente potere statistico ha indagato il rischio di morte fetale con la profondità necessaria.
Lo Studio di Coorte Danese (1997-2011): Analisi Approfondita degli Esiti Fetali
Per valutare la sicurezza della metoclopramide in gravidanza in modo più robusto, gli autori di uno studio osservazionale retrospettivo di coorte (Register-based cohort study in Denmark) hanno utilizzato i dati del registro nazionale delle nascite, prendendo in esame il periodo dal 1997 al 2011. In questo periodo sono state registrate 1.222.503 gravidanze. Le donne esposte e non-esposte alla metoclopramide sono state classificate sulla base di età, anno e propensity score, garantendo una comparabilità tra i gruppi.
Gli outcome primari valutati erano le malformazioni congenite maggiori (20 categorie di singole malformazioni, selezionate in accordo ai criteri di potenza), gli aborti spontanei e la mortalità neonatale. Nelle analisi abbinate, è stata usata la regressione logistica per stimare le odds ratio di prevalenza delle malformazioni e la regressione di Cox per stimare le hazard ratio dell’aborto spontaneo.
I risultati di questo ampio studio sono stati significativi:
- Tra 28.486 donne esposte alla metoclopramide nel primo trimestre, 721 avevano avuto un bambino con una malformazione congenita maggiore (25.3 [95% IC, 23.5-27.1] casi per 1000 nascite), rispetto a 3024 tra 113.698 donne non-esposte (26.6 [95% IC, 25.7-27.5] per 1000 nascite). Non è stata osservata alcuna associazione significativa tra l’uso della metoclopramide e le malformazioni complessive (prevalence odds ratio 0.93, IC 95% 0.86-1.02) o ciascuna delle 20 categorie di malformazioni individuali.
- Queste 20 categorie includevano, ad esempio, difetti del tubo neurale, trasposizione dei grossi vasi, difetti del setto ventricolare, difetti del setto atriale, tetralogia di Fallot, coartazione dell’aorta, labbro leporino, palatoschisi, atresia/stenosi anorettale e riduzione degli arti. Il limite superiore dell’Intervallo di Confidenza al 95% è risultato inferiore a 2.0 per 17 delle 20 categorie, fornendo ulteriore rassicurazione.
- La metoclopramide non era associata ad incremento del rischio di aborto spontaneo (757 casi [20.0 {95% IC, 18.5-21.4} per 1000] tra 37.946 donne esposte alla metoclopramide e 9414 casi [62.1 {95% IC, 60.9-63.3} per 1000] tra 151.661 donne non-esposte; HR, 0.35 [95% IC, 0.33-0.38]).
- Non è stata associata ad incremento del rischio di mortalità neonatale (142 casi [3.5 {95% IC, 2.9-4.1} per 1000] tra 40.306 donne esposte alla metoclopramide e 634 casi [3.9 {95% IC, 3.6-4.2} per 1000] tra 161.098 donne non-esposte; HR, 0.90 [95% IC, 0.74-1.08]).
- Da sottolineare che dalla sesta alla quattordicesima settimana di gravidanza, l'incidenza cumulativa di aborto spontaneo è risultata del 3% nelle donne esposte al farmaco e del 10% in quelle non esposte (P <0,001), tassi che si sono mantenuti costanti fino alla ventiduesima settimana.
- Inoltre, nella valutazione di esiti secondari, non è stata trovata nessuna associazione tra uso di metoclopramide e parto pretermine, basso peso alla nascita o dimensioni ridotte per l'età gestazionale e neppure con malformazioni nei feti abortiti.
Questi dati sono stati pubblicati in JAMA nel 2013 da B. Pasternak, H. Svanström, D. Mølgaard-Nielsen, M. Melbye, A. Hviid nel loro studio "Metoclopramide in pregnancy and risk of major congenital malformations and fetal death".
UTILIZZO DEI FARMACI IN GRAVIDANZA
Lo Studio di Coorte Israeliano (Clalit Health Services): Ulteriori Risultati di Sicurezza
Un ulteriore studio di coorte israeliano, pubblicato nel giugno di un anno precedente nel New England Journal of Medicine e condotto da Matok I et al., ha corroborato questi risultati. Gli autori hanno incrociato le prescrizioni di metoclopramide contenute nel database del Clalit Health Service relativo al distretto sud di Israele, con i dati materno/fetali presenti nel database dell'ospedale distrettuale, nel periodo compreso tra il 1° gennaio 1998 e il 31 marzo 2007.
Sono stati registrati 113.612 parti singoli durante il periodo di studio. In totale 81.703 neonati (71,9%) sono nati da donne registrate nel Clalit Health Services; 3.458 di loro (4,2%) sono stati esposti a Metoclopramide durante il primo trimestre di gravidanza. Lo studio ha confrontato 3.458 esposti con 78.245 controlli.
L’esposizione a Metoclopramide, rispetto alla non-esposizione al farmaco, non è risultata associata a un aumento significativo del rischio di:
- Malformazioni congenite maggiori (5,3% e 4,9%, rispettivamente; odds ratio, OR=1,04; nessuna differenza tra i due gruppi per difetti congeniti, RR=0,9; IC 95% 0,3-2,4).
- Basso peso alla nascita (8,5% e 8,3%; OR=1,01).
- Parto prematuro (6,3% e 5,9%; OR=1,15).
- Morte perinatale (1,5% e 2,2%; OR=0,87; aborti spontanei, RR=0,8; IC 95% 0,2-2,9).
- Età gestazionale o peso neonatale.
Questi risultati forniscono una rassicurazione sulla sicurezza della Metoclopramide per il feto quando il farmaco è prescritto alle donne per alleviare nausea e vomito in gravidanza.
Conclusioni sulla Sicurezza Fetale della Metoclopramide
In sintesi, l’uso di metoclopramide in gravidanza non è risultato associato ad un aumentato rischio di malformazioni congenite in generale, né ad alcuna delle 20 categorie di malformazioni specifiche valutate. Allo stesso modo, non è stata riscontrata un'associazione con un aumento del rischio di aborto spontaneo, mortalità neonatale, nascita pretermine, basso peso alla nascita o ridotta crescita fetale.
Questi dati di safety sono di fondamentale importanza e possono aiutare a prendere decisioni informate quando viene considerato il trattamento con metoclopramide in gravidanza, offrendo una solida base di evidenze sulla sua sicurezza in relazione agli esiti fetali più temuti.
Raccomandazioni Cliniche e Regolatorie sull'Uso della Metoclopramide in Gravidanza
Nonostante i dati rassicuranti sulla sicurezza fetale della metoclopramide, l'approccio al suo utilizzo in gravidanza varia a livello internazionale a causa delle diverse interpretazioni delle evidenze e delle normative locali.
Classificazione e Linee Guida Internazionali
- Australian Drug Evaluation Committee (ADEC): Ha inserito la metoclopramide nella categoria A. Questa categoria include farmaci assunti da un elevato numero di donne in età fertile e in gravidanza senza che si sia osservato un aumento dell'incidenza di malformazioni, o di altri effetti negativi diretti o indiretti sul feto.
- SSN Britannico (Clinical Knowledge Summaries, CKS): Afferma che, nonostante l'assenza di antiemetici registrati specificamente per il trattamento della nausea e del vomito in gravidanza, in caso di necessità, prometazina e ciclizina sono i farmaci di prima scelta. Metoclopramide o proclorperazina sono da utilizzare in seconda battuta se dopo 24-48 ore il controllo dei sintomi non risulta adeguato.
- Principali Società Scientifiche (ACOG, RCOG): Come già menzionato, inseriscono la metoclopramide tra le opzioni di seconda linea quando le misure non farmacologiche e i farmaci di prima scelta non sono sufficienti.
Disparità nelle Schede Tecniche Nazionali
Esistono sostanziali difformità nella collocazione della metoclopramide nelle schede tecniche dei diversi paesi, in particolare in quelli in cui non è registrata nel trattamento della nausea in gravidanza, come USA, Canada, Italia e Inghilterra.
- In quella italiana, la gravidanza viene addirittura riportata tra le controindicazioni.
- Le schede tecniche americana e canadese collocano la metoclopramide nel Pregnancy category B, ossia tra i farmaci per i quali "gli studi riproduttivi condotti nell'animale da esperimento, a dosaggi massimi superiori di 12-250 volte il dosaggio comunemente impiegato nell'uomo non hanno evidenziato alcuna compromissione della fertilità o danno fetale". Questa discrepanza sottolinea la necessità di un'attenta valutazione del rapporto rischio-beneficio da parte del medico curante.
Restrizioni Regolatorie sulla Durata del Trattamento
Le autorità regolatorie hanno introdotto restrizioni specifiche sull'uso della metoclopramide per limitare il rischio di effetti avversi, in particolare quelli neurologici, che possono essere cumulativi con l'uso prolungato:
- Europa (EMA): È raccomandato l’impiego a breve termine, in genere per un periodo non superiore a 5 giorni, con dosi massime giornaliere definite.
- Stati Uniti (FDA): Il foglietto illustrativo riporta un "boxed warning" (un avvertimento incorniciato, il più serio che la FDA possa imporre) e sconsiglia trattamenti superiori alle 12 settimane per il rischio di discinesia tardiva (TD).L'uso prolungato è sconsigliato per il rischio cumulativo di eventi neurologici. Prima di iniziare il trattamento, il medico valuta la storia clinica e i farmaci concomitanti per ridurre eventi avversi e interazioni. Il suo impiego deve seguire precisi principi di prudenza: limitare la durata, rispettare dosi e indicazioni, monitorare l'eventuale comparsa di sintomi neurologici e inserire il farmaco in una strategia graduale e personalizzata, come raccomandato dalle linee guida ostetriche.
Rischi e Controindicazioni della Metoclopramide: Attenzione agli Effetti Avversi
Sebbene i dati sulla sicurezza fetale siano rassicuranti, sul versante materno, l’attenzione principale riguarda gli effetti neurologici. Come tutti i medicinali, Plasil può causare effetti indesiderati sebbene non tutte le persone li manifestino.
Effetti Neurologici
Si possono verificare disturbi extrapiramidali, in particolare nei bambini e nei giovani adulti e/o con l’uso di dosi elevate. Queste reazioni si verificano in genere all’inizio del trattamento e possono presentarsi anche dopo una singola somministrazione. La metoclopramide deve essere immediatamente sospesa in caso di sintomi extrapiramidali. Questi effetti sono generalmente del tutto reversibili dopo l’interruzione del trattamento ma possono richiedere un trattamento sintomatico (benzodiazepine nei bambini e/o farmaci anticolinergici e antiparkinsoniani negli adulti).Le reazioni avverse comuni includono:
- Disturbi extrapiramidali: In particolare in bambini e giovani adulti e/o quando si superano le dosi raccomandate, anche in seguito alla somministrazione di una singola dose del farmaco. Questi includono distonia, discinesia, parkinsonismo (rigidità, tremore, bradicinesia) e acatisia (irrequietezza motoria).
- Discinesia tardiva: Può essere persistente e potenzialmente irreversibile, durante o dopo trattamento prolungato, in particolare nei pazienti anziani. La durata del trattamento non dovrebbe superare i 3 mesi a causa di questo rischio. Il trattamento deve essere interrotto se compaiono sintomi di discinesia tardiva.
- Sindrome neurolettica maligna: È stata segnalata con metoclopramide in associazione ai neurolettici come anche in monoterapia con metoclopramide. In caso di sintomi di sindrome neurolettica maligna (febbre, rigidità muscolare, alterazione dello stato mentale, instabilità autonomica), la metoclopramide deve essere interrotta immediatamente e deve essere istituito il trattamento adeguato.
- Convulsioni: Raro, in particolare in pazienti epilettici. Occorre particolare cautela in pazienti con patologie neurologiche concomitanti e in pazienti trattati con altri farmaci che agiscono sul sistema nervoso centrale.
- Esacerbazione del Morbo di Parkinson: I sintomi del morbo di Parkinson possono essere esacerbati dalla metoclopramide.
- Sonnolenza: Molto comune.
- Riduzione del livello di coscienza: Non comune.
- Confusione, allucinazioni: Non comune o raro.
- Ideazione suicidaria: Non nota.
Effetti Cardiovascolari
Sono stati riferiti gravi effetti cardiovascolari indesiderati, inclusi casi di collasso circolatorio, grave bradicardia, arresto cardiaco e prolungamento dell'intervallo QT a seguito di somministrazione di metoclopramide iniettabile, in particolare per via endovenosa.
- Bradicardia: Non comune, in particolare con la formulazione endovenosa.
- Arresto cardiaco, blocco atrioventricolare, arresto sinusale: Non nota, che si verifica poco dopo l’uso iniettabile, e che può essere conseguente a bradicardia.
- Prolungamento dell’intervallo QT dell’elettrocardiogramma, torsade de pointes: Non nota.
- Ipotensione: Comune, in particolare con la formulazione endovenosa.
- Shock, sincope: Non nota, dopo la somministrazione per via iniettabile.
- Ipertensione acuta: Non nota, nei pazienti con feocromocitoma.
Si deve prestare particolare cautela nella somministrazione di metoclopramide, in particolare per via endovenosa, agli anziani, a pazienti con disturbi della conduzione cardiaca (compreso il prolungamento dell'intervallo QT), a pazienti con squilibrio elettrolitico non corretto, bradicardia e a pazienti che assumono altri farmaci noti per prolungare l'intervallo QT. Le dosi endovenose devono essere somministrate in bolo lento (almeno della durata di 3 minuti) al fine di ridurre il rischio di effetti avversi (p. es., ipotensione, acatisia).
Effetti Endocrini
Il possibile incremento dei livelli di prolattina dovrebbe essere attentamente considerato, in particolare nei pazienti affetti da tumore al seno o da adenoma ipofisario secernente prolattina. Le patologie endocrine durante il trattamento prolungato in relazione all’iperprolattinemia possono includere amenorrea (non comune), galattorrea (raro) e ginecomastia (non nota).
Altri Effetti Indesiderati
- Metemoglobinemia: Non nota, possibilmente correlata al deficit di NADH citocromo b5 reduttasi, in particolare nei neonati. In tali casi, la metoclopramide deve essere interrotta immediatamente e permanentemente e devono essere adottate appropriate misure (come il trattamento con blu di metilene).
- Sulfemoglobinemia: Non nota, principalmente con la somministrazione concomitante di elevate dosi di prodotti medicinali che rilasciano zolfo.
- Diarrea: Comune.
- Astenia: Comune.
- Ipersensibilità, reazione anafilattica (incluso shock anafilattico): Non comune o non nota, in particolare con la formulazione endovenosa.
Controindicazioni Assolute
La metoclopramide è controindicata in determinate condizioni per evitare gravi rischi:
- Feocromocitoma: Rischio di crisi ipertensiva acuta.
- Epilessia non controllata.
- In caso di pregresse reazioni extrapiramidali severe al farmaco.
- Emorragia gastrointestinale, ostruzione meccanica o perforazione intestinale, dove l'aumento della motilità gastrointestinale potrebbe essere dannoso.
- Bambini di età inferiore a 1 anno.
Interazioni Farmacologiche Significative
Informare il medico o il farmacista se si è recentemente assunto qualsiasi altro medicinale, anche quelli senza prescrizione medica, poiché la metoclopramide può interagire con diversi farmaci.
- Associazioni controindicate: Levodopa o agonisti dopaminergici e metoclopramide si antagonizzano vicendevolmente.
- Associazioni da evitare: L'alcol potenzia l'effetto sedativo della metoclopramide.
- Associazioni da tenere in considerazione:
- Anticolinergici e derivati della morfina: Potrebbero entrambi avere effetto antagonista verso la metoclopramide sulla motilità del tratto digerente.
- Farmaci deprimenti il sistema nervoso centrale (derivati della morfina, ansiolitici, antistaminici H1 sedativi, antidepressivi sedativi, barbiturici, clonidina e farmaci correlati): Gli effetti sedativi di questi farmaci e della metoclopramide risultano potenziati. Cautela con farmaci che deprimono il sistema nervoso centrale.
- Neurolettici: La metoclopramide potrebbe avere un effetto additivo con altri neurolettici nel caso di disordini extrapiramidali.
- Farmaci serotoninergici: L'utilizzo di metoclopramide con farmaci serotoninergici come gli SSRI può aumentare il rischio di sindrome serotoninergica.
- Digossina: La metoclopramide potrebbe ridurre la biodisponibilità della digossina. È necessario un attento monitoraggio delle concentrazioni plasmatiche di digossina.
- Ciclosporina: La metoclopramide aumenta la biodisponibilità della ciclosporina (Cmax del 46% ed esposizione del 22%). È necessario un attento monitoraggio delle concentrazioni plasmatiche di ciclosporina. Le conseguenze cliniche sono incerte.
- Mivacurio e sussametonio: L'iniezione di metoclopramide può prolungare la durata del blocco neuromuscolare (tramite inibizione delle colinesterasi plasmatiche).
- Forti inibitori del CYP2D6: I livelli di esposizione della metoclopramide aumentano, quando somministrata in concomitanza a forti inibitori del CYP2D6 come fluoxetina e paroxetina. Benché la significatività clinica sia incerta, i pazienti dovrebbero essere monitorati per reazioni avverse.
- Cisplatino: Alcune osservazioni riportano, con metoclopramide, un aumento della tossicità renale del cisplatino.
- Insulina: Riducendo il transito intestinale anche del cibo, il trattamento con metoclopramide può richiedere un aggiustamento del dosaggio di insulina nel diabete.
- Apomorfina: La metoclopramide riduce gli effetti dell'apomorfina sul Sistema Nervoso Centrale.
Considerazioni Specifiche per l'Uso nel Terzo Trimestre di Gravidanza
La questione specifica dell'uso di Plasil nel terzo trimestre di gravidanza merita un'attenzione particolare, data la vicinanza al parto e le potenziali implicazioni per il neonato. Chiedere consiglio al medico o al farmacista prima di prendere qualsiasi medicinale in questo periodo è fondamentale.
Una vasta quantità di dati su donne in gravidanza (più di 1.000 esiti di esposizione) indica assenza di tossicità malformativa e fetotossicità. Pertanto, se clinicamente necessario, la metoclopramide può essere utilizzata durante la gravidanza. Tuttavia, l'attenzione si sposta sulle proprietà farmacologiche della metoclopramide, simili a quelle di altri neurolettici, che possono avere effetti sul neonato se somministrata nelle fasi finali della gestazione.
A causa delle sue proprietà farmacologiche, in caso di somministrazione di metoclopramide alla fine della gravidanza, non si può escludere la sindrome extrapiramidale nel neonato. Questa sindrome può manifestarsi con movimenti incontrollabili (spesso a carico di testa o collo), tremori, rigidità o difficoltà di alimentazione. Sebbene questi sintomi siano solitamente reversibili, la loro comparsa nel neonato può essere fonte di preoccupazione e richiedere interventi medici.
Per queste ragioni, la metoclopramide dovrebbe essere evitata alla fine della gravidanza, se possibile. Se l'uso della metoclopramide è considerato indispensabile nel terzo trimestre, si deve istituire un monitoraggio neonatale per rilevare precocemente eventuali segni di sindrome extrapiramidale o altri effetti avversi e gestirli tempestivamente.
Dosi e Modalità di Somministrazione
Le formulazioni disponibili includono compresse, gocce orali e fiale IM/EV, utili nei setting di pronto soccorso o ricovero. Per minimizzare i rischi e massimizzare l'efficacia, è essenziale seguire le dosi e le modalità di somministrazione raccomandate.
Dosi per Pazienti Adulti
Per tutte le indicazioni nella popolazione adulta:
- La dose singola raccomandata è di 10 mg, ripetibile per un massimo di 3 volte al giorno.
- La dose giornaliera massima raccomandata è di 30 mg o 0,5 mg/kg di peso corporeo.
- La durata massima raccomandata del trattamento è di 5 giorni.
Si consiglia la somministrazione del farmaco alle dosi indicate, preferibilmente prima dei pasti. Deve essere rispettato un intervallo minimo di 6 ore fra due somministrazioni, anche in caso di vomito o rigetto della dose, al fine di evitare casi di sovradosaggio e accumulo del farmaco che potrebbe aumentare il rischio di effetti avversi neurologici.
Dosi per Pazienti Pediatrici (età compresa tra 1 e 18 anni)
Per la prevenzione di nausea e vomito ritardati indotti da chemioterapia (CINV):
- La dose raccomandata è da 0,1 a 0,15 mg/kg di peso corporeo, ripetibile fino a tre volte al giorno per via orale.
- La dose massima in 24 ore è di 0,5 mg/kg di peso corporeo.
Di seguito una tabella di dosaggio indicativa:
- 1-3 anni (10-14kg): 1mg, fino a 3 volte al giorno.
- 3-5 anni (15-19kg): 2mg, fino a 3 volte al giorno.
- 5-9 anni (20-29kg): 2,5mg, fino a 3 volte al giorno.
- 9-18 anni (30-60kg): 5mg, fino a 3 volte al giorno.
- 15-18 anni (Oltre 60kg): 10mg, fino a 3 volte al giorno.
La durata massima del trattamento è di 5 giorni anche per la prevenzione di nausea e vomito ritardati indotti da chemioterapia (CINV) nella popolazione pediatrica. Le compresse non sono adatte all’utilizzo nei bambini con peso inferiore a 61 kg. Altre forme farmaceutiche/dosaggi possono essere più appropriate per la somministrazione in questa popolazione.
Aggiustamenti in Popolazioni Speciali
In pazienti con funzionalità renale o epatica compromessa, o negli anziani, è necessario un aggiustamento del dosaggio.
- Anziani: Occorre considerare una riduzione della dose in base alla funzionalità renale ed epatica e alla suscettibilità generale.
- Insufficienza renale:
- In pazienti con malattia renale in fase finale (Clearance della creatinina ≤ 15 ml/min), la dose giornaliera deve essere ridotta del 75%.
- In pazienti con insufficienza renale da moderata a grave (Clearance della creatinina 15-60 ml/min), la dose giornaliera deve essere ridotta del 50%.
- Insufficienza epatica: In pazienti con grave insufficienza epatica, la dose deve essere ridotta del 50%.
Altre forme farmaceutiche/dosaggi possono essere più appropriate per la somministrazione in queste popolazioni specifiche.
Uso in Allattamento
La metoclopramide è escreta nel latte materno a bassi livelli. Tuttavia, non si possono escludere reazioni avverse nel bambino allattato al seno. I possibili effetti sul lattante includono sonnolenza e irritabilità. Inoltre, la metoclopramide è nota per aumentare i livelli di prolattina, il che, sebbene possa favorire la lattazione, solleva interrogativi sulla sua sicurezza a lungo termine per il bambino.
Pertanto, la metoclopramide non è raccomandata durante l’allattamento al seno. Si deve prendere in considerazione l’interruzione della metoclopramide nelle donne che allattano al seno oppure l'interruzione dell'allattamento stesso, valutando caso per caso i benefici del farmaco per la madre contro i potenziali rischi per il lattante. È sempre consigliabile parlarne con il pediatra o il medico curante per una decisione informata e personalizzata.
tags: #plasil #in #gravidanza #terzo #trimestre