L’infertilità rappresenta una sfida clinica e sociale di crescente rilevanza, colpendo dal 10% al 20% delle coppie nei paesi occidentali. A fronte di questo scenario, un numero crescente di coppie fa ricorso alle tecniche di procreazione medicalmente assistita (PMA), tra cui l’inseminazione intrauterina, l’induzione farmacologica dell’ovulazione, la fecondazione in vitro con trasferimento dell’embrione (IVF) e la microiniezione intracitoplasmatica degli spermatozoi (ICSI). A oggi, il numero di bambini concepiti con la procreazione assistita rappresenta l’1-4% delle nascite nei paesi sviluppati.

La complessità della valutazione del rischio nelle tecniche di PMA
Se da un lato è importante sottolineare la necessità di un monitoraggio della sicurezza di queste procedure, nella valutazione del rischio è opportuno anche considerare la complessità del contesto. La maggior parte delle procedure di procreazione assistita prevede il trasferimento in utero di più embrioni, con conseguente aumento della frequenza di gestazioni multigemellari. A questo si associano maggiori rischi per la salute sia delle madri (per esempio parto cesareo) sia dei bambini (per esempio nascita pretermine, peso ridotto alla nascita, mortalità infantile, elevato rischio di malformazioni, disabilità).
Un rischio della procreazione assistita, compresa la fertilizzazione in vitro, sembra essere il peso ridotto alla nascita. L’impianto embrionale può essere alterato dal numero di embrioni trasferiti e dall’aborto di uno o più degli embrioni. Anche l’infertilità può influenzare l’esito perinatale, compreso il rischio di anomalie congenite. Questo effetto potrebbe essere dovuto alle cause sottostanti l’infertilità (per esempio patologie delle cervice, anovulazione, sindrome dell’ovaio policistico, bassa qualità dello sperma). Pertanto è difficile distinguere gli effetti derivanti dall’infertilità da quelli legati all’impiego delle tecniche di procreazione assistita sulla sicurezza dei bambini e delle madri. In ogni caso, la possibilità che sussistano cause alternative, spesso procedurali, a quelle farmacologiche all’insorgenza di eventi avversi rende particolarmente complessa sia la segnalazione spontanea del singolo caso sia la valutazione dei dati aggregati provenienti dalla segnalazione spontanea stessa.
Da queste considerazioni emerge la necessità di nuovi studi al fine di comprendere i meccanismi che stanno per esempio alla base delle anomalie congenite nei bambini concepiti attraverso procreazione assistita. Inoltre, per la valutazione della sicurezza d’impiego di queste tecniche e lo sviluppo di opportune strategie di prevenzione potrebbe essere utile istituire dei registri nazionali su tipo di procedura impiegata, caratteristiche dei genitori, anomalie congenite dei feti, esiti della gravidanza.
Implicazioni epigenetiche e tecniche di fecondazione
L’applicazione della tecnica ICSI non è esente da potenziali conseguenze dannose, come riportato da nuovi studi sulle possibili conseguenze sulla salute della prole. Metilazione del DNA e alterazioni epigenetiche negli spermatozoi di uomini infertili potrebbero aiutare a spiegare alcuni degli effetti avversi riportati negli studi ICSI sull’salute riproduttiva nelle generazioni future. La salute dei bambini ICSI negli ultimi trent’anni sembra sostenere l’idea che potrebbe esserci un aumento del rischio di disturbi epigenetici, malformazioni congenite, alterazioni cromosomiche e subfertilità nei bambini nati a seguito dell’ICSI rispetto ai bambini concepiti naturalmente.
cromatina e epigenetica
Esiste una panoramica dei meccanismi epigenetici e delle possibili alterazioni dell’imprinting in seguito all’utilizzo dell’ART, in particolare dell’ICSI. Evidenzia anche il contributo degli spermatozoi alla regolazione epigenetica dell’embrione e i rischi delle condizioni di coltura in vitro sulla disregolazione epigenetica. Il processo di fecondazione in vitro dipende principalmente da tre procedure: stimolazione ovarica, fecondazione in vitro o ICSI e coltura di embrioni. La maggior parte dei bambini sottoposti a ART sono sani. Tuttavia, studi recenti riportano che i nati a seguito di trattamenti IVF/ICSI hanno un rischio maggiore di eventi avversi perinatali, che potrebbero essere associati a disregolazione epigenetica, come anormali placentazione o basso peso alla nascita.
A causa dell’invasività dell’ICSI come metodo di fecondazione, la tecnica è spesso dibattuta come potenzialmente causa di disregolazione epigenetica. L’ICSI è una procedura consolidata applicata in tutto il mondo per il trattamento delle coppie con infertilità. Data l’importanza dell’epigenoma degli spermatozoi per l’embriogenesi precoce, è necessario affrontare la questione dell’utilizzo dello sperma di uomini con problemi di fertilità per l’ICSI. Circa il 15% dei casi di infertilità maschile comporta alterazioni genetiche, come anomalie nel cariotipo e microdelezioni sul cromosoma Y, con conseguente grave oligozoospermia e azoospermia. La regolazione epigenetica dell’attività genetica rappresenta un aspetto critico della funzione spermatica e della relativa capacità fecondante; l’interruzione dell’epigenoma paterno può indurre infertilità maschile e trasferire aberranti informazioni all’embrione.
La biologia del gamete e il ruolo della cromatina
Un elemento chiave del controllo della funzione dei gameti maschili riguarda la modificazione post-traduzionale degli istoni (organelli su cui è arrotolato il DNA), come metilazione, acetilazione e fosforilazione, che consente l’attivazione o la repressione dei geni sottostanti. Le modifiche degli istoni sono essenziali nel governare i processi cellulari, come la trascrizione, la riparazione del DNA, la replicazione del DNA e la condensazione dei cromosomi. Un recente studio ha riportato la riduzione complessiva dell’acetilazione H4 e alterazioni della metilazione negli uomini astenoteratozoospermici rispetto ai normozoospermici.
Nel 1942, Conrad Waddington sottolineò l’importanza dell’attenzione ai cambiamenti ambientali durante le prime fasi dello sviluppo dell’embrione introducendo il termine “epigenetica”, che rappresenta un meccanismo di regolazione genetica. I processi epigenetici includono la metilazione del DNA, le modifiche degli istoni e il rimodellamento della cromatina. Il DNA racchiuso attorno agli istoni dà luogo alla formazione di nucleosomi. La particolare disposizione del DNA stabilisce se un gene sarà trascrizionalmente attivo o silente. Porzioni altamente compattate del DNA, chiamate eterocromatina, sono trascrizionalmente silenziate, mentre tratti debolmente legati agli istoni sono chiamati eucromatina e sono trascrizionalmente attivi. L’epigenetica controlla la compattezza e la riprogrammazione del DNA, svolgendo un ruolo vitale nella regolazione di quali geni sono attivi, quando sono attivi e in quali tessuti.
A seguito della fecondazione dell’ovocita da parte dello spermatozoo si forma l’embrione, la prima cellula del nuovo individuo che si moltiplica sviluppando circa 200 cellule al 5°-6° giorno, prendendo il nome di blastocisti, già differenziate in due tipi: il trofettoderma (TE) e la massa cellulare interna (Inner Cell Mass), quest’ultima comprende un gruppo di cellule fissate all’interno del trofectoderma, che alla fine darà origine al feto. Le cellule TE sono quelle dello strato esterno della blastocisti, promuovendo il processo di impianto nel rivestimento dell’utero e nella formazione di altri tessuti extraembrionali, compresa la placenta. Le cellule embrionali vengono guidate durante lo sviluppo iniziale attraverso la riprogrammazione epigenetica e il successivo ristabilimento delle firme epigenetiche specifiche del tipo cellulare.
Questo coincide con il periodo in cui i gameti e gli embrioni vengono coltivati all’interno del laboratorio di embriologia. Pertanto, durante questa finestra temporale critica, eventuali perturbazioni artificiali potrebbero provocare modifiche epigenetiche nella prole con la possibile formazione di alterazioni dell’imprinting e di errori di metilazione del DNA nei geni impressi nei bambini nati dopo la ART rispetto a quelli concepiti naturalmente. I cambiamenti nella metilazione del DNA con l’invecchiamento potrebbero aumentare il rischio di sviluppare disturbi dello sviluppo neurologico nella prole.
Dinamiche della riprogrammazione durante la spermatogenesi
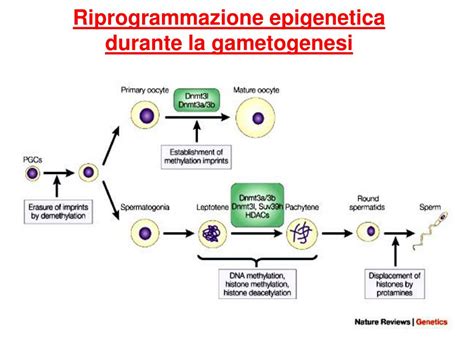
Le due principali ondate di riprogrammazione epigenetica si verificano durante la gametogenesi e dopo la fecondazione. Durante la gametogenesi, la maggior parte dei segni epigenetici parentali viene cancellata e ristabilita al momento dell’ovogenesi e della spermatogenesi. Una seconda onda di riprogrammazione epigenetica avviene subito dopo la fecondazione con una demetilazione paterna rapida e attiva e una demetilazione materna più lenta e passiva. La spermatogenesi può essere descritta da tre fasi principali: in primo luogo, la mitosi con la moltiplicazione degli spermatogoni, poi la meiosi per ridurre il numero di cromosomi da diploide ad aploide, e infine la spermiogenesi, che indica la riuscita maturazione degli spermatidi rotondi in spermatozoi.
Tutti questi processi sono collegati tra loro e sono responsabili della normale produzione di gameti; la dinamica della riprogrammazione epigenetica e i loro sistemi regolatori sono fondamentali per la normale spermatogenesi e qualsiasi alterazione durante la spermatogenesi può causare una riduzione della quantità e qualità dello sperma. Vi è una cascata di cambiamenti epigenetici durante le fasi iniziali dello sviluppo delle cellule germinali primordiali (PGC), che indicano eventuali alterazioni nella regolazione della funzione e dell’espressione genica durante la gametogenesi. Eventuali disturbi di queste regolazioni epigenetiche potrebbero provocare diversi stadi di infertilità, il che potrebbe essere trasferito alle generazioni future. Dopo che la spermatogenesi è completata, la maturazione extra avviene nell’epididimo.
Indicatori prognostici e selezione delle procedure
L’ICSI dovrebbe essere incoraggiata soprattutto in caso di grave infertilità maschile. La valutazione degli spermatozoi con l’analisi del liquido seminale presenta dei limiti; ad esempio, non valuta la funzione e la fisiologia dello sperma e la valutazione genetica o epigenetica. Il numero, la morfologia e la motilità vengono generalmente valutati per decidere sulla procedura ICSI piuttosto che l’inseminazione IVF standard. Nella oligoastenoteratozoospermia la morfologia degli spermatozoi è un altro parametro ampiamente utilizzato per scegliere l’ICSI, utilizzata di routine nei casi di pazienti con morfologia spermatica ridotta (<5%). L’esecuzione di ICSI o IVF non ha alcuna differenza negli esiti della gravidanza nei pazienti con teratozoospermia grave.
Il test di frammentazione del DNA viene applicato per valutare la rottura dei filamenti di DNA all’interno della testa dello sperma. La frammentazione del DNA spermatico (SDF) è generalmente indotto dallo stress ossidativo derivante da fattori ambientali e di stile di vita come il fumo, le infezioni del tratto genitale, l’obesità e la nutrizione. Inoltre, la SDF è frequentemente rilevata negli uomini con problemi di infertilità (ad esempio varicocele) ed è più diffuso in quegli individui rispetto alle controparti fertili. Le prove scientifiche indicano che un livello elevato di SDF compromette le probabilità di successo dopo la ART; i tassi di gravidanza clinica erano più alti nei pazienti sottoposti a fecondazione in vitro i cui partner maschi avevano bassi livelli di SDF. Pertanto, sembra ragionevole suggerire ICSI piuttosto che IVF standard nelle coppie con SDF elevato.
Con l’ICSI, tutti questi processi vengono superati, facendo nascere il dubbio che le tecniche di riproduzione assistita potrebbero alterare la riprogrammazione epigenetica e infine lo sviluppo. La regolazione epigenetica potrebbe essere modulata da fattori esterni ed interni, inclusa l’esposizione ambientale, l’alimentazione e lo stress. Su questa base, le condizioni di infertilità maschile influiscono sulla qualità dello sperma ed è stato suggerito che influenzino l’epigenoma degli spermatozoi. Infatti, la metilazione aberrante del DNA ai geni impressi è stata associata a spermatogenesi anormale e al fattore di infertilità maschile. È stata collegata l’ipometilazione del DNA nel locus del gene H19 negli spermatozoi all’oligozoospermia e all’azoospermia. Quindi, gli spermatozoi di pazienti infertili potrebbero avere maggiori probabilità di trasmettere impronte errate alla loro prole, suggerendo una correlazione tra genomica aberrante, imprinting e ipospermatogenesi. Gli spermatozoi di uomini oligozoospermici potrebbero comportare un rischio maggiore di trasmettere alterazioni dell’imprinting.
L’imprinting negli ovociti e negli embrioni è sensibile ai cambiamenti ambientali. I segni epigenetici vengono acquisiti durante la prima fase della gametogenesi, la formazione e migrazione delle PGC nella cresta gonadica, e successivamente durante i primi giorni di sviluppo dell’embrione. La corretta definizione dei modelli epigenetici è essenziale per lo sviluppo dell’embrione. L’uso eccessivo dell’ICSI dovrebbe essere attentamente valutato, date le sue potenzialità per rischi genetici ed epigenetici. Prove “limitate” suggeriscono che i bambini nati in seguito alla procedura ICSI hanno un rischio aumentato di malformazioni congenite, anomalie cromosomiche e profili ormonali riproduttivi alterati rispetto ai bambini concepiti naturalmente.
Procreazione Medicalmente Assistita e demografia: un contesto italiano
Dal 1861, il tasso di natalità è in costante calo, con la fertilità stabilmente sotto il tasso di sostituzione, minacciando la stabilità economica e sociale. Le cause principali includono stili di vita, fattori ambientali, età avanzata delle coppie e condizioni patologiche. La PMA aiuta a preservare la fertilità, ottimizzare il recupero ovocitario, superare barriere fisiche alla fecondazione e selezionare embrioni con maggiori possibilità di impianto, contribuendo alla lotta contro la denatalità con oltre 10 milioni di nascite in 40 anni.
La “Gravidanza per altri” (GPA) è un percorso di PMA nel quale una donna gestisce una gravidanza per conto di un’altra persona o coppia. È indicata in caso di assenza o malformazioni dell’utero, rischi per la salute della gestante o del nascituro, aborti ricorrenti o fallimenti di PMA. L’infertilità femminile è la condizione che ostacola la possibilità per la donna di ottenere una gravidanza. Esistono numerose cause di infertilità femminile: alterazioni dell’apparato riproduttivo, malformazioni congenite, infezioni, disfunzioni ormonali.
Diagnostica ormonale e anatomica
I dosaggi del 3° giorno (FSH, Estradiolo, Progesterone, LH, TSH, Prolattina) sono fondamentali. Questi ormoni sono prodotti dall’ipofisi (FSH, LH) o dall’ovaio (estradiolo e progesterone); variano a seconda del giorno del ciclo in cui si studiano ma, per lo studio di base, è necessario che FSH, LH ed estradiolo si analizzino tra il 3º e il 5º giorno del ciclo. Se alti valori di AMH possono fungere da indicatori della sindrome dell’ovaio policistico, bassi valori dell’AMH possono essere l’indice di un’insufficienza ovarica primaria o, comunque, possono consentire di valutare una progressiva riduzione della fertilità. Per la definizione di un quadro completo, da questo punto di vista, è opportuno accompagnare l’esame di questi valori a una valutazione globale diretta anche ad accertare i livelli di estradiolo, testosterone, progesterone e FSH e anche un’ecografia della Conta Antrale eseguita da uno specialista del settore.
In generale, nella ricerca di una gravidanza spontanea, più è basso il livello di AMH, più difficile sarà ottenerla, per il ridotto numero di follicoli a disposizione. I valori dell’ormone antimulleriano, oltre a consentire di valutare la riserva ovarica, sono particolarmente utili nei casi in cui si decida di procedere alla procreazione medicalmente assistita. Lo studio del livello dell’AMH consente di valutare in maniera adeguata il protocollo di stimolazione e la concentrazione farmacologica più adatta al singolo caso e, di conseguenza, permette di creare una terapia “ad hoc” in grado di massimizzare i risultati in base alle condizioni della paziente.
La sonoisterosalpingografia è un esame ambulatoriale mediante il quale è possibile valutare i contorni e l’elasticità della parete uterina, i rapporti con le salpingi (tube) ed anche la pervietà di queste ultime. Un’ostruzione di una o entrambe le tube ostacolerebbe il processo di fecondazione naturale. Sotto guida ecografica si segue il passaggio della soluzione fisiologica perfusa in utero e nelle salpingi con un semplice catetere a palloncino: in tal modo è possibile porre un sospetto di ostruzione tubarica, ma anche indagare la cavità uterina interna e rilevare eventuali miomi sottomucosi, polipi e sinechie grazie alla capacità della soluzione fisiologica di distendere la cavità uterina. L’ecografia pelvica transvaginale è un esame diagnostico semplice che consente di definire aspetti organici e funzionali dell’apparato genitale interno. La diagnostica endometriale comprende lo scratch endometriale, l’isteroscopia, la biopsia endometriale e test di nuova generazione.
Recettori KIR e compatibilità genetica
A livello uterino, tutte le donne hanno alcune cellule con un recettore chiamato KIR che presenta tre grandi gruppi genetici: KIR AA, KIR AB e KIR BB. Questi recettori sono responsabili di riconoscere la parte estranea dell’embrione. Nella riproduzione assistita con ovociti propri della donna e nella riproduzione naturale, questi recettori identificano solo un elemento estraneo: l’elemento paterno. Invece, nei trattamenti di ovodonazione sono riconosciuti due elementi estranei, quello paterno e quello della donatrice. Il numero di elementi non riconosciuti può aumentare ulteriormente nel caso di trasferimento di più embrioni. Come esseri umani, abbiamo tutti alcuni antigeni nelle nostre cellule noti come HLA-C, che sono suddivisi nei due grandi gruppi HLA-C1 e HLA-C2. Questa è una distinzione genetica simile a quella che può essere applicata, ad esempio, ai diversi gruppi sanguigni. È stato dimostrato che nei trattamenti di ovodonazione, quando a una donna con recettori KIR AA (tra il 30 e il 40% delle donne europee presenta questo tipo di recettore specifico) viene trasferito un embrione con antigeni HLA-C2, le probabilità di aborto spontaneo, fallimento dell’impianto e altre complicazioni aumentano notevolmente.
Nel contesto della PMA, i risultati dipendono da una catena complessa di attività che coinvolgono sia la parte clinica sia quella laboratoristica. Monitorare e valutare oggettivamente ogni fase del percorso è essenziale per migliorare efficacia, sicurezza e trasparenza. Il lavoro è frutto della collaborazione di clinici ed embriologi provenienti da centri pubblici e privati di tutta Italia, e ha coinvolto anche membri del Registro Nazionale ART dell’Istituto Superiore di Sanità. Il documento rappresenta un passo fondamentale per la standardizzazione della qualità nei trattamenti di PMA, integrando conoscenze biologiche, cliniche e gestionali in una prospettiva di miglioramento continuo della salute riproduttiva.