Il benessere umano, sin dai primi momenti di vita e per tutta l'età adulta, è intrinsecamente legato a un alleato invisibile ma potente: il microbiota. Questo complesso ecosistema di microorganismi, che include batteri, virus, funghi e protozoi, abita il nostro corpo e gioca un ruolo fondamentale nel promuovere la salute di diversi organi e apparati. Dalla regolazione delle funzioni gastrointestinali al supporto del sistema respiratorio e persino alla modulazione del sistema nervoso, l'importanza del microbiota è oggi riconosciuta a livello globale, tanto da essere il tema centrale di eventi dedicati alla sua comprensione, come la Giornata mondiale del Microbioma. L'obiettivo prioritario di tali iniziative è fornire informazioni chiare e facilmente accessibili per far comprendere l’importanza di questi piccoli organismi che influiscono sulla nostra salute, sull’ambiente e sulla vita quotidiana.
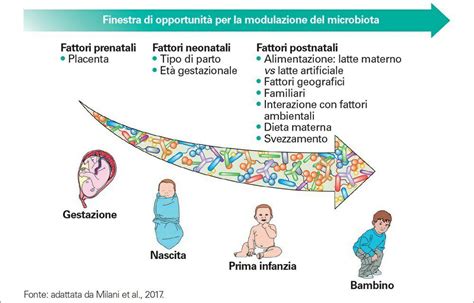
La colonizzazione del nostro organismo da parte dei microorganismi che andranno a costituire il nostro microbiota comincia già durante la gravidanza e prosegue poi nel corso dell’intera vita, con particolare importanza ai primi mille giorni di vita. Questo periodo cruciale, che va dal concepimento ai due anni di età, è considerato una finestra di enorme plasticità epigenetica, capace di influenzare lo sviluppo futuro del bambino in maniera significativa. La composizione del microbiota si modifica ed evolve nel tempo, assumendo caratteristiche specifiche e più o meno “sane” a seconda dell’esposizione a diversi fattori, soprattutto nel corso delle prime fasi della vita. È in questo contesto che il microbiota materno emerge come un determinante primario per la salute del neonato, specialmente attraverso l'allattamento al seno, un processo che modella attivamente l'ecosistema microbico del bambino e ne getta le basi per una salute duratura.
Il Microbiota Materno: Fondamento della Salute Neonatale e Inizi della Colonizzazione
Il microbioma intestinale materno svolge un ruolo cruciale nella salute del bambino e nello sviluppo del suo sistema immunitario, ponendo le fondamenta per una crescita sana e resiliente. La sua composizione nel neonato è infatti influenzata dalla dieta materna in gravidanza e, in seguito, dall’allattamento. Non è mai troppo presto per prendersi cura della popolazione di microbi “amici” che vivono nel nostro organismo: il legame tra la salute e questi microrganismi inizia nelle primissime fasi della vita.
Durante la gravidanza, il corpo della donna subisce variazioni fisiologiche e salutari che includono cambiamenti nel microbiota. Ad esempio, il microbiota vaginale - importante perché aiuta a contrastare le infezioni - diventa più stabile, sebbene la sua diversità possa diminuire. Questo adattamento materno è fondamentale, poiché durante il parto naturale avviene un trasferimento verticale e massiccio di microrganismi dalla madre al bambino. I bambini nati per via vaginale, infatti, vengono colonizzati dai batteri presenti nella vagina e nell’intestino della madre. Questo meccanismo di trasmissione naturale è essenziale per la costituzione del microbiota intestinale neonatale.
Un team di ricercatori del Dartmouth-Hitchcock Medical Center (USA) ha esaminato proprio il rapporto tra la dieta materna durante la gravidanza e il microbioma intestinale di neonati di 6 settimane, correlandolo alle modalità del parto (naturale o cesareo). Gli autori, analizzando le feci di 145 neonati iscritti al New Hampshire Birth Cohort Study e valutando la dieta prenatale materna mediante un questionario, hanno rivelato che il microbioma intestinale dei neonati di 6 settimane era composto prevalentemente da Enterobacteriaceae, Bifidobacterium, Bacteroides, Streptococcus e Clostridium. Questo studio, pubblicato su Microbiome con il titolo "Maternal diet during pregnancy is related with the infant stool microbiome in a delivery mode-dependent manner" (Sara N. Lundgren et al.), sottolinea come la dieta materna prenatale influenzi la composizione microbica infantile in modo dipendente dalla modalità del parto.
L'Impatto del Parto e i Fattori Pre-Natali sul Microbiota del Neonato
Il momento della nascita è ritenuto cruciale per la formazione del microbiota intestinale “core” del bambino. Il tipo di parto, sia esso naturale o con taglio cesareo, fa una differenza sostanziale nella colonizzazione iniziale del neonato. In particolare, è stato dimostrato che il microbiota del neonato è significativamente diverso per composizione e abbondanza a seconda che il parto avvenga per via vaginale oppure con taglio cesareo. Il parto vaginale, infatti, è in grado di fornire una molteplicità di batteri lattici, come i Lattobacilli, che svolgeranno un ruolo fondamentale per lo sviluppo del microbiota del neonato. Questi batteri sono spesso assenti nei nati da taglio cesareo, in mancanza di contatto diretto con le pareti vaginali materne che ne sono ricche. Questa iniziale impronta microbica è vitale per la protezione dalle prime infezioni e contribuisce anche alla digestione del lattosio, un processo che, se non ottimale, può aumentare le fastidiose coliche intestinali con frequenti crisi di pianto nei neonati.
Oltre al parto, altri fattori pre-natali rivestono un ruolo molto importante nel definire il microbiota intestinale del neonato. Questi sono legati al profilo genetico del bambino e alle caratteristiche e allo stile di vita della donna durante la gravidanza. In particolare, è stato osservato che l’alimentazione ricca di grassi, il peso corporeo materno elevato (obesità di base e incremento ponderale durante la gestazione), il fumo e l’assunzione di antibiotici in gravidanza hanno ripercussioni sfavorevoli sul microbiota del bambino. Al contrario, una dieta principalmente basata su frutta, verdura e latticini ha dimostrato effetti “protettivi”, favorendo la formazione di un microbiota neonatale più equilibrato. Ulteriori elementi presenti prima della nascita che contribuiscono a definire il microbiota intestinale del neonato sono lo sviluppo di diabete gestazionale nella madre, gli standard igienici e il numero di persone che condividono l’ambiente di vita della donna in gravidanza, la presenza o meno di fratelli e la coabitazione con animali domestici. Più precisamente, l’assenza di alterazioni metaboliche materne, ambienti di vita caratterizzati da un’igiene relativamente minore e frequentati da più persone e animali, e i nuclei familiari numerosi sono risultati vantaggiosi per l’equilibrio del microbiota neonatale.
Il Latte Materno: Una "Prima Medicina" e Modulatore Essenziale del Microbiota
Dopo la nascita, è l’alimentazione ad assumere un ruolo chiave per la modulazione del microbiota intestinale. Tra tutti i fattori, il latte materno si conferma una vera e propria “prima medicina” per il bambino, capace di plasmare il suo microbiota e influenzare positivamente la sua salute a lungo termine. Il latte materno non solo è l’alimento più idoneo per il neonato, essendo dinamico - è in grado di modificarsi a seconda delle esigenze del bambino - ma è anche sano, sicuro, economico ed ecocompatibile. Ma costituisce anche e soprattutto una lezione pedagogica: è cura e presa in carico.
Latte materno e benefici dell’allattamento al seno
L'Organizzazione Mondiale della Sanità (OMS) considera l’allattamento al seno uno degli obiettivi prioritari per la salute pubblica a livello mondiale, raccomandando il mantenimento dell'allattamento (almeno) per i primi sei mesi di vita del bambino, in considerazione degli innumerevoli benefici dimostrati per la salute del neonato nell’immediato e nel lungo termine. Questi benefici si manifestano soprattutto sul piano immunitario, con una migliore risposta alle infezioni e una riduzione del rischio di sviluppare dermatite atopica e allergie di vario tipo. Sul piano metabolico, si osserva un minor rischio di obesità nell’infanzia e in età adulta.
Contrariamente a quanto ritenuto in passato, il latte materno non è sterile. È dotato di un proprio microbiota, del tutto peculiare e differente da donna a donna, che viene trasferito al neonato attraverso l’allattamento al seno. Questo trasferimento di microrganismi modula l’equilibrio intestinale del bambino, contribuendo alla sua funzionalità e maturazione, nonché a ridurre il rischio di disbiosi e problematiche correlate. L’allattamento al seno diretto è vitale per il bambino: il latte materno non solo nutre il bebè appena nato, ma il contatto pelle a pelle gli offre protezione e con questa attività si aiuta a colonizzare il microbiota intestinale, contribuendo a sviluppare fin dalle prime ore di vita le fragili difese immunitarie.
Oligosaccaridi del Latte Materno (HMOs): Prebiotici Naturali e Protettivi
Un elemento distintivo e fondamentale del latte materno è la sua ricchezza di oligosaccaridi, noti come HMOs (Human Milk Oligosaccharides). Questi composti probiotici naturali stimolano la crescita di ceppi specifici del microbiota intestinale infantile, in particolare i Bifidobatteri. Gli HMOs, le cui caratteristiche sono peculiari e difficilmente riproducibili nella loro complessità, svolgono infatti un’azione prebiotica per il microbiota intestinale. Essi non vengono completamente digeriti e assorbiti nell’intestino tenue del neonato, arrivando inalterati (o degradati soltanto in parte) nel colon, dove sono utilizzati come substrato energetico dal microbiota residente, di cui influenzano la composizione e l’attività metabolica, comportandosi di fatto come “prebiotici”.
Gli HMO rappresentano circa un terzo della componente solida del latte materno, mentre sono presenti in quantità e numero molto minore nel latte vaccino. La promozione della crescita intestinale di Bifidobacteria e Bacteroidetes è risultata correlata all’abbondante presenza nel latte materno di oltre 200 diversi tipi di oligosaccaridi umani dal dimostrato effetto prebiotico e, più specificamente, bifidogenico.
Oltre a contribuire allo sviluppo di un microbiota intestinale più equilibrato e favorevole, è stato osservato che alcuni HMO presentano analogie strutturali con particolari recettori di superficie di batteri patogeni. Agiscono quindi come una sorta di “target tranello” che riduce l’adesione dei microrganismi dannosi all’epitelio intestinale e ne facilita l’eliminazione, proteggendo il bambino da gastroenteriti infettive. La composizione e il contenuto di HMO sono diversi non soltanto da donna a donna (anche in funzione del profilo più o meno secernente), ma anche nei diversi momenti della poppata e nelle varie fasi di crescita del bambino, contribuendo ad allineare la composizione complessiva del latte materno alle mutate esigenze nutrizionali del neonato nel corso del tempo. Studi hanno evidenziato che un latte materno più ricco di HMO è correlato sia a una maggiore quantità di bifidobatteri nell’intestino del neonato sia a una maggiore protezione da diarrea e infezioni respiratorie e a un minor rischio di sviluppare dermatite atopica nei bambini partoriti con taglio cesareo e/o ad aumentato rischio di allergie.
Il Microbiota del Neonato Allattato al Seno: Un Modello di Eubiosi
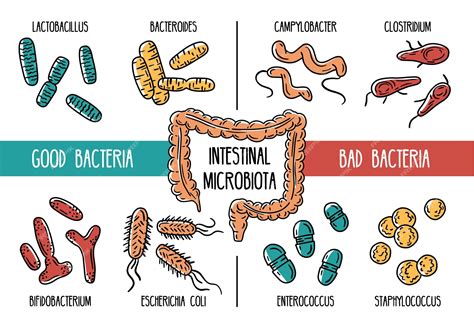
Il microbiota del neonato a termine allattato al seno materno rappresenta un modello di eubiosi, ovvero è un microbiota neonatale ottimale e differenziato, ricco di batteri protettivi, come Bifidobatteri e Lattobacilli. Gli studi che hanno confrontato l’ecosistema enterico dei bambini allattati al seno con quello dei neonati nutriti con latti in polvere hanno permesso di evidenziare numerose differenze di ricchezza, diversità e composizione microbica intestinale, tutte invariabilmente a favore dell’allattamento al seno come modalità di alimentazione ideale nei primi mesi di vita.

I bambini allattati al seno mostrano una flora stabile dominata da Bifidobatteri un mese dopo la nascita. Le popolazioni di enterococci, enterobatteri, clostridi e bacteroides sono soppresse e possono essere isolate in quantità relativamente basse. Al contrario, i neonati alimentati artificialmente non hanno una popolazione microbica prevalente e il loro microbiota include batteri come bacteroides, stafilococchi ed E. coli, con una diversità microbica diversa.
La α-diversità, che definisce il numero di specie presenti in una comunità di viventi all’interno di un ambiente definito, è un altro parametro significativo. Contrariamente a quanto avviene negli adulti, nella prima infanzia una ridotta α-diversità microbica intestinale risulta essere favorevole e auspicabile, in quanto associata a un migliore sviluppo dell’intestino e del sistema immunitario del bambino. Inoltre, pur nel contesto di un’ampia variabilità interindividuale, nel colon dei bambini allattati al seno tendono a essere presenti maggiori quantità di generi batterici “protettivi” per l’intestino stesso e per vari aspetti della salute generale, come i Bifidobacteria (in particolare, Bifidobacterium breve e B. bifidum) e i Bacteroidetes.
Uno studio pubblicato su Eur J Nutr. 2022 Sep 29 (doi: 10.1007/s00394-022-03020-9) ha ulteriormente confermato il ruolo dell’allattamento al seno nella composizione del microbiota intestinale del neonato. Questo studio ha suddiviso 61 neonati in quattro gruppi in base alla tipologia di parto (vaginale [V] o cesareo [C]) e alla modalità di allattamento (esclusivo al seno [B] o misto [M] con latte materno e formule artificiali): VB, CB, VM e CM. L'analisi del meconio e dei campioni fecali raccolti dopo una settimana, a un mese e a tre mesi di vita dei neonati, utilizzando il sequenziamento del 16S rRNA, ha rivelato che l’allattamento al seno garantiva una più fisiologica composizione del microbiota intestinale. Taxa potenzialmente patogeni, come Enterococcus e Enterococcaceae, erano infatti significativamente meno abbondanti nei bambini nati da parto naturale e alimentati con latte materno (gruppo VB). Il gruppo CM (cesareo e allattamento misto) ha mostrato un’abbondanza relativa significativamente più alta di Firmicutes (giorno 0 e mese 1), Enterococcaceae (mese 3) e Enterococcus (mese 3) rispetto al gruppo VB, e un’abbondanza significativamente più alta di Firmicutes (mese 1) e Blautia (mese 3) rispetto al gruppo CB. Inoltre, i gruppi VB e CB hanno esibito una variazione stabile degli acidi grassi a catena corta (SCFA) e un livello significativamente più basso di propionato rispetto ai gruppi VM e CM. Tutti i gruppi hanno mostrato un’intensa transizione degli enterotipi entro 1 mese, stabilizzandosi a 3 mesi. La conclusione di questi risultati ha indicato che il taglio cesareo era associato a una maggiore abbondanza del phylum Firmicutes e della famiglia Enterococcaceae, e a un’intensa fluttuazione degli SCFA, almeno per quanto riguarda il propionato.
Fattori che Alterano il Fisiologico Sviluppo del Microbiota e Rischio di Disbiosi
Purtroppo, non tutti i neonati possono beneficiare di un modello di eubiosi. La prematurità, l’esposizione precoce agli antibiotici (sia della madre durante la gravidanza e il parto che del neonato), la nascita da taglio cesareo, l’ambiente della terapia intensiva neonatale e le peculiari modalità di alimentazione (nutrizione parenterale, nutrizione enterale con sondino, utilizzo di latte formulato) inducono un’alterazione del fisiologico pattern di maturazione del microbiota. Questa alterazione, che merita attenzione e valutazione clinica, è associata al potenziale rischio di disbiosi.
La disbiosi è definita come cambiamenti quantitativi e qualitativi nella composizione di un microbioma ospite che contribuisce a malattie infiammatorie, sia acute che croniche. Il verificarsi di disbiosi può costituire un fattore di rischio, specie nel neonato gravemente prematuro, per patologie potenzialmente severe, quali la sepsi e l’enterocolite necrotizzante. Inoltre, sembra associarsi anche a conseguenze più a lungo termine, quali i disordini del neurosviluppo o l’aumento della suscettibilità a malattie croniche, come allergie, asma e obesità. È ormai noto come molte malattie croniche o disturbi nella vita adulta abbiano in comune scelte non sempre corrette effettuate nei primi mille giorni.
Un esempio di come la disbiosi possa influenzare la salute materna e indirettamente quella del neonato si riscontra nella mastite. Studi recenti che utilizzano tecniche coltura-indipendenti, compreso il sequenziamento metagenomico, hanno rivelato una perdita di diversità batterica nel microbioma dei campioni di latte mastitico rispetto ai campioni di latte sano. La mastite subacuta si verifica quando i lumi duttali si restringono a causa dei biofilm batterici in un contesto di cronica disbiosi mammaria. In condizioni fisiologiche, gli stafilococchi coagulasi negativi (CoNS) e gli streptococchi viridans (cioè S. mitis e S. salivarius) formano sottili biofilm che rivestono l’epitelio dei dotti mammari, consentendo un normale flusso del latte. Nel contesto della disbiosi, queste specie proliferano e, in circostanze opportunistiche, sono in grado di formare spessi biofilm all’interno dei dotti, infiammando l’epitelio mammario e costringendo il latte a passare attraverso un lume sempre più stretto. Questo meccanismo evidenzia la complessità delle interazioni microbiche e la loro influenza diretta sulla salute sia materna che, potenzialmente, infantile.
Strategie per Modulare il Microbiota: Dal Latte Materno ai Probiotici
Per queste ragioni, la possibilità di intervenire sui potenziali fattori di rischio per disbiosi, modulando così le caratteristiche del microbiota verso un profilo più favorevole, appare particolarmente importante per il neonato, ed in particolar modo per il neonato prematuro. Tra i fattori più noti, capaci di indirizzare lo sviluppo del microbiota verso l’eubiosi, va senza dubbio annoverato in primo luogo il latte materno. Nell’approccio alla nutrizione del neonato prematuro, in particolare, tutti gli sforzi dovrebbero essere volti a promuovere non soltanto l’utilizzo del latte materno, ma anche un precoce approccio all’alimentazione al seno, proprio per “sfruttare” al meglio l’effetto benefico del latte materno assunto attraverso l’attacco diretto al seno sulle caratteristiche del microbiota.

Benché i latti in polvere artificiali disponibili in commercio siano di elevata qualità e in grado di soddisfare i bisogni nutrizionali del neonato in rapida crescita, fornendogli tutti i macro e micronutrienti indispensabili, dalla loro composizione sono esclusi diversi elementi bioattivi che rendono il latte materno un alimento del tutto unico e non perfettamente riproducibile. Molti di questi elementi distintivi del latte materno sono proteine e oligosaccaridi che non vengono completamente digerite e assorbite nell’intestino tenue del neonato, arrivando inalterati (o degradati soltanto in parte) nel colon, dove sono utilizzati come substrato energetico dal microbiota residente, di cui influenzano la composizione e l’attività metabolica. In considerazione del riconosciuto ruolo favorevole degli HMO, negli ultimi anni sono stati sviluppati vari latti in polvere arricchiti di questi o altri composti dall’azione prebiotica, come FOS (frutto-oligosaccaridi) e GOS (galatto-oligosaccaridi).
Un secondo potenziale ambito di azione è rappresentato dall’utilizzo di prodotti che possano modulare in senso più o meno favorevole le caratteristiche del microbiota intestinale. Per contribuire a costruire un intestino sano e a rafforzare le difese immunitarie fin dai primi giorni di vita è fondamentale promuovere, anche in epoca neonatale, un utilizzo ragionato e attento degli antibiotici, per limitarne il più possibile l’effetto di induzione e il mantenimento della disbiosi. Inoltre, in considerazione della relazione tra disbiosi e patologie potenzialmente molto severe, quali la sepsi e l’enterocolite necrotizzante, si può valutare l’uso di prodotti per modulare le caratteristiche del microbiota verso un profilo più favorevole, quali i probiotici, batteri benefici che aiutano a mantenere o ripristinare la flora intestinale, i prebiotici, sostanze che ne supportano la crescita, e i postbiotici, composti attivi prodotti dai probiotici stessi che ne potenziano l’efficacia, contribuendo in modo sinergico al benessere intestinale e immunitario del neonato. Appare più complesso, invece, riprodurre la componente probiotica del latte materno, sia perché quest’ultima è ancora poco caratterizzata e variabile da donna a donna sia per la difficoltà di far arrivare vivi e vitali nell’intestino i microrganismi probiotici aggiunti ai latti in polvere che devono essere assunti per bocca e resistere all’attacco degli acidi gastrici e dei sali biliari del neonato.
I latti in polvere con probiotici che hanno fornito i migliori esiti in termini di arricchimento del microbiota intestinale del neonato sono quelli addizionati di alcuni ceppi di Bifidobacterium e Lactobacillus, ma con benefici variabili tra gli studi (anche in funzione degli specifici ceppi usati) e osservati soprattutto nel caso di neonati pretermine. Questo tipo di supplementazione si è dimostrata in grado di arricchire di bifidobatteri e lattobacilli l’ecosistema enterico del neonato allattato al seno anche quando ad assumerla è la donna durante la gravidanza/allattamento. Un esito che sembra essere legato all’esistenza di un trasferimento dei microrganismi probiotici presenti nell’intestino della donna al latte materno e, da qui, al bambino che se ne nutre.
Tra i batteri probiotici ritenuti sicuri e ben tollerati per l’impiego in neonati e bambini, e per questa ragione inseriti nella lista GRAS (Generally Recognised As Safe) della Food and Drug Administration (FDA) statunitense e nella lista QPS (Qualified Presumption of Safety) dell’European Food Safety Authority (EFSA), ci sono diversi ceppi di bifidobatteri e lattobacilli. Tra questi, Bifidobacterium lactis HN019, Bifidobacterium breve M-16V e Lactobacillus rhamnosus HN001.
- Bifidobacterium lactis HN019 è stato studiato per la sua capacità di supportare la funzionalità della barriera intestinale, ottimizzando indirettamente la risposta immunitaria enterica durante infezioni gastrointestinali da rotavirus, E. coli e Salmonella spp. Contribuisce inoltre ad alleviare i sintomi della dermatite atopica esacerbata dall’assunzione di particolari alimenti, ma non da antigeni ambientali, quando somministrato in combinazione con L. rhamnosus, suggerendo che l’azione protettiva dipende da una migliore modulazione della risposta immunitaria a livello gastrointestinale. (Riferimenti: Shu Q, et al. Probiotic treatment using Bifidobacterium lactis HN019 reduces weanling diarrhea…; Sistek D, et al. Is the effect of probiotics on atopic dermatitis confined to food sensitized children?).
- Bifidobacterium breve M-16V, oltre a essere caratterizzato da un elevato profilo di sicurezza, ha dimostrato di esercitare un’azione antibatterica nei confronti di E. coli e Klebsiella pneumoniae e altri patogeni enterici, contribuendo attivamente alla funzionalità e alla maturazione del sistema immunitario del bambino. È inoltre in grado di compensare le disbiosi intestinali nei neonati partoriti con taglio cesareo. (Riferimenti: Wong CB, et al. Exploring the Science behind Bifidobacterium breve M-16V in infant health; Chua MC, et al. Effect of synbiotic on the gut microbiota of cesarean delivered infants…).
- Lactobacillus rhamnosus HN001 è un ceppo che ha mostrato di ridurre lo sviluppo di riniti allergiche stagionali in bambini sensibilizzati al polline e con asma intermittente, quando somministrato in combinazione con B. Longum BB536 e B. breve. In generale, la supplementazione con batteri lattici è risultata sicura e associata a una migliore risposta immunitaria innata e adattiva, contribuendo a proteggere i bambini da infezioni batteriche e virali. Nello specifico, L. rhamnosus agevola il trattamento della diarrea acuta in bambini ospedalizzati di età compresa tra 1 e 3 anni, riducendo la durata degli episodi e del ricovero, quando assunto in associazione a B. lactis Bi-07 e L. acidophilus NCFM. (Riferimenti: Wickens K, et al. A protective effect of lactobacillus rhamnosus HN001 against eczema…; Gill HS, et al. Enhancement of natural and acquired immunity by Lactobacillus rhamnosus (HN001)…).
Ricerca e Prospettive Future: Un Approccio Olistico alla Salute Infantile
Il corretto sviluppo del microbiota del bebè corre sullo stesso binario con lo sviluppo generale dell’organismo. Non solo le difese immunitarie si irrobustiscono, ma anche il comparto neurologico si sviluppa, formando l’asse intestino-cervello. Proprio per questo motivo è fondamentale per le donne in dolce attesa mantenere in equilibrio il proprio microbiota intestinale. Una disbiosi intestinale in gravidanza può infatti portare con sé fastidi come l’irregolarità intestinale, ma anche minacce più gravi. I dati evidenziano che c’è una correlazione tra l’allattamento al seno e tassi più bassi di malattie autoimmuni, asma e obesità infantile, condizioni che oggi sappiamo essere collegate a cambiamenti del microbiota intestinale durante i primi anni di vita.
Il 25 marzo si è tenuto il Convegno online “I primi mille giorni di vita. La complessa interazione tra allattamento, dieta e modulazione del microbiota intestinale”, promosso dal Servizio di Gastroenterologia Funzionale e Microbiota, UOS di pediatria dell’Università Campus Bio-medico - UCBM, in collaborazione con la Fondazione Comitans e con l’Ospedale Pediatrico Bambino Gesù. Questa collaborazione non è casuale, poiché, come ha ricordato il rettore Prof. Raffaele Calabrò, l’Università Campus Bio-medico, l’Ospedale Bambino Gesù e Comitans sono realtà che credono soprattutto nella ricerca, nella formazione e nella scienza per la persona, più che nella scienza per la scienza.

Grazie alla borsa di dottorato promossa dalla Fondazione Comitans, la D.ssa Giulia Rocchi si avvarrà della collaborazione di lunga data tra UCBM e l’Unità di Parassitologia e del Microbioma Umano del Bambino Gesù per portare avanti il suo progetto di ricerca sull’impatto dei determinanti pre e post-natali nell’evoluzione e modulazione del microbiota intestinale infantile nei primi mille giorni. La D.ssa Rocchi studierà le variabili endogene ed esogene che influiscono sullo sviluppo del bambino, a partire proprio dallo studio del microbiota intestinale. Analogamente, il progetto di Marta Cioffi, laureanda del Corso Magistrale in Scienze dell’Alimentazione e Nutrizione Umana all’UCBM, con un’interessante proposta di tesi sperimentale sull’educazione alimentare nei nidi, sottolinea l’importanza di considerare nella loro globalità ed interazione alimentazione, ambiente e stile di vita.
Come ha ricordato il Prof. Pietro Ferrara, Responsabile dell’Unità di Pediatria dell’UCBM, il microbiota intestinale è stato definito un superorgano, il cui equilibrio assicura la nostra salute. Esiste un’interazione profonda tra il microbiota del neonato e l’allattamento al seno. Per questa ragione, è importante fare formazione ai futuri ed ai neogenitori su tutti questi aspetti. Non solo, quindi, sull’importanza di alimentarsi correttamente, bere tanta acqua, evitare l’abuso di sostanze, fare sport ma anche riscoprire l’importanza della socialità e della relazione con i bambini, con gli altri, con l’ambiente e, in questo caso, con il cibo.
Come ha ricordato la D.ssa Lorenza Putignani, Responsabile dell’Unità di Parassitologia e del Microbioma Umano, Ospedale Pediatrico Bambino Gesù, che da anni si occupa della materia, è fondamentale rafforzare altresì la conoscenza nella transizione dall’età pediatrica a quella adulta, tramite la condivisione di dati e studi per la creazione di biobanking digitale. Si rende sempre più necessario sviluppare una visione sistemica per riuscire a comprendere questi fenomeni e agire in modo adeguato. Cecilia Bartolucci, presidente Comitans, ha ricordato come la medicina ormai tenda ad applicare un approccio definito “delle 4 P”. Sappiamo infatti che i primi mille giorni sono un momento fondamentale nella tappa della crescita da cui dipenderanno gli esiti futuri (Predizione) e che ci permettono quindi di agire iniziando dalla Prevenzione, tenendo conto della Personalizzazione degli interventi (sia a livello individuale che a seconda delle caratteristiche del gruppo di appartenenza) e della Partecipazione personale e sociale, perché questo costituisce anche il maggior momento di empatia ed interesse da parte dei genitori. Un buon inizio, un inizio sano, è il mattone fondamentale della prevenzione. È proprio in quest’ottica che Cecilia Bartolucci ha sollecitato ricercatori e studenti a guardare sempre oltre, ponendo domande sia a sé stessi che agli altri, cercando punti d’incontro fra indagine scientifica e realtà sociale.
tags: #microbiota #e #allattamento