La fertilità maschile, un indicatore sensibile dello stato di salute generale di un individuo, può essere significativamente influenzata da una varietà di fattori, tra cui le condizioni mediche preesistenti e i regimi terapeutici. In particolare, le malattie cardiovascolari, ampiamente diffuse, incidono sulle capacità riproduttive sia direttamente, attraverso i loro meccanismi patologici, sia indirettamente, mediante le terapie farmacologiche utilizzate per il loro trattamento.
Sebbene non esista una prova inconfutabile che l'avanzare dell'età dell'uomo possa portare alla sterilità, a differenza di quanto è ben noto e assodato per le donne, la capacità di produrre sperma negli esseri umani di sesso maschile viene mantenuta, generalmente, dalla pubertà fino alla morte. Tuttavia, l'età avanzata e le patologie associate spesso comportano l'assunzione di farmaci che possono avere un impatto sulla funzione riproduttiva. La prescrizione di alcuni farmaci, in ogni fase della vita, dovrebbe essere criticamente presa in considerazione alla luce dei progetti di vita di un paziente, specialmente in età riproduttiva. Tale considerazione assume un'importanza ancor più rilevante alla luce dell'aumentato utilizzo di farmaci nei pazienti nella fascia di età pediatrica e adolescenziale, condizione che potrebbe compromettere la capacità riproduttiva nell'età adulta [1].
Va tuttavia considerato che gli effetti dei farmaci sulla riproduzione sono difficili da studiare poiché la fecondità è influenzata da molteplici fattori, tra i quali la salute riproduttiva della partner femminile e numerosi fattori ambientali. Lo stress, definito “il male del secolo”, è un elemento aggiuntivo che incide profondamente sulla fertilità maschile; il percorso della Procreazione Assistita, ad esempio, è una via tortuosa che senza dubbio aggiunge stress a quello che già normalmente una persona deve affrontare durante la vita. Spesso il partner maschile non estranea le sue preoccupazioni, mostrandosi apparentemente calmo e quasi distaccato, ma lo stress c'è e alterazioni, anche evidenti, dei parametri del liquido seminale, come la concentrazione e la motilità degli spermatozoi, possono esserne la prova.

Meccanismi d'Azione dei Farmaci sulla Funzionalità Riproduttiva Maschile
I farmaci che influenzano la fertilità maschile possono essere raggruppati in base ai meccanismi attraverso i quali portano allo sviluppo di un danno all’apparato genito-urinario. In base a tale principio si possono distinguere diverse categorie di farmaci.
In primo luogo, vi sono farmaci che alterano l’asse ormonale ipotalamo-ipofisi-gonadi (HPG). Questo asse è cruciale per la regolazione della produzione di testosterone e spermatozoi. Qualsiasi interferenza a questo livello può avere ripercussioni significative sulla fertilità.
Una seconda categoria comprende farmaci che influiscono direttamente sulla produzione dello sperma, riducendo complessivamente il numero di spermatozoi riscontrabile nel seme, un fenomeno noto come oligospermia o azoospermia in casi estremi.
In terzo luogo, esistono farmaci che compromettono la funzionalità intrinseca degli spermatozoi, indipendentemente dalla quantità di questi ultimi. Ciò significa che, anche con un numero adeguato di spermatozoi, la loro capacità di movimento, la vitalità o la capacità di fecondare un ovocita possono essere compromesse.
Infine, alcuni farmaci hanno un impatto negativo sulla funzione sessuale, in termini di capacità erettiva, funzione eiaculatoria, desiderio sessuale o libido. Questi effetti, pur non agendo direttamente sulla spermatogenesi, possono indirettamente impedire il raggiungimento di una gravidanza.
È importante notare, tuttavia, che uno stesso farmaco può dare origine a tossicità riproduttiva attraverso più di uno tra i meccanismi precedentemente elencati, rendendo la valutazione dell'impatto sulla fertilità complessa e multifattoriale.
Inibitori della Fosfodiesterasi di Tipo 5 (PDE5i) e la Loro Applicazione
Nel contesto della funzione sessuale, in particolare per migliorare la performance in caso di disfunzione erettile, vengono talvolta considerati farmaci come gli inibitori della fosfodiesterasi di tipo 5 (PDE5i). I prodotti come sildenafil (Viagra), tadalafil, vardenafil e avanafil non sono integratori ma farmaci, e si utilizzano per le disfunzioni erettili e non, come vengono spesso usati, come afrodisiaci. Detto questo, è comune il loro impiego come afrodisiaci anche da persone giovani, e vengono spesso acquistati in Internet o addirittura per vie illegali nelle discoteche ecc.
La disfunzione erettile (DE) è tutt'altro che rara, colpendo fino al 30% dei maschi tra i 40 e i 70 anni, e la sua incidenza aumenta con l'età. Probabilmente, però, il problema è sottostimato. Da un punto di vista cardiovascolare, la DE interessa perché può essere la spia di una futura malattia cardiaca, infatti ne è colpito circa il 57% dei pazienti affetti da cardiopatia ischemica. Questi ultimi a volte iniziano ad avere difficoltà durante i rapporti intimi proprio dopo un primo infarto o un primo ictus e danno erroneamente la colpa alle sole terapie mediche che hanno da poco iniziato.
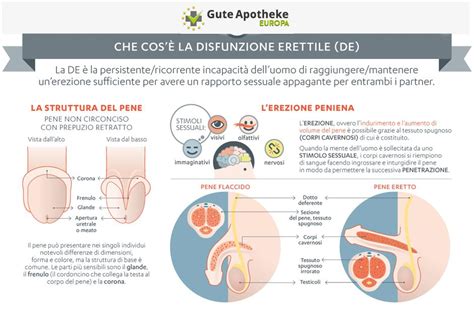
La chimica del sesso è una specie di gioco del domino. Quando scatta la scintilla dell’eccitazione sessuale, nei corpi cavernosi del pene si diffonde una sostanza “afrodisiaca” chiamata ossido nitrico. L'ossido nitrico attiva la guanilato ciclasi, che porta alla produzione di guanosina monofosfato ciclico (cGMP), una molecola che rilassa la muscolatura liscia dei corpi cavernosi, permettendo l'afflusso di sangue e l'erezione. Ma ogni molecola, nel nostro corpo, ha un proprio vigilante, che ne controlla azioni e comportamenti, e così pure la cGMP deve vedersela con un controllore chiamato PDE-5 (per esteso: fosfodiesterasi di tipo 5), la cui funzione è quella di degradarla, di toglierla di mezzo una volta concluso il suo lavoro. Ecco perché le “pillole dell’amore” intervengono sulla scena, come supereroi farmacologici, stoppando l’attività (pur fisiologica) della PDE-5 che, se lasciata agire, ostacolerebbe la cGMP, così cruciale per l’erezione. Bloccando il “bloccatore”, insomma, questa molecola può essere agevolata nel proprio mestiere in chi è alle prese con un deficit erettile.
Sicurezza dei PDE5i nei Cardiopatici
Sui giovani, in genere, i PDE5i non hanno effetti indesiderati a meno che non vengano associati a droghe, alcol ecc. Sui cardiopatici, invece, massima attenzione è richiesta soprattutto dal punto di vista clinico nei soggetti instabili con angina severa o con scompenso cardiaco. In questi casi, non fa male il farmaco in sé, ma l'eventuale tensione emotiva o lo sforzo fisico del rapporto sessuale.
I PDE5i non aumentano il rischio di infarto del miocardio o la mortalità cardiovascolare nei pazienti cardiopatici. Anzi, essi hanno anche un effetto positivo sulla circolazione polmonare (riducono le resistenze) e sulla circolazione in generale. Alcuni studi hanno persino dimostrato la riduzione della mortalità cardiovascolare in chi utilizza tali farmaci. Tuttavia, essendo un gruppo di farmaci che ha un effetto vasodilatatorio, quando assunti possono interagire con altri farmaci assunti dal cardiopatico aumentando gli effetti di abbassamento della pressione. Questo è particolarmente vero per i nitrati (carvasin, cerotti a rilascio prolungato di nitrati come il Nitroderm, il farmaco nicorandil), tutti farmaci che si usano in pazienti coronaropatici. Ovviamente, 24 ore prima del rapporto e della assunzione di tali farmaci vanno sospesi i nitrati, sia per bocca che trasdermici, per l'effetto che hanno di potenziare l'efficacia ipotensiva dell'associazione. Da qui, possibili svenimenti e malori vari.
Se prescritti dal medico, tali farmaci non hanno effetti indesiderati o pericolosi gravi, ma solo cefalea, rossore in viso o talvolta bruciori di stomaco. Tendenzialmente la scelta va operata in base alla condizione del paziente, ai farmaci in uso, alla durata di azione e alla comparsa di eventuali effetti collaterali. Il Sildenafil (Viagra) ha una breve durata di azione, alcune ore, e pertanto è il farmaco di scelta per testare la tolleranza del paziente. Si inizia solitamente con una dose test di 50 mg al giorno e successivamente aumentato a 100 mg al giorno se la dose non si dimostra adeguata. È un mercato che sta travalicando i confini imposti dalle raccomandazioni specialistiche, perché sei uomini su dieci si affidano alle compresse senza aver ricevuto una precisa diagnosi e nemmeno una ricetta da parte del medico. Naturalmente resta dominante la raccomandazione generale: i danni sono sempre dietro l’angolo se si esagera con i dosaggi degli inibitori della PDE-5.
Disfunzione erettile: cure
Terapia Sostitutiva con Testosterone (TRT)
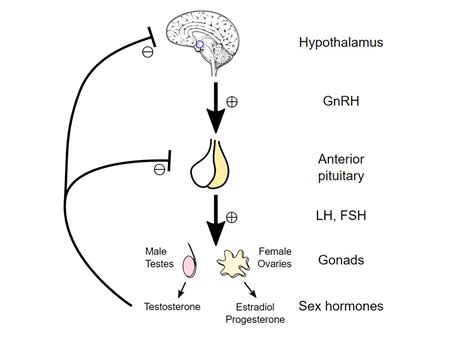
Negli ultimi 15 anni, la terapia sostitutiva con testosterone è diventata uno dei trattamenti farmacologici a più rapida crescita in tutto il mondo, con un utilizzo più che triplicato rispetto ai primi anni 2000 [3,4]. Come è noto, il testosterone viene prodotto dal testicolo sotto lo stimolo di un importante ormone rilasciato a livello cerebrale dalla ghiandola ipofisi: l’ormone luteinizzante (LH). L’ipofisi rilascia anche ormone follicolo-stimolante (FSH), capace di stimolare l’attiva produzione di spermatozoi sempre a livello testicolare. In condizioni fisiologiche il testosterone regola negativamente produzione di LH e FSH da parte dell’ipofisi, così da mantenere un equilibrio funzionale tra i due organi endocrini [6].
Alla luce dell’esistenza di tale circuito di regolazione, è facile intuire come la somministrazione di testosterone esogeno provochi una soppressione della produzione di LH e FSH, con forte riduzione dei livelli intra-testicolari di testosterone e della produzione di spermatozoi [7]. Questo effetto sembra essere transiente poiché nella maggior parte degli uomini si assiste a un recupero della produzione di sperma dopo la sospensione del farmaco [8,9]. In una recente revisione di 30 studi pubblicati sono stati analizzati la frequenza, l’entità e gli specifici parametri seminali modificati dalla terapia con testosterone, utilizzato anche come contraccettivo. In particolare, il recupero della concentrazione spermatica a valori superiori ai 20 milioni/ml si è verificato nel 90%, 96% e 100% degli uomini rispettivamente entro 12 mesi, 16 mesi e 24 mesi.
Rischi Cardiovascolari e Regolamentazione della TRT
I medicinali contenenti testosterone sono autorizzati nell’UE per il trattamento di uomini con livelli anormalmente bassi di ormone (ipogonadismo). Il rapporto beneficio-rischio di questi medicinali è stato rivisto a seguito della pubblicazione di recenti evidenze che indicano un aumento del rischio di eventi cardiovascolari, in particolare infarto del miocardio, negli uomini trattati con testosterone.
Il CMDh, un organismo regolatorio che rappresenta gli Stati Membri dell'UE, ha stabilito all'unanimità che non vi è alcuna evidenza consistente in relazione a un aumentato rischio di problemi cardiaci con i farmaci contenenti testosterone usati negli uomini che non producono abbastanza testosterone (una condizione nota come ipogonadismo). Tuttavia, le informazioni sul prodotto devono essere aggiornate in linea con le più attuali evidenze disponibili in materia di sicurezza, e con l’avvertenza che la mancanza di testosterone deve essere confermata da segni e sintomi e test di laboratorio prima di trattare gli uomini con questi farmaci.
La posizione del CMDh segue una revisione da parte del Comitato di Valutazione dei Rischi per la Farmacovigilanza dell'EMA (PRAC), che ha esaminato il rischio di gravi problemi che colpiscono il cuore e la circolazione, in particolare attacchi di cuore, negli uomini trattati con questi farmaci. La rivalutazione è stata avviata poiché alcuni recenti studi suggeriscono un aumento dei problemi cardiaci negli uomini trattati con testosterone, rispetto agli uomini che non lo utilizzano. Il PRAC ha considerato questi studi insieme ai dati disponibili provenienti da altri studi e analisi, alle informazioni sulla sicurezza raccolte dal momento della commercializzazione, e ha trovato che l’evidenza riguardante il rischio di problemi cardiaci era contraddittoria: alcuni studi indicavano un aumento del rischio, mentre altri non lo indicavano, e alcuni studi ancora presentavano problemi con il disegno che ne limitavano le conclusioni che si sarebbero tratte [1-3]. Il PRAC ha anche osservato che la stessa mancanza di testosterone potrebbe aumentare il rischio di problemi cardiaci.
Il PRAC ha raccomandato di aggiornare le informazioni sul prodotto in linea con le ultime evidenze e di fornire avvertimenti a coloro che potrebbero essere ad aumentato rischio di problemi cardiaci. Le informazioni sul prodotto devono segnalare chiaramente che il testosterone va utilizzato solo quando un livello anormalmente basso di ormone è stato confermato da segni e sintomi e appropriati test di laboratorio. I livelli di testosterone naturalmente diminuiscono leggermente con l'età, ma il ripristino di questi livelli negli uomini anziani sani non è un uso autorizzato del medicinale nell'UE.
Il PRAC ha ritenuto inoltre che i rischi degli effetti sul cuore e la circolazione, e ogni potenziale meccanismo alla base di tali effetti devono continuare a essere monitorati, e le informazioni provenienti dagli studi in corso dovranno essere fornite come parte della prossima solita revisione di sicurezza (a cui questi farmaci, come tutti i farmaci nell'UE, sono soggetti). Il CMDh ha approvato le raccomandazioni del PRAC all’unanimità ora verranno implementate direttamente secondo un calendario concordato dagli Stati Membri in cui sono autorizzati i medicinali.
In sintesi, i pazienti a cui viene prescritto testosterone devono ricordare ai loro medici se sono in trattamento per la pressione alta, poiché il testosterone può anche aumentare la pressione sanguigna. Le informazioni sul prodotto saranno modificate per chiarire che questi farmaci devono essere somministrati solo agli uomini, nei quali sia i segni e sintomi, sia i test di laboratorio confermano livelli anormalmente bassi di testosterone. Non ci sono molte informazioni sull'uso di farmaci contenenti testosterone negli uomini sopra i 65 anni di età. Il livello di testosterone si abbassa naturalmente con l'età e medicinali contenenti testosterone non sono approvati nell’UE per essere utilizzati al fine di aumentare i livelli di testosterone negli uomini anziani sani.
La terapia sostitutiva con testosterone deve essere somministrata solo quando la carenza di ormone è stata confermata da caratteristiche cliniche e test biochimici. I livelli di testosterone devono quindi essere monitorati regolarmente durante il trattamento. L'emoglobina, ematocrito, funzionalità epatica e il profilo lipidico del sangue devono anche essere controllati regolarmente. Nei pazienti affetti da grave compromissione cardiaca, epatica o renale o da cardiopatia ischemica, il trattamento con testosterone può causare gravi complicanze caratterizzate da edema con o senza insufficienza cardiaca congestizia. In tal caso, il trattamento deve essere immediatamente interrotto. È anche consigliata cautela nei pazienti con ipertensione pre-esistente, dal momento che il testosterone può causare un aumento della pressione sanguigna.
Mancano dati rilevanti di sicurezza ed efficacia in pazienti con ipogonadismo correlato all’età e valori fisiologici definiti di riferimento nei pazienti più anziani, e sono necessari ulteriori studi.
Farmaci Inibitori della 5-alfa Reduttasi (5ARI)
Fisiologicamente, circa il 10% del testosterone (T) prodotto dal testicolo viene convertito in diidro-testosterone (DHT), un derivato circa 5 volte più potente del T, a opera dell’enzima 5alfa-reduttasi [10]. Numerosi studi hanno valutato il potenziale effetto dei 5ARI, in particolare di finasteride e dutasteride, sulla produzione di spermatozoi. Tuttavia, i risultati emersi sono contrastanti, con generali effetti minimi su conta e funzione degli spermatozoi.
A titolo di esempio, uno studio condotto su uomini normospermici ha confrontato l’uso di dutasteride (0,5 mg al giorno), finasteride (5 mg al giorno) e assenza di trattamento per un anno. In entrambi i gruppi di trattamento, il numero totale di spermatozoi è diminuito di circa il 30% per ritornare al valore basale dopo la cessazione. Pur risultando statisticamente significative, non è chiaro se tali variazioni abbiano avuto un effetto sulla fertilità [13].
Oltre agli effetti sulla funzione spermatica, l’assunzione di 5ARI si associa a un aumentato rischio di disfunzione sessuale, incluse disfunzione erettile, diminuzione del desiderio sessuale e disfunzione eiaculatoria [14,15]. Questi effetti collaterali possono avere un impatto significativo sulla qualità della vita e sulla capacità riproduttiva.
Alfa-bloccanti
Il trattamento dei sintomi dell’ipertrofia prostatica benigna e delle affezioni del tratto urinario inferiore prevede l’utilizzo di farmaci con attività bloccante per i recettori di tipo alfa dell’adrenalina, noti come alfa-bloccanti [16]. La compromissione della fertilità da α‑bloccanti è principalmente causata dalla disfunzione eiaculatoria, che va dall’emissione seminale ridotta all’eiaculazione retrograda. Quest'ultima condizione si verifica quando il seme, invece di essere espulso all'esterno, rifluisce nella vescica, rendendo impossibile la fecondazione naturale.
Farmaci Psicopatici
I farmaci psicotropi sono usati in tutte le fasce d’età e sono noti per influenzare la funzione sessuale, in particolare la libido, la funzione erettile ed eiaculatoria. Gli antidepressivi triciclici e gli inibitori selettivi della ricaptazione della 5-idrossitriptamina (SSRI) sono tra le classi di farmaci psicotropi più comunemente usati, assieme agli inibitori della monoaminossidasi e il carbonato di litio per il trattamento dei disturbi bipolari.
Gli agenti psicotropi sono noti per influenzare l’asse ipofisi-testicolo a diversi livelli, in particolare aumentando il rilascio di prolattina a livello centrale che, riducendo i livelli di LH, provoca una diminuzione del testosterone [18]. Anche il trattamento con SSRI si associa a aumento della secrezione di prolattina, sebbene non tutti gli studi disponibili concordino su questo effetto. Negli uomini, l’uso continuativo di questi farmaci può provocare un’incidenza del 50-60% di disfunzione erettile e un grado variabile di eiaculazione ritardata o assente [19].
Farmaci Antipertensivi e la Funzione Sessuale
La maggior parte dei farmaci utilizzati per il trattamento dell’ipertensione si associa allo sviluppo di disfunzione sessuale con indiretta compromissione della fertilità. Questo è un aspetto cruciale per i pazienti cardiopatici che spesso assumono regimi terapeutici complessi.
In particolare, è noto che i farmaci β-bloccanti possono causare disfunzioni sessuali a causa dei loro effetti sui vasi sanguigni mediati dal sistema adrenergico. Possono ridurre la libido e causare disfunzione erettile.
Anche i diuretici possono potenzialmente influenzare la funzione sessuale, in analogia ai β‑bloccanti, attraverso effetti sul sistema adrenergico vascolare. Inoltre, lo spironolattone, farmaco diuretico risparmiatore di potassio, presenta una nota attività anti-androgenica inibendo la sintesi endogena di testosterone e compromettendo l’attività del DHT.
Lo ione calcio è fondamentale per le principali funzioni dello spermatozoo quali motilità, attivazione nell’apparato riproduttivo femminile e rottura del cappuccio acrosomiale [26]. Studi animali di laboratorio hanno dimostrato che il trattamento con nimodipina, un antipertensivo calcio-antagonista, determina una diminuzione della concentrazione di spermatozoi nel seme, della loro motilità e della penetrazione dell’ovocita [27]. Studi simili condotti con altri calcio-antagonisti, quali nifedipina, verapamil e diltiazem, hanno confermato questi risultati segnalando, inoltre, una riduzione del peso alla nascita [28].
Chemioterapia e Radioterapia
La chemioterapia oncologica, sia per i farmaci usati individualmente sia per le associazioni di molecole, può causare infertilità temporanea o permanente a seconda dell’agente utilizzato, della dose somministrata, dell’intervallo di somministrazione, del tipo di cancro trattato e della prescrizione di altri agenti adiuvanti usati contemporaneamente [30]. Uno degli obiettivi della terapia multi-farmacologica è ridurre al minimo gli effetti avversi di ogni singolo agente. Il contributo relativo dei singoli farmaci alla tossicità sulle cellule precursori degli spermatozoi può essere difficile da determinare, considerate le sopracitate variabilità.
Inoltre, gli effetti dannosi della chemioterapia sulla produzione di spermatozoi sono stati osservati negli adulti che hanno ricevuto chemioterapia durante l’infanzia. Ad oggi, non è disponibile alcun farmaco in grado di lenire gli effetti gonadotossici della chemioterapia. L’approccio di generare nel testicolo uno stato di quiescenza bloccando farmacologicamente il rilascio delle gonadotropine ha dato risultati contrastanti [31].
La radioterapia è un altro dei trattamenti utilizzati per la cura dei tumori di vario tipo che può impattare sull’apparato riproduttivo, causando danni diretti ai tessuti gonadi e compromettendo la spermatogenesi.
Immunosoppressori e FANS
I farmaci immunosoppressori, utilizzati per sopprimere il sistema immunitario, trovano applicazione nelle terapie post-trapianto, per impedire che gli anticorpi attacchino l’organo trapiantato, causando il rigetto. Alcuni di questi farmaci possono avere effetti negativi sulla fertilità, sebbene la natura e l'entità di tali effetti possano variare.
Anche i FANS (Farmaci Antinfiammatori Non Steroidei), una classe di farmaci (come l’ibuprofene) utilizzati per ridurre l’infiammazione, il dolore e la febbre, possono influenzare la fertilità, con alcuni studi che suggeriscono un impatto sulla produzione di testosterone e sulla qualità dello sperma in caso di uso prolungato o ad alte dosi.
La Disfunzione Erettile come Segnale di Allarme Cardiovascolare
Come detto in precedenza, la DE è un problema comune che può avere implicazioni più ampie per la salute. L’arteriosclerosi è alla base della disfunzione dell’endotelio (lo strato di cellule che ricopre l’interno dei vasi) e favorisce la formazione delle placche che restringono le arterie coronarie, le carotidi e anche i vasi del pene. Questi ultimi hanno dimensioni di 1-2 mm e sono molto più piccoli rispetto ad altri vasi quali le coronarie, i vasi del cuore, che misurano il doppio. Per tale ragione non è infrequente che un uomo incominci ad avere problemi di DE alcuni anni prima di avere il suo primo infarto o il suo primo ictus.
La DE condivide con le malattie cardiovascolari la stessa causa scatenante, ovvero il malfunzionamento della vasodilatazione delle arterie dipendente dall’endotelio, a sua volta favorita dalla progressione della malattia arteriosclerotica. Infatti, negli uomini affetti da DE è stata dimostrata la carenza di una corretta vasodilatazione per la ridotta produzione di Nitrossido da parte dell’endotelio colpito da arteriosclerosi. È proprio la ridotta concentrazione di Nitrossido il fattore che impedisce la vasodilatazione con conseguente ridotto afflusso di sangue all’organo genitale maschile che impedisce il raggiungimento di una erezione soddisfacente e duratura. Per tale ragione i farmaci più efficaci per combattere la DE sono quelli che consentono un aumento della concentrazione di Nitrossido a livello dei corpi cavernosi del pene.
Mi capita spesso di effettuare delle prime valutazioni di pazienti non ancora cardiopatici che giungono al mio ambulatorio per valutare una ipertensione o per abbattere i propri fattori di rischio cardiaco e avere una vita più sana. Parte importante della visita è acquisire anche informazioni su una eventuale DE. La presenza di una DE è un importante predittore di malattia coronarica silente. In questo caso, oltre a prescrivere una adeguata terapia, viene indagata la capacità di esercizio della persona, viene richiesta un esame del sangue per valutare i livelli di testosterone, il colesterolo LDL, la fosfolipasi A2 associata alla lipoproteina, la glicemia, l’emoglobina glicata, la PCR (proteina C reattiva), il Fibrinogeno, l’IL-6, l’acido urico, la microalbuminuria e nei casi ad elevato rischio viene prescritto un test da sforzo, un ecodoppler carotideo e in casi selezionati la valutazione dello score del calcio coronarico o un esame TAC delle coronarie con mezzo di contrasto.
Gestione dell'Attività Sessuale nei Pazienti Cardiopatici
Ma cosa succede se il paziente è già malato di cuore? Prima di tutto bisogna verificare se un soggetto cardiopatico è in grado di affrontare il carico che comporta lo svolgimento della attività sessuale con il partner. È stato ampiamente dimostrato che il carico metabolico di una attività sessuale anche intensa non eccede in generale i 5 - 6 equivalenti metabolici (METs). L’equivalente metabolico viene calcolato durante una provata sforzo eseguita al cicloergometro o al tappeto rotante. Per farci una idea grossolana 5-6 METs equivalgono a camminare 1,5 Km in piano in 20 minuti o salire velocemente 2 piani di scale. Quindi è inusuale che durante un rapporto la pressione arteriosa superi i 170 mmHg di massima e la frequenza cardiaca superi i 130 bpm.
Pertanto, in caso di dubbio sul possibile effetto negativo di un farmaco sulla funzione erettile è utile eseguire sotto supervisione medica cardiologica un periodo di qualche settimana di sospensione per valutare la ricomparsa della attività erettile normale. Questo approccio permette di discernere se la disfunzione erettile sia una conseguenza diretta del farmaco o piuttosto sia legata ad altri fattori, inclusa la patologia cardiaca stessa.
L'Importanza della Comunicazione e dell'Approccio Multidisciplinare
Un numero crescente di pazienti si trova nelle condizioni di assumere regimi terapeutici a lungo termine fin dalla giovane età e i medici dovrebbero tenere in considerazione i piani riproduttivi dei pazienti. Per molte di queste terapie, i dati circa gli effetti noti sulla fertilità maschile non sono definitivi, a causa della letteratura datata, delle piccole dimensioni dei campioni studiati e dei risultati contrastanti.
Quando si parla di farmaci che influenzano la fertilità maschile e femminile viene spontaneo pensare a tutti quei medicinali che hanno un impatto diretto sulla riproduzione. In realtà ci sono molte terapie che possono influire negativamente sulla fertilità di coppia. In alcuni casi l’infertilità è solo temporanea, ma la situazione cambia radicalmente quando si tratta di terapie che interessano tutta la vita dei pazienti.
L’intesa tra tutti gli operatori sanitari è di fondamentale importanza per la promozione e l’informazione sui corretti stili di vita e sui danni derivanti da comportamenti scorretti. Favorire l’incontro tra gli esperti, il coordinamento tra personale medico e infermieristico, è principio basilare per l’ottenimento di risultati efficaci nella prevenzione e nella tutela della salute in genere ed in particolare delle malattie cardiovascolari. È cruciale che i medici che hanno formulato la terapia per il caso specifico del paziente (per es. il cardiologo per il cardiopatico, l'oncologo per il paziente oncologico, ecc.) siano coinvolti nel dialogo sulla fertilità, assicurando che le preoccupazioni riproduttive siano indirizzate in modo completo e personalizzato.
tags: #medicine #per #cardiopatici #diminuisce #fertilita #negli