La “rivoluzione genetica” che ha caratterizzato l’inizio del terzo millennio e la più recente “rivoluzione genomica” hanno fatto sì che sempre più aspetti dell’esistenza umana siano diventati oggetto di controllo scientifico e tecnologico. Ciò ha creato grandi aspettative in merito alle potenzialità diagnostiche e terapeutiche in questo campo; tuttavia, alle aumentate capacità di controllo si accompagna un numero crescente di situazioni che pongono seri dilemmi morali per ricercatori, medici e pazienti. Il dibattito attuale, in un contesto pluralistico, richiede l'elaborazione di un adeguato quadro etico-normativo che sappia bilanciare il progresso scientifico con la dignità umana.
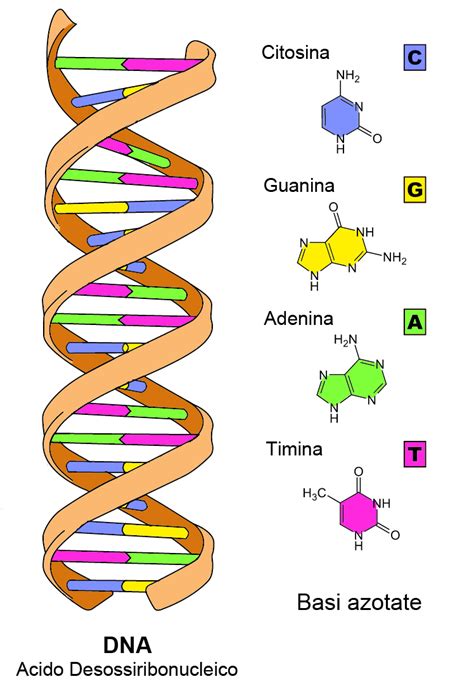
Geni e varianti genetiche: una premessa di natura scientifica
Prima di illustrare cosa sono e come vengono utilizzati i test genetici, è bene ricordare alcuni concetti di base su ciò che è di fatto l’oggetto di tali test, ossia la variabilità genetica nel genoma umano. Ognuna delle nostre cellule contiene, impacchettati nei 46 cromosomi che caratterizzano Homo sapiens, circa sei miliardi di paia di basi di DNA. La sequenza in cui tali basi si presentano è unica in ciascun individuo, con l’eccezione dei gemelli monozigoti.
Dal momento che tutti gli esseri umani appartengono alla stessa specie, le differenze genetiche inter-individuali riguardano solo una piccola parte dei sei miliardi di basi; in particolare, si stima che due persone non imparentate tra di loro differiscano in media per lo 0,1% delle loro basi. In altri termini, comparando la stessa regione genica di due individui, si trova in media una base di differenza ogni mille. Questo numero, che a prima vista potrebbe apparire quasi insignificante, corrisponde in realtà a circa sei milioni di basi sul genoma totale. Per capire quanto ciò sia rilevante in termini di effetti biologici, si pensi che tra noi e gli scimpanzé (Pan troglodytes), i nostri “parenti” più stretti attualmente viventi, c’è una differenza di circa l’1% in termini di sequenza di basi.
Queste variazioni genetiche, in cui in determinate posizioni una base viene sostituita da un’altra, vengono indicate genericamente con l’espressione single nucleotide polymorphisms o SNPs. Nel genoma umano esistono, tuttavia, altre variazioni - dette INDEL - che interessano più basi alla volta, fino a regioni piuttosto ampie di genoma. In questi casi, gruppi di basi contigue vengono aggiunte (“inserzioni”) o perse (“delezioni”). Sommando gli SNPs, gli INDEL e altri tipi di variazioni, si stima che le differenze genomiche totali tra due individui siano nell’ordine dello 0,5%, mentre tra noi e gli scimpanzé si arriva al 4% circa.
Le più recenti linee guida per i genetisti umani suggeriscono di eliminare la distinzione classica tra polimorfismi e mutazioni in favore della definizione generale di “varianti genetiche”, le quali vengono poi distinte in “patogene”, “probabilmente patogene”, “a significato incerto”, “probabilmente benigne” e “benigne”, a seconda del loro effetto sul fenotipo. Alcune varianti sono direttamente causa di malattia, come nel caso di quelle che portano all’insorgenza delle patologie genetiche mendeliane (fibrosi cistica, anemia falciforme, distrofia muscolare di Duchenne). Tuttavia, la maggior parte delle varianti sembra essere priva di un effetto immediato sul fenotipo.
Esistono inoltre polimorfismi di suscettibilità, che non sono di per sé causa diretta di patologia, ma la cui presenza aumenta il rischio di sviluppare la malattia rispetto alla media della popolazione. Specularmente, esistono varianti genetiche “protettive” e altre che determinano la diversa risposta individuale a molti trattamenti farmacologici.
Test genetici: applicazioni e scopi
Con l’espressione “test genetici” si indica una varietà piuttosto ampia di metodologie di analisi delle sequenze geniche di singoli individui, impiegate principalmente in campo medico e forense. In campo medico, l’analisi del DNA si effettua su persone la cui identità sia già nota per finalità diagnostiche, pronostiche o prescrittive.
Tra queste figurano la diagnosi differenziale in presenza di malattie mendeliane, la classificazione accurata di tumori solidi o leucemie, i test pre-sintomatici e quelli pre-natali. Ultimi, ma non meno importanti, sono i test genetici pre-impianto, che possono essere effettuati per verificare che un embrione ottenuto mediante tecniche di fecondazione in vitro non porti nel suo genoma una determinata mutazione patogena presente in almeno uno dei due genitori.

Negli studi di ricerca, si analizzano numeri elevati di individui per studiare la variabilità genetica nelle malattie multifattoriali (diabete, asma, schizofrenia). Un esempio è il programma del sistema sanitario nazionale del Regno Unito, che ha completato l’analisi del genoma di circa 85.000 individui. Sul versante forense, le analisi servono per stabilire la paternità o l’identità in casi di crimini o eventi catastrofici.
Un fenomeno recente è l’uso personale dei test genetici a fini “social” o “ricreativi”. Queste analisi, offerte da compagnie private come 23andMe, permettono di analizzare il background etnico o scoprire parenti ignoti tramite database genomici. Tuttavia, l'offerta di test medici direct-to-consumers ha suscitato critiche da parte dei genetisti: i risultati vengono inviati online senza consulenza, delegando ai consumatori, spesso privi delle competenze necessarie, l'interpretazione di complessi fattori di rischio. Esistono inoltre rischi etici e legali legati all'uso indebito di dati genetici da parte di datori di lavoro o assicuratori, pratiche che, sebbene in gran parte vietate per legge (come sancito dal Genetic Information Nondiscrimination Act negli USA), rimangono una minaccia potenziale.
La frontiera della genomica: limiti e nuove prospettive
Nonostante la capacità di sequenziare un intero genoma umano sia oggi ottenibile a costi contenuti (circa 600 euro), non siamo ancora in grado di stabilire sempre se una variante sia patologica o meno. Questo limite emerge con chiarezza nelle varianti missenso, silenti o in quelle che interessano regioni di DNA le cui funzioni sono ancora oggetto di studio.
Dobbiamo anche considerare il ruolo dell'epigenetica. Se la genetica rappresenta la spartitura di una composizione musicale, l’epigenetica è l’interpretazione che ogni orchestra offre di quella stessa spartitura. Modificando il DNA e gli istoni mediante l’unione di piccole molecole (come la metilazione del DNA), l'epigenetica stabilisce quali geni devono esprimersi e in che momento dello sviluppo, un processo essenziale nell'embrione.
Ingegneria genetica e biotecnologie: il caso CRISPR
Con il termine ingegneria genetica (o tecnologie del DNA ricombinante) si fa riferimento a un insieme eterogeneo di tecniche che permettono di isolare geni, modificarli, introdurli ed esprimerli in un ospite differente. Il genoma umano, composto da circa 30.000 geni, presenta ancora un'enorme quantità di materiale (97%) di cui non conosciamo ancora funzionamento e scopo, il cosiddetto junk DNA.
La metodologia CRISPR-Cas9 rappresenta oggi la punta di diamante di questa rivoluzione. Si tratta di una procedura di “taglia e incolla” che permette di cancellare geni, rimuovere segmenti difettosi o introdurne di estranei. Nel 2017, un team dell'University of Oregon ha pubblicato su Nature un articolo che descrive la correzione di una mutazione genetica in embrioni umani responsabili di una cardiomiopatia ipertrofica.
Crispr-cas 9 le forbici del DNA
Tuttavia, il cosiddetto “editing genomico” viene considerato da molti una nuova forma di eugenetica. L’Enciclopedia Treccani definisce l'eugenetica come la “disciplina che si prefigge di favorire e sviluppare le qualità innate di una razza”. Oggi, l'eugenetica tecnologica si articola su tre direttrici:
- La selezione genotipica dei soggetti a rischio (diagnosi pre-natale o pre-impianto).
- La selezione germinale (scelta di gameti).
- La geneterapia (modificazione dell’informazione genetica).
I rischi associati sono molteplici:
- Rischi epistemologici: La confusione tra “predisposizione” e “predestinazione”, credendo erroneamente che nel genoma sia racchiusa l'essenza della nostra umanità.
- Rischi socio-economici: L'ulteriore diseguaglianza nel diritto alla salute tra chi può accedere a tali terapie e chi non può.
- Rischi culturali: L'uso distorto della tecnica non solo per curare, ma per migliorare tratti somatici secondo le preferenze personali.
Clonazione e cellule staminali: dilemmi bioetici
La clonazione è un ambito che solleva profonde questioni morali. Tecnicamente, consiste nell'estrazione del nucleo di una cellula uovo non fecondata, la fusione con una cellula di chi si vuole clonare e il trasferimento in utero. Sebbene utile in agricoltura o per studiare patologie, la clonazione umana viola il diritto all’unicità genetica e riduce l’essere umano a un mezzo o a un oggetto programmabile.
Parallelamente, le cellule staminali rappresentano una grande speranza per la medicina rigenerativa. Queste cellule non specializzate hanno la capacità di autorinnovarsi e differenziarsi in diversi tipi di tessuti. Si distinguono in:
- Totipotenti: possono formare un organismo completo.
- Pluripotenti: possono dare vita a tutti i tipi di cellule dell'individuo.
- Multipotenti: possono specializzarsi in diversi tipi di tessuto.
- Unipotenti: possono specializzarsi in un solo tipo di cellula.
Il dibattito si concentra soprattutto sulle cellule staminali embrionali, la cui produzione richiede la distruzione dell’embrione. La Pontificia Accademia per la Vita ha evidenziato come, pur essendo la ricerca scientifica necessaria e potenzialmente benefica, essa debba confrontarsi con il valore intrinseco della vita. La ricerca si sta pertanto orientando verso l'uso di cellule staminali adulte, capaci di dare origine a tessuti specifici, cercando di evitare i rischi di tumorigenicità e le complicazioni immunologiche legate all'uso di cellule embrionali.
La sperimentazione come atto di responsabilità
La sperimentazione scientifica - sia in laboratorio, su animali o sull'uomo - è una fase imprescindibile della medicina. Tuttavia, essa deve essere regolata da principi etici rigorosi. Il codice di deontologia medica stabilisce con precisione i limiti della sperimentazione, richiedendo il consenso esplicito e scritto, vietando pratiche pericolose su soggetti sani e garantendo che, per minori e incapaci, sia ammessa solo la sperimentazione terapeutica.
Il medico deve imparare a conoscere le proprietà dei farmaci, agendo secondo il principio di solidarietà e di tutela della vita umana. Come suggerito nel dibattito tra bioetica laica (che vede lo Stato come arbitro neutrale) e bioetica cattolica (che difende principi universali non negoziabili), la soluzione pragmatica risiede nella ricerca di compromessi trasparenti. Non si tratta di cedere a un luddismo antitecnologico, né a una tecnofilia acritica, bensì di orientare l’innovazione verso forme sempre più umane.
La vita, nella sua fragilità, ci è affidata e la tecnologia può essere un meraviglioso modo per tutelarla o il più efficiente dei modi per sterminarla. Il compito della società contemporanea è dunque quello di abitare i luoghi civili di gestione dell’innovazione, fornendo argomentazioni efficaci in un dibattito pubblico che non può più essere rimandato. Il progresso biotecnologico non deve essere considerato un destino ineluttabile, ma una risorsa da governare con un “illuminismo ben temperato”, capace di distinguere tra ciò che è tecnicamente possibile e ciò che è umanamente desiderabile.
tags: #manipolazioni #genetiche #eugenetica #e #embrione