Introduzione: Oltre l'Ovulazione, un Ruolo Inaspettato per l'LH
L'ormone luteinizzante (LH), una gonadotropina secreta dall'ipofisi, è da tempo riconosciuto per il suo ruolo cruciale nella fertilità femminile, principalmente nell'induzione dell'ovulazione e nel supporto del corpo luteo nelle prime fasi della gravidanza. Tuttavia, recenti scoperte scientifiche stanno ampliando la nostra comprensione delle sue funzioni, rivelando un potenziale inaspettato nella protezione della salute riproduttiva femminile. Un gruppo di ricerca dell'Università di Tor Vergata, guidato dalla Dr.ssa Francesca Gioia Klinger e coordinato dal Prof. Massimo De Felici, ha identificato una nuova funzione dell'LH che potrebbe rivoluzionare la preservazione della fertilità, in particolare per le donne sottoposte a terapie oncologiche e per contrastare il declino fisiologico della funzionalità ovarica legato alla menopausa.
La Ricerca Rivoluzionaria: LH Come Scudo Protettivo per i Follicoli Primordiali
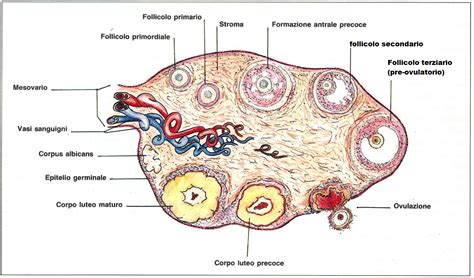
Fino ad oggi, le conoscenze sull'LH nella donna in età fertile si concentravano sul suo impatto diretto sull'ovulazione e sul mantenimento del corpo luteo. La ricerca condotta presso l'Università di Tor Vergata ha dimostrato che l'LH possiede una capacità sorprendente: quella di difendere i follicoli primordiali dagli effetti dannosi di alcuni agenti chemioterapici. I follicoli primordiali sono strutture microscopiche nelle ovaie che contengono gli ovociti destinati a maturare e ad essere rilasciati nel corso della vita riproduttiva di una donna.
Uno dei chemioterapici più studiati in questo contesto è il cisplatino, un farmaco ampiamente utilizzato nel trattamento di diverse neoplasie, inclusi tumori che colpiscono frequentemente le donne come il tumore al seno. Gli esperimenti condotti su modelli animali hanno rivelato che il trattamento con cisplatino da solo porta alla distruzione dei follicoli primordiali, inducendo sterilità nelle topoline in età prepubere. Tuttavia, quando il cisplatino veniva somministrato in concomitanza con l'LH, si osservava una protezione significativa dei follicoli primordiali. La maggior parte di essi non degenerava, e le topoline trattate con LH raggiungevano l'età adulta risultando fertili.
Meccanismi d'Azione: Riparazione del DNA e Prevenzione dell'Apoptosi
I ricercatori hanno indagato sui meccanismi molecolari alla base di questa funzione protettiva dell'LH. Si ipotizza che il cisplatino eserciti il suo effetto tossico danneggiando il DNA degli ovociti contenuti nei follicoli primordiali. L'LH, in questo scenario, sembrerebbe agire su due fronti: da un lato, stimolerebbe i meccanismi di riparo del DNA cellulare, aiutando a correggere i danni indotti dal chemioterapico; dall'altro, ostacolerebbe le vie di morte cellulare programmata (apoptosi) che il cisplatino attiva negli ovociti. Questi meccanismi congiunti spiegherebbero perché l'LH è in grado di preservare l'integrità e la vitalità dei follicoli primordiali.
Attualmente, il gruppo di ricerca sta approfondendo i dettagli di questi meccanismi e sta indagando se questa funzione protettiva dell'LH si manifesti anche nelle ovaie umane. La comprensione completa di questi processi potrebbe aprire la strada a nuove strategie terapeutiche per la preservazione della fertilità.
L'Importanza della Preservazione della Fertilità e della Funzionalità Ovarica
La preservazione della fertilità e il mantenimento della salute ovarica rappresentano sfide sanitarie emergenti. Sempre più donne in età fertile (tra i 18 e i 40 anni) si trovano ad affrontare patologie che portano a un progressivo o immediato esaurimento della riserva ovarica. Questo è particolarmente critico in caso di patologie oncologiche, dove una maggiore probabilità di sopravvivenza porta a una maggiore attenzione verso la qualità della vita post-trattamento, inclusa la possibilità di avere figli.
Lo sviluppo di nuove molecole, l'applicazione di terapie cellulari innovative e l'ottimizzazione delle terapie farmacologiche sono tutti approcci che mirano ad alleviare le problematiche legate alla perdita della funzionalità ovarica. La scoperta di un ruolo protettivo dell'LH si inserisce in questo contesto come una promettente nuova frontiera.
La Stimolazione Ovarica nei Trattamenti di Riproduzione Assistita: Un Contesto Chiave
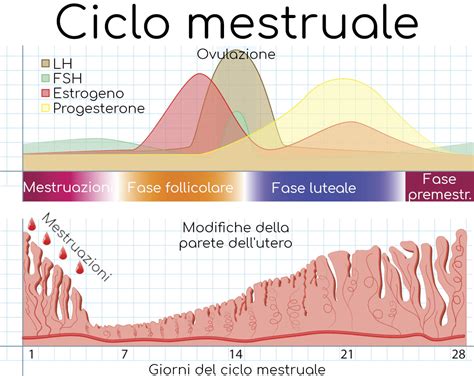
La comprensione dell'azione degli ormoni come l'LH è fondamentale anche nel campo della riproduzione assistita. La stimolazione ovarica controllata è una fase essenziale dei trattamenti come la fecondazione in vitro (FIVET) e l'inseminazione artificiale (IA). L'obiettivo è quello di indurre lo sviluppo di più follicoli in un singolo ciclo mestruale, aumentando così le probabilità di ottenere ovociti maturi e, conseguentemente, le percentuali di successo dei trattamenti.
In un ciclo naturale, solitamente solo un follicolo raggiunge la maturità e rilascia un ovulo. Nei trattamenti di riproduzione assistita, invece, è necessario ottenere un numero maggiore di ovuli. Questo si ottiene attraverso la somministrazione di farmaci ormonali, principalmente gonadotropine come l'FSH (ormone follicolo-stimolante) e l'LH.
Farmacologia della Stimolazione Ovarica: FSH, LH e Altri Agenti
- Gonadotropine (FSH e LH): Questi ormoni, prodotti naturalmente dall'ipofisi, sono fondamentali per stimolare la crescita dei follicoli ovarici. Nella stimolazione ovarica controllata, vengono somministrati in dosi più elevate rispetto ai livelli fisiologici per favorire lo sviluppo follicolare multiplo. L'FSH è il principale attore nella stimolazione iniziale della crescita follicolare, mentre l'LH gioca un ruolo nel supporto della maturazione follicolare e nella secrezione di estradiolo.
- Analoghi del GnRH: Questi farmaci, come gli agonisti (es. Decapeptyl, Enantone) e gli antagonisti (es. Cetrotide, Orgalutran), vengono utilizzati per controllare il ciclo ovarico e prevenire l'ovulazione prematura. Gli agonisti del GnRH sopprimono la produzione endogena di FSH e LH, creando uno stato ipogonadotropo relativo. Gli antagonisti del GnRH competono con il GnRH per il suo recettore, inibendo il rilascio di LH e prevenendo il picco prematuro di LH. Questo controllo è essenziale perché, nei trattamenti di FIVET, gli ovociti devono essere recuperati chirurgicamente prima che avvenga l'ovulazione spontanea.
- Ormone hCG (Gonadotropina Corionica Umana): Questo ormone viene somministrato come "trigger" o innesco dell'ovulazione. L'iniezione di hCG, solitamente 34-36 ore prima del prelievo ovocitario o dell'inseminazione, induce la maturazione finale degli ovociti e prepara l'ovaio all'ovulazione. L'emivita dell'LH endogeno è troppo breve per poter essere utilizzato efficacemente come trigger dell'ovulazione, a differenza dell'hCG.
- Citrato di Clomifene: Utilizzato in alcuni casi, specialmente in donne con sindrome dell'ovaio policistico (PCOS) o altri problemi ovulatori, il citrato di clomifene stimola lo sviluppo follicolare agendo sull'asse ipotalamo-ipofisi-ovaio attraverso un meccanismo di feedback negativo.
- Letrozolo: Questo farmaco è un inibitore dell'aromatasi. Bloccando l'enzima aromatasi, riduce la produzione di estrogeni. La riduzione degli estrogeni porta a una diminuzione del feedback negativo sull'asse ipotalamo-ipofisi, aumentando così la produzione di FSH e LH e stimolando lo sviluppo follicolare. Può essere utilizzato come induttore dell'ovulazione.
Protocollo di Stimolazione Ovarica: Personalizzazione e Monitoraggio
Il protocollo di stimolazione ovarica non è standardizzato ma viene personalizzato per ogni paziente, tenendo conto di diversi fattori:
- Età della paziente: L'età è un fattore determinante per la riserva ovarica e la risposta alla stimolazione.
- Morfologia delle ovaie: Caratteristiche ecografiche delle ovaie possono influenzare il protocollo.
- Massa corporea: Il peso corporeo può influenzare il metabolismo dei farmaci.
- Analisi ormonale: Livelli di ormoni come l'ormone antimulleriano (AMH) e la conta dei follicoli antrali (AFC) forniscono informazioni sulla riserva ovarica.
- Risposta alla stimolazione in cicli precedenti: Esperienze pregresse sono fondamentali per ottimizzare la terapia.
Il processo di stimolazione dura solitamente tra gli 8 e i 14 giorni, con iniezioni che iniziano il secondo o terzo giorno del ciclo mestruale. Il monitoraggio è costante e avviene tramite ecografie transvaginali periodiche per valutare la crescita dei follicoli e misurare lo spessore dell'endometrio, oltre ad analisi del sangue per dosare l'estradiolo e altri ormoni. L'obiettivo è raggiungere follicoli di circa 18 mm di diametro prima di somministrare l'hCG.
Somministrazione dei Farmaci e Gestione della Terapia
I farmaci per la stimolazione ovarica vengono solitamente somministrati tramite iniezioni sottocutanee, utilizzando aghi sottili simili a quelli usati per l'insulina. Le iniezioni sono generalmente effettuate nell'addome. Sebbene all'inizio possa suscitare apprensione, molte donne imparano rapidamente ad auto-somministrarsi le iniezioni, acquisendo autonomia nella gestione della terapia.
La durata del trattamento e il dosaggio dei farmaci sono attentamente calibrati. Per l'inseminazione artificiale (IA), la stimolazione è più "delicata" rispetto alla FIVET, mirando allo sviluppo di uno o al massimo due ovuli maturi. Le dosi ormonali sono basse e il processo dura tipicamente 10-12 giorni. Se si sviluppano più follicoli del previsto, l'IA può essere annullata per ridurre il rischio di gravidanze multiple.
Pergoveris®: preparazione e somministrazione del farmaco. Instituto Bernabeu
Rischi e Effetti Collaterali della Stimolazione Ovarica
La stimolazione ovarica è generalmente ben tollerata, ma come ogni trattamento medico, presenta potenziali rischi ed effetti collaterali:
- Sindrome da Iperstimolazione Ovarica (OHSS): Questa è la complicanza più seria, sebbene rara nei trattamenti di IA a causa della stimolazione lieve. L'OHSS si verifica quando le ovaie rispondono in modo eccessivo agli ormoni, portando a un ingrossamento significativo delle ovaie, accumulo di liquidi nell'addome e nel torace, e sintomi come dolore addominale, nausea, vomito e difficoltà respiratorie. Un attento monitoraggio consente di identificare precocemente un'elevata risposta e di intervenire, ad esempio interrompendo la somministrazione dei farmaci.
- Effetti collaterali lievi e transitori: Possono includere gonfiore addominale, mal di testa, tensione mammaria, stanchezza, alterazioni dell'umore, insonnia e irritabilità. Questi sintomi sono solitamente di lieve entità e si risolvono spontaneamente al termine del trattamento.
- Rischi meccanici: L'aumento delle dimensioni delle ovaie durante la stimolazione può, in rari casi, aumentare il rischio di torsione ovarica (l'ovaio si attorciglia sul suo peduncolo vascolare, compromettendo l'afflusso di sangue) o di rottura di follicoli con conseguente emoperitoneo (sanguinamento nella cavità addominale).
La comunicazione aperta tra paziente e medico è fondamentale per gestire al meglio questi aspetti e garantire la sicurezza del trattamento.
Nuove Prospettive e Ricerca Continua
La scoperta del ruolo protettivo dell'LH nei confronti dei follicoli primordiali, evidenziata dalla ricerca dell'Università di Tor Vergata e pubblicata sulla rivista Cell Death and Differentiation, rappresenta un passo avanti significativo. Il finanziamento di queste ricerche da parte di aziende come Merck e società scientifiche come la Società Europea per la Riproduzione Umana (ESHRE) sottolinea l'importanza clinica di questi studi.
La comunità scientifica continua a esplorare le potenzialità dell'LH, non solo per la preservazione della fertilità in contesti oncologici, ma anche per migliorare le strategie di stimolazione ovarica nei trattamenti di riproduzione assistita. La ricerca sui sottogruppi di pazienti con risposte subottimali alla stimolazione, come quelli identificati dalla classificazione POSEIDON (Patient-Oriented Strategy Encompassing IndividualizeD Oocyte Number), suggerisce che l'integrazione di LH potrebbe essere benefica per una popolazione specifica di pazienti che non rispondono adeguatamente alla sola stimolazione con FSH.
In sintesi, mentre l'LH continua a svolgere il suo ruolo consolidato nell'induzione dell'ovulazione, la sua funzione protettiva emergente apre nuove ed entusiasmanti prospettive per la salute riproduttiva femminile, offrendo speranza a donne che affrontano sfide legate alla fertilità e alla preservazione della loro capacità riproduttiva.