C’è spesso un conflitto intrinseco nei campi sovrapposti per quanto riguarda la fertilità e l’andrologia. Mentre l’obiettivo di tutti gli specialisti della fertilità maschile è facilitare e preservare la paternità biologica, molti professionisti si prendono cura anche di un numero significativo di pazienti che soffrono di ipogonadismo. Con aumenti costanti sia nell’incidenza dell’ipogonadismo che nell’età paterna media, i professionisti stanno ora incontrando uomini ipogonadici che desiderano una futura fertilità o uomini che soffrono gli effetti di un precedente uso di steroidi anabolizzanti androgeni con frequenza crescente.
La somministrazione esogena di testosterone, sebbene rappresenti il gold standard per la gestione dell'ipogonadismo in molti contesti, altera quasi universalmente la spermatogenesi e può persino eliminarla completamente in alcuni uomini, sollevando importanti questioni in merito alla fertilità. L'infertilità è una condizione diffusa che colpisce circa 70 milioni di persone in tutto il mondo, e l’Organizzazione Mondiale della Sanità stima che il 9% delle coppie in tutto il mondo lotta con problemi di fertilità. I fattori maschili contribuiscono al 30-50% dei casi di infertilità. In questo articolo, si esaminano le strategie di gestione per questi pazienti complessi e si esplorano nuovi farmaci che potrebbero essere utili in questa popolazione, fornendo una panoramica dettagliata delle cause, delle implicazioni e delle opzioni terapeutiche.
Ipogonadismo Maschile e Infertilità: Definizioni e Incidenza
L’ipogonadismo maschile è un’entità clinica caratterizzata da bassi livelli sierici di testosterone, l’ormone sessuale maschile primario, in combinazione con sintomi sistemici. Questi sintomi includono affaticamento, disfunzione erettile e cambiamenti dell’umore, e la condizione comporta inoltre rischi metabolici e cardiovascolari noti. Il testosterone basso, o insufficiente, è una condizione medica che può diagnosticare una significativa riduzione della qualità della vita e del benessere generale. Al contrario, gli uomini più giovani possono manifestare sintomi clinici di ipogonadismo nonostante abbiano valori di testosterone sierico "normali", sebbene nell'intervallo inferiore.
L’infertilità del fattore maschile, d'altra parte, è definita come l’incapacità di una coppia di concepire dopo 12 mesi di rapporti regolari e non protetti. Questa incapacità di stabilire una gravidanza è quasi sempre osservata in combinazione con parametri anormali di analisi del seme (SA), ma a volte può essere presente anche quando questi valori sono normali.
Sia l’incidenza dell’ipogonadismo maschile che l’infertilità del fattore maschile sono aumentate notevolmente negli ultimi anni, rendendo indispensabile per gli operatori sanitari espandere il loro armamentario quando si tratta della valutazione e del trattamento di questi disturbi. La carenza di testosterone negli uomini, conosciuta anche come “ipogonadismo”, è una condizione in cui il corpo produce livelli insufficienti di testosterone, un ormone chiave per lo sviluppo e il mantenimento delle caratteristiche sessuali maschili e della fertilità. Una carenza di testosterone può causare una varietà di sintomi, che variano in gravità da persona a persona. A seconda della causa della carenza di testosterone, i sintomi si sviluppano nel corso di settimane, mesi o anni. Nella maggior parte dei casi, i sintomi persistono per un periodo di tempo più lungo perché le persone colpite non assegnano correttamente i disturbi aspecifici. I sintomi menzionati non sono specifici, potendo indicare una carenza o varie altre malattie.
Il Ruolo Fisiologico del Testosterone e l'Asse Ipotalamo-Ipofisi-Gonadi (HPG)
Il testosterone è l’ormone sessuale maschile per eccellenza, fondamentale non solo durante la crescita, in particolare durante la pubertà e l’adolescenza per lo sviluppo delle caratteristiche sessuali secondarie, ma anche durante la vita adulta per la salute generale e la sfera della fertilità. Il suo funzionamento fisiologico nei testicoli è essenziale per la fertilità maschile e lo sviluppo delle caratteristiche del sesso secondario maschile. Negli uomini, gli scopi primari dei testicoli possono essere riassunti come la produzione di testosterone e la spermatogenesi.
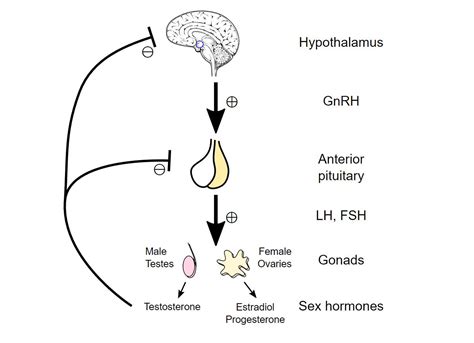
Queste funzioni critiche sono coordinate attraverso una complessa sinfonia di segnalazione ormonale nota come asse ipotalamico ipofisi gonadi (HPG). L’ipotalamo, situato nell’encefalo, secerne la gonadotropina rilasciando l’ormone (GnRH) in modo pulsatile che viaggia quindi attraverso il sistema portale ipofisario per raggiungere l’ipofisi anteriore. In risposta a questo stimolo, l’ipofisi anteriore secerne sia l’ormone follicolo-stimolante (FSH) che l’ormone luteinizzante (LH). L’FSH agisce sulle cellule di Sertoli dei testicoli per facilitare la spermatogenesi, mentre l’LH agisce sulle cellule di Leydig per stimolare la produzione di testosterone. Questo processo è regolato dal “funzionamento coordinato” di ipotalamo, ipofisi e gonadi.
Fisiologia e Fisiopatologia dell’Asse HPT: tra feedback negativi, ipogonadismo AAS-indotto e PCT
Ciò si traduce in concentrazioni intratesticolari straordinariamente alte di testosterone, che sono essenziali per la produzione di spermatozoi. Il resto del testosterone viene rilasciato sistematicamente ed esercita gli effetti fisiologici descritti sopra. Qualsiasi disregolazione di questo percorso può portare a ipogonadismo maschile, infertilità o a una loro combinazione. Nei testicoli, il ruolo del testosterone è cruciale per la maturazione degli spermatozoi. Per esempio, una bassa produzione ormonale porta a una ridotta qualità e quantità di spermatozoi.
Il testosterone è un ormone steroideo appartenente al gruppo degli androgeni, prodotto principalmente nei testicoli negli uomini e, in misura minore, nelle ovaie delle donne e nella corteccia surrenale di entrambi i sessi. Funziona penetrando nella membrana cellulare della cellula bersaglio e legandosi a una molecola intracitosolica nota come recettore degli androgeni. Questo complesso si trasferisce nel nucleo in cui si trova un omodimero che poi si interfaccia con un elemento di risposta agli androgeni sui geni bersaglio, sovraregolando la trascrizione genica e la sintesi proteica. Ciò si traduce in una cascata di effetti che possono essere visti in tutto il corpo.
Gli effetti del testosterone possono essere ampiamente classificati in due sottotipi: androgeno e anabolico. Gli effetti androgeni del testosterone includono quelli tradizionalmente associati alla virilizzazione, come gli effetti sul tratto riproduttivo, la crescita dei capelli e l’attività delle ghiandole sebacee. Questi effetti sono più comunemente correlati con la pubertà maschile. Gli effetti anabolizzanti del testosterone includono un aumento della fissazione dell’azoto, sintesi del collagene, crescita muscolare e metabolismo osseo con attività osteoblastica netta.
Per lo stato di salute generale e la sfera della fertilità è fondamentale che gli organi riproduttivi funzionino adeguatamente. Quando si cerca di concepire, i testicoli devono produrre una certa quantità di spermatozoi normali. Il testosterone è un ormone sessuale fondamentale per uno sviluppo adeguato degli organi riproduttivi in epoca puberale, per una buona funzione sessuale e per la salute generale maschile. Il testosterone agisce a livello cerebrale, stimolando il desiderio sessuale attraverso l’attivazione di neurotrasmettitori come la dopamina. Nelle prime settimane di sviluppo embrionale, il testosterone e la sostanza inibitrice dei condotti di Müller sono i responsabili della differenziazione del sesso maschile. Anche nelle donne il testosterone è importante perché è il precursore della sintesi dell’estradiolo, il principale ormone sessuale femminile; il corretto sviluppo follicolare viene regolato anche dagli androgeni.
Gli uomini producono molto più testosterone rispetto alle donne, con le donne che hanno significativamente meno testosterone nei loro corpi. Il livello medio di testosterone circolante si riduce progressivamente con l’avanzare dell’età. I livelli sierici normali di testosterone nel maschio adulto vanno da 300 a 1.000 ng/dL, con la normale produzione fisiologica di testosterone compresa tra 2,1 e 11,0 mg al giorno. Vi è un declino correlato all’età dei valori sierici totali di testosterone, con conseguente aumento dell’incidenza di ipogonadismo nella popolazione che invecchia. A partire dai 40 anni circa, diminuisce negli uomini a causa della ridotta funzione testicolare, una condizione che i medici definiscono “ipogonadismo ad esordio tardivo”. I livelli di testosterone tendono a seguire un ritmo circadiano naturale con valori che aumentano al mattino, rendendo i test di primo mattino essenziali per una misurazione accurata. La maggior parte del testosterone (98%) viene unito alle proteine, principalmente l’albumina e la globulina che fissa gli ormoni sessuali (SHBG). Solo una piccola parte (dall’1% al 3% circa) circola liberamente nel sangue come testosterone libero.
Gli Steroidi Anabolizzanti Androgeni (AAS) e i Loro Effetti Deleteri
Il testosterone, lo steroide androgeno-anabolizzante (AAS) prototipo, fu inizialmente isolato, caratterizzato e sintetizzato nel 1935. Poco dopo la sua introduzione, i ricercatori notarono la sua capacità di stimolare la crescita muscolare e l’interesse è cresciuto nelle sue potenziali applicazioni per uso sovraterapeutico e prestazioni atletiche. Questi effetti furono ulteriormente resi popolari dall’autore Paul de Kruif nel suo libro del 1945, “The Male Hormone”.

I primi usi documentati dell’AAS nello sport agonistico includono la squadra di canottaggio tedesca del 1952 e la squadra di sollevamento pesi russa del 1954. L’adozione diffusa tra gli atleti olimpici spinse il Comitato Olimpico Internazionale (CIO) ad avviare programmi di screening per l’AAS e i loro derivati negli anni ’60. L’uso dell’AAS è stato esplicitamente vietato a partire dal 1967 e nel 1999 è stata istituita l’Agenzia mondiale antidoping (WADA) per aiutare il CIO a combattere il doping illecito. Nonostante ciò, l’utilizzo dell’AAS continua ad essere pervasivo durante lo sport e, negli ultimi anni, è stato sempre più adottato da giovani che non sono atleti professionisti, ma desiderano semplicemente migliorare il proprio fisico. Gli steroidi anabolizzanti sono sostanze che favoriscono la crescita della massa muscolare e si abusa spesso di essi per migliorare la competitività nello sport.
Gli AAS funzionano tramite un meccanismo d’azione quasi identico a quello del testosterone. Le loro caratteristiche distintive derivano dai loro effetti anabolici preferenziali e dal successivo metabolismo. Per valutare la potenza relativa di AAS, Eisenberg e Gordan nel 1950 proposero un “Indice miotrofico-androgeno (MA)” che confronta i relativi effetti anabolici e androgeni dell’AAS. Questo indice è stato determinato misurando il peso della muscolatura dell’ano levatore del ratto e confrontandolo con il peso della vescicola seminale dopo l’integrazione di androgeni esogeni. Al testosterone, come l’AAS originale, è stato assegnato un indice MA di 1:1. In confronto, gli AAS sintetici mostrano rapporti MA molto più favorevoli. Ad esempio, il nandrolone possiede un indice MA di 11:1, mentre l'oxandrolone, un altro AAS, mostra un indice di 10:1. Di conseguenza, questi composti presentano un potenziale miogenico esponenzialmente maggiore rispetto alla molecola madre con minori effetti collaterali androgeni. Sfortunatamente, come tutti gli AAS, interrompono ancora il normale asse HPG in modo identico al testosterone esogeno.
L’uso prolungato di steroidi anabolizzanti genera non pochi effetti collaterali, poiché interrompe la produzione naturale del testosterone. Per quanto riguarda il potenziale di disfunzione testicolare, la minaccia che l’uso di AAS rappresenta per la futura fertilità e la corretta funzionalità cellulare di Sertoli e Leydig non può essere sopravvalutata. Numerosi studi hanno documentato l’ipogonadismo a lungo termine derivante dall’uso precedente di AAS. Un sondaggio in particolare ha dimostrato che il rimpianto numero uno tra i precedenti utenti di AAS era il non aver compreso le potenziali ramificazioni che il loro uso poteva avere sulla futura fertilità. Successivamente, quando il ciclo di steroidi anabolizzanti viene concluso, il corpo potrebbe non essere più in grado di produrre abbastanza testosterone autonomamente.
Molti utenti di AAS tentano di mitigare questo rischio organizzando il loro uso in “cicli” con periodi dedicati di “terapia post-ciclo” che utilizzano farmaci come il clomifene citrato (CC) per stimolare la funzione testicolare nativa. Sfortunatamente, non ci sono stati studi per documentarne l’efficacia. Sebbene l’insufficienza testicolare derivante dal precedente uso dell’AAS si sia dimostrata curabile nella stragrande maggioranza dei casi, il successo non è garantito e gli uomini che desiderano una futura fertilità dovrebbero essere avvertiti di conseguenza. Gli effetti negativi dell’AAS si estendono ben oltre il sistema riproduttivo, essendo di ampia portata e comprendendo, tra gli altri, i sistemi cardiaco, epatico, renale, muscoloscheletrico, endocrino ed ematopoietico. La sfida con lo studio degli effetti avversi dell’AAS è che ci sono stati pochi e preziosi studi clinici che hanno studiato le conseguenze di questi composti nell’uomo. La maggior parte degli studi che riportano effetti avversi da AAS sono stati di natura retrospettiva e aneddotica, senza standardizzazione delle sostanze o dei regimi di dosaggio precedentemente utilizzati.
Lo studio della prevalenza dell’uso di AAS spesso viene confuso con la parola steroide, corticosteroide, cortisone, spesso autoprescritta. Ciò ha portato a stime diverse sull’uso di AAS non prescritte che vanno dal 6,6% dei maschi di maggiore età delle scuole superiori al 7,3% delle donne delle scuole medie. Una revisione più rigorosa, che comprende diversi studi recenti, stima che da 2,9 a 4 milioni di americani di età compresa tra 13 e 50 anni abbiano provato l’AAS almeno una volta. I ricercatori hanno scoperto che l’età media del primo utilizzo di AAS è di 22 anni e che solo il 13,1% degli utenti aveva iniziato prima dei 18 anni. Meno dell’1% era stimato essere di sesso femminile.
Effetti Deleteri del Testosterone Esogeno sulla Riproduzione Maschile
Gli effetti deleteri del testosterone esogeno sulla riproduzione maschile derivano dalla sua interruzione dell’asse HPG maschile sopra descritto e dalle conseguenti diminuzioni sia del siero FSH che dell’LH. Senza un’adeguata stimolazione da parte dell’FSH, le cellule di Sertoli non sono in grado di supportare la spermatogenesi, mentre i livelli inferiori di LH portano alla riduzione della produzione di testosterone endogeno dalle cellule di Leydig. Sebbene i livelli sierici di testosterone siano mantenuti con la somministrazione esogena, adeguati livelli intra-testicolari di testosterone possono essere raggiunti solo dalla produzione endogena e sono essenziali per la normale spermatogenesi. Di conseguenza, il testosterone esogeno porta quasi universalmente a un basso livello di testosterone intratesticolare con conseguente atrofia dell’epitelio germinale e successiva azoospermia nel 40% degli uomini.
Sebbene la maggior parte degli uomini alla fine sperimenterà un ritorno dello sperma all’eiaculato dopo la cessazione dell’uso di testosterone, il completo ripristino della fertilità precedente è incerto. Anche con la terapia aggiuntiva, fino al 30% degli uomini precedentemente azoospermici potrebbe non riuscire a raggiungere conteggi mobili totali superiori a 5 milioni.
Una volta rilasciato nel siero, il testosterone può subire diversi destini metabolici con una porzione convertita in 17β-estradiolo tramite l’enzima aromatasi e un’altra nel potente androgeno diidrotestosterone (DHT) tramite 5α-reduttasi. Una quantità significativa di aromatasi si trova all’interno del tessuto adiposo, portando ad un aumento dei livelli di 17β-estradiolo spesso osservato negli uomini obesi. Questo eccesso di estrogeni è associato a ginecomastia, ritenzione idrica, disfunzione sessuale e aumento del rischio di tromboembolia. Il DHT d’altra parte ha un’affinità 3 volte maggiore per il recettore degli androgeni. Gli studi hanno dimostrato che ciò è essenziale per la normale libido e la funzione erettile, ma è anche noto per contribuire a effetti collaterali androgeni indesiderati, come acne, alopecia e iperplasia prostatica benigna.
Cause di Carenza di Testosterone e Infertilità Maschile
L’infertilità o la ridotta fertilità maschile possono derivare da una molteplicità di fattori, tra cui disfunzione testicolare, endocrinopatie, fattori legati allo stile di vita come il tabacco e l’obesità, fattori anatomici congeniti, esposizioni gonadotossiche, l’invecchiamento e anomalie genetiche. Si parla di “ipogonadismo primario” quando si caratterizza per una scarsa funzionalità dei testicoli nelle sue due funzioni principali: produzione di testosterone e spermatogenesi. Altre cause di carenza di testosterone includono la diminuzione della produzione di ormoni nei testicoli o nelle ovaie, malattie sistemiche come la cirrosi epatica, e l'assunzione di determinati farmaci.
I livelli di testosterone tendono a diminuire con l’età in entrambi i sessi, a partire dai 40 anni circa negli uomini a causa della ridotta funzione testicolare. L’abuso di droghe, alcol, nicotina e altri farmaci o tossine ambientali possono influenzare negativamente la produzione di testosterone sia negli uomini che nelle donne. Anche la malnutrizione sconvolge l’equilibrio ormonale del corpo, alterando il rilascio di vari ormoni.
L’obesità, ad esempio, è strettamente associata all’infertilità maschile, probabilmente a causa di cambiamenti ormonali secondari all’eccesso di tessuto adiposo. In letteratura, si è dimostrata una relazione inversa tra indice di massa corporea (BMI) e testosterone, rapporto testosterone/estradiolo, volume dell’eiaculato, concentrazione di spermatozoi e morfologia, con tassi più elevati di azoospermia e oligospermia tra gli uomini obesi. Inoltre, anche lo stress prolungato e uno stile di vita sedentario possono contribuire alla diminuzione dei livelli di questo ormone.
Anomalie Genetiche e Condizioni Mediche Comorbili
Le anomalie genetiche giocano un ruolo significativo nell'infertilità maschile. Le anomalie cromosomiche colpiscono sia i cromosomi sessuali che quelli autosomici e possono causare aberrazioni numeriche o strutturali. Le mutazioni genetiche legate all’autosoma sono principalmente coinvolte nell’ipogonadismo centrale, nella teratozoospermia o astenozoospermia monomorfa, nell’azoospermia ostruttiva congenita e nei casi familiari di disturbi spermatogeni quantitativi.
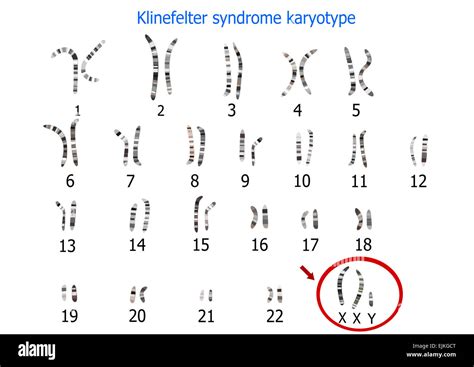
Invece, tra le anomalie dei cromosomi sessuali, che possono avere un ruolo importante nella grave compromissione spermatogenica, riconosciamo alcune sindromi come la Sindrome di Klinefelter (KS), l’aneuploidia genetica più comune dell’insufficienza testicolare negli uomini oligozoospermici e azoospermici, con una prevalenza del 10-15%. Colpisce da 1/1.000 a 1/500 maschi ed esistono due forme principali: 47XXY non a mosaico (80-90%) o 47XXY/46XY a mosaico (5-10%). Il fenotipo classico è quello di un maschio alto con testicoli piccoli e ginecomastia; tuttavia, il fenotipo può variare da un maschio completamente virilizzato a uno con carenza di androgeni. Di conseguenza, il 70% degli uomini affetti da KS rimane non diagnosticato fino alla tarda età adulta. Il profilo endocrino rivela ipogonadismo ipergonadotropo (testosterone basso-normale, livelli elevati di FSH e LH e inibina B non rilevabile, compatibile con insufficienza testicolare). L’analisi dello sperma normalmente rivela azoospermia e può essere l’unica anomalia fenotipica negli uomini con KS. Altre anomalie genetiche dei cromosomi sessuali comprendono le traslocazioni robertsoniane o le microdelezioni del cromosoma Y. A queste si aggiungono le anomalie idiopatiche dello sperma, che ad oggi, rappresentano ancora circa il 30% dell’infertilità maschile. Con gli sforzi attuali e futuri che esaminano i fattori molecolari e genetici responsabili della spermatogenesi e della fecondazione, potremmo essere in grado di comprendere meglio le eziologie dell’infertilità del fattore maschile e quindi migliorare i risultati per i nostri pazienti e le nostre coppie.
Tuttavia, sono state riscontrate anche una varietà di condizioni mediche comorbili in grado di influenzare i parametri dello sperma. Per citarne alcune, malattie renali, insufficienza epatica, emocromatosi, malattia polmonare ostruttiva cronica, fibrosi cistica e sclerosi multipla. Il meccanismo attraverso il quale le condizioni mediche possono avere impatto sulla fertilità comprende effetti sui livelli ormonali, sulla compromissione della funzione sessuale (inclusa la funzione eiaculatoria) o sulla compromissione della funzione testicolare/spermatogenesi. Ottimizzando dal punto di vista medico la salute di un uomo, i miglioramenti dello stato di malattia medica possono migliorare i parametri dello sperma, la funzione sessuale e il potenziale di fertilità.
Il Varicocele e Altri Interventi Chirurgici Riproduttivi
Il varicocele, caratterizzato da vene anormalmente dilatate e tortuose del plesso pampiniforme, è una causa comune di infertilità maschile. Si stima che i varicoceli siano presenti nel 15-20% della popolazione maschile generale e nel 35-40% degli uomini infertili.
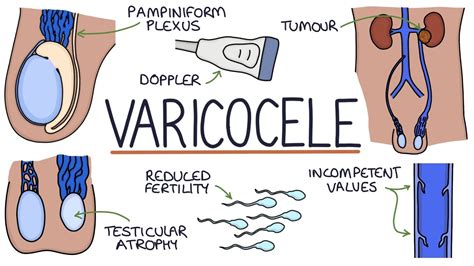
Si ritiene che il meccanismo d’azione con cui un varicocele influisce sulla fertilità sia correlato principalmente alla stasi del sangue nello scroto, creando un eccesso di calore, che a sua volta riduce la spermatogenesi. Tuttavia, esistono ulteriori teorie su come un varicocele possa influenzare negativamente la fertilità, incluso il reflusso di metaboliti nel testicolo e un aumento delle specie reattive dell’ossigeno che creano danni al DNA spermatico ed una disregolazione ormonale. È stato dimostrato che la varicocelectomia migliora i parametri dello sperma e aumenta anche i tassi di gravidanza con una diminuzione significativa dei tassi di aborti.
Il ruolo degli interventi chirurgici riproduttivi maschili convenzionali volti a migliorare o affrontare l’infertilità maschile è stato recentemente studiato nel tentativo di espandere le loro ristrette indicazioni. Questi interventi includono la varicocelectomia e l’estrazione dello sperma testicolare (TESE). Per quanto riguarda l’estrazione testicolare dello sperma, storicamente la TESE è stata utilizzata solo per gli uomini affetti da azoospermia. Studi recenti che hanno esaminato la frammentazione, la capacitazione e l’età paterna avanzata del DNA hanno fatto luce su argomenti precedentemente sconosciuti.
Diagnosi della Carenza di Testosterone e Infertilità
La valutazione dell’infertilità maschile e della carenza di testosterone comprende un’anamnesi dettagliata, un esame fisico mirato e test di laboratorio selettivi. Il quadro sintomatologico, infatti, è spesso uno strumento importante che il medico ha a disposizione per fare un’adeguata diagnosi differenziale, per questo è fondamentale informare il medico specialista di tutti i fastidi, disturbi, dolori e sensazioni che si provano.
Un elemento diagnostico chiave è l'analisi dello sperma, chiamato spermiogramma. Eseguire uno spermiogramma dopo la pubertà permette di misurare la fertilità, quantificando il numero e la qualità degli spermatozoi. Questo test può essere scelto se si desidera avere un bambino o se si desidera conoscere le proprie probabilità di concepimento futuro. Se si incontrano problemi di fertilità, i risultati dell’analisi del liquido seminale possono aiutare il medico curante a consigliare diverse opzioni di trattamento.

Oltre all’inchiesta sull’anamnesi e all'esame fisico, il medico eseguirà ulteriori accertamenti, prescrivendo un esame del sangue in cui determina il livello di testosterone. I livelli di testosterone tendono a seguire un ritmo circadiano naturale, con valori che aumentano al mattino, rendendo i test di primo mattino essenziali per una misurazione accurata. Quando le misurazioni del testosterone totale non sono conclusive, è necessario fare il test del testosterone libero, poiché solo una piccola parte (dall’1% al 3% circa) circola liberamente nel sangue. Se si hanno sintomi o segni di ipogonadismo o se i livelli di testosterone erano bassi in precedenza, il medico di base o lo specialista del follow-up potrebbe dosare anche l’ormone luteinizzante (LH). Finora, non ci sono soglie uniformi su quando esiste effettivamente una carenza di testosterone, rendendo la valutazione clinica e il contesto individuale essenziali. Il medico specialista può effettuare ulteriori accertamenti per confermare la diagnosi ed escludere altre malattie, considerando anche fattori come malattie precedenti, malattie in famiglia e l'ambiente psicosociale.
Opzioni Terapeutiche per l'Insufficienza di Testosterone e l'Infertilità
I trattamenti per l'insufficienza di testosterone e l'infertilità mirano a risolvere o rispondere alla problematica di base e possono variare da una proposta di ottimizzazione dello stile di vita all’utilizzo di un approccio terapeutico medico farmacologico empirico o mirato, fino alle terapie chirurgiche. È importante stabilire con certezza la causa del disturbo, in modo da ricevere una diagnosi adeguata e un piano di trattamento personalizzato.

Se le persone colpite hanno una carenza accertata di testosterone e non ci sono altre malattie dietro i sintomi, il medico specialista prescriverà nella maggior parte dei casi un trattamento ormonale con testosterone, noto come Terapia Sostitutiva del Testosterone (TRT). Questa prevede la somministrazione controllata di testosterone sotto varie forme:
- Gel: Il medico prescrive spesso un gel contenente testosterone che mantiene il livello nel sangue in gran parte costante. Per fare questo, si applica ogni giorno su una vasta area del corpo (ad es. sulla parte superiore delle braccia, sulle spalle o sull’addome). È importante rispettare i criteri di somministrazione e applicare il gel su una zona della pelle pulita e asciutta.
- Cerotti: Anche i cerotti cutanei sono adatti per fornire testosterone in modo uniforme nel corpo. Le persone colpite applicano una volta al giorno un cerotto sulla schiena, sullo stomaco, sulla parte superiore del braccio o sulla coscia, solitamente di notte, lasciandolo agire per 24 ore.
- Iniezioni: I medici spesso somministrano iniezioni intramuscolari per correggere la carenza di testosterone. A seconda delle esigenze, il medico lo inietta ogni due/tre settimane.
- Compresse o capsule: Il testosterone è disponibile anche in queste forme.
- Impianti: Con una piccola incisione nella pelle viene applicato l’impianto, che rilascia testosterone gradualmente.
È fondamentale notare che la TRT, sebbene efficace per gestire i sintomi dell'ipogonadismo, può produrre l’effetto indesiderato di sopprimere la fertilità. Questo è un aspetto critico da considerare per gli uomini che desiderano concepire. Secondo lo stato attuale delle conoscenze, la somministrazione di testosterone non aumenta la probabilità di sviluppare il cancro, ma spesso peggiora una malattia esistente, specialmente in presenza di livelli elevati di PSA (Antigene Prostatico Specifico).
Nuove Frontiere Terapeutiche e Procreazione Medicalmente Assistita (PMA)
Dalla sintesi originale del testosterone, sono stati sviluppati numerosi altri farmaci che sfruttano l’asse HPG per trattare l'ipogonadismo preservando o migliorando la fertilità:
- Gonadotropina Corionica Umana (HCG): L’HCG fu identificato per la prima volta nel sangue e nelle urine delle donne in gravidanza nel 1927. Il lavoro successivo ha mostrato che questa sostanza non ha origine dall’ipofisi, ma dai villi corionici della placenta. Fu durante quel periodo che fu usato per la prima volta il termine HCG, e la società olandese Organon iniziò a commercializzarlo come “Pregnon” nel 1931, poi rinominato “Pregnyl” nel 1932, nome con cui è ancora sul mercato. L’uso di HCG negli uomini è stato studiato già nel 1950 e da allora è stato dimostrato che aumenta efficacemente i livelli di testosterone endogeno. Uno studio recente ha dimostrato che gli uomini ipogonadi trattati con monoterapia con HCG hanno sperimentato un aumento del testosterone sierico di circa 250 ng/dL con un miglioramento accettabile dei sintomi ipogonadi. Un ulteriore vantaggio di HCG è che agisce direttamente sul testicolo, provocando una pronta risposta rispetto ai farmaci indiretti come il Clomifene Citrato (CC) che si basano sulla sintesi ipofisaria di LH. È per questo motivo che la terapia con HCG è diventata una pietra miliare nel trattamento della fertilità maschile.
- Clomifene Citrato (CC): È un noto modulatore selettivo del recettore degli estrogeni (SERM) che agisce inibendo il feedback negativo dell’estrogeno sull’ipotalamo. Probabilmente il farmaco più comunemente usato nella fertilità maschile, il CC ha dimostrato di aumentare i livelli sierici di LH, FSH e il testosterone endogeno preservando e persino potenzialmente migliorando i parametri dell'analisi del seme.
- Tamoxifene: Un altro SERM, possiede un meccanismo d’azione simile al CC.
Il meccanismo con cui il testosterone e il deidroepiandrostene aumentano gli androgeni è differente. Nonostante esistano diversi studi, il livello di evidenza non è elevato.
Quando le terapie mediche falliscono, la Procreazione Medicalmente Assistita (PMA) interviene come opzione valida in casi di ipogonadismo con infertilità, soprattutto se associata a tecniche avanzate come l'iniezione intracitoplasmatica di spermatozoi (ICSI) o la micro-TESE (Micro-Testicular Sperm Extraction). È, oramai, ampiamente riconosciuto nella letteratura scientifica come il testosterone possa essere utilizzato come coadiuvante nei cicli di fecondazione in vitro (FIVET) per migliorare la risposta ovarica in alcune donne, soprattutto per i soggetti con bassa riserva ovarica o scarsa risposta alla stimolazione ovarica. Per cui, somministrato prima della stimolazione ovarica, può aumentare la densità dei recettori per l’FSH nei follicoli, migliorando la risposta ovarica. L’uso corretto di questo trattamento potrebbe incrementare il numero di ovociti dopo la puntura follicolare, un minor tasso di aborto e maggiori probabilità di gravidanza clinica. Questi dati sono ancora poco chiari e sono necessari ulteriori studi per confermarli e per stabilire protocolli ottimali e selezionare le pazienti che ne possono beneficiare.
Stile di Vita e Strategie Naturali
Per aumentare i livelli di testosterone in modo naturale, si possono adottare diverse strategie. L’esercizio fisico regolare, soprattutto l’allenamento con i pesi e l’alta intensità, può stimolare la produzione di testosterone. È per questo che una dieta mediterranea bilanciata, ricca di proteine magre, grassi sani e micronutrienti, è l’ideale per mantenere livelli ottimali di testosterone.

Inoltre, è importante condurre uno stile di vita sano in generale. Evitare l’abuso di droghe, alcol, nicotina e l'esposizione a tossine ambientali può influenzare positivamente la produzione di testosterone. Anche lo stress prolungato e uno stile di vita sedentario possono contribuire alla diminuzione dei livelli di questo ormone. Prendersi cura della propria salute mentale può essere benefico; anche piccoli cambiamenti nel proprio stile di vita possono avere un impatto positivo sia sulla salute fisica che mentale.
Problemi di Fertilità e Testosterone nei Pazienti Oncologici
Qualsiasi uomo, anche chi non ha mai subito trattamenti antitumorali, può sviluppare problemi di fertilità, carenza di testosterone e/o disfunzione sessuale. Tuttavia, chi ha ricevuto trattamenti antitumorali può essere a maggior rischio di tali problemi con l’avanzare dell’età. I trattamenti specifici che aumentano questo rischio includono la chemioterapia con agenti alchilanti come ciclofosfamide e procarbazina, e 12 Gy o più di radioterapia a livello dei testicoli o a un’area che include i testicoli. È possibile verificare se si sono ricevuti uno di questi trattamenti consultando il proprio Passaporto del lungo-sopravvivente o la propria relazione di fine cura.
Anche se si hanno problemi di fertilità, carenza di testosterone o disfunzione sessuale, non è detto che siano necessariamente conseguenza dei trattamenti antitumorali; ci sono molti segni e sintomi che suggeriscono la presenza di tali problemi. I pazienti a maggior rischio dovrebbero sottoporsi a monitoraggi specifici:
- Misura della crescita e della progressione della pubertà: Almeno una volta all’anno, a partire dai 10-12 anni di età.
- Spermiogramma: Eseguire un’analisi del liquido seminale dopo la pubertà per misurare la fertilità, se si desidera avere un bambino o conoscere le proprie probabilità di concepimento futuro.
- Prelievo ematico per il testosterone: Almeno ogni 2-3 anni, di solito se il trattamento ha incluso radioterapia (12 Gy o più) ai testicoli o a un’area che include i testicoli. Il medico curante può indicare la frequenza necessaria.
- Dosaggio di LH: Se si hanno sintomi o segni di ipogonadismo o se i livelli di testosterone erano bassi in precedenza, il medico di base o lo specialista del follow-up potrebbe dosare anche l’ormone luteinizzante (LH).
- Discussione sulla disfunzione sessuale: È bene parlare dell’argomento con il proprio medico di base o con lo specialista del follow-up almeno ogni 5 anni se si hanno (o si sono avuti) sintomi e segni di disfunzione sessuale. Ciò è particolarmente importante se si è subito un intervento chirurgico al bacino, al midollo spinale o ai nervi che controllano gli organi riproduttivi.
Se si hanno problemi di fertilità, carenza di testosterone e/o disfunzione sessuale, il medico di base o lo specialista probabilmente indirizzerà a uno specialista. Quest'ultimo potrebbe discutere diverse opzioni di trattamento, come il trattamento riproduttivo assistito o la terapia ormonale sostitutiva. Non tutti desiderano diventare genitori, ma se lo si desidera, è importante conoscere le opzioni disponibili. Queste possono includere l’utilizzo di fecondazione in vitro (FIV), spermatozoi donati da un altro uomo, o l’utilizzo dei propri spermatozoi se ne erano stati conservati prima del trattamento antitumorale.
Affrontare problemi di fertilità, carenza di testosterone e/o disfunzione sessuale può essere difficile e influenzare le relazioni personali e sessuali. Se si hanno problemi legati alla sessualità, è consigliabile parlarne con il medico di base o con lo specialista che si occupa del follow-up, che potrebbero indirizzare a uno specialista in salute sessuale. Parlare con amici e familiari può essere utile, così come richiedere una consulenza specialistica e/o contattare gruppi di supporto, come le associazioni dei pazienti. È importante essere consapevoli della possibilità di sviluppare questi problemi e conoscerne i sintomi e i segni.
tags: #insufficienza #testosterone #fertilita