La fibrosi cistica (FC) è una malattia genetica complessa che, grazie ai progressi della medicina, oggi permette a chi ne è affetto di vivere più a lungo e con una qualità di vita decisamente migliore rispetto al passato. Tuttavia, le implicazioni della FC si estendono anche alla sfera riproduttiva, sollevando interrogativi sulla fertilità e sulla possibilità di avere figli. Spesso parlarne con chi sa fornire risposte corrette non è così semplice, un po’ per qualche (infondato) timore o vergogna, un po’ perché spesso certe cose si danno per scontate… anche quando non lo sono affatto! Questo articolo si propone di fare chiarezza su come la fibrosi cistica incide sulla fertilità e di esplorare le possibilità concrete per diventare genitori.
Le Basi Genetiche della Fibrosi Cistica
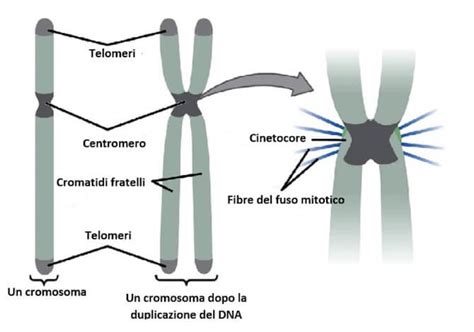
La fibrosi cistica è una malattia genetica autosomica recessiva causata da mutazioni del gene CFTR (Cystic Fibrosis Transmembrane Conductance Regulator). Questo gene, situato sul braccio lungo del cromosoma 7, contiene le istruzioni per produrre una proteina che agisce come un canale per il trasporto di ioni cloro e acqua attraverso le membrane cellulari. Quando il gene CFTR è alterato, si verifica un difetto nel trasporto di sali e acqua nelle cellule, portando a un ispessimento delle secrezioni mucose che coinvolgono diversi organi del corpo, tra cui i polmoni, l'intestino, il pancreas e il fegato.
Ogni persona possiede due copie del gene CFTR, una ereditata da ciascun genitore. Se una persona ha una sola copia del gene mutato, viene definita portatrice sana della malattia. I portatori sani non presentano sintomi evidenti di fibrosi cistica, ma possono trasmettere la mutazione ai propri figli. In Italia, si stima che una persona su 25 sia portatrice sana della mutazione della fibrosi cistica, con una frequenza di portatori compresa tra 1 su 26 e 1 su 30. Essere portatori sani significa avere una sola copia del gene mutato; non si è malati, non si hanno sintomi, e spesso non si sospetta nemmeno di esserlo.
Le mutazioni del gene CFTR sono numerose: a oggi ne sono state individuate più di 1.600. La frequenza relativa delle mutazioni varia in relazione all'area geografica. La mutazione più frequente, F508del, si concentra maggiormente nella popolazione dell'Europa settentrionale rispetto a quella meridionale. In Italia, F508del è la mutazione di gran lunga più frequente, rappresentando il 51% degli alleli responsabili della malattia. Le 12 mutazioni più diffuse caratterizzano il 73% degli alleli responsabili di malattia, con differenze significative tra regioni geografiche.
Le mutazioni sono state suddivise in 5 classi in base alle alterazioni di struttura o funzione che provocano nella proteina CFTR:
- Classe I: Riguardano la mancata produzione della proteina.
- Classe II (es. F508del): Impediscono la corretta maturazione della proteina.
- Classe III e IV: La proteina viene prodotta e raggiunge la membrana cellulare, ma il canale del cloro è mal regolato (si apre e si chiude con difficoltà) o è poco permeabile.
- Classe V: Consentono la produzione di una piccola quantità di proteina funzionante.
A rendere ancora più complessa la struttura del gene CFTR è la presenza di un polimorfismo (variante) chiamato polyT nell'introne 8. Questo tratto è costituito da una serie ripetuta di T (Timina) che possono essere presenti in varie lunghezze (variante 5T, 7T, 9T). La lunghezza del tratto polyT condiziona il buon funzionamento del gene e la produzione di una quantità normale di proteina CFTR. La variante 9T è associata a una produzione proteica quasi normale; la variante 7T a una produzione variabile tra il 50% e il 100% del normale; la variante 5T, invece, porta a una produzione ridotta di proteina CFTR (dal 5% al 30%). L'analisi di primo livello in laboratorio permette di identificare un pannello di mutazioni e il polyT (5/7/9) associati alla condizione di portatore sano o affetto da fibrosi cistica o patologie correlate al CFTR.
Il test del sudore è un esame diagnostico fondamentale per la fibrosi cistica, che misura la concentrazione di cloro nel sudore. Nei malati di fibrosi cistica, questa concentrazione risulta eccezionalmente alta.
Impatto della Fibrosi Cistica sulla Fertilità Maschile
Nei ragazzi e negli uomini con fibrosi cistica, le mutazioni del gene CFTR sono spesso responsabili di difetti significativi nelle capacità riproduttive, portando in una percentuale molto elevata di casi a uno stato di infertilità.
Nel 98% circa dei casi maschili, la fibrosi cistica comporta l'assenza o la malformazione dei dotti deferenti (CBAVD - Congenital Bilateral Absence of Vas Deferens). I dotti deferenti sono i canali attraverso cui gli spermatozoi si spostano dai testicoli verso l'uretra per essere espulsi durante l'eiaculazione. La loro assenza o ostruzione impedisce il passaggio degli spermatozoi, provocando una forma di infertilità chiamata azoospermia ostruttiva. Questo significa che i testicoli producono spermatozoi, ma questi non riescono a raggiungere l'eiaculato.
Un ampio gruppo di uomini malati di fibrosi cistica sono azoospermici, ovvero, nel loro seme non sono presenti spermatozoi, perché non posseggono i condotti attraverso cui circolano gli spermatozoi prima di essere espulsi nell'eiaculazione. La mancanza dei vasi deferenti è una causa genetica dell'azoospermia ostruttiva.
L'azoospermia ostruttiva è una condizione che può essere affrontata con successo attraverso le moderne tecniche di Procreazione Medicalmente Assistita (PMA). È possibile recuperare chirurgicamente gli spermatozoi direttamente dai testicoli o dall'epididimo attraverso procedure come la MESA (Microepididymal Sperm Aspiration), la TESE (Testicular Sperm Extraction) o la PESA (Percutaneous Epididymal Sperm Aspiration). Una volta recuperati, questi spermatozoi possono essere utilizzati per la fecondazione in vitro (FIVET) o, più frequentemente, per l'iniezione intracitoplasmatica dello spermatozoo (ICSI), dove un singolo spermatozoo viene iniettato direttamente nell'ovocita.
È importante sottolineare che non tutti gli uomini con fibrosi cistica sono completamente infertili. Alcune mutazioni, o la presenza di una sola mutazione (portatori sani con specifiche varianti come la 5T o la 7T), possono portare a una ridotta fertilità piuttosto che a un'infertilità completa, con alterazioni nella qualità e nella motilità degli spermatozoi o nel processo di spermatogenesi.
Impatto della Fibrosi Cistica sulla Fertilità Femminile
Nelle ragazze e nelle donne con fibrosi cistica, le anomalie dell'apparato riproduttore sono molto più rare rispetto ai maschi. Tuttavia, la fertilità femminile può essere comunque influenzata dalla malattia.
Le alterazioni più frequentemente riscontrate nelle donne con FC riguardano il muco cervicale e uterino. Questo muco, che normalmente facilita la progressione degli spermatozoi verso l'utero e l'ovulo, può essere più denso e viscoso a causa della fibrosi cistica. Questa alterazione può rendere più difficile la penetrazione degli spermatozoi, compromettendo la fecondazione naturale. Inoltre, il muco cervicale alterato può influenzare l'impianto dell'embrione nell'utero, riducendo le probabilità di una gravidanza.
Un altro fattore che può incidere sulla fertilità femminile è l'irregolarità dei cicli mestruali, spesso legata allo stato ipermetabolico e alla possibile magrezza che alcune donne con FC possono sperimentare. Cicli irregolari possono rendere più difficile prevedere il periodo fertile e ottimizzare i tempi per il concepimento.
Nonostante queste possibili difficoltà, è fondamentale sottolineare che tali alterazioni portano a reali difficoltà riproduttive solo in una minoranza delle ragazze e donne affette da fibrosi cistica. Molte donne con FC sono in grado di concepire spontaneamente e portare a termine gravidanze senza particolari problemi.
Con l'arrivo dei modulatori CFTR, farmaci innovativi che migliorano la funzione della proteina CFTR difettosa, è stato osservato un aumento dei tassi di gravidanza spontanea anche nelle donne con fibrosi cistica. Questi farmaci agiscono correggendo il difetto di base della malattia, migliorando la funzione dei canali del cloro e di conseguenza la qualità delle secrezioni corporee, inclusi il muco cervicale.
Considerazioni sulla Contraccezione e sulla Pianificazione Familiare
Tutto quanto esposto riguardo le potenziali difficoltà di fertilità non deve assolutamente portare all'errata convinzione che non sia necessario l'utilizzo di metodi contraccettivi. In particolare, l'uso del preservativo è fondamentale per diverse ragioni:
- La sterilità non è una condizione certa: Come evidenziato, l'infertilità non è una condizione assoluta e garantita in tutti i pazienti FC, in particolare nelle femmine. Esiste sempre una possibilità di concepimento spontaneo.
- Protezione dalle Malattie Sessualmente Trasmissibili (MST): L'uso del preservativo è cruciale per la protezione dalle MST, quali HIV, Epatite B e C, Sifilide, ecc. Queste infezioni sono al giorno d'oggi molto più diffuse di quanto ci si possa aspettare e rappresentano un rischio per la salute riproduttiva e generale.
Pertanto, anche per gli uomini con FC che presentano azoospermia, l'uso del preservativo rimane una pratica raccomandata per prevenire le MST.
Quando i malati di fibrosi cistica desiderano ampliare la famiglia, è essenziale richiedere una consulenza medica e genetica. Lo specialista suggerirà di ampliare lo studio genetico a entrambi i membri della coppia per valutare il rischio di trasmettere la malattia alla prole.
Test del portatore sano di fibrosi cistica quando si hanno casi in famiglia
Percorsi per Diventare Genitori: PMA e Diagnosi Genetica Preimpianto
Nonostante le sfide, l'idea di avere un bambino non deve assolutamente portare allo scoraggiamento. L'infertilità non è mai sicura al 100%, e soprattutto, grazie alle moderne tecniche di fecondazione assistita, tantissimi pazienti FC stanno crescendo i loro figli.
Le tecniche di Procreazione Medicalmente Assistita (PMA) offrono soluzioni concrete per le coppie in cui uno o entrambi i partner sono affetti da fibrosi cistica. Come accennato, per gli uomini con azoospermia ostruttiva, è possibile il recupero chirurgico degli spermatozoi e la loro successiva utilizzazione in cicli di fecondazione in vitro con ICSI.
Inoltre, per le coppie in cui entrambi i partner sono portatori sani di mutazioni CFTR, o in cui uno è affetto e l'altro portatore, la Diagnosi Genetica Preimpianto (DGP) rappresenta una tecnologia fondamentale. La DGP è una tecnica di riproduzione assistita che permette di analizzare geneticamente gli embrioni creati in vitro prima del loro trasferimento in utero materno. Questo consente di selezionare e trasferire solo gli embrioni sani, non affetti da fibrosi cistica, garantendo la nascita di un figlio sano, libero dalla malattia.
La DGP è particolarmente indicata in situazioni come quella descritta da un utente che ha scoperto di essere azoospermico e portatore di due mutazioni (D1152H e G1244E). In questo caso, poiché è stata ottenuta la presenza di spermatozoi tramite TESE, la DGP permetterebbe di escludere il rischio di trasmettere la malattia al figlio, qualora la partner fosse anch'essa portatrice o affetta. L'analisi genetica della coppia è un passo cruciale in questi scenari.
Quando si cerca un figlio e il test di gravidanza continua a non dare il risultato sperato, il primo passo da fare è sempre lo stesso: fermarsi, respirare e capire. Fare un test genetico per la fibrosi cistica è un gesto di amore e responsabilità. È una scelta che permette alla coppia di avere tutte le informazioni necessarie per affrontare consapevolmente il percorso verso la genitorialità.
L'Importanza della Consulenza Medica e Genetica
La fibrosi cistica è una malattia ereditaria che si trasmette di forma recessiva. La correlazione tra genotipo (le mutazioni specifiche presenti) e fenotipo (le manifestazioni cliniche) non è sempre così stretta da consentire giudizi prognostici definitivi sulla gravità della malattia o sull'insorgenza di specifici disturbi. Questo rende la consulenza genetica un pilastro fondamentale per le coppie che desiderano avere figli.
Il Dott. Massimiliano Pellicano, esperto nei casi di infertilità legata a condizioni sistemiche come la fibrosi cistica, e il Dr. José A., che si occupa di genetica, sottolineano l'importanza di questo percorso. Quando i malati di fibrosi cistica decidono di avere figli, devono richiedere al proprio medico o genetista una consulenza genetica. Lo specialista suggerirà di ampliare lo studio genetico a entrambi i membri della coppia per valutare il rischio riproduttivo.
Questa consulenza permette di comprendere appieno le implicazioni delle mutazioni CFTR sulla fertilità, di esplorare le opzioni disponibili per il concepimento (inclusa la PMA e la DGP) e di prendere decisioni informate per garantire la salute della futura prole.
Speranza e Prospettive Future
La fibrosi cistica è una malattia cronica e progressiva, ma i progressi nella ricerca e nella terapia stanno trasformando radicalmente la vita dei pazienti. Con un approccio proattivo alla salute riproduttiva, supportato da consulenza medica e genetica, e sfruttando le potenzialità delle tecniche di PMA e DGP, la possibilità di diventare genitori per le persone affette da fibrosi cistica è una realtà concreta e sempre più accessibile. L'obiettivo è sempre quello di garantire la nascita di bambini sani, liberi dalla malattia, e di permettere a tutte le famiglie di realizzare il proprio desiderio di genitorialità.
tags: #fibrosi #cistica #mutazione #eterozigote #fertilita