La "rivoluzione genetica" e, più recentemente, la "rivoluzione genomica" hanno trasformato radicalmente il campo della riproduzione umana, rendendo possibile un controllo scientifico e tecnologico su aspetti dell'esistenza che in passato erano impensabili. Questo progresso ha generato grandi aspettative riguardo alle potenzialità diagnostiche e terapeutiche, ma al contempo solleva complessi dilemmi morali per ricercatori, medici e pazienti. La diagnosi genetica preimpianto (DGP), oggi più correttamente denominata test genetico preimpianto (PGT), rappresenta una delle frontiere più dinamiche e influenti della Procreazione Medicalmente Assistita (PMA), offrendo la possibilità di identificare precocemente patologie ereditarie e anomalie cromosomiche negli embrioni prima del loro trasferimento in utero.
Il Contesto Scientifico: Geni, Varianti Genetiche e la Loro Rilevanza
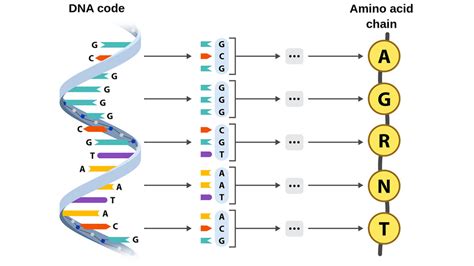
Ogni cellula umana racchiude un patrimonio genetico straordinariamente complesso, organizzato in 46 cromosomi, contenenti circa sei miliardi di paia di basi di DNA. La sequenza di queste basi è unica per ogni individuo, salvo minime discordanze tra gemelli monozigoti. Sebbene tutti gli esseri umani appartengano alla stessa specie, le differenze genetiche inter-individuali riguardano una piccola frazione di queste basi. Si stima che due persone non imparentate differiscano in media per lo 0,1% delle loro basi, equivalente a circa sei milioni di basi sull'intero genoma. Questa differenza, apparentemente minima, è cruciale per comprendere gli effetti biologici delle varianti genetiche. A titolo di paragone, la differenza di sequenza di basi tra noi e gli scimpanzé è di circa l'1%.
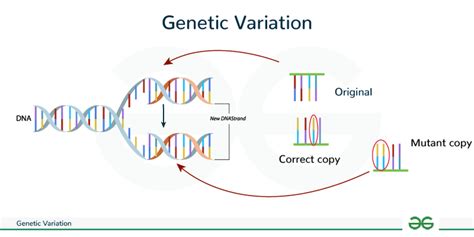
Le variazioni genetiche possono presentarsi come "single nucleotide polymorphisms" (SNPs), dove una base viene sostituita da un'altra, o come "INDEL", che coinvolgono l'aggiunta o la perdita di gruppi di basi contigue. In totale, le differenze genomiche tra due individui si attestano intorno allo 0,5%.
Storicamente, le varianti genetiche erano distinte in "polimorfismi" e "mutazioni", basandosi sulla loro frequenza nella popolazione e sugli effetti sul fenotipo. Le mutazioni erano considerate varianti rare (meno dell'1%) associate a fenotipi patologici, mentre i polimorfismi erano più comuni e privi di effetti patologici evidenti. Tuttavia, l'avanzamento delle tecniche di sequenziamento su larga scala ha dimostrato l'artificiosità di questa distinzione. Varianti coinvolte in patologie possono avere frequenze superiori all'1%, e varianti rare non sono sempre associate a malattie. Le linee guida più recenti suggeriscono quindi di utilizzare il termine "varianti genetiche", classificandole come "patogene", "probabilmente patogene", "a significato incerto", "probabilmente benigne" e "benigne", in base al loro effetto sul fenotipo.
Alcune varianti sono causa diretta di malattie mendeliane o monogeniche, come la fibrosi cistica, l'anemia falciforme o la distrofia muscolare di Duchenne. La maggior parte delle varianti genetiche, tuttavia, non ha un effetto immediato sul fenotipo. Esistono polimorfismi che conferiscono una maggiore suscettibilità a patologie non congenite (degenerative, tumorali, infettive), definiti "polimorfismi di suscettibilità", che aumentano il rischio di sviluppare una malattia rispetto alla media della popolazione. Allo stesso modo, esistono varianti genetiche "protettive" che riducono la probabilità di sviluppare una patologia o ne mitigano la gravità. È importante notare che la presenza di particolari varianti genetiche è anche associata a una diversa risposta individuale a molti trattamenti farmacologici.
Test Genetici: Applicazioni e Scopi Diversificati
I "test genetici" comprendono un'ampia varietà di metodologie per analizzare le sequenze geniche individuali, impiegate per scopi molto diversi. I principali campi di applicazione sono quello medico e quello forense, ma negli ultimi anni si è sviluppato anche l'uso personale per fini "social" o "ricreativi".
Applicazioni in Campo Medico
In medicina, l'analisi del DNA si effettua su persone con identità nota che hanno esplicitamente richiesto la procedura, con scopi diagnostici, pronostici o prescrittivi.
- Diagnosi Differenziale: Utile per identificare malattie genetiche mendeliane difficilmente riconoscibili con la sola analisi clinica.
- Classificazione dei Tumori: Permette una classificazione più accurata di tumori solidi o leucemie, con rilevanti implicazioni per le scelte terapeutiche.
- Test Pre-sintomatici: Mirano a identificare la presenza di varianti genetiche sicuramente patogene prima dell'insorgenza dei sintomi. Questi includono:
- Test Pre-natali: Rilevano varianti patogene prima della nascita.
- Test per lo status di portatore sano: Identificano mutazioni patogene recessive in individui clinicamente sani ma capaci di trasmettere la variante alla prole.
- Test Genetici Pre-impianto (PGT): Permettono di verificare che un embrione ottenuto tramite fecondazione in vitro non porti nel suo genoma una determinata mutazione patogena presente in almeno uno dei due genitori.
Un altro impiego medico dei test genetici, non necessariamente richiedente l'identità anagrafica degli individui, riguarda le indagini a scopo di ricerca. Queste analisi su ampi numeri di individui (anche migliaia) con specifiche caratteristiche (es. presenza o meno di una patologia) consentono di studiare il ruolo della variabilità genetica nelle malattie multifattoriali (diabete, asma, schizofrenia) e di ricercare i geni causativi in patologie mendeliane. Il rapido sviluppo delle tecnologie di analisi del DNA sta aumentando il numero di individui analizzati in questi studi, come dimostrato dal programma del sistema sanitario del Regno Unito, che ha analizzato il genoma di circa 85.000 individui.
The Future of Genetic Testing with Technology
Applicazioni Forensi
In campo forense, i test genetici sono impiegati per:
- Analisi di Paternità o Parentela: Su individui di identità nota.
- Identificazione di Identità Incerta: Come l'identificazione di vittime non riconoscibili (crimini, eventi catastrofici) o l'associazione di un sospettato a un campione biologico rinvenuto sulla scena del crimine.
Test Genetici per Uso Personale ("Social" o "Ricreativi")
Negli ultimi anni, test genetici offerti da compagnie private, come la 23andMe, permettono ai consumatori di analizzare il proprio background etnico ("da dove venivano i miei antenati?") e di scoprire parenti. Spesso, queste compagnie offrono anche analisi di tipo medico, come lo status di portatore per la fibrosi cistica o la presenza di mutazioni nei geni BRCA, con servizi "direct to consumers". Questo ha suscitato critiche da parte dei genetisti umani, poiché i risultati vengono inviati online senza consulenza genetica, delegando ai consumatori l'onere dell'interpretazione.
Il proliferare di queste società ha aperto a potenziali impieghi illeciti, come datori di lavoro o assicuratori che potrebbero effettuare analisi genetiche non autorizzate per verificare predisposizioni a patologie o il grado di rischio. Tali comportamenti sono spesso vietati per legge, come il Genetic Information Nondiscrimination Act (GINA) negli Stati Uniti, che dal 2010 proibisce alle compagnie assicurative di richiedere test genetici per le polizze sanitarie.
La Diagnosi Genetica Preimpianto (PGT): Una Panoramica Dettagliata
La diagnosi genetica preimpianto (PGT), precedentemente nota come PGD, è un insieme di tecniche che consentono di identificare la presenza di patologie genetiche o anomalie cromosomiche negli embrioni, o nei gameti, prima che vengano trasferiti nell'utero. Questa pratica è stata introdotta e regolamentata dalle Sentenze della Corte Costituzionale n. 96/2015 e n. 229/2015, che hanno superato i divieti iniziali della Legge n. 40 del 2004. Attualmente, l'accesso alle tecniche è consentito anche a coppie fertili portatrici di patologie genetiche trasmissibili, purché rispondano a criteri di gravità stabiliti dalla legge e siano riconosciute da strutture pubbliche. In questo contesto, entrambi i partner possono revocare il trasferimento dell'embrione in utero in qualsiasi momento se la diagnosi preimpianto ha rilevato una patologia embrionale.
La PGT si rivolge sia a coppie fertili che infertili portatrici o affette da determinate patologie genetiche. L'obiettivo è ottenere e trasferire in utero, tramite fecondazione in vitro, embrioni che non abbiano ereditato la patologia genetica.
Procedura della PGT
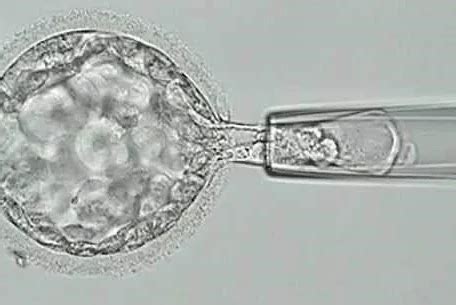
Una volta verificata la fattibilità della diagnosi molecolare, si procede con un ciclo di stimolazione ovarica, che dopo circa due settimane permette il prelievo degli ovociti. Questi ovociti vengono fecondati con spermatozoi in laboratorio, solitamente tramite la tecnica ICSI (iniezione intracitoplasmatica di spermatozoo), che prevede l'iniezione di un singolo spermatozoo direttamente nel citoplasma dell'ovocita. Gli embrioni così ottenuti vengono mantenuti in coltura per 5-7 giorni, fino allo stadio di blastocisti.
La blastocisti è composta da due parti principali: l'inner cell mass (da cui si formerà il feto) e il trofoblasto (da cui origineranno gli annessi embrionali, come la placenta e il sacco vitellino). La biopsia, un prelievo di materiale genetico assolutamente innocuo, interessa unicamente il trofoblasto, preservando la porzione che darà origine al feto. Dal materiale prelevato viene estratto e amplificato il DNA per verificarne la presenza di anomalie. L'analisi può essere effettuata anche sul fluido del blastocele, una tecnica meno invasiva sviluppata da S.I.S.Me.R., che non richiede il prelievo di cellule. L'accuratezza delle tecniche di analisi PGT è del 95-98%.
Tipi di PGT
Esistono tre principali tipologie di PGT, ciascuna con specifiche indicazioni:
1. PGT-M (Preimplantation Genetic Testing for Monogenic Disorders)
Questo test permette di individuare patologie ereditarie causate da una mutazione in un singolo gene. Vi si ricorre quando uno o entrambi i futuri genitori sono portatori o affetti da una patologia genetica potenzialmente trasmissibile alla prole. Fino al 2015, questa diagnosi era riservata solo a coppie infertili con patologie genetiche.
Per procedere con la PGT-M, è necessario uno studio preliminare del DNA degli aspiranti genitori e, in alcuni casi, di altri membri della famiglia, analizzando campioni biologici come sangue, saliva o liquido seminale. Questo studio rende più accurata la successiva diagnosi, che verifica la presenza della mutazione associata alla patologia.
2. PGT-A (Preimplantation Genetic Testing for Aneuploidies)
La PGT-A analizza l'assetto cromosomico degli embrioni per individuare anomalie nel numero di cromosomi, come la presenza di copie in più o in meno. Tali errori possono verificarsi quando si uniscono il patrimonio genetico materno e paterno. La Sindrome di Down, causata dalla presenza di tre copie del cromosoma 21, è l'anomalia cromosomica più nota.
A differenza della PGT-M e PGT-SR, la PGT-A è un test di screening e non richiede uno studio preliminare del DNA dei genitori. L'analisi verifica la presenza di anomalie cromosomiche. È particolarmente raccomandata per donne in età materna avanzata, poiché la probabilità di anomalie cromosomiche ovocitarie aumenta fisiologicamente con l'età. La PGT-A e le tecniche genomiche ad alta risoluzione hanno trasformato la selezione embrionale, consentendo una valutazione più precisa delle anomalie cromosomiche e del mosaicismo embrionale.
3. PGT-SR (Preimplantation Genetic Testing for Structural Rearrangements)
La PGT-SR è indicata quando uno o entrambi i futuri genitori sono portatori di una traslocazione cromosomica, ovvero alterazioni strutturali dei cromosomi. Come per la PGT-M, è necessario uno studio preliminare del DNA dei genitori e, a volte, di altri familiari, tramite l'analisi di campioni biologici, per rendere più accurata la diagnosi successiva. L'analisi verifica la presenza della traslocazione oggetto di studio.
Mosaicismo Embrionale
Un aspetto importante della PGT-A è la gestione del mosaicismo embrionale, cioè la contemporanea presenza in un embrione di cellule sane e malate. Negli ultimi dieci anni, si è scoperto che anche gli embrioni a mosaico possono dare origine a bambini sani. Questa è un'area di intensa ricerca scientifica e le linee guida sono in continua evoluzione, richiedendo un approccio appropriato e trasparente nella comunicazione con le coppie.
Vantaggi e Svantaggi della PGT
I vantaggi della PGT includono:
- Selezione embrionale accurata: Permette di selezionare embrioni geneticamente sani.
- Riduzione degli aborti spontanei: Scartando embrioni con alterazioni cromosomiche, il rischio di aborto diminuisce.
- Maggiore tasso di gravidanza: Aumenta le probabilità di successo delle tecniche di fecondazione in vitro.
- Tranquillità per i pazienti: Offre la sicurezza di trasferire embrioni vitali e sani.
Tuttavia, esistono anche degli svantaggi:
- Procedura invasiva: La biopsia embrionale, sebbene rara, può danneggiare l'embrione.
- Mosaicismo: L'interpretazione dei risultati può essere complessa a causa della presenza di cellule normali e alterate nell'embrione.
- Cancellazione del ciclo: Se tutti gli embrioni ottenuti presentano alterazioni genetiche, il ciclo di trattamento potrebbe essere annullato.

Il Dibattito Etico e le Implicazioni Sociali della Fecondazione Genetica Predittiva
La fecondazione genetica predittiva, con le sue promettenti capacità diagnostiche e selettive, ha innescato un acceso dibattito etico e sollevato profonde questioni sociali, trasformando l'idea di generare un figlio da un evento naturale a un "servizio premium". Questa "nascita programmata" si sta configurando come un processo sempre più orientato al branding e alla personalizzazione, introducendo un lessico che fonde pubblicità e biologia in modi inediti.
Nascita Programmata e Marketing
La commercializzazione di servizi come il "Nucleus Embryo" a New York, con slogan accattivanti come «Have Your Best Baby», evidenzia una crescente accettazione pubblica della genitorialità "ottimizzata". Il successo di tali campagne, con incrementi di vendita significativi, rivela una disponibilità a percepire la vita umana come un prodotto "aggiornabile".
Negli Stati Uniti, circa il 2% dei nuovi nati ogni anno è concepito tramite PMA, un numero che sposta la questione da una curiosità bioetica a un tema sistemico. Il mercato si allontana sempre più da una dimensione puramente clinica, adottando un linguaggio che promette non solo la nascita di un figlio, ma la sua "progettazione" e "selezione". Questo cambiamento culturale solleva interrogativi profondi per il diritto, la società e la scienza.
La Promessa Scientifica e la Narrazione Commerciale
Il pacchetto "Nucleus Embryo", al costo di circa 5.999 dollari, offre un'analisi genetica avanzata degli embrioni tramite polygenic risk score, stimando il rischio futuro di malattie, predisposizioni e tratti individuali. Questi strumenti statistici aggregano migliaia di varianti genetiche per fornire valori probabilistici. Tuttavia, l'eleganza matematica di questi punteggi può essere fuorviante. Studi autorevoli sottolineano la bassa affidabilità dei polygenic score nella scelta tra embrioni della stessa coppia, poiché le differenze genetiche sono minime e le previsioni statistiche spesso indistinguibili dal rumore di fondo.
Eppure, la narrazione promozionale trasforma queste lievissime oscillazioni in indicazioni quasi oggettive, suggerendo una concreta possibilità di "ottimizzare" il figlio futuro. Questo crea una distanza tra il dato probabilistico e la sua interpretazione pratica, che il marketing tende ad appiattire, come se l'incertezza fosse un problema di design grafico. Ciò che è venduto come un avanzamento oggettivo della medicina riproduttiva rischia di essere, più modestamente, una proiezione di desideri moderni sulla genetica predittiva, senza che la scienza possa garantire ciò che la comunicazione commerciale lascia intendere.

Il Nodo Etico della Disuguaglianza Genetica
Il primo e più immediato problema etico è quello della disuguaglianza. L'accesso alle tecniche di IVF e screening genetico, data l'elevato costo economico e simbolico, attribuisce a una parte della popolazione un "vantaggio riproduttivo" senza precedenti. Chi può sostenere tali spese si trova in una posizione privilegiata che trascende il potere d'acquisto, mentre chi non può permetterselo è escluso da questo nuovo modello di selezione prenatale.
Questo rischia di introdurre una stratificazione sociale inedita, fondata non solo su reddito, istruzione o capitale culturale, ma su "vantaggi genetici acquistabili". Il patrimonio genetico potrebbe diventare una dimensione economicamente modulabile e commerciabile. Il pericolo non è teorico: l'idea di "migliorare" statisticamente il proprio figlio crea una distanza crescente tra chi accede a questi strumenti e chi ne è escluso, con potenziali disparità sociali. Se predisposizioni, longevità o resistenze a patologie fossero percepite come risultato di scelte prenatali, la separazione tra "chi ha potuto scegliere" e "chi non ha potuto" assumerebbe un rilievo quasi antropologico. Rischiamo una società divisa non solo da condizioni materiali, ma da aspettative genetiche diverse, dove le opportunità biologiche riflettono direttamente il reddito familiare.
The Future of Genetic Testing with Technology
Il Paradigma Culturale: Tra Ottimizzazione e Selezione
Il secondo problema etico riguarda la cultura che si rischia di costruire attorno a questi servizi. La scelta dell'embrione non è un atto tecnico neutro, ma un gesto carico di aspettative, paure e proiezioni. Di fronte a un report genetico che indica un rischio maggiore di depressione o autismo, la reazione di privilegiare un embrione "più sicuro" è comprensibile. È in questa "zona grigia", tra emozioni legittime e informazioni parziali, che il confine tra prudenza riproduttiva e selezione implicita diventa sorprendentemente sottile.
Bioeticisti e associazioni di settore avvertono del rischio di derive eugenetiche commerciali. Le scelte potrebbero essere guidate non dalla scienza, che non offre certezze assolute, ma dal marketing, capace di trasformare una probabilità in una promessa e un'incertezza in un difetto da evitare. Questa "efficientamento" applicato alla vita, assimilando i futuri figli a prodotti da selezionare in base alle "specifiche" più rassicuranti, erode la riflessione sul valore intrinseco di ogni vita umana. Si rischia di sostituire tale valore con una narrazione in cui alcune esistenze sono più "accettabili" di altre, agganciandosi alla logica della performance: la vita merita se parte con le "giuste premesse" e non presenta "indicatori di rischio" vistosi.
Il pericolo è ridurre la complessità dell'essere umano a percentuali e grafici, delegando a un algoritmo e a chi lo commercializza la valutazione di ciò che è degno, desiderabile o compatibile con un ideale di normalità sempre più standardizzato. Senza una riflessione pubblica e consapevole, il passaggio dalla prevenzione alla selezione potrebbe diventare così graduale da passare inosservato, affermando le peggiori idee in modo "elegante".
Il Rischio Sistemico: Chi Decide Quale Vita Vale di Più?
Accettare slogan come «Have your best baby» significa delegare a soggetti privati - aziende, investitori, incubatori tecnologici - il potere di definire quali vite siano "preferibili", "ottimali" o più meritevoli di venire al mondo. Questo non è un trasferimento simbolico, ma effettivo, della capacità di orientare immaginari collettivi, criteri di desiderabilità e aspettative sulla "qualità" della prole. In altre parole, si permette al mercato di modellare l'idea stessa di normalità biologica.
Questa posizione è scivolosa perché sposta la discussione etica dal foro pubblico, dove potrebbe essere affrontata con consapevolezza e pluralismo, a un modello consumistico che appiattisce le complessità e segmenta la nascita in target e fasce di prezzo. La vita rischia di perdere il suo carattere intrinsecamente non negoziabile per assumere i contorni di un prodotto di fascia alta: differenziato, personalizzabile e potenziabile.
Il rischio non è solo teorico. Se la logica della scelta "migliore" si radica nel linguaggio e nelle abitudini, ciò che oggi appare provocatorio diventa banale. Si può facilmente scivolare dalla selezione per evitare patologie a un desiderio di intervenire su tratti "desiderabili" dalla cultura dominante. Si potrebbe immaginare un futuro in cui preferenze estetiche o inclinazioni cognitive siano offerte come opzioni aggiuntive, magari in pacchetti "premium plus". L'ironia, che la selezione del colore degli occhi o della predisposizione musicale del nascituro possa finire in abbonamento mensile, non è innocua. È attraverso questi piccoli paradossi che si intravede la deriva: una normalizzazione progressiva della scelta biologica guidata dal mercato, dove la distinzione tra desiderio, aspettativa sociale e pressione commerciale diventa sempre più sfumata. In questa sfumatura si annida la vera inquietudine, poiché quando la linea che separa l'innovazione dalla selezione si fa troppo sottile, è necessario interrogarsi apertamente su quale futuro stiamo consegnando all'umanità.
Uno Sguardo al Futuro
Il tema della fecondazione genetica predittiva non riguarda solo chi ricorre alla fecondazione assistita, ma l'intera società, poiché contribuisce a modellare il contesto culturale, giuridico e simbolico in cui le nuove generazioni nasceranno e si percepiranno. Le scelte odierne, apparentemente circoscritte alla biotecnologia riproduttiva, influenzano la maniera in cui la società definisce "normalità" e "possibilità". Come sempre quando il diritto incontra l'innovazione, la questione non è se cambierà qualcosa, ma come e a vantaggio di chi.
Le tecnologie genomiche avanzano a ritmo esponenziale, le promesse commerciali si moltiplicano, spesso in anticipo rispetto alle certezze scientifiche, e la sottile linea tra cura e potenziamento si assottiglia. Ciò che oggi è un supporto decisionale potrebbe diventare una prassi consolidata, un'aspettativa sociale o un criterio di responsabilità genitoriale. Il rischio è che la libertà di scelta si trasformi in un nuovo dovere implicito: scegliere "il meglio" per il proprio figlio, secondo parametri stabiliti dal mercato e non dalla comunità.
La sfida futura sarà costruire una cornice regolatoria e culturale che valorizzi l'innovazione senza trattare l'essere umano come un prodotto ottimizzabile, perfezionabile con algoritmi e statistiche. Non si tratta di frenare il progresso, ma di assicurarsi che esso non scavalchi gli spazi essenziali dell'etica, della dignità e del pluralismo sociale. Il diritto e la società devono affrontare queste questioni con consapevolezza e lungimiranza.
tags: #fecondazione #genetica #predittiva