La riproduzione è uno dei processi più fondamentali e affascinanti della vita, tradizionalmente legata all'incontro e alla fusione di due gameti altamente specializzati: lo spermatozoo maschile e l'ovulo femminile. Tuttavia, la scienza moderna sta esplorando frontiere che sfidano queste concezioni secolari, aprendo nuove prospettive sulla creazione e lo sviluppo embrionale. Sebbene la domanda se "due ovuli possano fecondarsi senza sperma" non trovi una risposta diretta nella biologia riproduttiva conosciuta, che prevede l'unione di un singolo ovulo con un singolo spermatozoo, o l'attivazione di un singolo ovulo per partenogenesi, le ricerche attuali stanno comunque delineando scenari in cui la necessità dello spermatozoo, o persino dell'ovulo stesso, potrebbe essere aggirata per avviare processi di sviluppo che mimano le primissime fasi della vita. Questo articolo esplorerà le recenti scoperte scientifiche che stanno ridefinendo la nostra comprensione della fecondazione e dello sviluppo embrionale, dalla creazione di strutture embrionali da cellule staminali alla partenogenesi, fino alle soluzioni innovative per superare l'infertilità maschile.
La Fecondazione Tradizionale e i Suoi Fondamenti Biologici
Per comprendere le innovazioni, è essenziale partire dal processo di fecondazione così come lo conosciamo. La fecondazione è l'unione di un ovulo e uno spermatozoo che dà origine a uno zigote, la prima cellula di un nuovo individuo. Nel contesto umano, questo processo è il culmine di complesse sequenze biologiche che coinvolgono sia il sistema riproduttivo maschile che quello femminile.
I gameti, ovvero gli ovuli e gli spermatozoi, si formano attraverso un processo chiamato gametogenesi. Nell'uomo, la spermatogenesi ha luogo nei testicoli, dove avviene costantemente la meiosi, un tipo di divisione cellulare che riduce il numero di cromosomi a metà. Questo processo porta alla formazione di cellule aploidi mature e competenti, gli spermatozoi, dotati della capacità di muoversi e raggiungere l'ovulo. La qualità seminale viene valutata sulla base della morfologia, della motilità e della concentrazione degli spermatozoi nel campione di sperma. Altri parametri, come il grado di frammentazione del DNA degli spermatozoi o il suo carico cromosomico, possono fornire indicazioni sulla qualità degli spermatozoi, strettamente correlata all'infertilità o alla probabilità di aborto spontaneo. È interessante notare come la qualità seminale possa variare nel tempo, poiché gli spermatozoi sono costantemente generati e il processo può essere influenzato da fattori esterni come processi febbrili, somministrazione di farmaci, stress, dieta, abitudini di vita (tabacco, alcol, ecc.). Lo studio del campione di sperma è quindi fondamentale nella valutazione del trattamento di fertilità da applicare in ogni caso.
Le donne, invece, nascono con un numero limitato di ovuli, la cui formazione, o ovogenesi, avviene nell'utero materno e termina con la formazione di cellule che si fermano a metà della meiosi. In questa fase, gli ovuli rimarranno quiescenti fino alla pubertà, momento in cui il loro numero inizierà a diminuire con ogni ciclo mestruale. La qualità e il numero di ovuli in ogni donna determineranno la sua fertilità. La qualità degli ovociti è infatti la chiave della fertilità femminile e determinerà il potenziale di sviluppo dell'embrione da ciascun ovulo. Gli errori nel processo di gametogenesi, che è estremamente complesso, possono portare a una formazione scorretta dei gameti, traducendosi in un basso tasso di fecondazione o in un fallimento totale della fecondazione.
Nel laboratorio di riproduzione assistita, la fecondazione avviene in vitro. Esistono due tecniche principali di fecondazione in vitro (FIVET): la FIV convenzionale o la microiniezione dello sperma (ICSI). In entrambi i casi, i gameti vengono preparati e capacitati in vitro, emulando i processi che avvengono in vivo e cercando di massimizzare le possibilità di una fecondazione corretta. Quando si verifica un fallimento della fecondazione in vitro, ossia nessuno degli ovuli viene fecondato correttamente, viene condotto uno studio esaustivo del caso per identificare la causa e proporre soluzioni ai pazienti. La bassa qualità degli ovuli o degli spermatozoi, o di entrambi, è spesso la ragione principale di questi fallimenti insoliti, poiché, come abbiamo visto, i processi che portano alla formazione dei gameti e degli zigoti sono molto complicati, e i fallimenti in essi o nella loro regolazione sono associati a un aumento della sterilità.
Sfidare i Limiti: Embrioidi da Cellule Staminali
Una delle scoperte più rivoluzionarie in questo campo riguarda la capacità di creare "embrioidi" o "modelli embrionali" a partire da cellule staminali, aggirando completamente la necessità sia di ovuli che di spermatozoi. Questo campo di studio è estremamente delicato e ha implicazioni profonde per la comprensione dello sviluppo umano e per la ricerca medica.
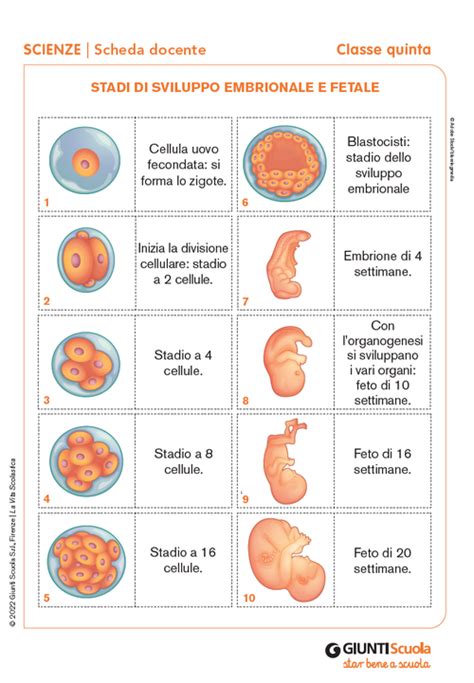
Già nel 2019, un team della Rockefeller University di New York aveva ottenuto dei "embrioidi", strutture complesse ricavate da cellule staminali embrionali. Queste cellule si sono organizzate dietro opportune stimolazioni, specializzandosi e replicando i primi stadi dello sviluppo umano. Fu, all'epoca, la prima volta, come testimoniato da uno studio pubblicato su Nature Cell Biology. Si trattava di modelli avanzati, ricavati senza l'impiego di ovuli e spermatozoi, che non sarebbero mai stati in grado di svilupparsi ulteriormente neanche se impiantati in utero. Un altro risultato significativo per questi "sosia" in laboratorio, sebbene gli specialisti non li etichetterebbero mai in questo modo, era stato ottenuto dall’università di Cambridge in seguito.
Ora, un ulteriore esito è arrivato dall'Istituto Scientifico Weizmann di Rehovot, in Israele, che aveva già condotto una simile sperimentazione sui topi. Sulla rivista Nature, il team ha infatti documentato di aver prodotto un embrioide umano che imita la struttura tridimensionale a circa 14 giorni di sviluppo. Questo risultato è stato ottenuto da cellule staminali embrionali non modificate dal punto di vista genetico ma solo con le giuste stimolazioni. Di solito, viene impiegata una proteina chiamata Bmp4 per guidare questo processo. Non c’è stata, insomma, nessuna manipolazione del DNA, ma solo la stimolazione delle cellule per indirizzarne lo sviluppo.
È inutile sottolineare l’importanza che avrebbe lo studio su questi modelli da staminali per approfondire patologie di vario tipo, dalle malformazioni congenite all’infertilità, e in generale rispetto ai meccanismi cellulari degli albori della vita. In particolare, questi modelli sono preziosi per studiare la gastrulazione, un processo chiave che termina appunto alla terza settimana di sviluppo embrionale, e per approfondire le ragioni degli aborti spontanei che avvengono con maggiore frequenza nelle prime settimane di gravidanza. La ricerca sugli embrioni è giuridicamente, eticamente e tecnicamente complessa.
La struttura ottenuta dagli scienziati israeliani ha portato al primo modello embrionale "completo" in grado di imitare tutte le strutture chiave che emergono in un embrione umano. Il materiale di partenza sono state cellule staminali riprogrammate per acquisire il potenziale di diventare qualsiasi tipo di tessuto nel corpo. Sono stati poi utilizzati prodotti chimici per indurre queste cellule staminali a diventare quattro tipi di cellule presenti nelle prime fasi dell'embrione umano: le cellule epiblastiche, che diventeranno l'embrione vero e proprio (o feto); le cellule del trofoblasto, che daranno origine alla placenta; le cellule dell'ipoblasto, che si trasformeranno nel sacco vitellino di supporto; e le cellule del mesoderma extraembrionale. Un totale di 120 di queste cellule sono state messe insieme e gli scienziati hanno poi osservato ciò che succedeva. Jacob Hanna del Weizmann Institute of Science ha commentato: "Do un grande merito alle cellule: devi portare la giusta miscela e avere l'ambiente giusto e tutto decolla. È un fenomeno sorprendente." I modelli embrionali sono stati lasciati crescere e svilupparsi fino a quando non sono diventati paragonabili a un embrione di 14 giorni dopo la fecondazione.
La speranza è che i modelli embrionali possano aiutare gli scienziati a spiegare come emergono i diversi tipi di cellule, a testimoniare i primi passi nella costruzione degli organi del corpo o a comprendere le malattie ereditarie o genetiche. Si parla addirittura di migliorare i tassi di successo della fecondazione in vitro, favorendo la comprensione di alcuni fallimenti.
Manuela Monti, professoressa associata di embriologia all’Università di Pavia, ha dichiarato al Corriere della Sera: "Si tratta di ricerche molto interessanti e utili, però è assolutamente necessario evitare sensazionalismi e ribadire che in questi casi non c’è proprio nessun embrione e anche la parola 'sosia' che circola in merito è sbagliata." Ha chiarito che si tratta invece di ricerche su cellule staminali, che permettono di comprenderne sempre meglio i processi di differenziazione grazie ai quali andranno a formare le linee cellulari specializzate e, alla fine, un individuo. Non sono stati utilizzati né spermatozoi, né ovuli e né utero. Nonostante ciò, il nuovo modello di embrione sviluppato dal gruppo di ricercatori del Weizmann Institute è quasi identico a un embrione umano vero di 14 giorni, in grado addirittura di rilasciare ormoni da far risultare positivo un test di gravidanza in laboratorio.
Le prime settimane dopo che uno spermatozoo feconda un ovulo mettono in moto una serie di straordinari cambiamenti: da un insieme di cellule indistinte a qualcosa che alla fine diventa riconoscibile, un bambino, tramite ecografia. È in questi primi momenti cruciali che avvengono con maggior frequenza aborti spontanei e si sviluppano difetti congeniti. Ma è ancora una fase di sviluppo poco compresa. Jacob Hanna ha spiegato: "È una scatola nera e non è un cliché: la nostra conoscenza è molto limitata."
Il lavoro tuttavia solleva anche la questione se lo sviluppo dell'embrione possa essere imitato oltre la fase di 14 giorni. Questo non sarebbe illegale, nemmeno nel Regno Unito, poiché i modelli embrionali sono giuridicamente distinti dagli embrioni. Tuttavia, esistono delle linee guida internazionali molto severe che impediscono di tenere in laboratorio ed effettuare esperimenti su embrioni umani oltre i 14 giorni di sviluppo. Gli embrioidi rispondono proprio all’esigenza di approfondire quelle fasi del processo mimandole dentro strutture che non potrebbero in alcun modo dare origine a una vita, ma che sono pur sempre di origine biologica e non artificiale. Questo fronte, pur abbattendo, non elude le questioni etiche di fondo. Per esempio, occorrerà normare come e per quanto tempo si dovrebbe consentire agli embrioidi di svilupparsi in laboratorio e quali potrebbero essere i livelli di sviluppo a cui arrivare. Insomma, questi modelli che stadio di complessità potrebbero toccare? E cosa farne, dopo?
Le cellule staminali raccontate da Luciano Conti: embrioni.
La Partenogenesi: Il Mito della "Nascita Vergine" nella Scienza
Un'altra via per ottenere uno sviluppo embrionale senza l'intervento diretto di uno spermatozoo è la partenogenesi. Fino a qualche anno fa, l'ipotesi è che la partenogenesi avrebbe potuto riguardare anche la specie umana e che le donne avrebbero potuto fare a meno degli uomini per riprodursi. La partenogenesi, che in greco significa "nascita vergine", avviene in maniera del tutto naturale nelle piante e in alcuni animali, quali le api, le formiche e persino alcune lucertole.
Negli umani, analogamente ad altri mammiferi, la partenogenesi non avviene naturalmente a causa di un processo di regolazione genica chiamato imprinting. L'imprinting richiede il contributo sia dei geni materni che di quelli paterni affinché l'embrione raggiunga il pieno sviluppo. I geni marcati (o imprinted) sono geni la cui espressione è determinata dal genitore che li ha trasmessi; questi geni violano la comune regola ereditaria secondo cui vengono espressi in egual misura i corredi genetici di entrambi i genitori. Dall'ultimo computo è emerso che nei mammiferi un esiguo numero di geni, circa 80, è soggetto a imprinting. La maggior parte dei geni marcati viene repressa e, di conseguenza, o si esprime unicamente il gene materno perché quello paterno è "imprinted" o viceversa. Il processo inizia durante la formazione dei gameti quando, nei maschi, alcuni geni ricevono l'imprinting nello sperma che si sviluppa e, nelle femmine, altri lo ricevono nell'ovulo che si sviluppa. Tutte le cellule dell'embrione che ne deriverà avranno lo stesso corredo di geni imprinted sia da parte del padre che della madre, tranne per quelle cellule ("germoplasma") che sono destinate a continuare a produrre gameti (ovuli o cellule spermatiche), in cui vengono cancellati tutti gli imprint - sia materni che paterni. L'imprinting è un processo molto importante: l'eredità intenzionale (sperimentale nei topi) o casuale (negli umani) di due copie di un particolare cromosoma da un genitore e di nessuna dall'altro è solitamente fatale; l'eredità di due copie di uno dei geni materni e di nessuna copia di quelli paterni (o viceversa) può altresì provocare gravi difetti di sviluppo. Inoltre, una mancanza di imprinting nelle cellule somatiche può causare il cancro.
Nonostante questi ostacoli naturali, gli scienziati hanno indotto artificialmente i partenoti in mammiferi come topi e scimmie, benché molto spesso ne sia scaturito uno sviluppo anomalo. Un esempio significativo di questa ricerca è venuto da Paul de Sousa dell'Università di Edimburgo, il quale ha annunciato al BA Science Festival di Dublino che il suo gruppo era riuscito a creare "embrioni vergini", o partenoti, stimolando un ovulo umano a iniziare a dividersi come un embrione senza l'aggiunta di alcun materiale genetico da parte di una cellula spermatica maschile. Il gruppo di Edimburgo, che svolge la propria attività presso il Roslin Institute (dove era stata clonata la pecora Dolly), ha utilizzato circa 300 ovuli umani di donatrici volontarie per creare una mezza dozzina di blastocisti partenoti, embrioni umani costituiti da circa 50 cellule, che possono essere impiegati come fonti di cellule staminali. Nella riproduzione normale, gli ovuli espellerebbero metà del loro materiale genetico per prepararsi a ricevere il complemento maschile rilasciato da una cellula spermatica. Per creare i partenoti, gli ovuli sono stati coltivati in laboratorio in modo tale che mantenessero tutti i loro cromosomi; è stato possibile portarne a maturazione e indurne la divisione tramite elettroshock di circa la metà. Tuttavia, solo cinque su cento sono riusciti a raggiungere lo stadio di blastocisti, presentando quindi solo la metà del normale numero di cellule. Respingendo le obiezioni sull'efficacia del processo, il dottor De Sousa ha dichiarato: "È un gioco numerico. Si tratta solo di fornire il tessuto che dovrà essere impiegato nella sperimentazione."
La partenogenesi offre anche la possibilità di coltivare cellule di donne affette da gravi malattie genetiche, consentendo di effettuare uno studio particolareggiato sugli effetti cellulari di queste malattie e, in teoria, le cellule staminali ottenute tramite questo metodo potrebbero essere utilizzate per coltivare tessuti di sostituzione per donne che hanno sviluppato determinate patologie. All'incontro della British Association, il dottor De Sousa ha dichiarato: "Per ora non siamo riusciti a ottenere cellule staminali da tali embrioni, ma questa continua a essere la nostra ambizione."
In un altro esperimento, pubblicato sulla rivista Nature Communication, gli spermatozoi non hanno fecondato la cellula uovo ma bozze di embrioni. In questo esperimento, il nucleo degli spermatozoi è stato trasferito nei partenoti. Questi ultimi, che possono essere utilizzati anche per produrre cellule staminali, contengono solo una serie di cromosomi, anziché le due serie che nascono dalla fusione dello spermatozoo e della cellula uovo. Redi ha definito questo "un buon lavoro" e un avanzamento della tecnica per riprodurre in laboratorio le prime fasi dello sviluppo embrionale. Inoltre, ha aggiunto, "è una dimostrazione che la riprogrammazione genetica può essere fatta anche impiegando cellule delle prime fasi embrionali." Commentando il risultato, Paul Colville-Nash, del britannico Medical Research Council (MRC), ha rilevato che "potrebbe aiutare a comprendere meglio come comincia la vita umana e i meccanismi che controllano la vitalità degli embrioni." Più a lungo termine, invece, "potrebbe avere implicazioni per mettere a punto nuove cure per l'infertilità."
Alcuni scienziati ritenevano che, impiegando i partenoti nella ricerca, si sarebbero potute evitare le obiezioni dei gruppi pro-vita; il dottor De Sousa non condivide questo parere, confermato dalle dichiarazioni di sgomento che tali gruppi hanno rilasciato alla stampa, e ha affermato che "chi ha un atteggiamento a favore della vita considererà opinabile qualsiasi utilizzo di ovuli ed embrioni a fini non riproduttivi." Il dottor De Sousa ha anche ribadito che non vi è alcuna intenzione di impiantare gli embrioni per dare origine a una gravidanza, eventualità che, peraltro, è vietata dalle clausole della licenza di ricerca che è stata concessa al suo gruppo.
Altri hanno espresso dubbi di carattere tecnico, affermando che il livello di manipolazione genetica necessario per realizzare la partenogenesi rende inutilmente complicata questa strada per le cellule staminali di embrione, tanto che persino la clonazione di embrioni umani sembrerebbe costituire un approccio più diretto. Il dottor De Sousa, tuttavia, ritiene che nelle fasi iniziali della ricerca sulle cellule staminali gli scienziati debbano lasciare aperte varie possibilità. "Vogliamo queste linee cellulari essenzialmente a scopi di ricerca", ha dichiarato.
Quando lo Sperma è Presente ma Non Funzionante: Soluzioni Innovative
Oltre a esplorare la riproduzione completamente senza sperma o ovuli, la scienza ha fatto passi da gigante anche nel superare le sfide legate a spermatozoi problematici, permettendo la fecondazione in situazioni che altrimenti la renderebbero impossibile. Questo non risponde direttamente alla domanda sulla fecondazione senza sperma, ma piuttosto al modo in cui la presenza di sperma, anche se immaturo o disfunzionale, può essere valorizzata per ottenere una gravidanza.
In alcuni casi, la formazione di spermatozoi nei testicoli (spermatogenesi) è bloccata in diversi stadi di sviluppo. Le cellule nell'ultima fase di sviluppo, prima di formare uno spermatozoo maturo, sono chiamate spermatidi. Inizialmente, gli spermatidi sono cellule rotonde, con una morfologia completamente diversa dagli spermatozoi tradizionali. Tuttavia, gli spermatidi rotondi contengono il materiale genetico aploide (ridotto alla metà per completare il materiale genetico dell'ovocita durante la fecondazione). Gli spermatidi rotondi non hanno flagello e non possono muoversi di conseguenza. Possono fecondare gli ovociti, purché posti al loro interno mediante una microiniezione nelle ovocita. In ogni caso, ci sono molti altri problemi da risolvere, legati all'immaturità degli spermatozoi, poiché sono diversi i componenti chiave del nucleo spermatide e del citoplasma.
Nel 1994, il Dr. Jan Tesarik insieme alla Dr. Carmen Mendoza ha realizzato un protocollo che ha portato alla nascita dei primi bambini (in tutto il mondo) attraverso la microiniezione di spermatidi rotondi in ovociti umani. Questo risultato è stato pubblicato nel 1995, dopo la nascita dei due bambini sani, sulla rivista medica The New England Journal of Medicine.
Gli spermatociti primari sono cellule ancora più immature degli spermatidi, poiché non hanno ancora dimezzato il loro materiale genetico. Pertanto, non possono fecondare con successo un ovocita se vengono iniettati in esso. Per superare questo problema, il Dr. Jan Tesarik e la Dr. Carmen Mendoza hanno sviluppato un metodo di coltura cellulare con il quale hanno raggiunto l'evoluzione degli spermatociti primari alla fase di spermatide rotondo. Usando questo metodo, hanno ottenuto la nascita dei primi bambini in caso di blocco della spermatogenesi nella fase degli spermatociti primari. Lo studio è stato pubblicato, nel 1999, sulla rivista medica The Lancet. Questi progressi dimostrano la capacità della scienza di intervenire in stadi molto precoci della gametogenesi maschile per superare ostacoli all'infertilità.
Scenari Futuri e Nuove Frontiere della Riproduzione
Le potenzialità della ricerca nel campo della riproduzione sono molteplici e per ora puramente speculative, ma indicano una direzione chiara verso una maggiore flessibilità nei processi di creazione della vita.
Un'area di ricerca particolarmente audace è la possibilità di ottenere embrioni da cellule non sessuali. Chiariamolo subito: è uno scenario improbabile nel breve termine, ma forse non impossibile in futuro. In futuro, le cellule uovo potrebbero non essere le uniche in grado di generare la vita in unione con gli spermatozoi. Ricercatori dell'Università di Bath, Inghilterra, sono riusciti a ottenere una cucciolata di topi sani con una tecnica che aggira le canoniche fasi del concepimento. Sono partiti da ovuli di topo non fertilizzati che hanno trasformato in pseudo-embrioni con l'aiuto di un mix di sostanze chimiche. Questi falsi embrioni hanno iniziato a svilupparsi come se fossero stati fertilizzati, ma dividendosi per partenogenesi, con una gestione del DNA analoga a quella di cellule non sessuali, come quelle della pelle. Se l'inserimento di spermatozoi negli pseudo-embrioni avesse dato origine ad embrioni sani, lo stesso risultato si sarebbe potuto ipoteticamente ottenere anche usando cellule diverse dai gameti femminili, come quelle della pelle. Tecnicamente possibile. Questa era l'ipotesi che, almeno per metà, è risultata esatta: iniettando spermatozoi nei finti embrioni, si sono ottenuti embrioni a tutti gli effetti, che trasferiti in una femmina di topo hanno dato vita, in un caso su quattro, a una cucciolata di topi sani. Questa "piccola rivoluzione", come definita dagli stessi ricercatori, è per ora indirizzata solamente a capire gli esatti meccanismi di fusione degli spermatozoi con la cellula uovo, ma dimostra che la normale fertilizzazione non è l'unico modo in cui i gameti maschili possono arrivare a produrre i tessuti necessari a un organismo vivente.
Questi scenari teorici aprono la porta a possibilità come la creazione di embrioni sani usando spermatozoi e cellule comuni - non necessariamente ovuli, una possibilità che potrebbe essere estremamente rilevante per le coppie infertili o per quelle omosessuali che desiderano una genitorialità biologica.
In un contesto più consolidato, ma comunque innovativo, si inserisce il metodo ROPA (Ricezione di Ovuli della Partner), una variante della fecondazione in vitro (FIV) specifica per le coppie lesbiche. In questo approccio, una delle due donne si sottopone a stimolazione ovarica per estrarre gli ovuli e fecondarli con sperma di donatore, mentre l’altra riceve l’embrione nel proprio utero e porta a termine la gravidanza. Un esempio è quello di Paula e la sua compagna: "Paula e io ci siamo incontrate cinque anni fa ed entrambe avevamo già ben presente il discorso della maternità, però abbiamo iniziato a pensarci seriamente da un anno, dopo che ho compiuto 38 anni. Lei è più giovane e pensavamo che fosse la più indicata per portare avanti la gravidanza, però quando ci hanno spiegato che con il metodo ROPA avremmo potuto partecipare entrambe ci è sembrato meraviglioso e abbiamo deciso che lei avrebbe donato gli ovuli e io avrei portato avanti la gravidanza." Hanno scelto un centro che ispirasse fiducia e avesse esperienza, Dexeus Mujer, trovando un approccio familiare e un costante supporto. "Ora sono incinta di quasi 22 settimane e la gente che ci vede ci chiede 'siete incinte?' e 'dite che siete entrambe madri biologiche, ma come funziona?' Il nome del metodo non è molto conosciuto, però quando spieghi in cosa consiste tutti lo capiscono." L'unico handicap per loro è che, per motivi legali, in alcuni contesti si può scegliere solo se si è sposati.
Questi sviluppi, dal laboratorio al clinico, mostrano un panorama in continua evoluzione, dove la comprensione e la manipolazione dei processi biologici aprono nuove strade alla riproduzione e alla comprensione della vita stessa. Sebbene il concetto di "due ovuli che si fecondano senza sperma" rimanga al di fuori della nostra attuale comprensione biologica diretta, le ricerche sulla partenogenesi, sulla creazione di embrioidi e sulle tecniche avanzate di fecondazione assistita stanno spingendo i confini di ciò che è possibile nella riproduzione, offrendo speranza e nuove prospettive a molti.