La tecnologia CRISPR/Cas9 rappresenta un approccio rivoluzionario nell'ingegneria genetica, consentendo di apportare modifiche mirate e precise al DNA delle cellule. Nata dalla scoperta del semplice ma efficace sistema immunitario dei batteri, questa tecnica ha rapidamente catturato l'attenzione della comunità scientifica per la sua versatilità e le sue innumerevoli applicazioni. Tuttavia, la sua estensione agli embrioni umani solleva interrogativi profondi e complessi, che spaziano dalle potenziali cure per malattie ereditarie alle preoccupanti prospettive di manipolazioni genetiche con implicazioni etiche e sociali di vasta portata. L'editing del genoma, in particolare sugli embrioni, promette di riscrivere il futuro della medicina, ma impone anche una riflessione urgente sui limiti e le responsabilità della scienza.
CRISPR/Cas9: Una Rivoluzione nell'Ingegneria Genetica
Il sistema CRISPR/Cas9, pronunciato "crisper-cas-nain" in inglese o talvolta "crisper" in italiano, è un approccio che consente di ingegnerizzare il genoma di una cellula con una precisione prima inimmaginabile. In sintesi, permette di modificare, rimuovere o aggiungere una specifica sequenza di DNA, agendo come una sorta di "forbice molecolare" capace di tagliare il DNA in corrispondenza di un punto scelto. Questo processo di "taglia e cuci" è conosciuto come "gene editing" o "genome editing", ovvero correzione del gene o del genoma. Rispetto ad altre tecniche di editing disponibili, CRISPR/Cas9 si distingue per la sua facilità d'uso, rapidità ed economicità, fattori che hanno contribuito al grande interesse da parte dei laboratori di ricerca a livello globale.
La scoperta di questo sistema affonda le sue radici nell'osservazione di un meccanismo di difesa naturale dei batteri. Già nel 1987, il ricercatore Yoshizumi Ishino dell'Università di Osaka clonò accidentalmente una porzione di quello che sarebbe stato chiamato CRISPR, insieme al gene iap. Nel 1993, gruppi di ricerca nei Paesi Bassi e in Spagna, guidati dal microbiologo Francisco Mojica, approfondirono lo studio di queste sequenze ripetute di DNA, denominate "clustered regularly interspaced short palindromic repeats" (CRISPR), presenti nel genoma di batteri e archei. Mojica ipotizzò un ruolo di questi cluster, che contengono frammenti di DNA estraneo derivati da virus che avevano precedentemente infettato la cellula, nell'immunità adattativa dei procarioti. Questi frammenti, detti "spaziatori", consentono al batterio di conservare memoria dell'incontro con virus patogeni.
Il ruolo cruciale del sistema CRISPR/Cas nell'immunità acquisita dei procarioti è stato pienamente compreso solo nel 2007. Da allora, e in particolare dal 2012, quando i gruppi di ricerca di Jennifer Doudna e Emmanuelle Charpentier riuscirono a ri-ingegnerizzare in provetta questo meccanismo biologico, trasformandolo in uno strumento molecolare personalizzabile, la biotecnologia ha assistito a una vera e propria rivoluzione. La scoperta di questo sistema, e la sua trasformazione in uno strumento così potente, è valsa alle due scienziate il Premio Nobel per la Chimica nel 2020. Le nucleasi con dominio a dita di zinco e le TALENs, tecniche preesistenti di editing del genoma, richiedevano la creazione di una proteina personalizzata per ogni sequenza di DNA da tagliare, rendendole più dispendiose in termini di tempo e risorse economiche. Il sistema CRISPR-Cas9, invece, utilizza RNA guida molto più semplici ed economici da creare.
Il Meccanismo d'Azione delle 'Forbici Molecolari'
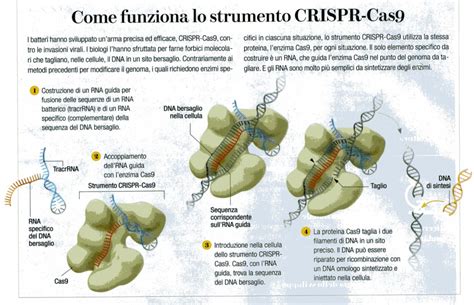
Il funzionamento del sistema CRISPR/Cas9 si basa sull'azione congiunta di una molecola di RNA guida e della nucleasi Cas9. In natura, quando un batterio incontra del DNA estraneo, per esempio di un virus, integra un frammento di tale DNA nel proprio genoma, in corrispondenza di una regione detta locus CRISPR. Successivamente, in caso di una nuova infezione, il batterio reagisce trascrivendo un mRNA (CRISPR RNA, crRNA), che contiene queste sequenze, e un altro mRNA chiamato tracrRNA (trans-activating crRNA). Queste due molecole si legano al DNA virale in corrispondenza della sequenza bersaglio, consentendo l'ancoraggio di Cas9 (CRISPR-associated protein 9), un enzima con attività nucleasica. Questo enzima è in grado di tagliare gli acidi nucleici che compongono il materiale genetico, disattivando così il virus.
Nel contesto dell'ingegneria genetica, un ricercatore progetta e sintetizza una singola molecola di RNA, l'RNA guida, che combina le funzioni del crRNA e del tracrRNA naturali. Questa molecola di RNA guida contiene una sequenza complementare a quella del DNA che si desidera correggere o modificare. Quando l'RNA guida e l'enzima Cas9 vengono introdotti in una cellula, interagiscono con la sequenza "bersaglio" nel genoma. L'enzima Cas9 viene inizialmente attivato mediante il legame a un RNA guida e poi mediante il legame alla sequenza genomica corrispondente che precede immediatamente una sequenza PAM (Protospacer Adjacent Motif) trinucleotidica. È proprio in corrispondenza di questa sequenza PAM che avviene il legame iniziale della nucleasi, dove si verifica il taglio a monte.
Crispr-cas 9 le forbici del DNA
Una volta creata una rottura a doppio filamento (Double-Strand Breaks, DSBs) in questa regione specifica del genoma della cellula ospite, la cellula attiva uno dei due meccanismi di riparazione del DNA: la giunzione terminale non omologa (Nonhomologous End Joining, NHEJ) o la ricombinazione omologa (Homology-Directed Recombination, HDR). Il meccanismo NHEJ è per sua natura impreciso e può introdurre "errori" nella sequenza, portando a volte alla non funzionalità del gene modificato. Questa modalità può essere sfruttata per eliminare l'espressione di un gene di cui si vuole studiare la funzione (generando un "gene knock-out"). Al contrario, il meccanismo di riparazione HDR agisce con precisione, permettendo di riparare il taglio e, crucialmente, di inserire sequenze desiderate fornite dal ricercatore. Grazie a questa strategia, è possibile non solo studiare l'effetto dell'introduzione di determinate mutazioni, ma anche correggere le mutazioni che causano malattie genetiche.
Mentre le altre tecniche di gene editing disponibili usano proteine per colpire il DNA, il metodo CRISPR/Cas9 utilizza l'RNA, che è per certi aspetti più semplice da usare, più economico e più facile da introdurre nelle cellule. Questo rappresenta un grande vantaggio. Inoltre, è possibile colpire più sequenze contemporaneamente e quindi effettuare più correzioni alla volta, accelerando enormemente i progressi nella ricerca biologica.
Vantaggi e Applicazioni Attuali del Sistema CRISPR/Cas9
Le possibili applicazioni del sistema CRISPR/Cas9 sono molteplici e toccano diversi settori. Già ampiamente utilizzato nella ricerca di base, questo strumento ha aperto nuove frontiere nello studio della funzione dei geni e delle malattie. Può essere impiegato, per esempio, per generare animali geneticamente modificati, come quelli con geni knock-out, fondamentali per comprendere il ruolo di specifici geni nell'organismo. Consente anche di creare popolazioni di cellule, ognuna con un solo gene mutato, permettendo di studiare il comportamento delle cellule in risposta a un farmaco e stabilire connessioni tra uno o più geni e una certa risposta biologica. Il sistema è già stato utilizzato con successo per risolvere controversie scientifiche di lunga data e comprendere il ruolo di molti geni a funzione sconosciuta.

Recentemente, alcune applicazioni del CRISPR/Cas9 sono state approvate in alcuni Paesi per uso clinico, in particolare per correggere mutazioni genetiche all'origine della β-talassemia, una malattia ereditaria. È allo studio per correggere altre mutazioni genetiche responsabili di diverse malattie ereditarie e tumori. Le maggiori probabilità di successo sono attese per la cura di malattie del sistema immunitario, poiché le cellule immunitarie possono essere isolate, modificate in vitro e reintrodotte nel paziente una volta "corrette". Questa strategia ha già permesso di generare in vitro linfociti T resistenti all'HIV. Inoltre, in un'applicazione più inaspettata, il sistema CRISPR/Cas9 è stato sperimentato per rilevare la presenza del coronavirus (che causa il COVID-19) nei tamponi naso-faringei.
In ambito vegetale, il sistema CRISPR/Cas mostra sorprendenti potenzialità. Non solo si rivela uno strumento importante per la ricerca di base, ma permette anche di generare piante con migliori caratteristiche nutrizionali o resistenti a patogeni. Un esempio è una recente varietà di pomodoro resistente all'oidio, in corso di perfezionamento in laboratorio. Sebbene risultati simili possano essere ottenuti con incroci tradizionali, il sistema CRISPR/Cas è molto più specifico e permette di ottenere i risultati in pochi mesi anziché anni. Un altro vantaggio significativo rispetto alle tecniche di biologia molecolare utilizzate finora è che non necessita dell'introduzione di porzioni di DNA proveniente da altre specie, come geni per resistenze ad antibiotici o erbicidi, evitando così il dibattito sui "transgenici".
L'Editing del Genoma negli Embrioni Umani: Potenzialità e Dibattito
L'applicazione più allettante del CRISPR/Cas9, ma anche la più delicata e controversa, è la sua potenziale utilizzazione per correggere sequenze mutate responsabili di malattie genetiche e tumori direttamente negli embrioni umani. L'idea è di inserire una mutazione correttiva in una fase precoce dello sviluppo embrionale, affinché essa sia presente in tutte le cellule dell'organismo, comprese quelle della linea germinale (ovuli e spermatozoi). In questo scenario, la manipolazione avrebbe un effetto non solo nell'individuo in cui è effettuata, ma anche nella sua discendenza, permettendo l'eliminazione "definitiva" - per tutta la discendenza - di malattie ereditarie.
In teoria, l'editing embrionale potrebbe servire per liberarsi di patologie ereditarie gravi come la fibrosi cistica, il morbo di Huntington o alcune forme di anemia. Potrebbe anche essere usato per introdurre geni che conferiscono protezione da malattie comuni come l'infarto o il morbo di Alzheimer. Tuttavia, questa prospettiva apre anche l'inquietante possibilità di agire sugli embrioni per creare "bambini con le caratteristiche volute", sollevando il grosso dilemma dell'eugenetica.
Mentre l'applicazione di CRISPR alle cellule somatiche (quelle non riproduttive) permette di modificare solo tessuti specifici del paziente, eliminando la componente ereditaria e riducendo i rischi legati alla trasmissione della mutazione alle generazioni future, l'intervento sulla linea germinale introduce cambiamenti ereditabili. Un gruppo di ricercatori, ritenendo plausibile che i primi tentativi e risultati in questo campo fossero imminenti, ha pubblicato un commento sulla rivista Nature chiedendo una moratoria su questo genere di ricerca, sostenendo che tali interventi sono prematuri e potenzialmente pericolosi.
Primi Esperimenti su Embrioni Umani e Sfide Tecniche
Nonostante le preoccupazioni etiche, gli esperimenti con CRISPR su embrioni umani sono stati condotti. I primi risalgono a cinque anni fa, ma i passi avanti sono stati numerosi. Tuttavia, la ricerca sottolinea quanto poco si sappia di come l'embrione umano si difenda dai danni al DNA causati dal sistema di editing genomico.
Un caso molto controverso è stato uno studio cinese apparso nell'aprile 2015 sulla rivista Protein&Cell, condotto dal Prof. Junjiu Huang e dal suo team. Hanno provato a utilizzare la tecnica per correggere la mutazione genica della beta-talassemia in embrioni umani non vitali, ovvero destinati alla ricerca e non in grado di svilupparsi. Le conclusioni furono positive, in quanto alcuni degli embrioni sottoposti a taglio CRISPR/Cas e ricombinazione omologa avevano sostituito il gene corretto a quello mutato ed erano quindi "guariti". Tuttavia, i numeri erano impietosi: solo 28 embrioni su 54 avevano subito il taglio di Cas e solo in quattro embrioni alcune cellule avevano effettuato la ricombinazione omologa riparatrice. Si era anche osservato un alto numero di mutazioni indesiderate, potenzialmente pericolose, le cosiddette mutazioni "off-target", lontane dal sito di azione del meccanismo di editing.

Successivamente, un altro gruppo di ricercatori cinesi ha fatto un passo in avanti utilizzando la tecnica di editing genetico CRISPR-Cas9 per correggere una mutazione dannosa nelle cellule di tre embrioni umani. In questo studio, i ricercatori hanno usato cellule uovo normali, sebbene immature (solitamente scartate dalle cliniche di fecondazione in vitro), che hanno poi fecondato con lo sperma di due donatori portatori di mutazioni genetiche: una mutazione G1376T nel gene per l'enzima G6PD, che provoca una forma di favismo, e una mutazione beta41-42, causa della beta-talassemia. Nel caso del primo donatore, l'intervento con CRISPR ha permesso di ottenere due embrioni in cui la mutazione G1376T è stata corretta, ma nel terzo l'operazione è riuscita solo in alcune delle cellule, ottenendo così un "embrione a mosaico". Dei quattro embrioni ottenuti nel secondo caso, solo in uno la rimozione della mutazione è riuscita in tutte le cellule, due sono diventati embrioni a mosaico e nell'ultimo l'operazione è fallita. Questo fenomeno di "mosaicismo", dove la correzione riesce solo in una parte delle cellule, evidenzia la necessità di molta più ricerca per rendere l'utilizzo della CRISPR più sicuro. Una possibile soluzione per evitarlo potrebbe essere modificare il genoma negli spermatozoi e nelle cellule uovo prima di eseguire la fecondazione in vitro, anziché intervenire direttamente sull'embrione.
Studi più recenti hanno continuato a evidenziare i rischi e le sfide. La scienza non è fatta di dati inconfutabili: man mano che la ricerca prosegue le informazioni cambiano, le tecniche migliorano e le scoperte fanno evolvere il sapere. Sebbene il rischio più discusso sia da tempo quello delle mutazioni "off target", studi recenti hanno posto l'accento anche sul rischio di grosse anomalie indesiderate vicino all'obiettivo desiderato. Attualmente, le conoscenze sui meccanismi di riparazione del DNA sono ancora troppo limitate per poter modificare in tranquillità il materiale genetico in un embrione. Gli ultimi dati dimostrano che il sistema di editing non si limita a correggere la mutazione obiettivo: a causa dei meccanismi di riparazione cellulari, può creare "scompiglio genetico" nelle vicinanze del sito bersaglio. Sono state riscontrate varie tipologie di danno conseguenti alla rottura del DNA e ai processi di riparazione, tra cui macrodelezioni, riarrangiamenti più o meno ampi, traslocazioni e persino la perdita di un cromosoma.
A inizio giugno, uno studio firmato da Kathy Niakan e colleghi ha usato CRISPR-Cas9 per inserire mutazioni nel gene POU5F1, importante nello sviluppo, in 18 embrioni umani inutilizzati da pratiche di fecondazione assistita. In questo lavoro sono state trovate modifiche indesiderate, che interessavano ampie porzioni di DNA attorno al gene bersaglio, nel 22% delle cellule embrionali umane. Analogamente, un altro studio dell'Oregon Health & Science University, che mirava al gene MYH7 (collegato alla cardiomiopatia familiare ipertrofica), ha evidenziato che il 40% delle correzioni trovate era causato da un fenomeno chiamato conversione genica, nel quale il processo di riparazione del DNA copia la sequenza da un cromosoma per aggiustare il suo omologo. Il terzo studio, condotto da ricercatori della Columbia University, ha avuto come obiettivo il gene EYS, coinvolto nella retinite pigmentosa. Questo lavoro ha dimostrato che a seguito della rottura del doppio filamento di DNA indotta da Cas9, nella metà degli embrioni trattati le lesioni non vengono riparate con conseguenti danni durante il processo di divisione cellulare.
Questi esperimenti, seppur pionieristici, sottolineano la complessità e i rischi intrinseci dell'applicazione di una nuova tecnica in un contesto così delicato. Se da un lato l'editing genomico promette di essere la base per importanti innovazioni terapeutiche, dall'altro la sua applicazione agli embrioni umani, e le conseguenti modificazioni trasmissibili alle generazioni future, richiedono una cautela estrema e una comprensione approfondita dei meccanismi biologici coinvolti.
Le Implicazioni Etiche: Dal Superamento delle Malattie ai 'Bambini su Misura'
L'avvento del sistema CRISPR/Cas ha aperto molti nuovi interrogativi di natura bioetica, smantellando la frontiera tra terapie e eugenetica. Il potenziale di eliminare malattie ereditarie "per tutta la discendenza" è allettante, ma si accompagna all'inquietante prospettiva di agire sugli embrioni per creare "bambini con le caratteristiche volute", spingendo la discussione verso il concetto di "bambini su misura". La possibilità di effettuare modifiche genetiche sull'uomo, anche se solo a scopo terapeutico o di ricerca di base, e la questione se studi di tale genere debbano essere incoraggiati e resi pubblici, sono al centro di un intenso dibattito etico. Secondo quanto dichiarato dagli stessi autori del discusso articolo di Huang, le prestigiose riviste Nature e Science avrebbero rifiutato la pubblicazione della loro ricerca proprio per ragioni etiche.
Crispr-cas 9 le forbici del DNA
I ricercatori che hanno chiesto la moratoria su Nature, e che lavorano nel settore della terapia genica sulle cellule somatiche, temono inoltre che questa ricerca sulle cellule germinali possa far crollare l'interesse per il loro settore, che è quello da cui al momento vengono le maggiori speranze di cura di malattie genetiche, e che è considerato meno rischioso poiché le modifiche non sono ereditabili. Vi è, dunque, una preoccupazione che la ricerca sulla linea germinale possa distogliere l'attenzione e le risorse da approcci terapeutici considerati più sicuri e meno controversi.
La discussione non si limita solo alla comunità scientifica. Molti scienziati e bioeticisti hanno sottolineato la necessità di aprire il dibattito alla società civile, poiché l'impatto che avrà l'editing genomico in futuro riguarda tutti e pone un vero e proprio problema di democrazia. "Sul dove, quando e come l'editing genomico possa diventare uno strumento utile, la scienza non è la sola a dover dare risposte", ha dichiarato Giuseppe Testa, professore di biologia molecolare e partecipante attivo al dibattito. Questa tecnologia, infatti, permette di manipolare il DNA a costi bassi ed è già al centro di studi per la terapia di alcune malattie rare, tra cui la Distrofia muscolare di Duchenne. Tuttavia, applicare queste terapie avanzate, spesso per malattie rare o patologie molto gravi e senza speranza, è in parte giustificato dai rischi intrinseci della nuova tecnica, ma nel caso della linea germinale, i rischi si estendono a generazioni future con conseguenze ancora inesplorate.
Il Quadro Normativo e Le Differenze Globali
La confusione che circonda l'editing del genoma, specialmente sugli embrioni umani, deriva soprattutto dal fatto che le norme bioetiche riguardo alla sperimentazione su embrioni e sull'uomo non sono le stesse in tutti gli Stati, né vengono interpretate e applicate allo stesso modo. In molti paesi, tra cui l'Italia, ci sono leggi specifiche che vietano le manipolazioni sull'embrione e le cellule germinali. In altri paesi, per esempio gli Stati Uniti, non c'è un bando esplicito, sebbene la ricerca sia spesso limitata da regolamentazioni sui finanziamenti federali.
Ricerca di base a parte, ottenere l'autorizzazione per studi applicativi appare ancora molto difficile in Paesi dell'Unione Europea o negli Stati Uniti, dove comunque sono nate diverse start-up con l'obiettivo di creare terapie con CRISPR/Cas, quali Editas Medicine, Intellia Therapeutics e CRISPR Therapeutics. Al contrario, il governo cinese sembra più aperto all'ipotesi di autorizzare e finanziare queste ricerche, come dimostrato dai vari esperimenti condotti in Cina sugli embrioni umani.
Dopo la pubblicazione del controverso studio di Huang nel 2015, la comunità scientifica ha cominciato a correre ai ripari. Su iniziativa delle Accademie di Scienza e Medicina statunitensi e cinesi e della britannica Royal Society, si è svolto, dal 1 al 3 dicembre scorso a Washington, un summit internazionale sull'editing genomico applicato all'uomo. Erano presenti scienziati, bioeticisti, giuristi, storici della scienza e associazioni di pazienti provenienti da tutto il mondo. Alcuni, come David Baltimore, premio Nobel nel 1975 e presidente dell'AAAS (Associazione Americana per l'Avanzamento delle Scienze), hanno chiesto una moratoria, ovvero un blocco temporaneo della ricerca in questo ambito. La dichiarazione finale del summit si è limitata ad asserire l'"irresponsabilità" dell'utilizzo di CRISPR sulla linea germinale o sugli embrioni per applicazioni cliniche, e a invitare a procedere con cautela nella ricerca, valutando periodicamente il bilancio tra rischi e benefici. Molti scienziati hanno sottolineato l'importanza di non bloccare la ricerca di base, perché grazie a questa sarà possibile studiare a fondo il funzionamento delle nuove straordinarie "forbici molecolari" e capire come poter applicare al meglio la tecnica per la salute dell'uomo. La frontiera, per ora, resta senza regole uniformi.
CRISPR e il Mondo Agricolo: La Questione OGM
In ambito agronomico, il metodo CRISPR/Cas scatena meno problemi etici rispetto all'applicazione sugli embrioni umani, ma sta comunque complicando l'aspro dibattito sugli OGM (Organismi Geneticamente Modificati). Le mutazioni introdotte da questa tecnica possono infatti essere così piccole e localizzate da diventare indistinguibili da quelle "naturali", dovute cioè a fattori di stress come un eccessivo irraggiamento solare o mutazioni spontanee.
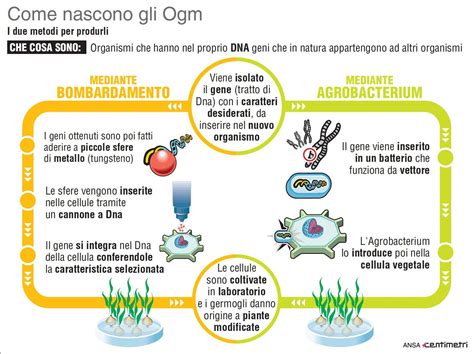
Questo solleva un interrogativo fondamentale: queste mutazioni sarebbero sufficienti per classificare tali piante come OGM? Per ora, gli Stati Uniti sembrano propendere per il no, mentre in Europa si va in direzione del sì. Nell'Unione Europea, infatti, un OGM è definito tale non in base alle caratteristiche finali del prodotto, ma in base alla tecnologia scelta per generarlo. La Direttiva 2001/18/CE del Parlamento europeo e del Consiglio del 12 marzo 2001 definisce OGM ogni organismo "il cui materiale genetico è stato modificato in modo diverso da quanto avviene in natura con l'accoppiamento e/o la ricombinazione genetica naturale". Tuttavia, le norme vigenti sono state adottate in un'epoca in cui il sistema CRISPR/Cas era ancora sconosciuto e quindi non era stato preso in considerazione. Se, come previsto, i centri di ricerca pubblici e privati genereranno a breve piante di interesse commerciale con questo sistema, sarà necessario colmare il vuoto legislativo sia in Europa sia nel resto del mondo, in modo da disciplinare la produzione e l'immissione sul mercato di questi prodotti.
Alcune compagnie stanno già cercando di approfittare il più possibile dell'attuale inadeguatezza nelle regolamentazioni per acquisire notorietà e guadagnare mercato. È il caso di Cibus, un'industria biotecnologica statunitense con filiale in Olanda che utilizza un sistema di modifica genetica mirato detto "Rapid Trait Development System", di fatto molto simile a CRISPR/Cas. L'azienda ha già immesso sul mercato americano una varietà di manioca resistente a un erbicida e sul suo sito internet sponsorizza i propri prodotti sottolineandone l'accettabilità anche in Paesi contrari agli OGM, in quanto "non transgenici". Questo evidenzia come la rapidità della scienza stia superando la capacità di adattamento dei quadri normativi esistenti.
Prospettive Future e Interrogativi Ecologici: Il 'Gene Drive'
L'utilizzo più controverso del CRISPR/Cas, al di fuori dell'ambito umano, è forse quello in cui il sistema è "autoreplicante", noto come "gene drive". In questo scenario, una copia del gene Cas e della sua sequenza guida si inseriscono all'interno del genoma della cellula bersaglio, con la particolare caratteristica che la mutazione introdotta venga ereditata con una frequenza molto superiore a quella mendeliana. Ad ogni generazione successiva, il meccanismo può quindi riattivarsi e riprodurre la mutazione nel 100% della progenie.
I vantaggi potenziali di questa tecnologia sarebbero enormi, non solo nella biotecnologia vegetale ma anche, e forse soprattutto, per il controllo degli insetti vettori di malattie. Ciò consentirebbe, ad esempio, di mutare le zanzare in modo da renderle immuni al plasmodio portatore della malaria (come è già stato fatto con successo in laboratorio) e debellare così la malattia, oppure rendere completamente innocui insetti pericolosi per le coltivazioni. Allo stesso modo si potrebbe agire su altri vettori di malattie come il virus Zika.
Tuttavia, la scarsa prevedibilità delle conseguenze ecologiche suggerisce di procedere in questo settore con molta cautela. L'introduzione di una modifica genetica che si diffonde rapidamente in una popolazione naturale potrebbe avere effetti a cascata imprevedibili sull'ecosistema, alterando equilibri ecologici complessi e con potenziali ripercussioni sulla biodiversità. La comunità scientifica è divisa tra l'entusiasmo per le promesse di salute pubblica e la profonda preoccupazione per i rischi ecologici incontrollabili che un "gene drive" potrebbe scatenare.
La Corsa all'Oro Biotecnologico: Brevetti e Investimenti
A meno di cinque anni dal primo studio biotecnologico che ne fece uso, CRISPR/Cas sta rivoluzionando l'ingegneria genetica e nel prossimo futuro promette di essere la base per importanti innovazioni in ambito terapeutico, alimentare ed ecologico. Al contempo, ha scatenato anche un'altra bufera: quella della proprietà intellettuale della scoperta scientifica, una vera e propria "corsa all'oro".
La battaglia sui brevetti è tra Jennifer Doudna e Emmanuelle Charpentier, le due ricercatrici che per prime hanno dimostrato la possibilità di utilizzare CRISPR per l'editing genomico, e Feng Zhang, che ha ottimizzato il sistema CRISPR/Cas9 e lo ha utilizzato per primo nelle cellule umane. Nonostante le due ricercatrici abbiano avviato la procedura di richiesta di brevetto per la nuova tecnica di editing a marzo 2013 e Zhang a ottobre 2013, i diritti di proprietà intellettuale di CRISPR sono andati inizialmente a quest'ultimo. Zhang ha inoltre ottenuto, successivamente, altri brevetti per le diverse versioni di Cas9 messe a punto per aumentare l'efficienza dell'enzima. Doudna e Charpentier hanno avviato una causa per la detenzione del brevetto, affermando di essere le prime ideatrici della nuova tecnica, d'altra parte Zhang ribatte che il brevetto è suo di diritto perché è stato il primo ad aver saputo applicare efficacemente la tecnica in cellule eucariotiche. Proprio in questi giorni, lo US Patent and Trademark Office (Uspto) ha dichiarato di voler stabilire al più presto chi sarà a raccogliere i frutti dell'innovativa tecnica.
Il pasticcio della proprietà intellettuale, tuttavia, non ha fermato le aziende farmaceutiche e biotech che hanno già capito che CRISPR potrebbe essere una "gallina dalle uova d'oro" e hanno iniziato una frenetica corsa per arrivare per prime all'applicazione clinica. Gli investimenti sono notevoli e molte startup sono state avviate dagli stessi pionieri di CRISPR. Ad esempio, Editas Medicine, cofondata da Zhang e George Church, sta portando avanti la ricerca preclinica sulla distrofia di Duchenne e altre malattie, e ha raccolto 120 milioni di dollari da un gruppo d'investitori tra cui spiccano nomi come Bill Gates e Google Ventures. Novartis ha firmato accordi con Intellia Therapeutics e con Caribou Biosciences, entrambe cofondate da Doudna, per la scoperta e lo sviluppo di nuovi farmaci che utilizzano la tecnica CRISPR. Anche Bayer ha annunciato la costituzione di una joint venture con CRISPR Therapeutics, biotech cofondata da Charpentier, investendo almeno 300 milioni di dollari in cinque anni. Questa effervescenza testimonia l'enorme potenziale percepito della tecnologia, ma anche la pressione e la competizione che ne derivano.
Gli sviluppi di questa nuova tecnologia non dipenderanno, quindi, soltanto dai risultati sperimentali ma anche dall'esito di un urgente dialogo tra scienza e società, a cui siamo tutti invitati a partecipare attivamente.