L’orizzonte della medicina contemporanea si sta spostando rapidamente da un approccio generalista a uno orientato alla specificità del singolo individuo. Questo cambiamento epocale coinvolge la gestione della vita sin dai suoi primordi, le tecniche di fecondazione assistita e l’applicazione clinica delle cellule staminali, in un intreccio complesso tra biotecnologia, etica e diritto.
L’evoluzione della fecondazione assistita in Italia
Nella versione originaria della legge, le disposizioni erano chiare ed estremamente ristrette. Tuttavia, il panorama è mutato significativamente negli ultimi anni. Secondo i dati contenuti nel Rapporto sull’andamento delle nascite realizzato dall’Ufficio Statistica del Ministero della Salute, l’uso delle procedure di fecondazione assistita è salito del 73% dal 2012 al 2022. L’indagine è stata condotta su 359 punti nascita e rileva che nel 2022, ogni 100 gravidanze ci sono stati 3,7 parti con PMA (Procreazione Medicalmente Assistita).
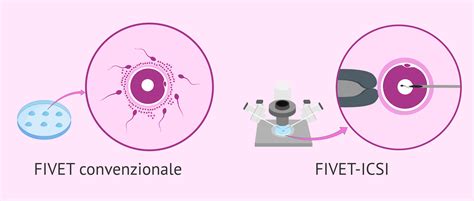
La distribuzione geografica delle prestazioni mostra una concentrazione significativa: su quasi 15 mila casi, più del 25% delle gravidanze con PMA è stata effettuata in Lombardia, il 10% in Lazio e l’8% in Campania. La fecondazione in vitro si conferma essere la procedura più utilizzata. In particolare, nel 2022 nel 47,8% delle fecondazioni assistite hanno utilizzato la FIVET (fecondazione in vitro con trasferimento di embrioni in utero). L’ICSI (fecondazione in vitro tramite iniezione di spermatozoo) è stato impiegato nel 35% dei casi.
Ad oggi le liste d’attesa per eseguire una procedura di fecondazione assistita sono lunghissime. Da gennaio, però, il ministro della Salute Orazio Schillaci al convegno “Natalità: work in progress” ha sottolineato che la procedura omologa sarà gratuita, segnando un passo verso una maggiore accessibilità alle cure per la sterilità.
Le cellule staminali: origine e prospettive terapeutiche
La ragione per cui un ostetrico ginecologo parla delle cellule staminali è iniziata con la sua specializzazione, quando sotto la direzione del prof. Luigi Cattaneo, fui assegnato al centro trasfusionale della Clinica ostetrica e ginecologica della Sapienza. Il sangue in ostetricia è un bene preziosissimo per prevenire la mortalità materna da emorragie nel e dopo il parto che era allora vaginale e spesso operatorio.
L’etimologia di staminale deriva dal greco stamis che significa trave, puntello, origine dal latino stamen: “filo dell’ordito” che compone un tessuto. Questo vocabolo staminale è utilizzato da biologi e medici per esprimere le proprietà di una cellula indifferenziata progenitrice di tutte le cellule che ha la proprietà di replicarsi e differenziarsi. Le cellule staminali sono cellule primitive, non specializzate, dotate dalla capacità di trasformarsi, a partire dall’embrione per tutta la durata della vita di ogni individuo, in circa 200 diversi tipi cellulari che formano l’organismo.
La fecondazione di una cellula uovo da parte di uno spermatozoo produce lo zigote che inizia dopo 24 ore la prima divisione con due cellule, proseguendo nei due tre giorni successivi alla moltiplicazione di 4 e 8 cellule, i blastomeri. Le cellule staminali adulte pluripotenti sono presenti in alcuni dei nostri organi e tessuti e hanno generalmente il compito di rigenerare l’organo o il tessuto in cui risiedono.
Le fonti delle cellule staminali sono quelle embrionali, la cui applicazione presenta grossi ostacoli per l’eventualità di un rigetto immunitario, possibili tumori teratogenici ed obiezioni etiche dovute alla distruzione dell’embrione stesso. Shinya Yamanaka dell’Università di Kyoto dimostrò che le cellule di topi possono essere riprogrammate e diventare immature, creando una cellula staminale pluripotente indotta (iPSC induced Pluripotent Stem Cell), dette anche “staminali etiche”.
CHE COSA SONO E COME FUNZIONANO LE CELLULE STAMINALI (e anche un po' la leucemia) | #TELOSPIEGO!
Medicina di precisione e rivoluzione biotecnologica
La medicina classica si trasformerà in medicina preventiva, predittiva e di precisione, in base al profilo genetico, molecolare e ultrastrutturale di ciascun paziente. “La medicina a taglia unica che abbiamo conosciuto negli ultimi cento anni cederà il passo ad una medicina confezionata su misura per ciascun individuo”.
Dobbiamo tener conto della diversità genetica inter-individuale insita nei genomi umani, che comprende SNPs, inserzioni, delezioni e intere sequenze: alcune contribuiscono alla variabilità della risposta terapeutica. La piattaforma d’elite è oggi la “Next Generation Sequencing”, che coniuga velocità e accuratezza: il genoma è frammentato in sequenze corte, amplificate su un chip, sequenziate e riallineate mediante complessi calcoli bioinformatici.
Tuttavia, sorgono interrogativi cruciali: in tema di privacy, a chi appartengono i dati raccolti? Come interpretare, pubblicizzare e utilizzare dati “sensibili” per definizione? Conoscere informazioni e predisposizioni rilevate nel genoma proprio e dei figli potrebbe innescare ansie e timori comprensibili.
Il mosaico genetico e la ricerca contemporanea
Le cellule del corpo umano non contengono tutte la stessa sequenza di DNA, né i geni il medesimo livello di espressione: le variazioni genetiche sono tante e tali nei diversi tessuti che si dovrebbe parlare di “mosaico genetico”. Siamo caratterizzati da un ventaglio di cellule con caratteristiche genetiche parzialmente non sovrapponibili, in condizioni basali e fisiologiche, ancor più accentuate in caso di deviazione patologica, conseguenza di mutazioni specifiche nei singoli citotipi.
Lo studio del DNA di un tessuto non rispecchia quanto osservabile in un altro istotipo. La tecnica che permette di studiare queste specificità è denominata MALBAC, “Multiple annealing and looping based amplification”, utilizzata nel progetto internazionale “GTEx, Genotype-Tissue Expression”. I dati raccolti confluiscono nella redazione di “Human Cell Atlas” e “Human Protein Atlas”, disponibili in rete per ricercatori e clinici, offrendo una mappa dettagliata dell’espressione genica umana.
Sfide etiche e normative nell’era dell’editing genomico
Modificare (editare) tratti di un genoma viene eseguito già da alcuni anni con tecniche lunghe, costose e di non semplice praticabilità; l’introduzione della CRISPR-Cas9 sta rivoluzionando e semplificando le procedure di manipolazione. Nata come memoria genetica di precedenti infezioni virali integrata nel genoma di numerosi batteri, abbiamo imparato a sfruttare quest’arma naturale per allestire forbici molecolari che tagliano nelle cellule il DNA in un target specifico.
Sarà necessario investire di più e meglio nell’alfabetizzazione degli operatori sanitari e dell’opinione pubblica, soprattutto in temi quali “inizio e fine vita”, terapia del dolore, privacy e corretto impiego dei dati genetici. La tecnologia oggi mette a disposizione strumenti di fruizione potenzialmente allargata e democratica, ma rischiosa e per ora aliena da controlli, normative e “paletti” universalmente concepiti e condivisi. La sfida del futuro non sarà solo tecnica, ma risiederà nella capacità delle istituzioni di governare tale evoluzione, trasformandola in una reale opportunità per la salute pubblica.