La beta-galattosidasi è un enzima idrolitico di fondamentale importanza biologica, noto soprattutto per il suo ruolo nella digestione del lattosio, il disaccaride presente nel latte. Tuttavia, la sua rilevanza si estende ben oltre la fisiologia umana, abbracciando anche il campo della biologia molecolare grazie al suo impiego come modello classico per lo studio della regolazione genica. Questo articolo esplorerà in dettaglio la natura molecolare della beta-galattosidasi, il suo meccanismo d'azione, il suo significato nell'organismo umano e il suo contributo storico e pratico alla ricerca scientifica.
Struttura e Meccanismo d'Azione della Beta-Galattosidasi
La beta-galattosidasi appartiene alla famiglia delle glicosidasi, enzimi che catalizzano l'idrolisi dei legami glicosidici. Specificamente, la beta-galattosidasi agisce sui legami β-glicosidici che collegano le molecole di galattosio in composti noti come β-galattosidi. Il suo compito principale nell'organismo umano è l'idrolisi del lattosio, un disaccaride composto da una molecola di glucosio e una di galattosio, legate da un legame β-glicosidico. La reazione catalizzata dalla beta-galattosidasi rompe questo legame, liberando i due monosaccaridi costituenti, glucosio e galattosio, che possono poi essere assorbiti e utilizzati come fonte di energia dalle cellule.
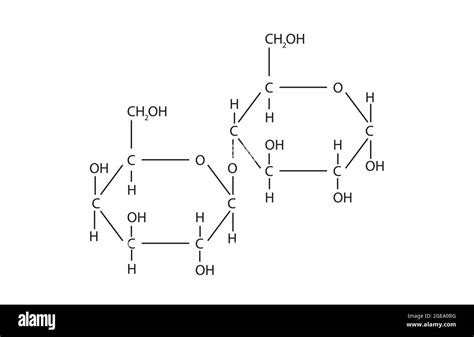
La struttura tridimensionale della beta-galattosidasi è complessa. Nell'organismo batterico Escherichia coli (E. coli), il gene lacZ codifica per questo enzima. La struttura quaternaria dell'enzima in E. coli è un omotetramero, ovvero una proteina composta da quattro subunità identiche, con un peso molecolare di circa 464 kDa. Ogni subunità è ulteriormente suddivisa in cinque domini, con il terzo dominio che ospita la maggior parte del sito attivo. È importante notare che il sito attivo è un'area complessa che coinvolge elementi provenienti da domini diversi e anche da altre subunità, permettendo un'interazione sofisticata con il substrato.
Il sito attivo della beta-galattosidasi è in grado di catalizzare l'idrolisi del substrato disaccaridico attraverso due tipi di interazione: un legame "poco profondo" e un legame "profondo". Per un funzionamento ottimale, l'enzima richiede la presenza di specifici ioni: lo ione monovalente potassio (K+) e lo ione divalente magnesio (Mg2+). Questi ioni agiscono come cofattori, facilitando il corretto allineamento del substrato e la catalisi della reazione.
Inizialmente, si riteneva che il residuo di acido glutammico (Glu-461) fosse il nucleofilo nella reazione di sostituzione all'interno del sito attivo di E. coli. Tuttavia, ricerche successive hanno chiarito che il Glu-461 agisce piuttosto come un catalizzatore acido. Studi più recenti indicano che il Glu-537 è il nucleofilo effettivo nel sito attivo della beta-galattosidasi da Escherichia coli.
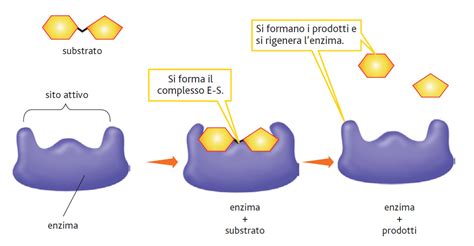
La Beta-Galattosidasi nell'Organismo Umano: Lattasi e Intolleranza al Lattosio
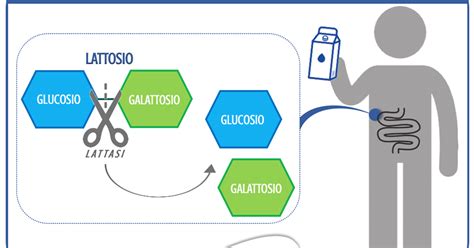
Nell'uomo, la beta-galattosidasi più significativa è la lattasi. Questo enzima è secreto dalla mucosa dell'intestino tenue e svolge il ruolo cruciale di digerire il lattosio ingerito con la dieta, sia esso presente in alimenti, farmaci o integratori. Come accennato, l'azione della lattasi scinde il lattosio nei suoi monomeri costituenti, glucosio e galattosio, rendendoli disponibili per l'assorbimento e il metabolismo energetico.
La lattasi è particolarmente attiva alla nascita, garantendo ai neonati la capacità di digerire il latte materno, la loro principale fonte di nutrimento. Tuttavia, subito dopo lo svezzamento, si verifica un fenomeno biologico diffuso in tutte le specie di mammiferi: un netto declino funzionale dell'attività della lattasi. Questo calo è geneticamente determinato e porta a una ridotta capacità di idrolizzare il lattosio nell'adulto.
Questo fenomeno è la causa diretta della cosiddetta "intolleranza al lattosio". In presenza di un'attività lattasica insufficiente, il lattosio non digerito raggiunge l'intestino crasso (colon), dove viene fermentato dai batteri intestinali. Questa fermentazione produce gas (come idrogeno e metano) e acidi, scatenando un corteo sintomatologico caratterizzato da gonfiore addominale, crampi, flatulenza e diarrea.
L'unico modo efficace per gestire questi disturbi è adottare una dieta specifica, spesso definita "dieta di esclusione". Questa dieta si basa sul consumo prevalente di alimenti naturalmente privi di lattosio o formulati come tali, e sulla moderazione più o meno scrupolosa dei cibi che lo contengono. La tolleranza individuale gioca un ruolo fondamentale: alcune persone con deficit di lattasi possono tollerare piccole quantità di lattosio, specialmente se presente in alimenti fermentati come lo yogurt o in formaggi stagionati a pasta dura, nei quali il lattosio è parzialmente degradato. Altre persone, invece, sono costrette a escludere completamente il lattosio dalla loro alimentazione. L'integrazione con enzimi lattasi esogeni, disponibili in commercio sotto forma di compresse o gocce, può rappresentare un'ulteriore strategia per migliorare la digestione del lattosio in occasioni specifiche.
Apparato digerente
La Beta-Galattosidasi nella Biologia Molecolare: Il Modello lacZ
Oltre al suo ruolo fisiologico, la beta-galattosidasi ha un'importanza storica e pratica immensa nel campo della biologia molecolare. Il gene lacZ di E. coli, che codifica per la beta-galattosidasi, è stato uno dei primi sistemi genici ad essere studiato in dettaglio per comprendere i meccanismi di regolazione dell'espressione genica nei batteri. Questo sistema è diventato un modello classico, ampiamente utilizzato per insegnare e studiare come i geni vengono attivati o disattivati in risposta a segnali ambientali.
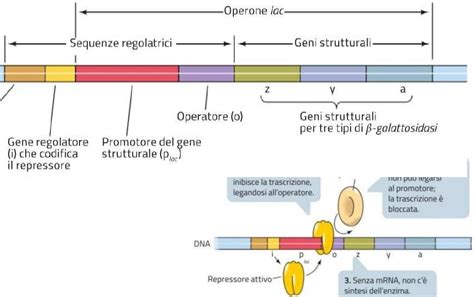
Il sistema del gene lac in E. coli è un esempio emblematico di operone batterico. Un operone è un'unità funzionale del DNA che comprende un gruppo di geni strutturali, un promotore e un operatore. Questi geni sono trascritti insieme in un unico mRNA messaggero e svolgono funzioni correlate. Nel caso dell'operone lac, i geni codificano per enzimi necessari alla metabolizzazione del lattosio.
Il lattosio, quando presente, agisce come induttore del sistema. Si lega a una proteina repressore che normalmente impedisce la trascrizione dei geni dell'operone. Il legame del lattosio al repressore ne modifica la conformazione, facendogli perdere l'affinità per l'operatore. Di conseguenza, la RNA polimerasi può legarsi al promotore e iniziare la trascrizione dei geni strutturali, inclusi quelli che codificano per la beta-galattosidasi.
La beta-galattosidasi prodotta in questo sistema ha un ruolo doppio. Innanzitutto, idrolizza il lattosio nei suoi monosaccaridi costituenti, glucosio e galattosio, che possono essere utilizzati dal batterio per produrre energia. In secondo luogo, una piccola quantità di lattosio viene convertita in una molecola chiamata allolattosio, che è un induttore più potente del sistema. L'allolattosio si lega al repressore, garantendo l'espressione continua dei geni dell'operone finché il lattosio è disponibile nell'ambiente.
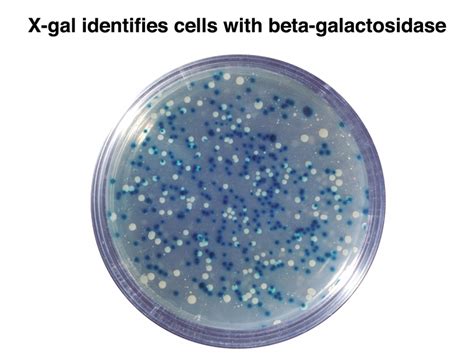
L'uso del gene lacZ come reporter è una tecnica fondamentale nella biologia molecolare moderna. Il gene lacZ può essere fuso geneticamente ad altri geni di interesse. Se il gene fuso è espresso, la beta-galattosidasi viene prodotta e può essere facilmente rilevata utilizzando substrati cromogenici (che producono un colore quando idrolizzati dall'enzima) o fluorogenici. Questo permette ai ricercatori di monitorare l'espressione genica, la localizzazione delle proteine e persino l'interazione tra proteine. Ad esempio, la beta-galattosidasi troncata inattiva può essere utilizzata in saggi di complementazione per studiare le interazioni proteiche: due frammenti proteici, se interagiscono, possono ricostituire una beta-galattosidasi funzionale, generando un segnale rilevabile.
Altri Ruoli e Applicazioni della Beta-Galattosidasi
Sebbene la lattasi sia la beta-galattosidasi di maggior rilievo per l'uomo, enzimi simili sono presenti in altri organismi e svolgono ruoli specifici. Ad esempio, in alcuni batteri e funghi, la beta-galattosidasi è essenziale per la digestione di carboidrati complessi presenti nelle pareti cellulari vegetali, come il verbascosio, il raffinosio e lo stachiosio. L'assenza di un enzima analogo nell'uomo rende questi zuccheri difficili da digerire, contribuendo ulteriormente alla fermentazione nel colon e ai sintomi associati al consumo di legumi e altri vegetali ricchi di questi oligosaccaridi.
La beta-galattosidasi è stata anche studiata in altri tessuti mammiferi, come la ghiandola mammaria di ratto, dove è implicata nella biosintesi di particolari glicolipidi. La sua purificazione e lo studio delle sue proprietà hanno contribuito alla comprensione dei processi biosintetici e delle vie metaboliche.
In sintesi, la beta-galattosidasi è un enzima poliedrico. Nella sua forma di lattasi, è indispensabile per la digestione del lattosio, e la sua disfunzione porta a una condizione comune come l'intolleranza al lattosio. Sul fronte della ricerca, il suo studio ha aperto le porte a una comprensione profonda della regolazione genica, fornendo strumenti potenti per la biologia molecolare e la biotecnologia. La sua struttura complessa e il suo meccanismo d'azione continuano ad essere oggetto di studio, rivelando continuamente nuove sfaccettature della sua importanza biologica.
tags: #beta #galattosidasi #e #lattanti