L'emoglobina (Hb) è una proteina fondamentale, contenuta all’interno dei globuli rossi, il cui ruolo primario consiste nel trasportare l’ossigeno ai tessuti del nostro organismo. Questa proteina è costituita da quattro subunità, o catene globiniche, ciascuna delle quali presenta al suo interno una struttura chiamata gruppo eme, contenente ferro e responsabile del legame dell’ossigeno. Ogni molecola di emoglobina, infatti, è formata da quattro proteine globulari strettamente associate tra di loro; ognuna di esse ospita una molecola non proteica, l'eme, un tetrapirrolo a cui è associato un atomo di Ferro, che lega a sè l'ossigeno prelevato dagli alveoli polmonari. Esistono quattro tipi diversi di catene globiniche, designate come: α (alfa), β (beta), γ (gamma), δ (delta).
Durante lo sviluppo, l'essere umano esprime diversi tipi di emoglobina, a seconda dei geni che vengono attivati in quel determinato periodo di vita. Queste emoglobine presentano una struttura quaternaria diversa, ma in linea generale svolgono la stessa funzione, pur presentando affinità differenti per l’ossigeno. Le emoglobine di un adulto sono composte in massima parte da HbA, costituita da due coppie di catene, denominate α (alfa) e ß (beta). In bassa percentuale si trova l'HbA2, costituita da due catene α e due catene δ (delta).
L'Emoglobina Fetale (HbF): Struttura, Funzione e Sviluppo
Nei globuli rossi del feto è possibile identificare una forma di emoglobina diversa da quella adulta. Questa è l'Emoglobina F (HbF), nota con il nome di emoglobina fetale, ed è costituita da due catene alfa e due catene gamma (α2γ2). L'emoglobina fetale (HbF od emoglobina F) è la prima emoglobina prodotta durante la vita fetale. Le due catene alfa sono identiche a quelle presenti nell'emoglobina adulta, mentre quelle gamma differiscono dalle Beta per 39 amminoacidi. Questa modifica strutturale conferisce all'emoglobina fetale un'affinità per l'ossigeno superiore; in altre parole, si lega all'ossigeno in modo più tenace rispetto all'emoglobina adulta.
Dal punto di vista funzionale, l'emoglobina fetale (HbF od emoglobina F) permette al feto di estrarre con maggiore efficacia l'ossigeno dal sangue materno. Riesce infatti a trasportare percentuali comprese tra il 20% e il 30% di ossigeno in più, rispetto all’emoglobina materna. Il trasferimento di ossigeno al sangue fetale attraverso la barriera placentare è favorito anche dalla maggiore concentrazione di emoglobina, più alta di circa il 50% rispetto a quella del sangue materno.
La sintesi delle globine Beta, caratterizzanti l'emoglobina adulta, appena percettibile durante la vita fetale, raggiunge il normale regime soltanto verso la fine del terzo mese della vita extrauterina. Normalmente, la produzione di HbF diminuisce progressivamente alla nascita per poi stabilizzarsi su valori molto bassi intorno a 1-2 anni. Entro il primo anno di vita, le concentrazioni di emoglobina fetale scendono a livelli generalmente inferiori all'1%. La differente espressione nel tempo, dal concepimento alla vita adulta, delle diverse catene globiniche nell'uomo dipende dall'attivazione e dallo spegnimento di specifici geni.

Emoglobinopatie: Un Quadro Generale
Un’emoglobinopatia è un disordine ematico ereditario caratterizzato dalla presenza di forme anomale dell’emoglobina (varianti emoglobiniche) o dalla riduzione della produzione della stessa (talassemia). La presenza di mutazioni nei geni codificanti per le catene globiniche può determinare la produzione di emoglobine anomale e quindi la presenza di emoglobinopatie. Le mutazioni possono influenzare la struttura dell’emoglobina, la sua funzionalità, la sua velocità di produzione o anche la sua stabilità. Tali mutazioni possono comportare la produzione di catene globiniche strutturalmente alterate o anche la perdita della produzione di uno o più tipi di catene globiniche.
Circa il 7% della popolazione mondiale è portatore in eterozigosi di una variante genetica in una delle catene dell’emoglobina; il tasso di mutazione può variare notevolmente in base all’etnia. Attualmente, sono stati rilevati circa 1000 tipi di emoglobinopatie.
Le Talassemie
La talassemia è causata dalla diminuita produzione o carenza di una delle catene globiniche. Le Talassemie sono un difetto ereditario che impedisce la normale sintesi delle catene α (α-talassemia) o delle catene ß (ß-talassemia).
Alfa-Talassemia: L'informazione genetica per le catene α è contenuta in 4 geni. Nel caso dell'α-talassemia, il difetto può derivare dall'alterazione di tutti e quattro i geni, una condizione non compatibile con lo sviluppo del feto. L'alterazione di tre geni porta alla presenza di Hb formata da complessi di quattro catene ß, chiamata HbH (β4), accompagnata da anemia emolitica, splenomegalia, ecc. L'emoglobina H (HbH) si forma in alcuni casi di alfa-talassemia ed è prodotta in caso di grave carenza delle catene alfa. L'alterazione di due geni si manifesta come tratto talassemico con presenza di anemia, globuli rossi di volume ridotto, ma con percentuali di HbA2 e HbF di solito normali. L'alterazione di un solo gene è una condizione indistinguibile dalla normalità, ma con possibile trasmissione del carattere alla prole. L'Emoglobina di Bart (γ4) si sviluppa nei feti affetti da alfa-talassemia ed è prodotta in caso di grave carenza delle catene alfa in maniera analoga a quanto avviene per l'HbH.
Beta-Talassemia: L'informazione genetica per le catene ß è contenuta in 2 geni. Nel caso della ß-talassemia, il difetto può derivare dall'alterazione di entrambi i geni (forma omozigote), e in questo caso la malattia è definita ß-talassemia major o morbo di Cooley. Questa si manifesta subito dopo la nascita con una anemia molto grave, che necessita di trasfusioni periodiche di sangue. Oppure può derivare dall'alterazione di un solo gene (forma eterozigote), e in questo caso il difetto viene chiamato ß-talassemia minor o tratto talassemico. La maggior parte delle persone con talassemia minor non presenta sintomi; i globuli rossi nel loro sangue sono in numero maggiore che nel normale, ma di volume ridotto (da cui il termine di microcitemia) e poveri di emoglobina. L’aumento dell’emoglobina A2 è uno dei marker più tipici del portatore di geni Β-talassemici, ed è utilizzato per quantificare il rischio che la prole della coppia sia affetta da Beta talassemia, un rischio elevato nel caso entrambi i genitori siano portatori del difetto genetico, evidenziato da percentuali di HbA2 superiori alla norma. Purtroppo, in alcuni casi i livelli di HbA2 risultano invariati nonostante il soggetto sia portatore di geni Β-talassemici (ad esempio in caso di contemporanea presenza di una severa carenza di ferro); inoltre, la differenza dei valori di HbA2 tra soggetti sani e portatori di tratto talassemico è piccola. Per questo motivo le misure analitiche devono essere particolarmente accurate ed i risultati interpretati insieme a quelli di altre indagini ematologiche.
Talassemia: che cos'è e come diagnosticarla
Varianti Emoglobiniche Anomale
Esistono molteplici varianti emoglobiniche. Alcune sono silenti, ossia senza segni e sintomi evidenti, mentre altre sono in grado di influenzare la funzionalità e/o la stabilità della molecola emoglobinica. È possibile che la stessa persona erediti due differenti geni anomali, uno da ciascun genitore, con conseguente combinazione delle varianti emoglobiniche rilevate dai test. Questa condizione è nota come eterozigosi composta o doppia eterozigosi.
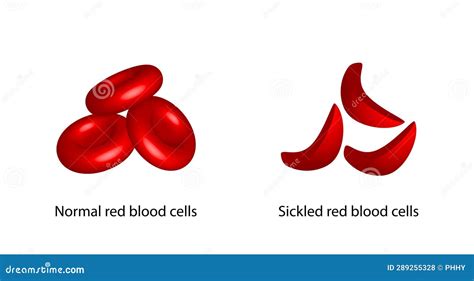
Emoglobina S (HbS): È la variante responsabile dell’anemia falciforme. Si tratta di una patologia a frequenza molto variabile, ma comunque maggiormente presente nelle aree nelle quali la malaria è o è stata endemica, a causa di un vantaggio evolutivo dei portatori nei confronti della malaria. Le persone affette da anemia falciforme presentano entrambe le copie del gene responsabile della produzione di HbS, e pertanto presentano elevate quantità di HbS. Le persone con “tratto” falciforme (eterozigoti) presentano circa il 40% di HbS e il 60% di HbA normale. La presenza di HbS determina, in presenza di basse concentrazioni di ossigeno (come può accadere durante un esercizio fisico o in caso di infezioni polmonari), la variazione della forma dei globuli rossi che assumono la caratteristica forma a falce. Gli eritrociti falciformi possono bloccare i piccoli vasi, causando episodi dolorosi, scompensi circolatori e diminuzione dell’apporto di ossigeno ai tessuti con diminuzione della sopravvivenza cellulare.
Emoglobina C (HbC): Lo stato di portatore di HbC (eterozigoti) è presente in circa il 2-3% delle persone di origine africana. Lo stato di omozigosi comunque è un evento raro ed è responsabile di effetti relativamente lievi.
Emoglobina E (HbE): È una delle varianti beta-globiniche più comuni nel mondo, con una maggiore prevalenza nelle persone originarie del sudest asiatico. I soggetti omozigoti per HbE in genere hanno una lieve anemia emolitica, macrocitosi ed un moderato ingrossamento della milza.
Spesso, le forme meno comuni prendono il nome dal luogo di appartenenza della/e famiglia/e in cui la variante genetica è stata identificata per la prima volta.
Assetto Emoglobinico: Metodologie Diagnostiche
L’assetto emoglobinico si prefigge di rilevare eventuali varianti emoglobiniche e/o la quantità relativa dei diversi tipi di Hb. Per la diagnosi delle emoglobinopatie l’esecuzione di un singolo test non è sufficiente. Questa richiede la valutazione complessiva di una serie di esami, eseguiti secondo processi ben definiti. I test di primo livello per la ricerca delle emoglobinopatie in genere utilizzano metodiche volte alla determinazione del tipo e della quantità di emoglobine presenti nel sangue del paziente in esame. La maggior parte delle varianti emoglobiniche più comuni o delle talassemie possono essere identificate utilizzando una combinazione di questi test. La rilevazione della quantità relativa della variante emoglobinica presente è un valido ausilio diagnostico.
Nella valutazione delle emoglobinopatie deve essere prestata molta attenzione all’interpretazione dei risultati. I risultati in genere riportano il tipo di Hb presenti (quando identificabile) e la loro quantità relativa. Questo esame è un ausilio alla ricerca delle varianti emoglobiniche o di una classe di patologie note con il nome di talassemie, caratterizzate dalla diminuita produzione o carenza di una delle catene globiniche.
Test Molecolari: Ricercano le mutazioni presenti nei geni codificanti per le catene globiniche alfa e beta. Questi test sono cruciali per una diagnosi definitiva e per la consulenza genetica.
Significato Clinico dell'Emoglobina Fetale Elevata nell'Adulto
In un adulto, i livelli di emoglobina fetale considerabili normali oscillano tra 0.1 e 1.1%. Adulti normali presentano valori di emoglobina fetale compresi tra lo 0.3% e l'1.2%, meno del 3.5% di emoglobina A2 (α2, δ2), e la rimanente percentuale (in genere > 96%) è coperta dall'emoglobina di tipo A. Quando negli adulti si hanno valori superiori a 1.1%, si parla di emoglobina F alta. È comunque necessaria una precisazione. Nella norma i valori di Hb F sono inferiori all’1%. Tuttavia, l’attività dei geni γ può persistere nella vita adulta con presenze più o meno importanti di Hb F, segno distintivo di uno spettro molto eterogeneo di condizioni. Quando l’Hb F supera il 2% nell’adulto, è buona norma approfondirne sempre il significato.
Una piccola percentuale di emoglobina fetale viene espressa anche durante la vita adulta ed i suoi livelli possono variare anche di molto sotto l'influenza di fattori quali l'età, il sesso o peculiarità genomiche.
Condizioni Associate a Livelli Elevati di HbF nell'Adulto:
- Disordini ereditari: Sindromi talassemiche, varianti Hb, geni γ mutati, mutazioni di BCL11A o HBS1L-MYB.
- Disordini acquisiti: Malattie del sangue, neoplasie, risposte a trattamenti terapeutici, altre condizioni.
- Ipertiroidismo
- Anemia emolitica
- Anemia megaloblastica (deficit di vitamina B12 e/o folati)
- Pazienti positivi per HIV-1 trattati con farmaci retro-virali.
- Presenza di gene α triplicato.
- Una condizione di recupero dovuta a ipoplasia di midollo osseo, ovvero un disturbo delle cellule staminali ematopoietiche.
Alcuni soggetti sono affetti dalla cosiddetta persistenza ereditaria dell'emoglobina fetale (HPFH), una condizione benigna in cui concentrazioni importanti di emoglobina fetale (> 10%) persistono anche in età adulta. Si è notato come tale peculiarità, generalmente asintomatica, possa alleviare la severità di certe emoglobinopatie e talassemie.
L’Hb F ha un ruolo rilevante nella vita adulta dei pazienti con emoglobinopatie importanti. Nei soggetti con morbo di Cooley, dove le catene γ sostituiscono le catene β non prodotte, quote elevate di Hb F, anche superiori al 95%, contribuiscono in parte a compensare l’anemia. Una terapia farmacologica capace di aumentare la concentrazione di emoglobina fetale apporta benefici significativi ad alcune categorie di pazienti, come quelli affetti da anemia falciforme o da talassemia Beta. Il prototipo di questi farmaci è stata l'idrossiurea, farmaco antineoplastico ad azione mielosoppressiva, che si è dimostrato efficace nell'aumentare i livelli di emoglobina fetale e nel ridurre l'incidenza di crisi dolorose in pazienti affetti da anemia falciforme.
L'Esame dell'Emoglobina Fetale: Quando e Come
L’esame per l’emoglobina fetale viene svolto per la diagnosi di patologie a carico del sangue, quali talassemia e anemia falciforme. Il test per la ricerca delle emoglobinopatie viene richiesto come parte dei programmi di screening neonatale (attualmente attivo solo in alcune regioni in Italia). L’esame può essere richiesto nel caso in cui si sospetti un’emoglobinopatia in presenza di segni e sintomi caratteristici.
Per l’esame dell’emoglobina fetale viene richiesto un digiuno di almeno otto ore. È importante informare il medico di tutti i farmaci, integratori o terapie ormonali che si stanno assumendo, poiché alcuni di essi potrebbero influenzare i risultati dell’esame. I valori di riferimento degli esami di laboratorio possono variare a seconda della metodologia di analisi dei campioni; quelli indicati in questa scheda hanno uno scopo puramente informativo.
Le trasfusioni di sangue possono interferire con la valutazione delle emoglobinopatie, poiché il metodo analitico non è in grado di distinguere tra l’emoglobina del donatore e quella del paziente, interferendo potenzialmente con i risultati del test. Un paziente dovrebbe aspettare diversi mesi dopo una trasfusione prima di sottoporsi a questo esame. Questo esame non viene eseguito in tutti i laboratori.

Interpretazioni Cliniche e Casi di Pazienti
L’interpretazione dei livelli di Hb F, sulla base degli esami di primo livello, può suggerire ipotesi diagnostiche che potranno richiedere conferme molecolari. L’obiettivo di un "Caso Clinico" è quello di presentare pazienti con fenotipi diversi caratterizzati dalla presenza di Hb F variabilmente espressa, in soggetti adulti.
Paziente 1: Presenta microcitosi, Hb A2 nella norma e Hb F superiore al 15%. La sua origine italiana ci fa pensare a una δβ-talassemia, definita probabilmente «Tipo Siciliano», con il contributo di polimorfismi. Meno probabile è la presenza di una β-talassemia + HPFH da difetto puntiforme come si ha nella cosiddetta δβ-talassemia «Tipo Sardo». Data l’età, potrebbe essere utile esaminare i genitori, ma l’esame molecolare è comunque necessario per una conferma.
Paziente 2: Mostra un modesto aumento dell’Hb F in un quadro di normalità degli indici eritrocitari. I risultati degli esami eseguiti consentono di escludere le forme classiche di talassemia. Si ipotizza una probabile presenza di polimorfismi dei geni γ o di altri geni non globinici. Il quadro generale non richiede approfondimenti molecolari se non in relazione ad una eventuale consulenza di coppia in previsione di una gravidanza.
Paziente 3: Gli indici eritrocitari sono fuori norma, l'Hb F è elevata e l'Hb A2 può essere considerata "normale/al limite". La paziente non è stata trasfusa negli ultimi tre mesi, quindi si possono fare alcune ipotesi. È possibile la presenza di una HPFH da delezione allo stato eterozigote (con eventuale polimorfismo HPFH puntiforme associato e alfa talassemia). Questa ipotesi può essere più verosimile considerando l’origine africana della paziente. Un'altra possibilità è una delta-beta talassemia associata a polimorfismi che incrementano ulteriormente l’HbF. Per una definizione dell'assetto genetico è necessaria l'analisi molecolare, soprattutto in previsione di una gravidanza, così come gli esami preventivi al partner e una consulenza dedicata.
Paziente 4: Tutti i dati disponibili definiscono un quadro β-talassemico con una quota significativamente elevata di HbF. Si possono fare alcune ipotesi: presenza di un composto talassemico β+/β++; presenza di un composto talassemico β+/β+; oppure presenza di β0-talassemia eterozigote + polimorfismi dei geni γ e/o mutazioni di altri geni che favoriscono la presenza di Hb F. È opportuno un approfondimento molecolare per la caratterizzazione dei geni β e la ricerca di eventuali difetti associati ad altri geni. È consigliabile la consulenza presso una struttura clinica dedicata.
Screening e Trattamento delle Emoglobinopatie
Lo screening delle emoglobinopatie consente di identificare e quindi potenzialmente anche trattare i neonati con disordini congeniti entro pochi giorni dalla nascita. In questo modo possono essere evitati problemi di salute potenzialmente letali o anche responsabili di disabilità permanenti. L'esame di screening neonatale è una pratica vitale in molte regioni.
Il trattamento di alcuni tipi di emoglobinopatie può comportare l’utilizzo di terapie di supporto, ad esempio durante la comparsa di crisi in corso di anemia falciforme. L’obiettivo è quello di alleviare il dolore e di minimizzare le complicanze. Talvolta, in caso di anemia grave, è necessario ricorrere a trasfusioni di sangue. Meno frequentemente, possono essere utilizzati anche altri trattamenti, inclusa la terapia farmacologica per modulare i livelli di HbF.
tags: #assetto #emoglobinico #hb #fetale