La comprensione dei meccanismi che regolano lo sviluppo embrionale e il successo di una gravidanza in ambito di Procreazione Medicalmente Assistita (PMA) richiede un’analisi approfondita della genetica preimpianto. Il fenomeno dell’aneuploidia rappresenta una delle sfide cliniche più significative, condizionando non solo le probabilità di attecchimento, ma anche l’esito a lungo termine della gestazione.
Il fondamento genetico: Euploidia e Aneuploidia
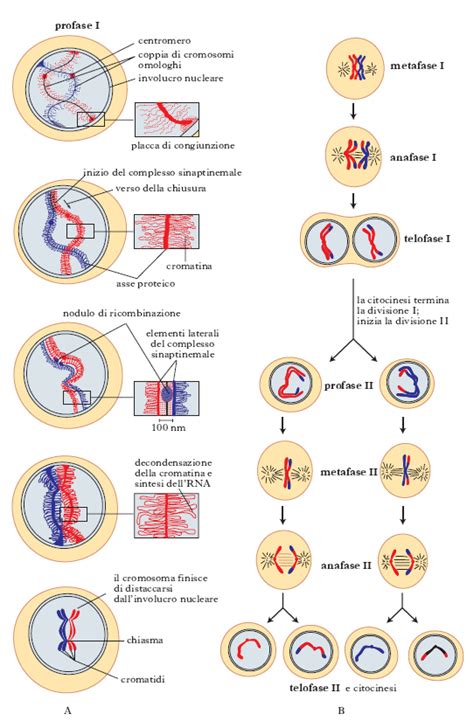
Gli esseri umani possiedono 23 coppie di cromosomi (46 in totale) nelle cellule che compongono i tessuti del proprio organismo. Nei cromosomi si conserva il materiale genetico. Le coppie di cromosomi dalla 1 alla 22 sono conosciute come autosomi e la coppia 23 come cromosomi sessuali che determinano il sesso. Il fatto di avere 23 coppie di cromosomi permette al corpo umano di avere uno status cromosomico conosciuto come euploide.
L’aneuploidia è presente ogni volta che abbiamo un numero anormale di cromosomi in una cellula, diverso dal solito 46 tipico delle cellule euploidi negli umani. Normalmente, tutte le cellule umane hanno esattamente 23 paia di cromosomi. L’unica eccezione sono i gameti (ovociti e spermatozoi) perché le loro cellule sono aploidi, cioè contengono una sola copia di ogni cromosoma. La meiosi è il processo attraverso il quale si forma una cellula aploide da una cellula diploide, vitale affinché l’embrione che ne risulta abbia il numero corretto di cromosomi.
L'impatto della qualità gametica sull'infertilità
La competenza dell’embrione dipende ovviamente dalla qualità dei gameti coinvolti nella fecondazione. La funzione spermatica difettosa contribuisce all’infertilità umana. L’aumento delle frequenze di aneuploidia, una delle principali cause di perdita di gravidanza e ritardo mentale negli esseri umani, mostra un parallelo con la crescente gravità dell’infertilità. Si ritiene che il danno al DNA dello sperma sia aumentato negli uomini con infertilità e precedenti studi suggeriscono una correlazione tra frammentazione del DNA spermatico e aneuploidia.
Gli spermatozoi immaturi valutati dalla cromatina spermatica mostrano un livello più elevato di frammentazione del DNA, espresso come indice di frammentazione del DNA (DFI). È fondamentale considerare che, poiché la capacità di riparazione del DNA da parte dell’ovocita è limitata, è possibile che spermatozoi con DNA frammentato penetrino nell’ovocita, compromettendo lo sviluppo dell’embrione in termini di velocità e correttezza.
Dinamiche di sviluppo in vitro e tempistiche di coltura
Le cliniche di riproduzione assistita osservano costantemente la morfocinetica degli embrioni tramite sistemi Time-lapse. Una questione di grande dibattito clinico riguarda la tempistica del trasferimento, in particolare se la formazione ritardata di blastocisti (al 6° giorno anziché al 5°) sia indice di una minore qualità genetica.
Studi analitici su ampi campioni indicano che le morule che progrediscono allo stadio di blastocisti al 6° giorno hanno significativamente meno probabilità di essere aneuploidi (79,8%) rispetto alle morule che non progrediscono. È interessante notare che, confrontando le blastocisti formatesi al 5° giorno rispetto a quelle del 6°, non si evidenziano differenze sostanziali nei tassi di aneuploidia. Pertanto, il ritardo nella formazione della blastocisti non è intrinsecamente associato a un aumento drastico delle percentuali di aneuploidie rispetto ai campioni che non raggiungono mai tale stadio.
FASI DI UN TRATTAMENTO FIVET (Fecondazione In Vitro). Coltura embrionale
L'età materna come fattore determinante
La ragione più sostenuta dagli esperti per l'insorgenza delle aneuploidie è legata alla produzione dei gameti, influenzata profondamente dall’età della donna. Con l’avanzare dell’età materna, aumenta la probabilità che gli ovociti presentino un corredo cromosomico anomalo a causa di errori nella non-disgiunzione durante la meiosi I.
Le statistiche sono chiare: gli embrioni anomali costituiscono in media il 35% degli embrioni generati da una donna di 35 anni, una percentuale che aumenta progressivamente fino ad arrivare a circa l’85% in una donna di 44 anni. La classificazione morfologica convenzionale non è in grado di identificare lo stato cromosomico di un embrione; pertanto, la diagnosi genetica preimpianto diviene una risorsa tecnologica imprescindibile per il management clinico del paziente.
Diagnosi Genetica Preimpianto (PGT-A): Oltre la morfologia
Il PGT-A (Preimplantation Genetic Testing for Aneuploidy) permette di analizzare il corredo cromosomico degli embrioni prima del trasferimento. La procedura prevede una biopsia del trofoectoderma allo stadio di blastocisti (giorno 5 o 6), dove vengono prelevate 5-8 cellule. Queste cellule sono successivamente analizzate tramite la tecnica Next Generation Sequencing (NGS).
È importante sottolineare che il PGT-A non "migliora" l'embrione, ma ne consente la selezione. I vantaggi principali includono:
- Aumento delle probabilità di successo per transfer eseguito.
- Riduzione del rischio di aborto spontaneo, portandolo a circa il 10% per embrioni euploidi.
- Abbreviazione del tempo necessario per ottenere una gravidanza a termine.
Il fenomeno del mosaicismo embrionale
Oltre all'euploidia e all'aneuploidia completa, esiste il mosaicismo embrionale, una condizione in cui nell'embrione coesistono linee cellulari normali e anormali. Il mosaicismo si verifica a causa di errori nella divisione mitotica post-fecondazione.
In passato, le tecnologie meno avanzate avrebbero classificato questi embrioni esclusivamente come aneuploidi, escludendoli dal trasferimento. Oggi, previa consulenza genetica approfondita, alcuni centri valutano il trasferimento di embrioni a mosaico, qualora non siano disponibili embrioni euploidi, poiché la presenza di cellule sane può ancora permettere lo sviluppo di una gravidanza sana, monitorabile tramite successiva diagnosi prenatale.
Applicazioni cliniche e criteri di selezione
La Società Italiana di Genetica Umana (SIGU) identifica chiaramente i gruppi di pazienti che traggono il massimo beneficio dal PGT-A:
- Pazienti con età materna avanzata (>35 anni).
- Casi di ripetuti fallimenti di impianto (>3 cicli senza gravidanza).
- Coppie con storia di ripetuti aborti spontanei.
- Fattori maschili gravi che necessitano di prelievo chirurgico degli spermatozoi.
L'integrazione di queste tecnologie in un percorso di fecondazione in vitro con microiniezione (ICSI) permette di ottimizzare la scelta dell'embrione da trasferire, riducendo drasticamente il carico emotivo e fisico dei pazienti associato ai tentativi fallimentari. La ricerca continua a dimostrare che, per pazienti sopra i 37 anni, il trasferimento di un singolo embrione euploide garantisce risultati clinici superiori rispetto al trasferimento di molteplici blastocisti non testate, confermando l'importanza della precisione diagnostica nella medicina della riproduzione contemporanea.
tags: #anuploide #percentuale #di #attecchimento