La villocentesi è una procedura medica invasiva che offre una finestra cruciale sulla salute genetica del feto. Attraverso il prelievo di villi coriali, tessuti placentari che condividono lo stesso patrimonio genetico dell'embrione, è possibile individuare e diagnosticare una vasta gamma di anomalie cromosomiche e malattie genetiche. Questa tecnica, eseguita sotto guida ecografica, permette di ottenere informazioni vitali per una gestione informata della gravidanza, fornendo ai futuri genitori la tranquillità o la preparazione necessarie per affrontare eventuali diagnosi.
Comprendere la Villocentesi: Procedura e Tempistiche
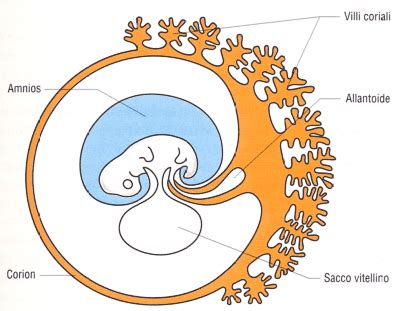
La villocentesi è una tecnica di diagnosi prenatale che consente di effettuare un prelievo di villi coriali dalla placenta. Questo prelievo avviene inserendo un ago sottile, sotto guida ecografica, attraverso l'addome materno. I villi coriali sono costituiti da cellule che derivano dallo stesso uovo fecondato che dà origine all'embrione e alla placenta. Pertanto, il loro patrimonio genetico è identico a quello dell'embrione, rendendoli un campione ideale per l'analisi genetica. Le cellule dei villi, una volta prelevate, vengono coltivate in vitro e successivamente studiate per analizzare il loro assetto cromosomico o il loro DNA. L'esame dei villi coriali è primariamente indicato per esaminare il cariotipo fetale, allo scopo di evidenziare la presenza di eventuali anomalie cromosomiche, o per la diagnosi di specifiche malattie genetiche.
La villocentesi può essere eseguita a partire dall'11ª settimana di gestazione, offrendo un vantaggio di precocità diagnostica rispetto all'amniocentesi, che solitamente viene eseguita più avanti nella gravidanza. Questa tempistica anticipata è particolarmente utile in presenza di patologie, poiché consente una gestione più tempestiva del caso. La procedura, pur essendo invasiva, è generalmente ben tollerata. L'operatore esegue preliminarmente un esame ecografico per confermare l'epoca gestazionale, il numero dei feti, la loro vitalità e morfologia, la quantità di liquido amniotico e la localizzazione placentare. Il prelievo dei villi coriali viene eseguito sotto controllo ecografico, per via transaddominale. Un ago sottile viene inserito lungo la placenta, parallelamente alle membrane, per minimizzare il rischio di perforazioni, e i villi vengono aspirati con un movimento ripetuto di va e vieni. La tecnica descritta è quasi indolore e dura pochi secondi, circa 20. Altri operatori possono utilizzare una tecnica a doppio ago, considerata da alcuni più traumatica e invasiva. Il materiale aspirato viene posto in una capsula sterile; in rarissimi casi, se la quantità è insufficiente, si procede a una seconda aspirazione.
Come viene eseguita la villocentesi - Altamedica Artemisia Roma
Indicazioni Principali per la Villocentesi
Le principali indicazioni per sottoporsi alla villocentesi sono simili a quelle dell'amniocentesi e includono:
- Età materna maggiore di 35 anni: L'incidenza di anomalie cromosomiche, come la Sindrome di Down, aumenta con l'età materna. Sebbene le donne più giovani possano avere figli con anomalie, il rischio è statisticamente più elevato nelle donne over 35. Ad esempio, a 20 anni il rischio di Sindrome di Down è di circa 1:1105, a 30 anni sale a 1:723, e a 40 anni raggiunge 1:92.
- Risultato positivo dei test di screening: Test di screening del primo trimestre, come la misurazione della traslucenza nucale (NT), possono indicare un rischio aumentato di anomalie cromosomiche.
- Traslucenza Nucale (NT) elevata: Un valore elevato della NT all'ecografia del primo trimestre è un indicatore di potenziale rischio.
- Malformazioni fetali rilevate all'ecografia: La presenza di anomalie strutturali del feto può suggerire la necessità di un'indagine genetica più approfondita.
- Analisi del DNA per malattie genetiche: Se vi è il sospetto o la storia familiare di specifiche malattie genetiche.
- Alterazioni cromosomiche nei genitori: Se uno o entrambi i genitori presentano alterazioni cromosomiche note.
- Storia familiare di aneuploidie o malattie genetiche: La presenza di casi pregressi nella famiglia aumenta la probabilità di ricorrenza.
- Pregressa aneuploidia fetale: Aver avuto in precedenza un feto con anomalie cromosomiche.
Anomalie Cromosomiche: Il Focus Principale della Villocentesi
I cromosomi sono le strutture all'interno delle cellule che contengono il nostro DNA e le informazioni genetiche. Normalmente, ogni cellula umana possiede 46 cromosomi, organizzati in 23 coppie. Queste coppie derivano in parti uguali dal padre e dalla madre. Le anomalie cromosomiche possono riguardare il numero (aneuploidia) o la struttura dei cromosomi.
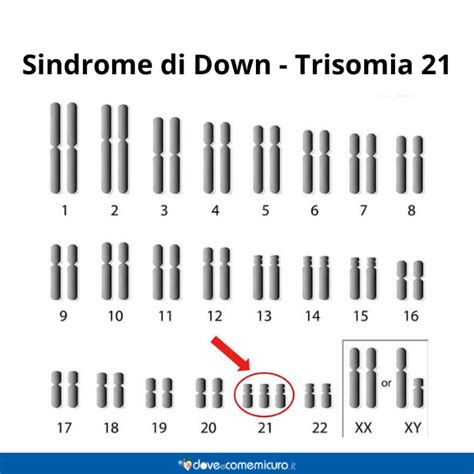
Sindrome di Down (Trisomia 21)
Il caso più noto e frequente di anomalia cromosomica è la Sindrome di Down, causata dalla presenza di un cromosoma 21 in eccesso (47 cromosomi totali invece di 46). Questo stato è definito Trisomia 21.
Altre Aneuploidie Comuni
La villocentesi è particolarmente efficace nell'identificare le aneuploidie cromosomiche più comuni, che includono:
- Sindrome di Edwards (Trisomia 18): Caratterizzata dalla presenza di un cromosoma 18 in eccesso.
- Sindrome di Patau (Trisomia 13): Causata da un cromosoma 13 in eccesso.
- Aneuploidie dei cromosomi sessuali (X e Y): Come la Sindrome di Turner (monosomia X, 45,X) o la Sindrome di Klinefelter (XXY, 47,XXY).
Il nostro Centro offre una risposta rapida su queste aneuploidie comuni mediante una tecnica molecolare avanzata di amplificazione genica (PCR), nota come Quantitative Fluorescent - Polimerase Chain Reaction (QF-PCR). Questa tecnica completamente automatizzata consente di ottenere risultati in sole 24/48 ore, fornendo una valutazione estremamente attendibile.
Diagnosi di Malattie Genetiche Specifiche
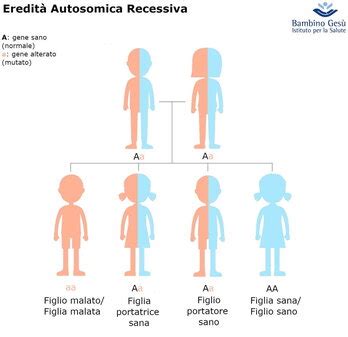
Oltre alle anomalie cromosomiche, la villocentesi permette di diagnosticare specifiche malattie genetiche determinate da alterazioni di singoli geni. Queste malattie sono spesso trasmesse con modalità autosomica recessiva, il che significa che i genitori possono essere portatori sani, ignari della loro condizione.
Fibrosi Cistica (FC)
La fibrosi cistica è una grave malattia ereditaria che colpisce circa 1 bambino su 2500 alla nascita. È causata da mutazioni nel gene CFTR (Cystic Fibrosis Transmembrane Regulator). Nei pazienti affetti, le secrezioni corporee (muco, sudore, saliva) sono molto più dense e viscose del normale, causando problemi respiratori e infezioni polmonari.
La FC si trasmette con modalità autosomica recessiva. Gli individui con una sola copia alterata del gene sono portatori sani, senza sintomi. Se entrambi i genitori sono portatori sani, ogni figlio ha una probabilità del 25% di essere affetto, del 50% di essere portatore sano e del 25% di essere sano.
Attraverso un test genetico sul liquido amniotico o sui villi coriali, è possibile ricercare le mutazioni più frequenti che causano la FC (screening di 34 o 48 mutazioni). Questo screening permette di identificare circa l'85% dei casi di FC nella popolazione. Tuttavia, permane un rischio residuo di circa 1 su 500 per la presenza di mutazioni più rare.
Sindrome dell'X Fragile
La Sindrome dell'X Fragile è una malattia ereditaria causata dall'alterazione del gene FMR1, localizzato sul cromosoma X. Colpisce più frequentemente i maschi. La causa è solitamente l'espansione di una sequenza ripetuta di DNA (CGG) nel gene FMR1. Nelle persone normali, queste ripetizioni variano da 5 a 58, mentre nelle persone affette superano le 200. Un numero intermedio di ripetizioni (59-200) può rendere un individuo portatore "premutato" senza causare la malattia.
Distrofia Muscolare di Duchenne (DMD)
La DMD è una malattia determinata da alterazioni del gene della distrofina, situato sul cromosoma X. Queste mutazioni causano l'assenza totale della proteina distrofina, essenziale per la salute muscolare. La DMD si manifesta tipicamente nei maschi, mentre le femmine sono solitamente portatrici sane, grazie alla presenza di un secondo cromosoma X che compensa la funzione. Le mutazioni più frequenti sono delezioni di ampi tratti del gene.
Sordità Congenita
La sordità congenita è una condizione comune. L'analisi molecolare prenatale del gene CX26 (che codifica per la proteina connexina 26) permette di ricercare le mutazioni più frequenti responsabili di circa la metà dei casi di sordità ereditaria. Sono state identificate circa 90 mutazioni del gene CX26, e il nostro screening raggiunge un'accuratezza dell'80-90% per le mutazioni più comuni.
Integrazione Diagnostica: Tecniche Molecolari Avanzate
La villocentesi può essere integrata da diagnostica prenatale molecolare avanzata per una copertura diagnostica più ampia.
QF-PCR per Aneuploidie
Come menzionato, la Quantitative Fluorescent - Polimerase Chain Reaction (QF-PCR) è una tecnica molecolare rapida ed efficiente per la rilevazione delle aneuploidie più comuni (cromosomi 13, 18, 21, X e Y) in 24-48 ore.
Array-CGH (Cariotipo Molecolare)
La tecnica microarray-Comparative Genomic Hybridization (Array-CGH) è un approfondimento diagnostico di secondo livello che utilizza la biologia molecolare. A differenza della coltura cellulare tradizionale, non richiede questo passaggio, riducendo i tempi diagnostici a 3-5 giorni. L'Array-CGH può identificare non solo le aneuploidie tradizionali, ma anche patologie derivanti da alterazioni cromosomiche submicroscopiche, non visibili con il cariotipo tradizionale (es. Sindrome di DiGeorge, Cri-du-chat, Prader-Willi). È particolarmente indicata in feti con malformazioni o elevata traslucenza nucale.
Diagnostica Prenatale Molecolare Infettivologica
In caso di necessità diagnostica, la villocentesi Genetica può essere integrata dalla ricerca di agenti infettivi tramite tecniche molecolari (PCR). Queste tecniche ricercano direttamente il genoma dell'agente infettivo (come Citomegalovirus, Herpes simplex, Varicella Zooster, Rubeovirus, HIV, Toxoplasma gondii, Parvovirus), superando i limiti dei metodi tradizionali che si basavano sulla produzione anticorpale fetale (IgM), la cui accuratezza è influenzata dalla maturità del sistema immunitario fetale.
Rischi e Gestione della Procedura
La villocentesi, come ogni procedura invasiva, comporta dei rischi, seppur generalmente bassi. Il rischio di aborto spontaneo viene quantificato tra lo 0,5-1%, ovvero 1 caso ogni 100-200 procedure. L'incidenza di aborto e complicanze è strettamente legata all'esperienza dell'operatore. In centri specializzati con operatori esperti, questo rischio può essere significativamente ridotto. Nella nostra casistica, l'esperienza degli operatori ha permesso di ridurre il rischio di aborto sotto lo 0,5% e di azzerare quasi le complicanze.
Consigli Post-Procedura
Si consiglia di assumere un antispastico dal giorno precedente l'esame e di rimanere a riposo per 2-3 giorni a casa. È sconsigliabile eseguire l'esame in presenza di febbre materna o minaccia di aborto in corso.
Gestione Madre Rh Negativa
Nel caso di madri con Rh negativo, è opportuno eseguire l'immunoprofilassi anti-D dopo la villocentesi per prevenire la possibile formazione di anticorpi anti-Rh.
Villocentesi Tradizionale vs. Tecniche Molecolari Avanzate
È importante comprendere le differenze tra la villocentesi tradizionale e le opzioni più avanzate:
- Villosintesi Tradizionale di Base: Indaga principalmente le anomalie nel numero e nell'aspetto grossolano dei cromosomi. Non fornisce informazioni su piccole alterazioni cromosomiche o su geni specifici.
- Villosintesi con Studio Parziale del DNA: Oltre allo studio tradizionale dei cromosomi, include la ricerca delle mutazioni principali che causano le malattie geniche più frequenti.
- Villosintesi Genomica (TRIO): Rappresenta l'indagine più ampia disponibile, utilizzando tecniche sofisticate di analisi del DNA, inclusi i panel basati sullo studio dell'esoma. Questo approccio può diagnosticare una percentuale molto alta di malattie genetiche note, escludendo quelle estremamente rare, di origine incerta o per le quali non è eticamente opportuno indagare.
La scelta del tipo di analisi da eseguire deve essere discussa con il proprio medico, tenendo conto della storia familiare e delle preoccupazioni individuali. La villocentesi, con le sue diverse opzioni diagnostiche, rappresenta uno strumento fondamentale per la salute perinatale, offrendo la possibilità di una diagnosi precoce e di una gestione informata della gravidanza.
tags: #villocentesi #che #malattie #individua