La gravidanza è un periodo di profondi cambiamenti fisiologici per il corpo di una donna, e tra questi, la tiroide gioca un ruolo cruciale. Questa fondamentale ghiandola, situata nel collo, ha il compito di produrre una serie di ormoni che rivestono importanti funzioni nel meccanismo dell'intero organismo. Le alterazioni nella produzione di ormoni tiroidei in gravidanza sono estremamente frequenti, tuttavia vanno monitorate con attenzione. Il TSH (ormone tireostimolante) è prodotto dall’ipofisi e rappresenta il principale indicatore per valutare la funzionalità della tiroide. Questo ormone stimola la tiroide a produrre e rilasciare gli ormoni tiroidei T3 (triiodotironina) e T4 (tiroxina).
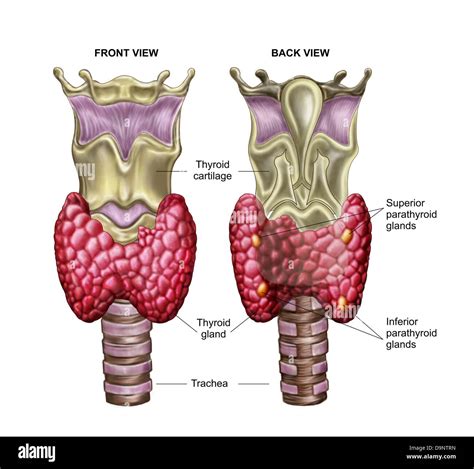
Durante la gravidanza, il corpo della donna si adatta per sostenere la crescita e lo sviluppo del feto, e la tiroide non fa eccezione. Già dalla 7ª settimana di gestazione aumenta la concentrazione di T4, che raggiunge il picco intorno alla 16ª settimana e resta elevata fino al parto. La tiroide aumenta leggermente di volume e la produzione di T4 cresce per soddisfare i bisogni del feto. Questo comporta tra l’altro un maggior fabbisogno di iodio, che durante la gravidanza passa da 150 a circa 250 microgrammi al giorno.
Comprendere il TSH e i suoi Valori in Gravidanza
Cosa significa avere il TSH basso in gravidanza? Si tratta di una condizione in cui la concentrazione di ormone tireostimolante nel sangue è inferiore ai valori di riferimento considerati normali. Generalmente, i valori normali di TSH si attestano tra 0,4 e 4,0 mUI/L (milliunità internazionali per litro). Quando i livelli scendono al di sotto di 0,4 mUI/L, si parla di TSH basso. È importante sottolineare che i valori di riferimento possono variare leggermente in base ai laboratori e alla popolazione di riferimento, e che i livelli di riferimento del TSH sono diversi durante la gravidanza, con il range di normalità che varia a seconda del trimestre.
Il calo del TSH è più marcato nel primo trimestre, per poi risalire gradualmente nel secondo e terzo trimestre, senza mai tornare ai valori pre-gravidanza. L'ormone hCG, prodotto fisiologicamente dalla placenta, può modificare leggermente la produzione degli ormoni tiroidei, i quali determinano poi la presenza di un valore di TSH in gravidanza basso, in particolare durante il primo trimestre. Questo effetto degli elevati livelli di hCG stimola la tiroide sana e si associa a nausea e vomito insistenti, caratterizzando l'ipertiroidismo gestazionale, una sorta di falso ipertiroidismo che colpisce l’1-3% delle gravidanze e si verifica nella prima metà della gravidanza, con maggiore frequenza nelle gravidanze gemellari.
Le cause del TSH basso possono essere molteplici e spesso richiedono un'indagine approfondita per essere identificate correttamente. Una delle principali ragioni è l'ipertiroidismo, una condizione in cui la ghiandola tiroidea produce una quantità eccessiva di ormoni tiroidei. Questo eccesso porta a una diminuzione della produzione di TSH da parte dell'ipofisi, in un tentativo di regolare la funzione tiroidea. Oltre all'ipertiroidismo, altre cause possono portare a un TSH basso, tra cui l'assunzione di determinate terapie farmacologiche, come i corticosteroidi o la terapia sostitutiva con ormoni tiroidei in dosi eccessive. Anche alcune condizioni mediche non direttamente legate alla tiroide possono influenzare i livelli di TSH, come disturbi dell'ipofisi o malattie sistemiche gravi.
L'Ipertiroidismo in Gravidanza: Una Causa Chiave del TSH Basso
L’ipertiroidismo è una sindrome clinica a diversa eziologia caratterizzata da un incremento della produzione degli ormoni tiroidei. I sintomi dell’ipertiroidismo variano in funzione della gravità della malattia e tipicamente consistono in un aumento della frequenza cardiaca (tachicardia) spesso superiore a 100 battiti per minuto, perdita di peso (dimagramento), stanchezza, irritabilità, ansietà, insonnia e vomito (iperemesi). Alcuni sintomi tipici della gravidanza possono essere accentuati, come la tendenza a facile affaticamento, l’intolleranza al caldo e l’ipersudorazione. Talvolta è ben evidente un gozzo, cioè l’ingrandimento diffuso della ghiandola tiroidea posta nella regione anteriore del collo. Nella storia familiare di queste donne è frequente il riscontro di altri casi di patologia tiroidea.
Gravidanza e ipertiroidismo sono due condizioni che, quando presenti insieme, vanno monitorate con attenzione attraverso regolari analisi del sangue. L'ipertiroidismo non controllato può portare ad effetti sia sulla madre che sul feto, che vanno da una maggiore probabilità di aborto a problemi cardiovascolari per la madre, fino all’aumento del rischio di morte perinatale. I neonati di queste pazienti possono presentare anche un’alterata funzione tiroidea e hanno una maggiore incidenza di mortalità prenatale.
La diagnosi di ipertiroidismo, oltre che sul quadro clinico, si basa su indagini ormonali di laboratorio. Nell’ipertiroidismo tipicamente FT3 ed FT4 saranno più alti del normale (in alcuni casi può aumentare solo l’FT3) ed il TSH sarà molto basso o indosabile. Trattandosi nella gran parte dei casi di una malattia autoimmune (cioè scatenata e mantenuta da una auto-aggressione del proprio sistema di difesa immunitario), il dosaggio degli anticorpi non solo è importante per la diagnosi ma lo è anche per il monitoraggio della malattia. Il morbo di Basedow è la causa più comune di ipertiroidismo in gravidanza e può portare a complicanze ostetriche anche gravi se non trattato.
Gestione Terapeutica dell'Ipertiroidismo in Gravidanza
Il trattamento dell’ipertiroidismo in gravidanza pone alcuni problemi perché ogni scelta terapeutica deve tener conto della presenza del feto e del passaggio transplacentare dello iodio e dei farmaci impiegati nel trattamento della tireotossicosi. In gravidanza le scelte terapeutiche per l’ipertiroidismo sono limitate al trattamento farmacologico e all’intervento di tiroidectomia. Nella maggior parte delle gravide ipertiroidee l’iperfunzione ghiandolare viene controllata somministrando i farmaci antitiroidei, che rappresentano la terapia di prima scelta.
La terapia farmacologica tiroidea in gravidanza
Le tionamidi (metimazolo/MMI, carbimazolo e propiltiouracile/PTU) bloccano la sintesi degli ormoni tiroidei, inibendo l’organificazione e l’incorporazione dello ioduro nei residui tirosinici della tireoglobulina e il successivo accoppiamento delle iodotirosine. Il propiltiouracile (PTU), oltre a bloccare la sintesi degli ormoni tiroidei, agisce anche sui tessuti periferici inibendo la conversione della T4 a T3, l’ormone metabolicamente attivo. Seppure sia stato suggerito che il PTU possa essere preferibile in gravidanza, molti ritengono MMI ugualmente sicuro ed efficace. Dati che dimostrerebbero un legame tra somministrazione di MMI con l’aplasia cutis ed altre malformazioni del neonato sembrerebbero controversi e non conclusivi.
Il metimazolo (MMI) è il farmaco più utilizzato in Europa, mentre il propiltiouracile (PTU) è il farmaco di scelta negli Stati Uniti. Quest’ultimo inoltre non è commercialmente disponibile in Italia, ma può essere comunque ottenuto su prescrizione medica “galenica” in alcune farmacie. Nel primo trimestre è consigliabile sostituire il metimazolo con il propiltiouracile, per poi tornare al metimazolo dal secondo trimestre di gravidanza in poi. Le dosi “di attacco” nei franchi ipertiroidismi sono generalmente di 20-30 mg di MMI e 200-400 mg di PTU suddivise in due (MMI) o tre (PTU) somministrazioni giornaliere. Le tionamidi, a dosi appropriate, non interferiscono con la funzione tiroidea fetale e la terapia con tionamidi nel primo trimestre di gravidanza non ha effetti sul successivo sviluppo intellettivo. Al contrario, l’aumentata frequenza di malformazioni congenite nei neonati di donne ipertiroidee non trattate in gravidanza si riduce nettamente se la funzione tiroidea è normalizzata dalla terapia con tionamidi.
Talvolta, per il controllo della sintomatologia cardiaca materna (tachicardia) e dell’ipertensione, può essere indispensabile l’utilizzo di farmaci beta-bloccanti. Il propanololo è molto usato ma anche l’atenololo è un ottimo farmaco. Queste molecole non sono controindicate in gravidanza e consentono anche di controllare e migliorare tremori ed ansietà spesso presenti in situazioni di elevata frequenza cardiaca. Il monitoraggio di queste pazienti e del feto costituisce un altro momento di fondamentale importanza. Mensilmente è bene controllare anche l’emocromo ed il dosaggio di TSH, FT3, FT4. Il dosaggio dell’FT4 ha una particolare importanza e l’obiettivo è quello di mantenerlo nei limiti medio-alti della norma.
Nelle donne ipertiroidee che desiderano programmare una gravidanza è consigliabile ottenere prima un buon controllo della malattia fino ad arrivare ad assumere dosi basse del farmaco anti-tiroideo; a quel punto si può provare. In alternativa, si potrebbe risolvere il problema dell’ipertiroidismo alla radice, prima di affrontare la gravidanza, ad esempio asportando la tiroide chirurgicamente. Dopo il parto, il puerperio e l’allattamento richiedono particolare attenzione sia a livello materno che neonatale. Mamma e neonato vanno attentamente controllati, clinicamente e laboratoristicamente; nel neonato è importante cercare anche i TRAb.
Il Ruolo Cruciale della Tiroide nello Sviluppo Fetale e le Conseguenze degli Squilibri
La tiroide ha un ruolo cruciale durante la gravidanza, sia per la salute della donna che per quella del bambino. Gli ormoni tiroidei giocano un ruolo cruciale sia per la fertilità che nel consentire di portare a termine una gravidanza normale e soprattutto per il normale sviluppo del sistema nervoso del bambino. Perché alterazioni anche lievi della funzione tiroidea, sia in senso di aumentata funzione (ipertiroidismo) che ridotto funzionamento (ipotiroidismo), possono influenzare lo sviluppo neurologico del feto, l’andamento della gestazione e il benessere della madre.
Nel primo trimestre di gravidanza, il feto non ha ancora sviluppato la propria tiroide e dipende quindi completamente dagli ormoni tiroidei materni. All'inizio della gravidanza, il trasferimento materno di tiroxina (T4) contribuisce in modo significativo ai fabbisogni del feto di questo ormone tiroideo fino a quando la tiroide fetale non diventa funzionale e indipendente (intorno alla 12° settimana di gravidanza). Questo ormone aumenta rapidamente nei fluidi fetali ed il suo livello è determinato dalla disponibilità materna di T4; il trasferimento materno costituisce quindi un processo cruciale e continua ad avere un importante ruolo protettivo nel neurosviluppo del feto fino al momento della nascita.
Se la madre in gravidanza è ipotiroidea, il sistema nervoso fetale può essere danneggiato dalla mancanza di tiroxina materna nelle prime settimane di gestazione, quando la tiroide del feto non è ancora capace di produrre ormoni, o successivamente se la tiroide del feto è ipofunzionante. Questa situazione può verificarsi nelle gestanti esposte a grave carenza iodica, che è causa di ipotiroidismo materno, fetale e neonatale. Per questo motivo, il trattamento immediato dell'ipotiroidismo materno è fondamentale per mitigare un effetto negativo sulla donna e sul suo bambino. L’ipotiroxinemia in gravidanza, ovvero una condizione caratterizzata da bassi livelli di concentrazione di T4 nel sangue e concentrazioni normali di ormone stimolante la tiroide (TSH), è stata descritta in casi di parti prematuri.
Inoltre, l'ipotiroidismo subclinico materno e l'ipotiroidinemia sono state in passato associate a riduzioni del quoziente intellettivo infantile, abilità aritmetiche, prestazioni scolastiche e abilità motorie, oltre a tempi di reazione più poveri, ritardi nell'attenzione e maggiori sintomi di disturbo da deficit di attenzione e iperattività. Studi ulteriori hanno ampiamente confermato che lo sviluppo psicomotorio e mentale è ritardato nei bambini nati da madri con valori di FT4 sotto il decimo percentile alla 12a settimana di gestazione.
Ma quali condizioni possono influire sulla funzione tiroidea materna? Malnutrizione o anemia durante il periodo della gravidanza sono state segnalate come possibili fattori di rischio in grado di alterare la funzione tiroidea materna, sospendendo di conseguenza il trasferimento dell'ormone tiroideo al feto e portando, nei casi più gravi, alla compromissione dello sviluppo del cervello fetale. Per questo è fondamentale che la donna in gravidanza, oltre a monitorare i suoi valori tiroidei, segua una dieta bilanciata e ricca di tutti i macro- e micro-nutrienti, in particolare di iodio e selenio.
Ipotiroidismo in Gravidanza: Diagnosi e Trattamento
L’ipotiroidismo è una condizione in cui la tiroide non produce una quantità sufficiente di ormoni. La prevalenza dell’ipotiroidismo in gravidanza è minore rispetto a quella rilevata nella popolazione generale perché l’ipotiroidismo è causa, di per sé, di ridotta fertilità, ed è una patologia più frequente dopo la quinta decade di vita. Le cause più comuni di ipotiroidismo in gravidanza sono la tiroidite autoimmune, l’ipotiroidismo post ablativo per morbo di Basedow e quello post-tiroidectomia per carcinoma della tiroide o gozzo. L’aumento dei valori del TSH nel siero è l’indice più sensibile e specifico per la diagnosi di ipotiroidismo primitivo in gravidanza. Spesso il TSH è elevato e gli ormoni tiroidei, FT4 e FT3, sono nella norma (ipotiroidismo subclinico).
Una condizione di ipotiroidismo nel primo trimestre di gravidanza può avere serie ripercussioni sullo sviluppo neurologico del bambino e sul suo quoziente intellettivo. Ma anche nel secondo e terzo trimestre, un ipotiroidismo materno può aumentare il rischio di sofferenza fetale e di basso peso alla nascita o provocare un parto prematuro. La tiroidite cronica autoimmune (tiroidite di Hashimoto) è la causa principale di ipotiroidismo in una donna in età fertile. Questa è una condizione che si associa ad un rischio aumentato di poliabortività, non solo per la cattiva funzionalità della tiroide, ma anche per la presenza di un sistema immunitario iperattivo, che può determinare aborti precocissimi nelle prime settimane di gravidanza.
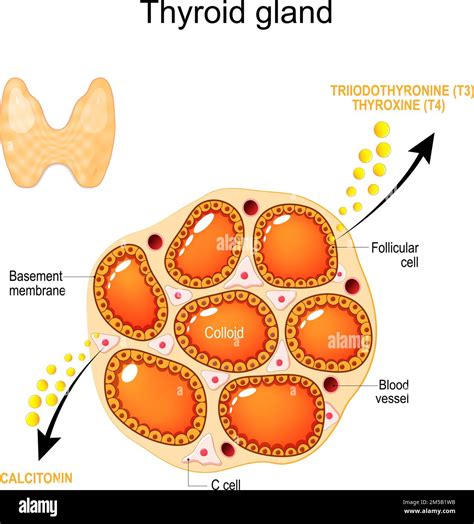
La terapia sostitutiva tiroidea deve essere effettuata in tutte quelle occasioni in cui si è in presenza di una ipofunzione della produzione degli ormoni tiroidei T4 e T3. Il farmaco di scelta per il trattamento sostitutivo dell’ipotiroidismo è la l-tiroxina (L-T4), un preparato sintetico, chimicamente puro, che assicura una potenza uniforme. La sua azione si esplica dopo conversione periferica in T3. Altro vantaggio della somministrazione di l-tiroxina è che il preparato ha una emivita biologica abbastanza lunga, consentendo il mantenimento di un livello costante di ormoni tiroidei durante le 24 ore con un’unica somministrazione giornaliera. La L-T4 deve essere assunta a digiuno 20 minuti prima della colazione. In presenza di vomito è comunque possibile assumere L-T4 anche dopo aver mangiato.
In assenza di controindicazioni cardiache, è sempre consigliabile raggiungere lo stato di normale funzione tiroidea o eutiroidismo nel più breve tempo possibile per evitare le complicanze dell’ipotiroidismo sul decorso della gestazione e sul prodotto del concepimento. Nelle donne già in terapia sostitutiva con L-tiroxina (o perché tiroidectomizzate o perché in ipotiroidismo per una tiroidite autoimmune), durante la gravidanza devono aumentare del 30-50% il dosaggio abituale del farmaco, per far fronte a questa maggiore richiesta di ormoni tiroidei materni. L’incremento della dose di tiroxina necessario a mantenere l’eutiroidismo è di solito maggiore nelle pazienti con ipotiroidismo post terapia ablativa per morbo di Basedow o carcinoma della tiroide rispetto a quelle con tiroidite autoimmune. In uno studio recente l’aumento medio della dose di L-T4 necessario per mantenere il TSH nella norma era del 45% (50 µg/die) nelle gravide con ipotiroidismo postablativo e del 25% (28 µg/die) in quelle con ipotiroidismo autoimmune.
L’aumentato fabbisogno di L-T4 può rendersi evidente già nelle prime 4 settimane dal concepimento. In tutte le ipotiroidee che entrano in gravidanza è quindi consigliabile misurare il TSH immediatamente dopo la prima mancanza mestruale. Se in questa fase precoce della gestazione il TSH sierico non è ancora aumentato, il dosaggio deve essere ripetuto ogni 40 giorni poiché la necessità di aumentare la dose può rendersi evidente anche in fasi più avanzate della gravidanza. Uno studio prospettico recente ha dimostrato un aumentato fabbisogno di L-T4 nell’85% della popolazione studiata. In questi soggetti l’incremento medio di L-T4 era del 47% e l’incremento della dose era necessario nelle prime 16-20 settimane. La raccomandazione pratica che ne deriva è che tutte le donne ipotiroidee in trattamento con L-T4 dovrebbero aumentare la dose di L-T4 di circa il 30% al momento della conferma dell’inizio della gravidanza, ancora prima di eseguire i dosaggi ormonali. Il solfato ferroso, somministrato frequentemente in gravidanza per correggere la carenza di ferro, può ridurre l’assorbimento della L-tiroxina se i due farmaci sono assunti contemporaneamente. Dopo il parto, la dose di l-tiroxina dovrebbe essere ridotta e riportata alla dose precedente alla gravidanza.
La terapia farmacologica tiroidea in gravidanza
Quando è necessaria una terapia con LT4, questa può essere effettuata con l’accortezza di iniziare sempre con dosi subottimali e di incrementarle progressivamente. Se in caso di un valore di TSH circolante compreso fra 2.5 e 4 mU/L, si suggerisce di iniziare la terapia con ormone tiroideo accompagnato da una terapia antiossidante come il selenio e la vitamina D3, come anti-infiammatoria e anticoagulanti. È importante sapere che i rischi di una ipofunzione tiroidea, anche subclinica, sono tali da non giustificare tentativi di sospensione della terapia sostitutiva con L-T4.
Malattie Autoimmuni della Tiroide e Gravidanza
Per comprendere la rilevanza di questo argomento va tenuto presente che la Tiroidite di Hashimoto (chiamata anche tiroidite linfocitaria) è l’infiammazione della tiroide più diffusa al mondo. Nella maggior parte dei casi, invece, l’esordio è lento e spesso asintomatico e per molto tempo la tiroide mantiene una normale produzione ormonale ed i sintomi insorgono solo quando c’è l’evoluzione verso l’ipotiroidismo. L’evoluzione, spesso lenta, verso una ridotta funzionalità tiroidea è infatti frequente. I sintomi tipici dell’ipotiroidismo sono il facile affaticamento, la depressione, l’intolleranza al freddo, la difficoltà di concentrazione e la perdita dei capelli. Si verifica spesso anche un ingrossamento della ghiandola (gozzo) che progressivamente diviene più dura alla palpazione. Questa malattia può essere associata ad altre malattie tipicamente legate ad una alterata funzione del sistema immunitario quali: malattia di Basedow-Graves, gastrite atrofica, morbo celiaco, epatite C, miastenia, cheratocongiuntivite sicca, deficit surrenalico, insufficienza ovarica prematura.
La tiroidite del post-partum (TPP) è una forma particolare di infiammazione tiroidea sempre su base autoimmune che esordisce molto presto dopo il parto, con ipertiroidismo transitorio seguito da ipotiroidismo. La prevalenza della TPP varia, in base ai criteri diagnostici utilizzati ed alle aree geografiche, tra l’1.1 e il 16.7% delle donne nel periodo post-partum, con una media dell’8.1%. Nella forma classica, la prima fase, caratterizzata dalla tireotossicosi, compare dopo 2-6 mesi dal parto e dura circa 1-3 mesi. Questa è sostenuta dal processo tiroiditico che induce il rilascio in circolo degli ormoni tiroidei. Il trattamento della tireotossicosi, quando necessario, si basa sulla severità dei sintomi quali il cardiopalmo, l’irritabilità ed il nervosismo. L’uso delle tionamidi non è indicato, poiché la tireotossicosi è sostenuta da una tiroidite distruttiva che porta al rilascio dell’ormone preformato e non da un’iperfunzione ghiandolare. Il propranololo rappresenta il farmaco di prima scelta, poiché consente una facile titolazione. Il trattamento dura solitamente meno di 3 mesi e la posologia viene aggiustata in base ai livelli di ormoni tiroidei e ai sintomi. La fase ipotiroidea può non richiedere alcuna terapia, mentre viene trattata con L-T4 se l’ipotiroidismo è sintomatico e/o se le concentrazioni di TSH superano le 10 mUI/L. Il potenziale beneficio del trattamento dell’ipotiroidismo subclinico (TSH tra 4.0 e 10.0 mUI/L) include il miglioramento degli eventuali sintomi. È importante sapere che le pazienti che hanno avuto una tiroidite post-partum la potranno ripresentare ad una successiva gravidanza. La tiroidite post-partum può contribuire o peggiorare la depressione del post-partum.
Noduli Tiroidei in Gravidanza: Approccio Diagnostico e Terapeutico
Il nodulo tiroideo costituisce la più frequente patologia tiroidea e, come tutte le malattie della Tiroide, incide più frequentemente nella donna rispetto all’uomo, colpendo circa il 6,4 % di quelle con età tra i 30 ed i 59 anni. In realtà, probabilmente la sua incidenza è ancora più alta, ma non diagnosticata per assenza di sintomatologia. Il riscontro avviene palpatoriamente e/o visivamente (spesso durante un esame clinico) oppure nel corso di un’indagine ecografica mirata alla regione del collo.
La valutazione della funzione tiroidea attraverso il dosaggio del TSH e degli ormoni tiroidei (frazioni libere circolanti) FT3, FT4 è essenziale. Il riscontro di un aumento degli ormoni tiroidei (particolarmente dell’FT3) potrebbe deporre per un nodulo iperfunzionante (adenoma tossico), mentre valori bassi (FT4) con TSH aumentato sono più tipici ad esempio di una tiroidite cronica autoimmune con ipotiroidismo. L’ecografia tiroidea ha un ruolo molto importante nello studio morfologico del parenchima ghiandolare e nella valutazione delle sue dimensioni. La scintigrafia tiroidea, attraverso lo studio della captazione di un isotopo radioattivo dello iodio, aiuta a distinguere i noduli autonomamente funzionanti (noduli caldi, ipercaptanti) da quelli non funzionanti (noduli freddi) o isocaptanti rispetto al resto della ghiandola, ma trova una controindicazione assoluta in gravidanza.
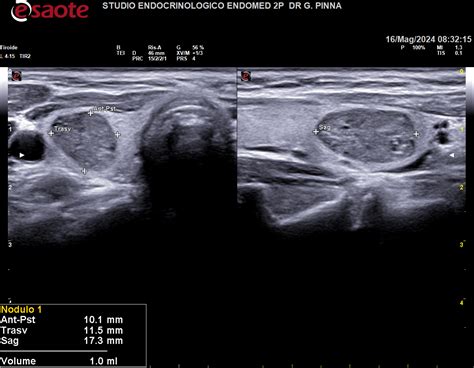
L’agoaspirato costituisce una preziosissima indagine nella diagnosi differenziale tra noduli tiroidei benigni e maligni. Con un ago e sotto controllo ecografico si procede all’aspirazione del nodulo e le cellule così asportate vengono analizzate citologicamente. È importante che il campione sia adeguato ai fini della diagnosi citologica. In gravidanza il riscontro di uno o più noduli tiroidei genera un’ansietà forse anche maggiore del normale e non è giustificato attendere per fare una diagnosi; infatti, gran parte delle indagini può essere fatta anche durante il periodo gestazionale, compreso l’agoaspirato.
La terapia dipende dalla benignità o malignità del nodulo tiroideo, dalla concomitanza di un gozzo e dalle condizioni cliniche generali del paziente, compreso un eventuale stato di gravidanza. Una buona parte (fino a quasi il 50%) dei noduli benigni va incontro a una regressione spontanea. Noduli benigni che hanno dimostrato una crescita documentata o che danno problemi estetici o di compressione possono essere trattati con la somministrazione di levo-tiroxina (LT4); la somministrazione esogena di ormoni tiroidei sopprime infatti la secrezione ipofisaria di TSH e ciò determina in molti casi una significativa riduzione delle dimensioni del nodulo. Il tentativo viene fatto sempre con le dosi minime efficaci e richiede una selezione dei pazienti per escludere controindicazioni. Nei noduli dubbi può essere ragionevole mantenere una stretta sorveglianza e rimandare ulteriori valutazioni e scelte terapeutiche a dopo il parto (in alcuni casi può essere giustificato anche il trattamento con LT4). Nei noduli la cui citologia depone per malignità è indicato l’intervento chirurgico: la scelta del momento operativo dovrebbe tener conto dei rischi potenziali per madre e feto ed andrebbe ampiamente discussa con la paziente. Il rilievo di un carcinoma papillare (il più frequente) non è una indicazione all’interruzione della gravidanza; questi tumori hanno una crescita lenta e scarsa tendenza a metastatizzare; forme più maligne sono fortunatamente molto rare.
Screening e Monitoraggio della Funzione Tiroidea in Gravidanza
Le patologie della tiroide rappresentano la problematica endocrinologica in gravidanza più comune dopo il diabete. Per questo è importante sapere quali controlli della tiroide effettuare prima del concepimento, durante la gravidanza e dopo la nascita del bambino. Una tiroide malfunzionante in eccesso (ipertiroidismo) o in difetto (ipotiroidismo) può dare problemi di fertilità. Se una coppia ha difficoltà a concepire, una delle cose da controllare è proprio la funzionalità tiroidea.
Prima di affrontare una gravidanza, oltre agli esami di routine consigliati dal ginecologo, è importante dosare il TSH per essere certi di affrontare la gravidanza con una tiroide che funziona correttamente, soprattutto se si è over 30 (a quest’età il 7-8% delle donne ha un ipotiroidismo subclinico) o se si ha familiarità per patologie autoimmuni o malattie tiroidee. Se dagli esami emerge un ipotiroidismo, è quindi necessario regolarizzare la funzione tiroidea prima di affrontare la gravidanza. Il medico di famiglia, come richiede un prelievo per esami generali, altresì dovrebbe sempre aggiungere un dosaggio del TSH prima della gravidanza. In caso di presenza di un valore del TSH circolante superiore a 2.5 mU/L, si consiglia di eseguire anche un dosaggio degli anticorpi antitiroidei (AbTg e AbTPO, Ab antirecettore del TSH o TRAb).

Il monitoraggio della funzione tiroidea in gravidanza è semplice e non invasivo. Una donna ipotiroidea che assuma terapia sostitutiva con L-tiroxina deve controllare il TSH prima della gravidanza, poi ogni 4 settimane nel primo trimestre di gravidanza, infine ogni due mesi fino a fine gravidanza; ad ogni cambio di terapia, poi, gli esami vanno ripetuti a distanza due settimane. Alla 32° settimana vanno dosati gli anticorpi anti-recettore del TSH (TRAb) che possono essere presenti nei soggetti ipertiroidei; trattandosi di immunoglobuline della classe IgG, questi possono attraversare la placenta e andare a stimolare la tiroide del feto, esponendolo al rischio di ipertiroidismo fetale/neonatale che è una condizione seria. Questi anticorpi vanno misurati anche nelle donne ipotiroidee per tiroidite cronica autoimmune, perché ne esiste una variante che può essere ‘bloccante’, cioè inibire il TSH; gli anticorpi bloccanti possono permanere nel sangue del neonato per alcuni mesi dopo la nascita e bloccare la sua tiroide che invece deve funzionare alla perfezione, perché altrimenti si possono determinare importanti alterazioni dello sviluppo cerebrale e della mielinogenesi, realizzando una condizione analoga a quella dell’ipotiroidismo congenito. Gli ipotiroidismi neonatali da anticorpi anti-TSH bloccanti sono forme transitorie ma vanno gestiti con attenzione insieme al neonatologo.
Il dosaggio degli anticorpi anti-TSH è consigliabile anche per le donne che sono state trattate con radioiodio o chirurgicamente per un ipertiroidismo da malattia di Graves-Basedow, perché gli anticorpi che causano la malattia possono permanere in circolo per alcuni anni, anche dopo la rimozione della tiroide. Il monitoraggio della funzione tiroidea è consigliato a tutte le donne che desiderano una gravidanza o che si trovano già in stato di gravidanza, in particolare nelle donne considerate a rischio.
Dopo la nascita del bambino, la madre può tornare al dosaggio abituale di L-tiroxina (quello pre-parto). È bene fare un controllo della tiroide a 6-8 settimane dal parto, perché nel post-partum c’è il rischio di una recidiva di ipertiroidismo (in caso di malattia di Graves-Basedow), o del peggioramento di una tiroidite di Hashimoto o della comparsa di una tiroidite del post-partum, che può verificarsi nell’8% delle donne.
Lo iodio è essenziale per la produzione di ormoni tiroidei. La richiesta di iodio aumenta in gravidanza e durante l’allattamento, poiché viene eliminato anche attraverso il latte materno. Una carenza marcata di iodio può portare a un aumento del TSH, sviluppo di gozzo tiroideo e formazione di noduli. Il consiglio è dunque di usare sempre sale iodato, a partire già da diversi mesi prima del concepimento o di assumere supplementi se si è in carenza di iodio. Le fonti principali di iodio sono pesce, latticini e sale iodato.
La buona notizia è che, con un controllo adeguato e una terapia mirata, la maggior parte delle disfunzioni tiroidee può essere gestita efficacemente, garantendo il benessere sia della madre che del bambino.
tags: #tsh #basso #in #gravidanza #rischi