La diagnosi prenatale rappresenta una pietra miliare nella medicina moderna, offrendo ai futuri genitori la possibilità di acquisire informazioni cruciali sulla salute e sullo sviluppo del feto. Tra le metodiche più significative e ampiamente utilizzate, l'amniocentesi si distingue come procedura invasiva che, combinata con avanzate tecniche di analisi molecolare e citogenetica come la FISH (Fluorescence In Situ Hybridization), il QF-PCR e l'Array-CGH, permette di identificare un ampio spettro di anomalie. Questo articolo esplora in dettaglio la tecnica FISH e il suo ruolo nell'amniocentesi, delineando le procedure, le indicazioni, i rischi e le alternative disponibili, fornendo una visione completa delle possibilità diagnostiche attuali.
L'Amniocentesi: Fondamenti e Procedura Dettagliata
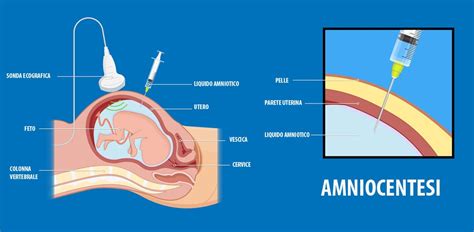
L'amniocentesi è una metodica di diagnosi prenatale invasiva che consiste nel prelievo di una certa quota di liquido amniotico, il liquido nel quale il bambino è immerso durante la sua crescita nell’utero. Lo scopo principale di questo esame è quello di studiare la struttura ed il numero dei cromosomi presenti nel nucleo delle cellule del feto. Questa procedura implica l'introduzione di un ago collegato ad una siringa nella cavità amniotica attraverso la parete addominale della madre.
La Procedura di Prelievo
Il sacco amniotico è la cavità ripiena di liquido (liquido amniotico) nel quale il feto è immerso durante la sua crescita nell’utero. Per prima cosa, quindi, si visualizza, con l’ecografia, il sacco amniotico ed il feto in essa contenuto. Successivamente, si controlla la posizione esatta del bambino e della placenta e si sceglie con cura il punto esatto in cui far passare l’ago che preleverà il liquido amniotico, evitando, se possibile, la placenta ed individuando un’area colma di liquido lontano dal corpo fetale. Se la placenta non può essere evitata, possibilmente, si cercherà di infiggere l’ago nel punto di minore spessore dell’organo. La pelle sopra l’area dell’utero viene disinfettata a lungo con una soluzione antisettica prima dell'inserimento dell'ago. Molte donne hanno riferito come l’Amniocentesi sia fastidiosa ma non veramente dolorosa. Essa dura normalmente qualche minuto. In alcuni casi, dopo l’esecuzione dell’esame, si percepisce una sensazione di tensione al basso ventre o in sede specificamente uterina; queste sensazioni possono durare da pochi minuti a qualche giorno e sono alleviate dalla terapia farmacologica che alcuni Centri prescrivono. Per quel che concerne il materiale prelevato, la coltura abbisogna di una sufficiente cellularità; la quantità minima di liquido richiestaci non deve essere inferiore ai 10 ml.
Quando Sottoporsi ad Amniocentesi: Indicazioni e Tempistiche
L'amniocentesi presenta indicazioni che possono essere differenti a seconda dell’epoca di gravidanza nella quale la si esegue. La scelta dell’epoca di esecuzione è strettamente correlata alle indicazioni specifiche. Le tempistiche si distinguono in:
- Amniocentesi precoce o precocissima (early amniocentesis): eseguita tra la 10^ e la 20^ settimana. Tale procedura, almeno agli inizi della sua introduzione clinica, era gravata da un maggior rischio abortivo ed è tutt’ora innegabilmente caratterizzata da una più alta incidenza di insuccessi diagnostici, o per mancata coltura o per errori di genere tecnico. L’indicazione specifica dell’amniocentesi intorno alla 11^ settimana rimane quella citogenetica, in alternativa alla villocentesi. I risultati diagnostici ritardano circa 2/3 settimane rispetto ai tempi medi di risposta di una villocentesi. Il rischio sembra però sovrapponibile. Anche la percentuale di insuccessi diagnostici per problemi di coltura è la medesima. L’indicazione specifica dell’amniocentesi intorno alla 14^ settimana risulta quindi essere quella citogenetica. Si tratta quindi di una accettabile alternativa al prelievo dei villi coriali rispetto ai quali risulta gravata da un ridotto rischio abortivo.
- Amniocentesi del II trimestre (midtrimester amniocentesis): eseguita tra la 15^ e la 20^ settimana. L’amniocentesi eseguita tra la 16^ e la 18^ settimana rappresenta a tutt’oggi la metodica più frequentemente utilizzata ai fini diagnostici di citogenetica prenatale.
- Amniocentesi tardiva (late amniocentesis): eseguita oltre la 24^ settimana. Nel terzo trimestre, fra la 32a e la 39a settimana di gravidanza, l'amniocentesi può essere utilizzata per valutare la maturazione dei polmoni del feto nelle donne in cui si consideri di anticipare il parto prima del termine della gravidanza.
La sempre maggiore richiesta di ottenere risposte citogenetiche precoci ha indotto, negli ultimi anni, ad eseguire il prelievo del liquido amniotico sempre più precocemente. Ciò anche in relazione alla possibilità che il prelievo del liquido amniotico in epoca inferiore alla 15a settimana di gestazione si ponesse come una valida alternativa al prelievo dei villi coriali.
Le indicazioni per l'amniocentesi genetica convenzionale, eseguita generalmente tra la 15^ e la 20^ settimana di gestazione, rientrano fondamentalmente in due categorie:
- In presenza di un rischio procreativo prevedibile a priori: quali età materna avanzata (> 35 anni alla nascita del feto), genitore portatore eterozigote di anomalie cromosomiche strutturali, genitori portatori di mutazioni genetiche, o genitore con aneuploidie dei cromosomi sessuali compatibili con la fertilità.
- Presenza di un rischio fetale evidenziato nel corso della gravidanza: malformazioni fetali rilevate all’esame ecografico, malattie infettive insorte durante la gravidanza, positività dei test di screening (test combinato, bi test, tri test, spessore della traslucenza nucale, etc.) che configurino un rischio di anomalia cromosomica uguale o superiore a 1:300.Inoltre, l'amniocentesi è consigliata alle donne che abbiano avuto figli con malattie cromosomiche o difetti del tubo neurale, come la spina bifida, o in caso di familiari (storia familiare) con specifiche malattie genetiche.
Rischi e Considerazioni Etiche dell'Amniocentesi
Ogni tecnica invasiva è gravata da un rischio di perdite fetali che è correlato all’esperienza dell’operatore, alla tecnica utilizzata, all’entità del prelievo e all’indicazione, all’epoca gestazionale e all’età della donna. Il rischio abortivo dell'amniocentesi è stimato intorno allo 0,5-1%. La letteratura ritiene che per le amniocentesi eseguite intorno alla 14^ settimana il rischio abortivo è sovrapponibile a quello delle amniocentesi della 17^ settimana. Di tale percentuale si deve tener conto quando si valuta il rischio/beneficio della procedura diagnostica. Il rischio abortivo va infatti comparato con le percentuali di anormalità cromosomiche per l’età. Va inoltre considerato che la percentuale di anomalie riscontrate nelle procedure è sempre maggiore rispetto alla nascita. Ciò è dovuto ad una selezione naturale operante durante la gravidanza per i feti patologici.
A prescindere dalle indicazioni mediche, la donna e il partner sono liberi di decidere se effettuare o non effettuare il test, dopo averne parlato con il medico, in un percorso di consenso informato che includa un accurato counseling che tratti correttamente i vari aspetti inerenti la procedura.
La Tecnica FISH: Ibridazione Fluorescente In Situ
La tecnica FISH (Fluorescence In Situ Hybridization) è una tecnica di diagnostica molecolare che permette l’identificazione e la localizzazione in situ di specifiche sequenze di DNA nei cromosomi. È la sigla di “fluorescent in situ hybridization” (ibridazione fluorescente “in situ”). Il suo obiettivo principale è rilevare anomalie cromosomiche come aneuploidie, duplicazioni, delezioni e traslocazioni.
Come Funziona la FISH
La tecnica FISH permette di rilevare sequenze di DNA su cromosomi in metafase o su nuclei interfasici di preparati citogenetici, in coltura o non coltivati. Questa è una nuova tecnica mediante la quale sonde fluorescenti possono essere attaccate a segmenti di DNA. Queste sonde, marcate con molecole fluorescenti, si legano specificamente a regioni complementari del DNA fetale. Dopo l’ibridazione con il DNA, queste sonde fluorescenti sono visibili al microscopio ottico come puntini colorati sui cromosomi o nel nucleo in interfase (cioè non in divisione).
Questa tecnica è applicabile sia a cellule in mitosi che a cellule non in mitosi. Quando viene applicata a cellule non in mitosi, la lunghezza dei tempi di risposta viene notevolmente abbreviata: nella pratica può essere utilizzata per avere, nel giro di poco tempo, il numero dei cromosomi 21, 13 e 18 e dei cromosomi sessuali, permettendo così di escludere rapidamente le anomalie cromosomiche più frequenti. Se vi è la necessità di conoscere in breve tempo solo il numero dei cromosomi del bimbo, nel sospetto di una malattia specifica, sulle cellule all’inizio della loro coltura in capsula di vetro (clonazione), si esegue un test detto FISH che permette una risposta nel giro anche di 48 - 72 ore (test rapido) nei confronti dei cromosomi 13, 18 e 21 e dei cromosomi sessuali X ed Y. L’affidabilità di questa metodica è superiore al 99,9%.
La Fish
Anomalie Cromosomiche Rilevabili con FISH
La tecnica FISH è particolarmente efficace nella rilevazione di diverse tipologie di anomalie cromosomiche:
- Aneuploidie: sono alterazioni del numero di cromosomi. Una delle più note è la sindrome di Down, in cui invece di esserci 2 copie del cromosoma 21, ce ne sono 3. In questo caso, la FISH mostrerà tre segnali sul cromosoma 21, anziché 2.
- Delezioni e duplicazioni: si rilevano attraverso l’assenza o l’eccesso di fluorescenza in regioni specifiche dei cromosomi.
- Traslocazioni: è un’anomalia genetica in cui un segmento di cromosoma si rompe e si unisce a un altro cromosoma. La FISH può identificare queste traslocazioni visualizzando i segmenti cromosomici riarrangiati.
Vantaggi e Limitazioni della Tecnica FISH
La tecnica FISH è un metodo diagnostico rapido, specifico e molto versatile, poiché può essere utilizzato sia nell’analisi dei gameti che degli embrioni. In medicina riproduttiva questa metodica viene anche utilizzata per la diagnosi genetica preimpianto (PGD) in pazienti selezionati che eseguono la fecondazione in vitro; lo scopo è di trasferire in utero solo embrioni che non abbiano anomalie cromosomiche.
Tuttavia, presenta alcune limitazioni, tra cui il fatto che può analizzare solo un numero limitato di cromosomi (tra 5 e 9) e che è una tecnica distruttiva, pertanto le cellule analizzate non possono essere riutilizzate nei trattamenti successivi.
Le Anomalie Cromosomiche Rilevabili nella Diagnosi Prenatale
Le anomalie cromosomiche sono alterazioni del numero o della struttura dei cromosomi. Queste possono avere un impatto significativo sullo sviluppo fetale e post-natale.
Anomalie Numeriche: Le Aneuploidie
Le anomalie numeriche dei cromosomi, che vengono chiamate anche aneuploidie, sono caratterizzate da un numero maggiore o inferiore di cromosomi rispetto al numero standard.
- Trisomie: Si parla, ad esempio, di trisomia, quando si riscontra la presenza di un cromosoma in più. A questo gruppo di anomalie cromosomiche appartengono patologie note come Sindrome di Down o Trisomia 21, dove l’individuo presenta 47 cromosomi, ovvero possiede una copia in più del cromosoma 21. Si stima che la trisomia 21 colpisca all’incirca 1 neonato su 700. I bambini affetti dalla sindrome di Down presentano un ritardo nella capacità cognitiva e nella crescita fisica e sono anche maggiormente soggetti a sviluppare alcune patologie. La sindrome di Down non si manifesta allo stesso modo in tutte le persone che ne sono affette e non v’è modo di stabilire prima della nascita il livello di disabilità. La trisomia 13, invece, prende il nome di Sindrome di Patau, la quale si associa ad elevata abortività e i neonati non sopravvivono oltre i primi mesi di vita. La trisomia 18, nota come Sindrome di Edwards, si associa anch'essa ad una elevata abortività ed è causa di grave ritardo mentale. Neonati affetti da trisomia 18 hanno spesso difetti cardiaci congeniti, nonché altre condizioni patologiche che riducono la loro aspettativa di vita.
- Monosomie: Si parla, invece, di monosomia, quando si riscontra l’assenza di un cromosoma.
Tra le aneuploidie, le trisomie 21, 18, 13 e le aneuploidie dei cromosomi sessuali (es. monosomia X), comprendono circa l’80%-95% delle possibili anomalie cromosomiche rivelabili tramite la determinazione del cariotipo. Tali anomalie cromosomiche sono senz’altro quelle maggiormente responsabili di malformazioni fetali che portano a gran parte degli aborti precoci ossia durante il primo trimestre di gravidanza. In alcuni casi le gravidanze con feti affetti da trisomia 21, 18 e 13 possono procedere nel corso dell’età gestazionale e portare alla nascita di neonati affetti dalla relativa patologia cromosomica (probabilità di sopravvivenza alla nascita rispettivamente del 22,1%, 5,4% e 2,8%).
Anomalie dei Cromosomi Sessuali
Per quanto riguarda i cromosomi sessuali, X ed Y, la situazione è diversa. Infatti in questi casi l’aberrazione non è una vera e propria trisomia bensì la perdita o l’aggiunta di uno dei due cromosomi rispetto all’assetto normale XX che caratterizza il sesso femminile od XY proprio di quello maschile.
- Sindrome di Turner (Monosomia X): È la più frequente aneuploidia dei cromosomi sessuali. La maggior parte delle bambine affette dalla sindrome di Turner hanno soltanto una copia del cromosoma X. Molte di queste gravidanze vanno incontro ad aborto spontaneo. Le donne affette da sindrome di Turner hanno solitamente una statura più bassa della media. La loro pubertà è ritardata o del tutto assente e possono essere sterili. La maggior parte dimostra capacità cognitive normali, anche se alcune presentano difficoltà di apprendimento.
- Sindrome di Klinefelter (XXY): I bambini maschi affetti dalla sindrome di Klinefelter hanno due cromosomi X e un cromosoma Y. Si tratta di bambini con una tendenza ad avere una statura più elevata della media, la cui pubertà può essere ritardata o del tutto assente e che spesso sono sterili. I soggetti affetti da queste condizioni possono avere una statura più elevata della media e di solito presentano capacità cognitive normali. In qualche raro caso si possono manifestare problemi psicologici o di apprendimento. Queste condizioni non sono associate a difetti alla nascita e possono rimanere non diagnosticate.
In genere, le anomalie dovute al numero dei cromosomi sessuali non causano gravi deficit cognitivi né dello sviluppo fisico-motorio. La diagnosi precoce può aiutare questi bambini a ricevere i servizi di cui necessitano per raggiungere il loro massimo potenziale.
Meccanismi e Fattori di Rischio delle Aneuploidie
Il meccanismo principale con cui si producono le aneuploidie è costituito dalla non-disgiunzione, ovvero dalla mancata separazione dei cromosomi omologhi o dei cromatidi durante la meiosi nel corso della gametogenesi.
È ormai noto che l’incidenza di anomalie cromosomiche è direttamente proporzionale all’età materna. In particolare per la sindrome di Down si calcola che oltre i 40 anni una gravidanza su 100 sia interessata da questo tipo di anomalia. Tale fenomeno ha avuto, in questi ultimi anni, un impatto non indifferente a livello etico - sociale in quanto l’età media al primo parto è aumentata in maniera considerevole. Si pensi infatti che nell’ultimo trentennio, si è passati dai 20-21 anni ai 29-30 attuali.
Anomalie Strutturali: Traslocazioni e Inversioni
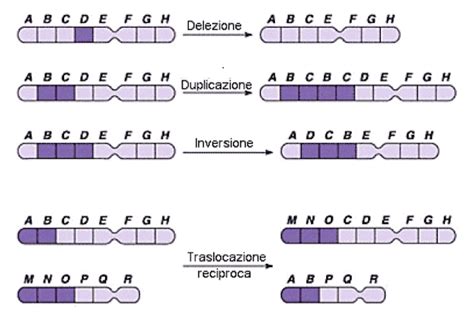
Oltre alle anomalie numeriche, esistono anche anomalie strutturali dei cromosomi:
- Traslocazioni Robertsoniane: Le traslocazioni tra due cromosomi acrocentrici (numeri 13, 14, 15, 21 e 22) sono chiamate traslocazioni robertsoniane. È noto che nei Down, la cui alterazione risulta da una traslocazione sbilanciata (per esempio 46xx, -14,+t.14q;21q.) uno dei due genitori ha la stessa traslocazione, ma in modo bilanciato dal 25% al 50% dei casi. Il rischio teorico, pertanto, di un genitore che presenta una traslocazione bilanciata del tipo 14q;21q, di avere un figlio Down, è piuttosto elevato. In effetti però la reale incidenza dell’anomalia è bassa.
- Traslocazioni Reciproche: Sono rare. Esse non coinvolgono la fusione centromerica ed i cromosomi acrocentrici.
- Inversioni: L’inversione avviene quando una normale sequenza di geni su di un cromosoma è alterata. Così come per le traslocazioni bilanciate, il fenotipo è del tutto normale. La possibilità, che durante la meiosi tali inversioni determinino una perdita di materiale, non è ben chiara.
Quando non si abbia a disposizione un laboratorio in grado di eseguire esami di tale tipo, oppure se tali esami richiedessero un tempo di esecuzione tale da renderli inutili al punto di non poter fruire dell’informazione ai fini prenatali, si informi che il rischio empirico che il feto sia portatore di un’anomalia è stimato intorno al 10-20%. I veri problemi insorgono quando si riscontrano anomalie cromosomiche particolari, per le quali siamo sicuri della tecnica, ma non conosciamo l’espressività fenotipica. Si tratta il più delle volte di piccoli cromosomi sovrannumerari, inversioni, traslocazioni apparentemente bilanciate, che interessano essenzialmente gli autosomi. L’indagine sui genitori è di grande ausilio poiché, spesso, riscontriamo la stessa anomalia in uno di essi. Qualora ci trovassimo di fronte ad una mutazione “de novo” avvenuta nel feto, vale la pena, ove possibile, eseguire attenti bandeggi o utilizzare sonde per micromappature geniche onde poter stabilire se nella traslocazione o inversione vi sia stata perdita di materiale.
Per quel che concerne le numerose alterazioni che si associano ai cromosomi sessuali ( es. 45,x ; 47,xxx ; 47,xxy ; ecc) i genitori vanno informati che il più delle volte sono compatibili con un fenotipo perfettamente normale.
Il Cariotipo Parentale e il Rischio di Ricorrenza
Tra le condizioni parentali che inducono ad eseguire la diagnosi prenatale va considerata la presenza di un precedente figlio affetto da una cromosomopatia. Per quanto ci è oggi noto, il rischio per un secondo figlio non aumenta in nessun caso qualora il cariotipo della coppia genitoriale risulti del tutto normale. Diverse e più complicate risultano le probabilità legate alla presenza, nei genitori, di anomalie del cariotipo. La possibilità che uno dei genitori presenti un’anormalità del numero dei cromosomi, detta aneuploidia, è piuttosto rara. Ciò in relazione al fatto che molte di queste condizioni si accompagnano a sterilità, come ad esempio avviene nel maschio Down. Va inoltre detto che le aneuploidie si accompagnano a modificazioni spesso sostanziali del fenotipo, tali da rendere la vita di relazione e la possibilità di generare inferiore alla media. Esistono comunque delle situazioni, quali i mosaicismi, nelle quali ci si trova di fronte alla possibilità di una gravidanza.
Altre Metodologie di Diagnosi Prenatale Molecolare
Oltre alla FISH, la diagnostica prenatale ha visto l'introduzione e il perfezionamento di altre tecniche molecolari, che offrono vantaggi specifici in termini di velocità, risoluzione e tipo di anomalie rilevabili.
QF-PCR (Quantitative Fluorescent Polymerase Chain Reaction)
QF-PCR (Quantitative Fluorescent Polymerase Chain Reaction, ovvero reazione a catena della polimerasi quantitativa fluorescente) è una tecnica molecolare rapida per identificare aneuploidie comuni (es. le trisomie 21, 13, 18 e le aneuploidie dei cromosomi sessuali X e Y). Oggi tale tecnica si è ormai sostituita completamente alla tecnica di ibridizzazione fluorescente in situ (FISH) per questo scopo, affiancando le analisi citogenetiche tradizionali eseguite di routine. La QF-PCR si differenzia per una maggiore rapidità (risultato disponibile entro 24h-48h dal prelievo), per la necessità di una minore quantità di liquido amniotico (1-1,5 ml), 1-2 villi coriali, 0,1 ml di sangue fetale, partendo da DNA estratto da materiale cellulare non coltivato.
Il fattore più importante, rispetto alle tecniche tradizionali, è legato alla possibilità di eseguire test di laboratorio precisi, affidabili e soprattutto rapidi partendo da una minima quantità di materiale, a volte anche da poche cellule. La verifica in termini qualitativi e quantitativi della segregazione degli alleli parentali mediante QF-PCR e corsa elettroforetica fluorescente dei prodotti di amplificazione permette di poter evidenziare nel feto la presenza di eventuali trisomie. Un pattern allelico non informativo si ha in presenza di un solo picco fluorescente per ogni locus polimorfico testato. Per quanto riguarda i cromosomi sessuali viene impiegata una sequenza relativa al gene dell’amelogenina. In questo caso un campione che presenta 1 picco nell’amelogenina ed 1 o 2 picchi nel DXS8377 indica un assetto cromosomico femminile normale (XX); mentre un campione con 2 picchi di differente dimensione a livello dell’amelogenina ed 1 picco nel DXS8377 un assetto cromosomico maschile normale (XY).
L’applicazione della tecnica QF-PCR in epoca prenatale per il riconoscimento di alcune anomalie cromosomiche di numero, ha alcune limitazioni. Nel caso di QF-PCR positiva per una trisomia, l’esame non permette di distinguere tra una vera trisomia fetale ed un mosaicismo confinato alla placenta (o ad altri tessuti extra fetale) privo di significato patologico per il feto. Tuttavia, rappresenta un utile supporto diagnostico nei casi di fallimento della coltura cellulare, referti ecografici dubbi in gravidanze inoltrate, o riscontro immediato di sindromi polimalformative.
CGH Array (Array-Comparative Genomic Hybridization)
Il CGH Array è basato su un’analisi comparativa del DNA in esame con un DNA genomico di riferimento di un soggetto sano. Entrambi i campioni (quello da analizzare e quello di riferimento) sono marcati con delle molecole fluorescenti (fluorocromo rosso per il DNA da analizzare e fluorocromo verde per il DNA di riferimento). Successivamente vengono uniti e fatti incubare (ibridazione) su un vetrino particolare (array) la cui superficie è ricoperta da frammenti di DNA (le sonde). L'analisi array-CGH rappresenta anche una tecnica ideale di approfondimento diagnostico di secondo livello, eseguita per integrare l’analisi citogenetica prenatale al fine di definire più accuratamente eventuali anomalie cromosomiche precedentemente identificate o per rivelare microriarrangiamenti non evidenziabili con l’indagine del cariotipo fetale.
Rispetto all’esame citogenetico tradizionale, l’analisi molecolare dei cromosomi con CGH Array ha una risoluzione molto più elevata (circa 100 volte). Ciò consente di identificare alcune patologie derivanti da alterazioni cromosomiche submicroscopiche (microdelezioni e le microduplicazioni), non evidenziabili tramite il cariotipo tradizionale, aumentando sensibilmente l’accuratezza dell’esame. Il cariotipo molecolare, infatti, consente di effettuare rapidamente non solo lo studio dell’assetto cromosomico fetale, ma anche di un gruppo di 100 patologie causate da microdelezione / microduplicazione cromosomica. Questa tecnica innovativa si differenzia dal cariotipo tradizionale prenatale in quanto è meno laboriosa e facilmente automatizzabile, e quindi meno soggetta a rischio di errore.
Il Cariotipo Tradizionale
L’approccio tradizionale nella diagnosi prenatale di anomalie cromosomiche comporta la messa in coltura di cellule fetali ricavate da prelievi di liquido amniotico e la determinazione del cariotipo tramite l’analisi al microscopio dei cromosomi in metafase. Benchè tale analisi sia abbastanza accurata, le colture cellulari impongono lunghi tempi di attesa che si aggirano intorno ai 15-20 giorni. La diagnostica citogenetica prenatale consiste nella determinazione del cariotipo fetale. Questo viene effettuato attraverso varie tecniche di bandeggio e di colorazione dei cromosomi (ad es. bandeggio G e FISH).
Il cariotipo tradizionale, inoltre, non garantisce che il feto sia esente da malattie genetiche o alterazioni cromosomiche (delezioni o duplicazioni) di piccole dimensioni. Infatti, questo tipo di esame fornisce informazioni solo sulle principali anomalie cromosomiche (ad esempio la trisomia 21, o Sindrome di Down, le trisomie 18 e 13, la monosomia X, o Sindrome di Turner) attraverso la determinazione dell’intero assetto cromosomico fetale. Con il cariotipo tradizionale si indaga essenzialmente su quelle forme patologiche che interessano il numero e l’aspetto grossolano dei cromosomi. Lo studio del cariotipo fetale, a differenza dell’amniocentesi rapida con la tecnica QF-PCR, presenta un’importanza diagnostica elevatissima perché evidenzia le anomalie cromosomiche più severe e frequenti (come ad esempio le trisomie) a carico di tutti i cromosomi; tuttavia, a causa dei limiti di risoluzione della tecnica, piccoli riarrangiamenti cromosomici potrebbero non essere facilmente evidenziabili.

Analisi Complementari sul Liquido Amniotico
Il liquido amniotico, oltre a fornire cellule per lo studio cromosomico, può essere utilizzato per una serie di altre indagini diagnostiche che forniscono informazioni preziose sulla salute fetale.
L'Alfa-fetoproteina (AFP) nel Liquido Amniotico
Nel liquido amniotico si è usi valutare anche la quantità di alfa-feto-proteina (AFP). Tale sostanza, individuata negli anni ’50 in alte percentuali, incontrò l’interesse degli ostetrici quando ci si avvide dell’aumento della sua presenza nel compartimento materno in relazione a differenti problemi fetali ed in particolare a difetti del tubo neurale: anencefalia, spina bifida aperta, gastroschisi ed onfalocele ed altri difetti “aperti” del tronco fetale. Si tratta di soluzioni di continuo non rivestite da cute, che portano ad un sostanziale incremento di tale proteina nel siero materno. Partirono così numerosi programmi di screening, in Inghilterra e negli Stati Uniti. Studi che mostrarono accuratezze elevatissime nello screening dei difetti del tubo neurale.
Ben presto iniziarono però le critiche a tale metodo, che risulta influenzato da troppe variabili e caratterizzato da un elevato numero di falsi positivi e negativi. Al giorno d’oggi nessuno riterrebbe il dato di elevati valori di AFP sufficiente per la diagnosi di anomalia fetale. L’ecografia morfologica appare estremamente più sensibile ed accurata. Il dosaggio dell’AFP nel liquido amniotico appare oggi complementare ad altre più importanti e dirette valutazioni sul liquido stesso ed assolutamente inferiore per screening all’ecografia. Fino a pochi anni or sono, alcuni insistevano sulla prognosi negativa di alti valori di AFP nel siero materno solo quando questi erano superiori a 5 multipli della mediana. In tali casi, le complicanze risultavano le più diverse e non soltanto legate ad anomalie del tubo neurale, ma anche ad anomalie placentari e complicanze ostetriche diverse. Inoltre gli Autori ricordano che il dato biochimico non fornisce mai una diagnosi di conferma essendo necessario sempre un dato ecografico.
Diagnosi di Infezioni Fetali
Sempre nel secondo trimestre di gravidanza accade di dover diagnosticare la presenza di eventuali malattie infettive. L’introduzione delle metodiche di amplificazioni genica ed in particolare della reazione a catena della polimerasi (PCR), permette oggi di riconoscere, amplificandole, anche piccole sequenze di materiale genomico dell’agente infettivo.
La nostra casistica (dati personali in via di pubblicazione) dimostra l’assoluta superiorità in termini di accuratezza diagnostica dell’amniocentesi nella diagnosi di infezione da Citomegalovirus rispetto alla stessa indagine condotta sui villi coriali e soprattutto sul sangue fetale. La differenza diviene tanto più evidente quanto più tempo è trascorso dalla data dell’infezione. Gli stessi risultati non sono ottenibili sulle infezioni da virus rubeolico o da Toxoplasma per i quali il riscontro nei villi coriali appare più persistente e nel sangue fetale più accurato sempre però tenendo conto dei limiti temporali in cui l’agente infettivo è presente nel sangue. Si consideri comunque che la diagnosi molecolare delle malattie infettive anche sul liquido amniotico presenta comunque il vantaggio di non incorrere in false positività.
Mediatori della Flogosi nel Liquido Amniotico
L’esistenza di un’infezione endoamniotica è anche causa di diverse patologie che possono impedire un buon svolgimento della gravidanza. Per questo, infatti, sta prendendo sempre più piede la ricerca sul liquido amniotico di alcune sostanze mediatrici della flogosi quali le CITOCHINE. In particolare, la ricerca dell’INTERLEUCHINA-6 sul liquido amniotico presenta una straordinaria efficacia nella diagnosi predittiva di numerose patologie del feto in utero. Per tale condizione si è anche cercato di stabilire in passato la quantità di sangue necessario affinché tale risposta immunitaria avvenga. L’esame della letteratura, vecchia oramai di quasi trent’anni, indicava in dosi variabili, dai 3 ai 10 ml la quantità minima necessaria.
Valutazione della Maturazione Polmonare Fetale
Nel terzo trimestre, l'amniocentesi può essere utilizzata per valutare la maturazione dei polmoni del feto. L’immunizzazione, prima dell’introduzione della profilassi, era presente in circa l’8% delle madri Rh negative che davano alla luce figli Rh-positivi. Tale dato aumentava di un altro 8% alla seconda gravidanza. La trasfusione feto-materna avviene in 3 gravidanze su 4. Alcune condizioni ostetriche quali il distacco di placenta, le emorragie da minaccia d’aborto, ecc., aumentano il rischio di sensibilizzazione. In condizioni normali la bilirubina nel liquido amniotico deriva dalla trachea e dal polmone fetale e solo raramente, come si è detto in precedenza, da cause materne (iperbilirubinemia materna).
Nel 1971 Gluck presentò i suoi primi dati sulla correlazione tra maturazione polmonare fetale e presenza di surfattante nel liquido amniotico. Prima di questa data la valutazione della maturità fetale non si basava su alcun dato certo. Lo studio qualitativo, più che quantitativo dei fosfolipidi disciolti nel liquido amniotico riflette le diverse fasi del processo maturativo. La struttura di base dell’alveolo polmonare è costituita da una intricata rete di capillari, disposta a modo di canestro, all’interno della quale vi è un rivestimento di un sottile stato di cellule monostratificate: i pneumociti di primo ordine. La lecitina è il fosfolipide più largamente rappresentato, costituendo circa il 50-70%: essa tende a saturarsi progressivamente durante tutta la gestazione. All’inizio si pensava che la lecitina svolgesse il ruolo di surfattante. Le attuali conoscenze sul fosfatidilinositolo (PI) ed il fosfotidilglicerolo (PG) attribuiscono a questi la funzione di stabilizzatori del composto. La lecitina pertanto deve essere intesa come il maggior componente fosfolipidico del surfattante ma non è il surfattante stesso.
In considerazione degli straordinari progressi della neonatologia, feti sempre più prematuri sono trattati con successo dopo la nascita. Di conseguenza, per ragioni pratiche, il numero dei feti che per poter nascere necessitano di un accurato profilo polmonare è sempre più ridotto. Tra questi noi preferiamo eseguire il test spettrofotometrico di Sbarra. Tale test necessita di una semplice analisi del campione di liquido amniotico, prelevato tramite amniocentesi, ed esaminato ad una lunghezza d’onda di 650 nm, azzerando lo strumento con l’acqua distillata.
Villocentesi: Un'Alternativa Precoce alla Diagnosi Prenatale
La villocentesi è un prelievo di minuscoli frammenti di placenta (VILLI CORIALI) che, come l’embrione, hanno origine dalla stessa cellula uovo. Tale analisi consente di studiare i cromosomi del bambino senza penetrare neppure nel sacco che lo contiene, il sacco amniotico. I cromosomi (CARIOTIPO) sono studiati con metodo diretto e dopo cultura a lungo termine.
La Procedura e le Tempistiche della Villocentesi
L’asportazione di villi coriali viene effettuata attraverso la parete addominale materna e viene eseguita attualmente sotto controllo ecografico in modo da evidenziare la zona migliore dove effettuare agevolmente il prelievo. Il prelievo viene eseguito tra la 11° e la 13° settimana di gestazione. La villocentesi non è consigliata prima della 10ma settimana di gestazione. Le prime esperienze si ebbero in particolare ad opera di studiosi statunitensi. Infatti la Food and Drug Administration aveva, già dall’inizio dell’introduzione della villocentesi, ristretto molto il numero dei Centri, sia pubblici che privati, abilitati a tale procedura. In effetti, attualmente, in relazione ai possibili rischi malformativi della villocentesi prima delle 7/8 settimane di gestazione, tale procedura viene solitamente eseguita alla 9^/10^ settimana. E se a questo aggiungiamo gli altri 15 gg di tempo necessario alla coltura dei villi (poiché spesso la lettura diretta fallisce o lascia dubbi), si arriva così, spesso, ad ottenere il risultato solo intorno alla 12^/13^ settimana.
Vantaggi, Rischi e Affidabilità
Il prelievo di villi coriali è sperimentato ormai da molti anni e non comporta rischi per la donna. Non sono inoltre mai stati descritti casi di malformazioni neonatali dovute al prelievo di villi coriali eseguito nel periodo consigliato. Il rischio di aborto legato alla villocentesi si aggira intorno all’1%; è consigliato comunque dopo il prelievo un periodo di attività ridotta per un paio di giorni.
La prima risposta (analisi dei cromosomi X, Y, 21, 18, 13) ha un’attendibilità del 99% entro la giornata successiva; l’esito definitivo di tutte le 23 coppie di cromosomi si avrà dopo circa 20 giorni dal prelievo. Il risultato di questo esame permette di valutare il corredo cromosomico del bambino. Ogni individuo normale ha un corredo cromosomico composto da 23 coppie di cromosomi, di cui due cromosomi che determinano il sesso (XX per la femmina e XY per il maschio). Di ogni coppia di cromosomi uno deriva dalla mamma ed uno dal papà. Dall’esame cromosomico (detto anche “cariotipo fetale”) delle cellule dei villi coriali si visualizzano perciò i cromosomi del bimbo, il sesso maschile o femminile e si può diagnosticare la presenza di eventuali anomalie.
Molti sono i vantaggi legati alla villocentesi: è un esame abbastanza veloce i cui risultati arrivano in brevissimo tempo. Inoltre si rivela abbastanza accurato, in quanto, il prelievo dei villi coriali permette di conoscere il patrimonio genetico e cromosomico del bambino con una sicurezza che si attesta intorno al 99%. Tuttavia in alcuni casi, molto molto rari i risultati potrebbero non rivelarsi pienamente attendibili in quanto l’embrione e la placenta potrebbero presentare linee genetiche diverse. Questo può dare vita ad una discrepanza tra l’assetto cromosomico dei villi coriali e quello della placenta con la possibilità che siano sviluppati falsi positivi o falsi negativi del test.
Indicazioni e Confronto con l'Amniocentesi
Un’indicazione all’esecuzione del prelievo di villi coriali è la presenza di screening ecografico del primo trimestre positivo. Le indicazioni agli esami consigliate dal Ministero della Sanità includono: età materna > 35 anni, figlio precedente affetto da anomalia cromosomica, familiarità per malattie genetiche, diagnosi di sesso per malattie legate al cromosoma X, familiarità per malattie congenite del metabolismo, e anomalie strutturali del feto all’esame ecografico.
Rispetto all’amniocentesi, la villocentesi può essere effettuata in epoca più precoce: questo consente di conoscere in anticipo il corredo cromosomico e genetico definito e permette inoltre di prevedere e di individuare alcune malattie specie in famiglie a rischio. L’accesso alle tecniche invasive è sempre subordinato alla scelta libera, consapevole ed informata da parte della gestante.
tags: #tecnica #fish #amniocentesi