La terminologia medica, spesso complessa, utilizza il termine "eterologo" in contesti radicalmente differenti: se in oncologia si riferisce alla natura di una massa tumorale, in ambito ginecologico ed endocrinologico descrive tecniche di procreazione medicalmente assistita. Comprendere queste distinzioni è fondamentale per interpretare correttamente le diagnosi e le opzioni terapeutiche disponibili.
L’eterogeneità tumorale: quando la posizione e il tempo definiscono l'aggressività
In ambito oncologico, la presenza di cellule con caratteristiche diverse all’interno di una stessa massa tumorale può spiegare molti dei comportamenti della malattia, inclusa la resistenza alle terapie. I ricercatori chiamano “eterogeneità intra-tumorale” la diversità tra le cellule di un singolo tumore. Ciò è verosimilmente dovuto al fatto che le cellule di un tumore nel tempo si differenziano le une dalle altre a causa di caratteristiche genetiche, epigenetiche e fisiche.
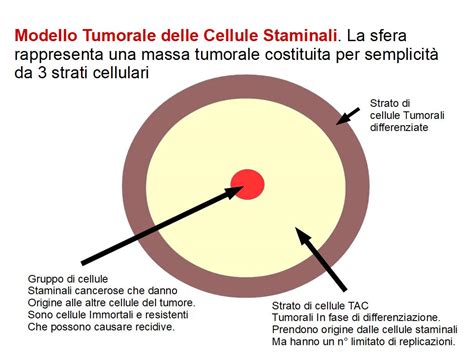
Come si legge in un articolo da poco pubblicato da Kevin Litchfield e colleghi sulla rivista Nature Ecology & Evolution, queste caratteristiche dipendono anche dalla posizione nella quale le cellule si trovano nella massa tumorale, la quale può influenzare la crescita e l’aggressività delle cellule stesse. È solo una delle tante ricerche condotte recentemente che hanno identificato proprio nell’eterogeneità intra-tumorale una delle chiavi per comprendere meglio la malattia.
Coordinate spaziali e metastasi
Studiando l’evoluzione spaziale del carcinoma renale a cellule chiare, gli autori dello studio hanno scoperto che le metastasi di questo tumore prendono il via da cloni di cellule nella parte più interna della massa tumorale. A differenza di quelle che si trovano ai margini della massa tumorale, le cellule più centrali devono sopravvivere a un ambiente più ostile, per esempio privo di ossigeno, e ci riescono diventando più forti e aggressive. Queste cellule centrali proliferano di più, mostrano segni di necrosi, una sorta di blocco delle attività biologiche, e accumulano un numero maggiore di alterazioni nel genoma.
Conoscere questi aspetti potrebbe aiutare a comprendere meglio i meccanismi alla base delle metastasi e a guidare i medici nella scelta della terapia migliore per evitare la diffusione della malattia. "Le biopsie dovrebbero arrivare anche nel centro del tumore per poter analizzare queste cellule, ma con le tecnologie oggi disponibili non sempre è possibile analizzare con successo un tessuto così particolare come quello del cuore della massa", affermano gli autori.
Meccanismi molecolari cancro
Evoluzione temporale e microambiente
Alla base dell’eterogeneità intra-tumorale c’è un continuo processo di evoluzione che coinvolge tutte le cellule del tumore nel tempo e nello spazio. Oggi sappiamo che le cellule del tumore primario sono diverse dal punto di vista genetico rispetto alle metastasi (eterogeneità spaziale) e che cambiano nel tempo a causa delle terapie (eterogeneità temporale). Le differenze si manifestano su diversi aspetti - genetico, metabolico, eccetera - e possono verificarsi indipendentemente le une dalle altre. Non bisogna dimenticare che l’eterogeneità intra-tumorale è determinata anche dal microambiente che circonda il tumore: ogni cambiamento del microambiente può spingere le cellule tumorali a modificarsi. Inoltre, le diverse terapie possono dare origine a cloni resistenti, che diventano sempre più numerosi, causando il fallimento della terapia stessa.
Interpretazione dei reperti radiologici: "lesione eterologa"
In ambito diagnostico, l'espressione "sospetta lesione eterologa" viene spesso utilizzata nei referti di risonanza magnetica o TAC per indicare una formazione di natura non propria del tessuto in cui è stata rinvenuta, ovvero una massa che ha origine altrove o che presenta caratteristiche cellulari diverse dal parenchima circostante.
Casi clinici e complessità diagnostica
Spesso, pazienti vengono sottoposti a esami approfonditi dopo eventi critici, come una crisi epilettica. In tali contesti, la diagnostica per immagini (RMN encefalo con mezzo di contrasto) può rilevare formazioni iperintense con impregnazione variabile dopo somministrazione di contrasto. Queste lesioni richiedono un'attenta analisi differenziale per escludere o confermare processi neoplastici, infiammatori o vascolari. Ad esempio, in un paziente con una lesione temporale di circa 3.8 cm priva di significativo edema vasogenico, il sospetto di una lesione eterologa deve essere correlato con l'assenza di malformazioni vascolari evidenti tramite angio-RM. Il percorso di diagnosi può includere anche il monitoraggio nel tempo, come nei casi di consolidamenti polmonari disomogenei, dove il comportamento della lesione (incremento dimensionale o stabilità) guida la scelta tra chirurgia, radioterapia (come la tecnica RapidArc) o semplice osservazione.
Lesioni precancerose: la diagnosi precoce
L'evoluzione delle tecniche diagnostiche ha aumentato la capacità di individuare le cosiddette lesioni precancerose, alterazioni che possono evolvere in un tumore, ma che al momento della diagnosi non lo sono ancora.
- Carcinoma duttale in situ (DCIS): Spesso rilevato con la mammografia, è considerato dagli esperti una lesione pretumorale. Il trattamento è solitamente chirurgico, talvolta affiancato da radioterapia o, in casi selezionati con recettori per gli estrogeni, da terapia con tamoxifene per prevenire recidive.
- Carcinoma lobulare in situ (LCIS): Il rischio di progressione è inferiore rispetto al DCIS; spesso si predilige un monitoraggio attivo (sorveglianza) e, nei casi a rischio individuale elevato, la chemioprevenzione.
- Lesioni della cervice uterina: Spesso associate all'infezione da HPV, le lesioni note come CIN (neoplasia cervicale intraepiteliale) o SIL possono regredire spontaneamente. Il Pap-test e la colposcopia sono strumenti essenziali per monitorare queste alterazioni e intervenire solo se necessario.
- Iperplasia endometriale: Ispessimento della mucosa uterina causato spesso da uno squilibrio estrogenico. Si distingue in forma con o senza atipie, con la seconda che presenta un rischio di progressione verso il tumore decisamente più contenuto.
La fecondazione eterologa: definizione e contesto normativo
Il termine "fecondazione eterologa" descrive una tecnica di procreazione medicalmente assistita (PMA) che impiega gameti, ovociti o spermatozoi, di donatori esterni alla coppia. Diverse sono le ragioni che rendono la via della fecondazione eterologa un’opzione necessaria.
Quando si ricorre all'eterologa
La fecondazione eterologa con donazione di gameti viene indicata, previa valutazione medica in un centro specializzato, per diverse ragioni cliniche che possono riguardare uno o entrambi i partner. Si ricorre a questa procedura quando non sono disponibili i gameti di uno dei partner o per evitare la trasmissione di malattie genetiche. Le casistiche includono:
- Infertilità femminile: Assenza di ovuli (causata ad esempio da sindrome di Turner o menopausa precoce). In questo caso si parla di ovodonazione.
- Infertilità maschile: Mancanza di spermatozoi o condizioni che impediscono la fecondazione naturale.
- Prevenzione genetica: Possibilità di richiedere ulteriori approfondimenti per escludere la trasmissione di patologie genetiche di rilievo.
Il quadro legale in Italia
Il divieto iniziale introdotto dalla legge 40/2004 è caduto nel 2014 con la sentenza della Corte Costituzionale n. 162/2014. Oggi, la procedura è accessibile a coppie (coniugi o conviventi di sesso diverso) maggiorenni, in età potenzialmente fertile e viventi. Il sistema italiano prevede l'anonimato assoluto del donatore, escludendo a priori parenti o amici.
Il percorso della fecondazione eterologa
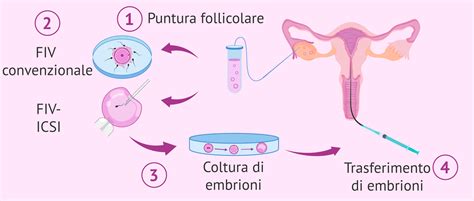
La procedura segue passaggi rigorosi e personalizzati:
- Diagnostica: La coppia viene sottoposta a indagini cliniche per verificare l'idoneità alla gravidanza e psicologiche.
- Selezione del donatore: Si ricerca un profilo compatibile dal punto di vista fenotipico (colore di capelli, occhi, pelle, altezza) e biologico (gruppo sanguigno).
- Stimolazione e prelievo: Nella donna, si procede con una stimolazione ormonale per indurre la crescita follicolare, seguita dal prelievo degli ovociti (pick up) in anestesia locale sotto controllo ecografico.
- Fecondazione: In laboratorio, gli ovociti vengono fecondati con il seme del donatore o del partner (a seconda del caso), spesso utilizzando tecniche avanzate come l'IMSI (selezione degli spermatozoi ad alto ingrandimento) per ottimizzare la qualità degli embrioni.
- Embrio transfer: Gli embrioni vengono trasferiti nell'utero tramite un catetere sottile sotto guida ecografica.
La donazione da congelato è attualmente la tecnica più frequente in Italia, poiché permette l'importazione di gameti da centri esteri autorizzati, sopperendo alla scarsità di donatori nel territorio nazionale. Gli aspetti economici variano a seconda che la struttura sia privata o convenzionata con il Servizio Sanitario Nazionale, rendendo fondamentale una valutazione trasparente dei costi e delle fasi del percorso clinico.