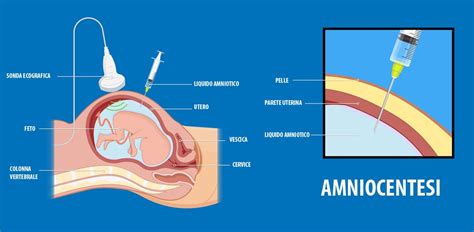
L'amniocentesi è una procedura medica fondamentale nel campo della diagnosi prenatale, che consente di ottenere informazioni preziose sulla salute e sul corredo genetico del feto. Si tratta di un prelievo transaddominale di liquido amniotico dalla cavità uterina, un liquido che circonda e protegge il bambino durante la gravidanza, e rappresenta la metodica più diffusa per ottenere campioni biologici utili a questo scopo. Le sue radici affondano agli inizi del XIX secolo, quando era una pratica chirurgica per il polidramnios o per l'instillazione di soluzioni ipertoniche finalizzate a indurre l'aborto, ma con il tempo si è evoluta in uno strumento diagnostico di precisione.
La decisione di sottoporsi a test diagnostici invasivi come l'amniocentesi è molto importante e spetta alla coppia, la quale dovrebbe consultarsi con il proprio medico (ed in famiglia) per decidere quali ricerche vuole eseguire sul liquido amniotico. In generale, l'amniocentesi genetica viene consigliata quando i risultati dei test prenatali potrebbero avere un impatto significativo sulla gestione della gravidanza, per esempio in presenza di una condizione cromosomica anomala o un difetto del tubo neurale in una precedente gravidanza, o una storia familiare di una condizione genetica specifica, o ancora quando i genitori sono portatori di una malattia genetica. Si configurano in genere due situazioni cliniche: quella routinaria, la cui scelta è legata alle decisioni della coppia e al loro più o meno profondo interesse a conoscere lo stato di salute del proprio figlio, e quella in cui gli accertamenti sono mirati alla presenza di una problematica specifica, definita per le coppie "a rischio". In questi casi, la diagnosi genetica va a esplorare proprio quella che si ritiene essere la patologia con un maggior rischio di ricorrenza nella coppia o per la quale esistono segni ecografici tali da indicarne l'opportunità di ricerca.
L'amniocentesi genetica è fatta solitamente dopo la 15esima settimana di gravidanza. Preliminarmente all’indagine, presso un centro specializzato, vengono effettuate un’ecografia e una consulenza genetica. La consulenza genetica prevede la valutazione dei possibili rischi di coppia, sulla base della storia personale e familiare della signora in gravidanza e del partner. Il prelievo del liquido amniotico si esegue tra la 15esima e la 18esima settimana di gestazione e consiste nell’aspirare, sotto diretta guida ecografica, una modesta quantità di liquido amniotico, che altro non è che un po’ di urina del bambino.
Le Diverse Tipologie di Amniocentesi e le Loro Capacità Diagnostiche
Con il passare degli anni, le ricerche sul liquido amniotico si sono sempre più arricchite mediante l'impiego di metodiche di biologia molecolare sempre più raffinate. Schematicamente, si propongono tre pannelli diagnostici principali, la cui scelta è, in genere, affidata al medico e discussa con la coppia a seguito di una consulenza genetica approfondita.
Amniocentesi Tradizionale di Base: Un Primo Sguardo ai Cromosomi
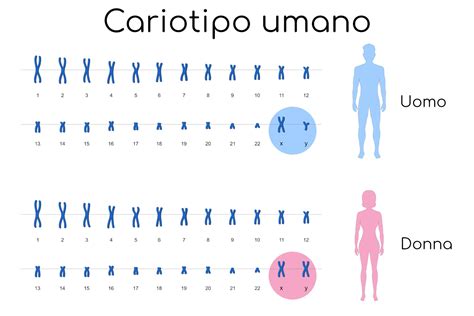
La prima opzione è quella dell'amniocentesi tradizionale di base, che rappresenta il primo pannello ad essere utilizzato ed è ancora il più diffuso. Essa indaga essenzialmente su quelle forme patologiche che interessano il numero e l’aspetto grossolano dei cromosomi. È una tecnica citogenetica che analizza il cariotipo, la rappresentazione ordinata del corredo cromosomico di un individuo, approfondendo l’analisi con tecniche di bandeggio, una sorta di colorazione a "bande" dei cromosomi per indagarne la struttura. Questo esame fornisce "certezze" ma limitatamente alle maggiori problematiche, come ad esempio la sindrome di Down. Tuttavia, va precisato che l'amniocentesi tradizionale di base non garantisce affatto che il feto sia esente da tutte le malattie genetiche. Nulla si potrà sapere delle piccole alterazioni dei cromosomi e sull’esistenza di alterazioni dei geni in essi contenuti. Questo tipo di amniocentesi svela solo circa il 5% dei portatori di anomalie genetiche rispetto alle indagini più avanzate. Essa include, in genere, anche uno studio dell'alfa-fetoproteina, una proteina che, se presente in quantità marcata, può far insorgere il sospetto dell'esistenza di un difetto nel tubo neurale. Gli esiti delle analisi rapide per sindrome di Down, sindrome di Edwards, sindrome di Patau e la determinazione del sesso saranno disponibili entro 2 giorni e saranno comunicati alla coppia direttamente dal genetista.
Amniocentesi con Studio Parziale del DNA: Ampliando lo Spettro Diagnostico
La seconda opzione è quella dell'amniocentesi con studio parziale del DNA. Questa procedura comprende, oltre allo studio tradizionale dei cromosomi, anche la ricerca delle mutazioni principali che causano le malattie geniche più frequenti nella popolazione. A quest'indagine si aggiungono spesso ricerche specifiche, come quelle riguardanti la fibrosi cistica, il ritardo mentale da X-fragile, la sordità congenita, la distrofia muscolare e l'atrofia muscolare spinale (SMA). Queste malattie sono in genere trasmesse da genitori portatori sani che non sanno di esserlo. Questa metodologia è in grado di studiare molto più approfonditamente le varie porzioni dei cromosomi in modo da analizzare la loro integrità strutturale. In pratica, oltre a fornire un’indicazione sul numero dei cromosomi, come l’amniocentesi tradizionale, è in grado di diagnosticare numerose sindromi da microdelezione o microduplicazione, che sono più di 100 sindromi.
Amniocentesi e villocentesi: cosa sono e quando farle
Amniocentesi Genomica (NGPD/TRIO): La Rivoluzione Diagnostica Completa
Esiste poi una terza opzione che rappresenta l’indagine più ampia che possa essere oggi eseguita nel liquido amniotico e che utilizza tecniche sofisticate ed estese di analisi del DNA. La vera rivoluzione diagnostica è avvenuta con l’attuale introduzione dei panel basati sullo studio dell’esoma, quella porzione del DNA che progetta il nostro organismo. Tali indagini hanno permesso di conoscere un numero teoricamente completo di patologie genetiche note. Questo tipo di ricerca, nota come amniocentesi genomica o Next Generation Prenatal Diagnosis (NGPD), arriva a diagnosticare tra il 50-60% delle malattie genetiche note, e può arrivare a diagnosticare l'80% delle malattie genetiche note, contro il 7% delle tecniche attuali.
La Next Generation Prenatal Diagnosis (NGPD) fornisce tutte le informazioni oggi eticamente diagnosticabili con le più recenti metodologie genomiche. Prevede lo studio del cariotipo fetale, affiancato alle moderne tecniche di citogenetica molecolare (array-CGH) e di biologia molecolare (Next Generation Sequencing - NGS). Questo approccio consente di ridurre il rischio che il feto sia affetto da una specifica patologia genetica come nessun’altra indagine prenatale ha potuto e può fare. Le anomalie genetiche più frequenti verranno studiate ed escluse, e le eventuali alterazioni individuate saranno valutate e illustrate in sede di consulenza genetica alla gestante.
La NGPD non permette di giungere al 100% di diagnosi solo perché vengono escluse tutte quelle patologie estremamente rare, quelle ad origine genetica dubbia o sconosciuta, oppure quelle per le quali non è "eticamente" permesso di indagare. Si premette che la NGPD non studierà i cosiddetti polimorfismi di suscettibilità (SNP), cioè quelle varianti geniche che ci rendono suscettibili a qualsiasi malattia e soprattutto al cancro. In teoria, ogni anomalia fetale geneticamente determinata, dai più grandi difetti fino alle sindromi più rare, potrebbe oggi essere individuata prima di nascere. Tuttavia, sapere tutto non solo non è utile ed eticamente accettabile, ma addirittura sarebbe pericoloso e inammissibile per la dignità dell’individuo. Per evitare questa pericolosa ed ossessiva indagine genetica, si sono escluse tutte le ricerche sui "polimorfismi di suscettibilità" per malattie degenerative, per patologie tumorali e per quelle patologie a insorgenza tardiva nella vita. Si è allontanato così il rischio, anche remoto, di aprire il passo verso una "deriva eugenetica", fornendo invece ai genitori tutte quelle informazioni che possano rasserenare pienamente e consapevolmente sullo stato "concreto e sostanziale" circa la salute del proprio figlio. Si è lavorato pertanto su quelle centinaia di geni i cui difetti o "mutazioni" determinano solo malattie note, molte delle quali addirittura "trattabili" se conosciute fin dalla nascita.
Il TRIO Prenatal Diagnosis è un’innovativa procedura di diagnosi che può rilevare fino a 8.000 malattie genetiche conosciute. È progettato per fornire una diagnosi precoce e precisa delle condizioni genetiche del bambino. Utilizzando tecniche all’avanguardia, tra cui la mappa cromosomica completa e la Next Generation Sequencing (NGS), sia sui villi coriali che sul liquido amniotico, oltre a test sui genitori, il TRIO permette di identificare mutazioni patogenetiche associate a sindromi complesse. Vengono inoltre utilizzate la Multiple Ligand Polymorphism Assay (MLPA) e la PCR Sequencing per un’analisi più dettagliata. Questo studio genetico completo ed innovativo viene chiamato AMNIOCENTESI GENOMICA, ovvero Next Generation Prenatal Diagnosis (NGPD).
La residua possibilità di avere un figlio con problemi genetici resta legata a forme patologiche rarissime ed a difetti multifattoriali a volte non determinabili con certezza neanche dopo la nascita. Si deve essere consapevoli che la natura potrebbe creare, occasionalmente, una nuova mutazione oggi non ancora conosciuta e questo purtroppo non potrà essere diagnosticata come patologica fino a quando gli studi scientifici su questa nuova mutazione non abbiano stabilito una correlazione clinica precisa. In conclusione, ad oggi, la NGPD è la sola tecnica in grado di fornire in tempi strettissimi, ed in maniera assoluta, la massima quantità di informazioni sullo stato di salute del feto. Le informazioni che fornisce la NGPD possono essere di guida per l’ostetrico, sia nella fase diagnostica della gravidanza che al momento del parto. Facciamo l’esempio di un feto che presenta, già dallo studio dei villi coriali a 11 settimane, un difetto genetico per cardiopatia congenita; in questo caso il ginecologo seguirà con attenzione lo sviluppo del cuoricino onde studiare con maggiore attenzione il tipo e la gravità della malformazione cardiaca derivante dal messaggio genetico alterato, che, come sappiamo, può esprimersi in misura diversa da caso a caso.
Non è possibile raggiungere il 100% di diagnosi perché anche utilizzando la NGS non si può escludere l'insorgenza di una nuova mutazione genetica; inoltre, un discreto numero di errori genetici non può essere analizzato e riferito per ragioni etiche e cliniche.
Patologie Genetiche Rilevabili Tramite Amniocentesi e il Caso della SMA
Diverse patologie genetiche possono essere identificate attraverso l'amniocentesi. L'amniocentesi e la villocentesi sono diagnosi che permettono di analizzare la forma ed il numero dei cromosomi del feto. Inoltre, all’interno delle valutazioni di routine nell’amniocentesi e nella villocentesi, è possibile eseguire una serie di analisi aggiuntive, finalizzate al controllo delle malattie mendeliane e cromosomiche meno frequenti. Esiste infatti un rischio, comune a tutte le coppie, che il figlio possa presentare microdelezioni e microduplicazioni cromosomiche (non evidenziabili con l’analisi del cariotipo né con tecniche non invasive, come il Prenatal Advance) o possa essere affetto da malattie mendeliane frequenti nella popolazione italiana. Questi esami diagnostici si effettuano a tutte le età, in quanto le patologie che vengono controllate non sono necessariamente associate all’età materna avanzata, sebbene sia noto che le trisomie dei cromosomi 13, 18 e 21 diventano più probabili con l’avanzare dell’età della madre.
Tra le malattie mendeliane più conosciute e rilevabili figurano:
Atrofia Muscolare Spinale (SMA): La SMA rappresenta un gruppo di 4 forme di gravi disordini neuromuscolari piuttosto conosciute per gli effetti devastanti che conducono alla progressiva degenerazione dei neuroni fino all’impossibilità di compiere movimenti. È una patologia genetica rara che colpisce i motoneuroni, le cellule responsabili del controllo dei movimenti, e comporta una progressiva deboleazione muscolare. Nelle forme più gravi, rappresenta una delle principali cause genetiche di morte infantile. Si trasmette in modalità autosomica recessiva e dall’unione di 2 genitori portatori sani (si stima che in Italia vi sia 1 portatore sano ed inconsapevole ogni 35-50 soggetti). La SMA è causata dalla mancanza del gene SMN1, essenziale per la produzione della proteina necessaria alla sopravvivenza dei motoneuroni, e nel 95% dei casi da specifiche mutazioni del gene SMN1 localizzato sul cromosoma 5 (e, in misura minore, del gene SMN2), che codifica per la proteina SMN (Survival Motor Neuron). La forma più grave è la SMA1 (detta anche Malattia di Werdnig-Hoffmann), provocata da una gravemente insufficiente produzione di proteina SMN, e l'insufficienza respiratoria è, in assenza di trattamento efficace, la causa di morte per i pazienti. La variante SMA2 può avere esito infausto anche durante l'infanzia, e i sintomi sono tipici di tutte le atrofie muscolari spinali, ma la progressione della patologia è più lenta e l'aspettativa di vita più lunga, ma sempre dipendente dall'eventuale sopraggiungere di complicazioni respiratorie. I neonati affetti da SMA manifestano molto precocemente segni di scostamento negli standard di accrescimento e sviluppo rispetto ai loro coetanei sani, crescendo, non sono in grado di camminare e faticano a stare seduti da soli (nelle forme più gravi stare seduti da soli risulta impossibile), a tenere dritto il collo. I test genetici diagnosticano circa il 95% delle forme di SMA, che può essere accertata nella fase prenatale attraverso l'esecuzione della villocentesi o dell'amniocentesi. Dal 2017 è disponibile in Italia il primo farmaco specifico per questa malattia, Nusinersen, che ha mostrato di migliorare la funzionalità motoria e ritardare invalidità e morte. Risdiplam (nome commerciale Evrysdi), un oligonucleotide antisenso (ASO), è in commercio da qualche anno per il trattamento della SMA, e l'Agenzia Italiana del Farmaco (AIFA) ha esteso le indicazioni di risdiplam, approvando il trattamento per i bambini affetti da atrofia muscolare spinale di tipo 1, 2 o 3 oppure aventi da 1 a 4 copie di SMN2 anche al di sotto dei due mesi di vita. Nel 2019 è stata approvata negli Stati Uniti la prima terapia genica per la SMA, onasemnogene abeparvovec (Zolgensma), autorizzata per le diagnosi di SMA di tipo 1 e di tipo 2.
Fibrosi Cistica: È una malattia a trasmissione autosomica recessiva che si manifesta solo quando il gene viene ereditato da entrambi i genitori eterozigoti asintomatici (detti portatori). Attualmente sono note circa 1500 mutazioni responsabili con incidenza variabile, e altre mutazioni sono ancora sconosciute.
Sindrome di Martin Bell o X-Fragile: Causata dall’alterazione di un gene situato nel cromosoma X che determina quadri variabili di ritardo mentale. Esistono inoltre pazienti portatori (detti pazienti premutati). L’esame rileva feti di sesso maschile affetti dalla patologia, feti di sesso maschile e femminile premutati (portatori), e rari casi di sesso femminile affetti.
Sordità Congenita: Il rischio di ricorrenza della sordità congenita per cause genetiche, ambientali o infettive alla nascita è di 1 caso su 1000. Il presente screening rileva esclusivamente le sordità da alterazione del gene GJB2 che codifica per la proteina connexina 26, le cui mutazioni sono responsabili di circa la metà dei casi di sordità ereditaria. Con lo screening non è possibile rilevare tutte le mutazioni del gene GJB2 ma, con la metodica utilizzata in alcuni centri, si giunge ad un’accuratezza di circa l’80-90% delle mutazioni.
Distrofia Muscolare di Duchenne: È una malattia causata dall’alterazione del gene della distrofina situato sul cromosoma X. La patologia colpisce solo i maschi e viene trasmessa da femmine portatrici sane. Raramente anche le femmine possono risultare affette. Con lo studio genetico in alcuni centri si analizza circa il 70% dei casi dovuti alle principali delezioni (18 esoni) e perdita di vaste regioni geniche.
Oltre a queste, l'amniocentesi avanzata può rilevare altre condizioni come le malattie metaboliche e lisosomiali. Recentemente, per ragioni etiche, in alcuni centri si è iniziato ad includere, gratuitamente e di routine, lo screening delle malattie metaboliche, basato sulla rilevazione dei composti amminoacidici e purinico-purimidinico nel liquido amniotico. Queste mutazioni genetiche comportano l'alterazione di una proteina coinvolta in processi metabolici fondamentali per la vita delle cellule, potendo colpire e danneggiare organi e tessuti diversi.Tra le malattie lisosomiali, si sono estesi gli screening usuali a patologie come:
- Malattia di Pompe: una glicogenosi (Glicogenosi di tipo II), malattia da accumulo nei lisosomi di glicogeno, causata dalla carenza dell'enzima deputato al suo metabolismo. È una patologia neuromuscolare, cronica, debilitante e spesso letale, che colpisce i muscoli, compreso quello striato involontario del cuore e i muscoli respiratori.
- Malattia di Fabry: malattia che comporta l'accumulo dei glicosfingolipidi e scatena sintomi multisistemici, tra cui neurologici (dolore), neurovascolari (ictus, ischemie transitorie) dermatologici (angiocheratoma), renali (proteinuria, insufficienza renale), cardiovascolari (cardiomiopatia, aritmia).
- Mucopolisaccaridosi di tipo I: malattia causata da accumulo di glicosaminoglicani, con varianti più lievi (Sindrome di Scheie) e più gravi (Sindrome di Hurler).
- ADA-Scid: la più grave forma di immunodepressione congenita, dovuta al deficit di adenosin-deaminasi.
- Adrenoleucodistrofia: comporta l'accumulo di acidi grassi saturi a lunga catena all'interno degli oligodendrociti, le cellule di sostegno ai neuroni che producono la mielina.
- Leucodistrofia metacromatica: una patologia lisosomiale degenerativa che porta all'accumulo di sulfatidi, in particolare a livello della guaina mielinica.
Un Caso Pioniere: Il Trattamento Intrauterino della SMA
Per la prima volta nella storia della medicina, una bambina affetta da una grave forma di atrofia muscolare spinale (SMA) è stata trattata con successo mentre era nel grembo materno con una terapia somministrata alla madre. Questo caso pionieristico, la cui decisione è partita dai genitori che avevano già perso un figlio a causa della SMA, ha visto la diagnosi confermata mediante test genetici prenatali, che non hanno rilevato copie del gene SMN1 ma due copie di SMN2. Grazie a un’autorizzazione speciale della Food and Drug Administration (FDA) statunitense, alla madre è stato somministrato risdiplam per sei settimane a partire dalla 32esima settimana di gravidanza. Il farmaco è stato assunto quotidianamente dalla madre, permettendo il suo passaggio attraverso la placenta al feto. Durante il trattamento, la madre è stata monitorata settimanalmente per valutare eventuali effetti collaterali e per controllare lo sviluppo del feto tramite ecografie e analisi specifiche.
Le analisi condotte al momento della nascita hanno confermato che il farmaco era riuscito a raggiungere il feto, aumentando i livelli della proteina SMN e riducendo i danni ai motoneuroni. La bambina ha poi iniziato ad assumere lo stesso farmaco pochi giorni dopo il parto e probabilmente continuerà ad assumerlo per tutta la vita. Risdiplam sembra essere stato efficace anche se assunto dalla madre in gravidanza: a due anni e mezzo dalla nascita, la bambina non presenta sintomi della malattia. Sebbene la neonata appariva sana alla nascita, è stato identificato un soffio al cuore, risolto in seguito. Presenta anche un’acuità visiva ridotta e altri sintomi collegati allo sviluppo - nessun altro disturbo genetico è stato identificato - ma non sono presenti caratteristiche della SMA. Questo è stato possibile perché la diagnosi è stata fatta ancor prima della nascita, cosa che accade solo quando ci sono stati altri casi in famiglia e vengono fatti i dovuti accertamenti. Altrimenti, per ottenere la diagnosi prima della nascita, è necessario sottoporsi a test diagnostici prenatali, come la villocentesi e l’amniocentesi.
Questo caso rappresenta una pietra miliare nella lotta contro l’atrofia muscolare spinale e potrebbe rivoluzionare l’approccio terapeutico a molte malattie genetiche. Anche se si tratta di un singolo caso, questa esperienza apre nuove possibilità per la medicina prenatale, e studi futuri potrebbero valutare l’efficacia di trattamenti simili in altri bambini affetti da SMA e da altre patologie genetiche per cui i trattamenti postnatali sono insufficienti.

Sicurezza e Rischi dell'Amniocentesi: Dati Attuali e Prevenzione
L’amniocentesi è un esame delicato, considerato invasivo, che un tempo era ritenuto rischioso. Il rischio di aborto spontaneo connesso all’amniocentesi è stato ritenuto, per 30 anni, dell’1%. Tuttavia, studi attuali mostrano che nei centri di eccellenza l’incidenza di abortività spontanea, natimortalità, e mortalità neonatale non sono statisticamente differenti nel gruppo sottoposto ad amniocentesi rispetto a chi non la esegue. La letteratura più recente dimostra come questo rischio, nei vari centri del mondo, si aggiri intorno allo 0,1%. Questo rischio è equivalente rispetto a quello generico di chi non la esegue, poiché anche la popolazione generale di donne che non si sottopongono ad amniocentesi può abortire spontaneamente.
Il classico lavoro di Tabor, che per anni ha fissato il rischio dell'1%, è stato superato da uno studio di eguale disegno clinico, il più grande Trial Randomizzato fino ad oggi pubblicato sulle amniocentesi. Questo trial, eseguito su una popolazione di 36.247 soggetti reclutabili, ha dimostrato che il rischio di aborto, nelle donne che vennero sottoposte ad amniocentesi dopo aver assunto un antibiotico-profilassi, è risultato bassissimo (0,031%). Come necessaria conseguenza di tale risultato scientificamente provato, in considerazione della sua evidenza clinica classificata come Livello IB, l'utilizzo di un antibiotico prima di eseguire un'amniocentesi è divenuta Raccomandazione A. Tutti gli operatori debbono attenervisi fino a quando un trial successivo (di adeguato o maggiore livello di evidenza) non dimostri il contrario. La rottura del sacco amniotico nella stragrande maggioranza dei casi guarisce da sola.
Oltre al rischio di aborto, esiste poi tutta una serie di problematiche che vale la pena di ricordare. La più frequente di queste risulta essere la lipotimia che segue la procedura, determinata da fattori emozionali come la tensione e l'ansia dell'aspettativa, ma anche da vere componenti neurovegetative. L'insorgenza di attività contrattile è un'evenienza piuttosto frequente e transitoria, e l'uso dei betamimetici in tali casi è comunque indicata. La corionamnionite rappresenta una rara complicanza, piuttosto temibile, che conduce ad aborto e, seppur molto raramente, può determinare gravi problemi per la madre. In tali casi, al solo sospetto di tale eventualità, bisogna non porre il minimo indugio al trattamento con antibiotici a dosi generose ad ampio spettro e, se il feto è morto, non differire assolutamente l'intervento di revisione della cavità uterina. La complicanza più temibile risulta comunque la rottura traumatica delle membrane, che accade con un'incidenza di circa 1 caso su 300 amniocentesi, e conduce all'aborto in un caso su 3. Nei casi in cui ciò avvenisse, può essere indicato, oltre al riposo a letto e alla terapia antibiotica e tocolitica, la collocazione di una coppetta cervicale, il più precocemente possibile, monitorizzando attentamente la possibile insorgenza di infezione endoamniotica. È fondamentale eseguire immediatamente un tampone cervicale per riconoscere l'agente infettivo eventualmente presente e trattarlo di conseguenza. Bisogna inoltre ribadire che la rottura traumatica delle membrane accade sovente in soggetti che sono già portatori di un'infezione, in particolare da Mycoplasma o Ureaplasma, dove il trauma determina una riacutizzazione locale del processo infettivo. L'esistenza di un'infezione endoamniotica è anche causa di diverse patologie che possono impedire un buono svolgimento della gravidanza, e per questo sta prendendo sempre più piede la ricerca sul liquido amniotico di alcune sostanze mediatrici della flogosi quali le citochine.
Tempistiche e Specificità delle Procedure di Amniocentesi
Vi sono due momenti distinti della gravidanza in cui è possibile eseguire l'amniocentesi, con scopi diagnostici assai diversi. La sempre maggiore richiesta di ottenere risposte precoci ha indotto, negli ultimi anni, ad eseguire il prelievo del liquido amniotico anche in epoca inferiore alla 15esima settimana di gestazione, come valida alternativa al prelievo dei villi coriali (amniocentesi precocissima).
Amniocentesi Precocissima (Prima della 15ª Settimana)
Per quel che concerne il materiale prelevato per l'amniocentesi precocissima, la coltura abbisogna di una sufficiente cellularità; la quantità minima di liquido richiesto non deve essere inferiore ai 10 ml. In merito al rischio specifico, la letteratura ritiene che per le amniocentesi eseguite intorno alla 14esima settimana il rischio abortivo è sovrapponibile a quello delle amniocentesi della 17esima settimana. Dalle casistiche delle amniocentesi eseguite prima della 14esima settimana, si deduce che tra la 10esima e la 12esima settimana non si hanno informazioni specifiche, anche perché in tali settimane vi è comunque un alto rischio generico abortivo di difficile computo nel calcolo del rischio relativo.
L'esperienza di grandi centri specializzati, che effettuano circa 5000 procedure all'anno, porta a concludere che l'amniocentesi intorno alla 14esima settimana è lievemente meno rischiosa della villocentesi (2 aborti su 1000 procedure). La percentuale di fallimenti di coltura è equivalente all'amniocentesi precoce (1 caso su 300). La percentuale di errori diagnostici è la medesima (inferiore ad 1 caso su 1000 colture), qualora la biopsia dei villi consenta una lettura diretta degli stessi. L'indicazione specifica dell'amniocentesi intorno alla 14esima settimana risulta quindi essere quella citogenetica. Si tratta quindi di un'accettabile alternativa al prelievo dei villi coriali rispetto ai quali risulta gravata da un ridotto rischio abortivo. L'indicazione specifica dell'amniocentesi intorno alla 11esima settimana rimane quella citogenetica, in alternativa alla villocentesi. I risultati diagnostici ritardano circa 2/3 settimane rispetto ai tempi medi di risposta di una villocentesi. Il rischio sembra però sovrapponibile. Anche la percentuale di insuccessi diagnostici per problemi di coltura è il medesimo. Non si vede pertanto il motivo di preferirla alla biopsia dei villi coriali qualora si volessero ottenere risposte in tempi veramente precoci. Per ciò che concerne le problematiche della coltura e della refertazione esse non sembrano differire da quelle dell'amniocentesi precoce.
Amniocentesi tra la 16ª e la 18ª Settimana: La Metodica più Diffusa
L'amniocentesi eseguita tra la 16esima e la 18esima settimana rappresenta a tutt'oggi la metodica più frequentemente utilizzata ai fini diagnostici di citogenetica prenatale. Come si è detto, il rischio abortivo della tecnica si aggira mediamente intorno allo 0,1%. Di tale percentuale si deve tener conto quando si valuta il rischio/beneficio della procedura diagnostica. Il rischio abortivo va infatti comparato con le percentuali di anormalità cromosomiche per l'età. Va inoltre considerato che la percentuale di anomalie riscontrate nelle procedure è sempre maggiore rispetto alla nascita. Le metodiche più precoci sono caratterizzate da un maggior numero di riscontri patologici; ciò è dovuto a una selezione naturale operante durante la gravidanza per i feti patologici.
Esistono tuttavia alcune possibili problematiche nel processo diagnostico. La prima è data dall'insuccesso della coltura, cosa che avviene in 1 caso su 300. La seconda è dovuta alla possibile contaminazione del liquido amniotico con materiale materno. Tale errore, secondo alcuni studi, avviene molto raramente (0,3%) se si ha l'accortezza di gettare le prime gocce di liquido che fuoriescono dall'ago. La terza è il riscontro di aberrazioni cromosomiche generatesi in vitro, durante la coltura, note come pseudomosaicismi. Errori ed artefatti a parte, c'è la possibilità che le sole cellule del liquido amniotico siano portatrici di un vero mosaicismo.
Amniocentesi e villocentesi: cosa sono e quando farle
Screening Neonatale e la Sua Estensione: Un Impegno per la Salute Futura
Lo screening neonatale è fra i più importanti programmi di prevenzione in salute pubblica e ha l’obiettivo di diagnosticare precocemente alcune gravi malattie congenite. Il prelievo viene effettuato dal Centro Nascita e il campione inviato al Centro di Screening Neonatale di riferimento. Nel 2016 è stato introdotto l’obbligo di esecuzione dello screening neonatale, un semplice prelievo di sangue che può diagnosticare malattie potenzialmente mortali che, se trattate tempestivamente, possono consentire una vita quasi normale ai bambini colpiti. Dall’introduzione della Legge Taverna, tutti i neonati sono stati sottoposti alla nascita a screening metabolico per 40 malattie metaboliche o rare, potenzialmente invalidanti o letali.
Attualmente, lo screening neonatale obbligatorio non comprende il test per la SMA. Tuttavia, diverse Regioni si sono attrezzate (o si stanno accingendo a farlo) per estendere gli screening anche all’atrofia muscolare spinale e ad altre malattie. In particolare, nella Regione Lazio è partito un progetto pilota coordinato dall’Università Cattolica del Sacro Cuore di Roma che coinvolge tutti i Centri Nascita del territorio, offrendo il test genetico volontario e gratuito per la SMA. In Toscana lo screening metabolico è obbligatorio dal 2004.
Alla luce dei successi ottenuti con lo screening già introdotto e con le iniziative locali nelle Regioni del territorio, nel 2018 è stato approvato un emendamento alla Legge 167 (AC1334), proposto dall’onorevole Leda Volpi, che prevede l’estensione dello screening alle malattie neuromuscolari genetiche, alle immunodeficienze congenite severe e alle malattie da accumulo lisosomiale. Perché questa norma sia effettivamente attuata, è necessario un Decreto Ministeriale di aggiornamento del panel. Proprio di questa ipotesi di ampliamento si è discusso alla presenza di medici, associazioni pazienti e istituzioni in un convegno tenutosi a Roma.
Amniocentesi vs. Test del DNA Fetale: Una Scelta Informata
Nella scelta tra amniocentesi o test del DNA fetale, è essenziale comprendere le differenze sostanziali che caratterizzano queste due procedure diagnostiche prenatali. L’amniocentesi coinvolge il prelievo di una piccola quantità di liquido amniotico per l’analisi dei cromosomi fetali, offrendo una vasta panoramica genetica del feto. Dall’altro lato, il test del DNA fetale si basa su un semplice prelievo di sangue materno e offre risultati più rapidi. Tuttavia, non è altrettanto dettagliato come l’amniocentesi. La scelta tra le due procedure dipende dalle esigenze della paziente e da una consulenza genetica approfondita. I test di screening, ad esempio translucenza nucale o bitest, sono solo valutazioni ecografiche e biochimiche (ricerca di alcuni marcatori nel sangue materno) utili per valutare il rischio, con più o meno accuratezza, esclusivamente della Sindrome di Down e Trisomia 18. Un tempo la si riteneva utile anche ad ipotizzare un rischio di cardiopatia.
Considerazioni Pratiche e Etiche
Ogni donna deve essere certa che il Centro a cui si rivolge possegga i requisiti idonei stabiliti dalla legge. In pratica, oggi, non è più consentita l’esecuzione di procedure di Diagnosi Prenatale Invasiva in studi medici, ambulatori o poliambulatori medico-specialistici che non rispondano ai requisiti previsti per l’ambulatorio chirurgico o dal day surgery. È importante prestare attenzione a non eseguire tale esame in studi medici o semplici ambulatori specialistici.
Il costo medio di un esame nelle strutture private varia da 500 a 700 euro per l'amniocentesi tradizionale nella quale si ha soltanto l'esame citogenetico tradizionale con una risposta ottenibile in 15-20 giorni. Questo costo però può variare grandemente ed aumentare a seconda degli esami aggiuntivi che oggi, quasi abitudinariamente, vengono eseguiti sul liquido amniotico. Inoltre, in molti laboratori di genetica, si eseguono sul liquido amniotico anche metodiche di biologia molecolare quali l'ibridazione fluorescente in situ (FISH) o, ancor meglio, la reazione a catena della polimerasi (PCR) che permettono di ottenere un risultato in tempi brevissimi (24 o 48 ore). Questo comporta costi aggiuntivi.
Altamedica, da oltre 50 anni, ha un unico obiettivo: dare ai propri pazienti un servizio completo di diagnosi prenatale. La loro struttura, grazie anche alla mano del suo fondatore il professor Claudio Giorlandino, è sempre stata all’avanguardia in questo campo. Il Dr. Pietro Cignini esegue amniocentesi ed altri esami diagnostici a Roma, e per conoscere lo stato di salute del bambino e accedere ai servizi di TRIO Prenatal Diagnosis è possibile contattarli al numero 06 85 05 505 o compilare un modulo di contatto.
Le informazioni riportate non sono consigli medici e potrebbero non essere accurate. È sempre consigliabile consultare un professionista sanitario qualificato.
tags: #sma #con #amniocentesi