Le cellule staminali emopoietiche (HSC) rappresentano una risorsa preziosa per la medicina rigenerativa e per il trattamento di numerose patologie, in particolare quelle oncoematologiche. La loro capacità di rigenerare il midollo osseo danneggiato da malattie, radiazioni o trattamenti chemioterapici le rende fondamentali in ambito clinico. Inizialmente, il midollo osseo era l'unica fonte di HSC, ma la difficoltà nel reperire donatori compatibili e la necessità di interventi terapeutici rapidi hanno spinto la ricerca verso fonti alternative. Il sangue placentare, e successivamente il sangue del cordone ombelicale (SCU), si sono rivelati fonti promettenti di cellule staminali emopoietiche, aprendo nuove frontiere terapeutiche.
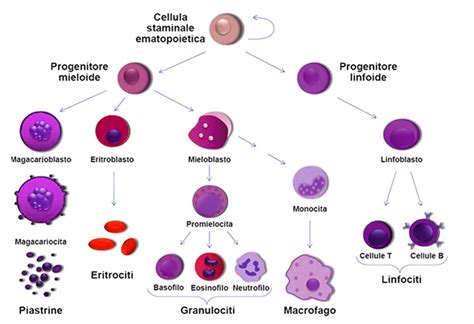
La Cellula Chiave: CD34+
La proteina CD34 è universalmente riconosciuta come il marcatore primario delle cellule staminali ematopoietiche e delle cellule progenitrici emopoietiche. La sua espressione sulla superficie della maggior parte di queste cellule le rende un target fondamentale per i processi di isolamento e purificazione. L'efficacia dei trapianti di cellule staminali è strettamente legata alla quantità e alla vitalità delle cellule CD34+ isolate. Nei trapianti di terapia standard per pazienti oncoematologici, è necessario un numero elevato di cellule staminali per ripristinare la funzione del midollo osseo. Al contrario, nella medicina rigenerativa, le dosi cellulari potrebbero essere meno definite e potenzialmente inferiori.
Tecnologie di Isolamento e Purificazione: Evoluzione e Innovazione
L'isolamento e la purificazione delle cellule CD34+ da sangue cordonale sono passaggi critici per garantire la qualità e l'efficacia delle terapie cellulari. Storicamente, i processi di isolamento hanno comportato una notevole perdita di cellule, richiedendo tempi lunghi e processi complessi. Tuttavia, l'innovazione tecnologica ha portato allo sviluppo di piattaforme avanzate che mirano a massimizzare la resa, la purezza e la vitalità delle cellule.
Piattaforme a Circuito Chiuso e Automazione
Le piattaforme moderne come SEPAX e AXP rappresentano un progresso significativo in questo campo. La piattaforma SEPAX, in particolare, consente una lavorazione a circuito chiuso, garantendo un ambiente sterile e riducendo il rischio di contaminazione. Questa tecnologia è riconosciuta per la sua capacità di fornire un prodotto finale di alta qualità, anche dopo la criopreservazione per il bancaggio a lungo termine. Smart Cells, un'entità che utilizza queste tecnologie, svolge regolarmente controlli per verificare la resa del campione non solo dopo la processazione, ma anche dopo le fasi di congelamento e scongelamento. L'efficacia di queste metodologie è attestata dal successo di migliaia di pazienti trapiantati in tutto il mondo con unità di sangue cordonale processate con metodi Sepax o AXP. Un parametro chiave per l'utilizzo clinico accettato dai centri più importanti è una resa post-scongelamento di circa il 70% delle cellule staminali CD34+ vitali.
La piattaforma MARS® di Applied Cells introduce un approccio trasformativo alla separazione cellulare. La sua tecnologia "in-flow" senza colonne offre flessibilità nell'ottimizzazione del flusso di lavoro, massimizzando purezza e tassi di recupero. Permette l'isolamento diretto di cellule target, anche quelle presenti in basse percentuali, da diversi tipi di campioni, tra cui il sangue del cordone ombelicale (CBMC) e il sangue periferico. Questo sistema promette una riduzione significativa dei costi di analisi (fino al 60%) e dei tempi di sperimentazione (quasi il 50% per un campione di 50 mL). Il processo di isolamento automatizzato e semplificato garantisce elevata purezza e tassi di recupero cellulare superiori con tempi di intervento minimi, grazie a un arricchimento cellulare automatizzato da uno a tre passaggi e all'isolamento senza matrice.
Tecniche Innovative di Separazione
La ricerca sperimentale continua a esplorare nuove vie per migliorare l'efficienza della purificazione. Una nuova tecnica, basata sul partizionamento bifasico per immunoaffinità in ambiente acquoso, è stata sviluppata per la separazione e purificazione di staminali/progenitrici CD34+ da sangue cordonale non processato. Questo sistema impiega due fasi: una contenente glicole polietilenico (PEG) per il recupero delle cellule CD34+ e una seconda fase ricca in destrano per la raccolta delle cellule contaminanti (non CD34). Gli autori di questa ricerca riportano un recupero di staminali CD34+ del 95% e un fattore di purificazione pari a 245, dimostrando un potenziale significativo per l'ottimizzazione dei processi.
Contesto Storico e Applicazioni Cliniche
L'utilizzo del sangue del cordone ombelicale per il trapianto di cellule staminali ha una storia di successo che risale a oltre 30 anni fa. Il primo trapianto di cellule staminali derivate dal sangue cordonale fu eseguito nel 1988 dalla ricercatrice francese Éliane Gluckman e dallo statunitense Hal Broxmeyer su un bambino affetto da anemia di Fanconi. Questo evento pionieristico ha aperto la strada a un'ampia gamma di applicazioni cliniche.
La prof.ssa Joanne Kurtzberg, figura di spicco nel campo, è stata la prima a eseguire un trapianto di cellule staminali da sangue cordonale tra donatori non imparentati nel 1993, estendendo poi questa pratica anche agli adulti. Sotto la sua guida, il Marcus Center for Cellular Cures e lo Stem Cell Transplant Laboratory alla Duke University hanno ampliato l'uso del sangue cordonale come fonte di cellule staminali per il trattamento di diverse patologie, utilizzando questa preziosa risorsa al posto del midollo osseo o del sangue periferico.
ADISCO UN DONO PER LA VITA ep 02
Oltre l'Ematopoiesi: Nuove Frontiere Terapeutiche
Il potenziale delle cellule staminali cordonali non si limita alla rigenerazione del midollo osseo. Il laboratorio della prof.ssa Kurtzberg ha sviluppato la terapia cellulare DUOC-1, coltivando cellule microgliali/macrofagiche derivate dal sangue cordonale. Queste cellule, analoghe ai macrofagi, hanno dimostrato la capacità di promuovere la remielinizzazione, un processo vitale per il ripristino della guaina mielinica danneggiata nel sistema nervoso. DUOC-1 è destinata al trattamento di malattie neurodegenerative e demielinizzanti, mostrando risultati promettenti nella prevenzione della progressione della paralisi in modelli sperimentali di encefalite autoimmune, una condizione utilizzata per studiare la sclerosi multipla.
Il team della Duke University ha sviluppato protocolli innovativi che utilizzanoDUOC per trattare le leucodistrofie e la sclerosi multipla. Un approccio sperimentale prevede l'utilizzo di una frazione di unità di sangue cordonale per la ricostituzione ematopoietica e la restante parte per produrre cellule DUOC, somministrate in seguito per favorire la memorizzazione dell'innesto e accelerare il raggiungimento delle cellule al cervello. Attualmente, è in corso uno studio clinico di Fase Ia per testare la sicurezza e l'efficacia delle DUOC come unico agente in pazienti adulti con sclerosi multipla progressiva primaria, valutando anche la remielinizzazione tramite risonanza magnetica.
Un'altra area di ricerca attiva è l'applicazione del trapianto di sangue cordonale autologo nella paralisi cerebrale. Studi preclinici e clinici di fase II hanno mostrato risultati promettenti, suggerendo che infusioni di sangue cordonale autologo, somministrate in dosi adeguate, possono migliorare la connettività cerebrale e la funzione motoria nei bambini con paralisi cerebrale. L'effetto più significativo è stato osservato nei bambini con paralisi cerebrale moderata, incoraggiando l'avvio di nuovi studi clinici per dimostrare l'efficacia di queste infusioni.
Fattori che Influenzano la Qualità delle Unità di Sangue Cordonale
La qualità delle unità di sangue cordonale raccolte è un fattore cruciale per il loro utilizzo clinico. Uno studio condotto dalla dott.ssa Stefania Fumarola ha evidenziato come diversi fattori prenatali e materni influenzino significativamente il contenuto di cellule staminali. Ad esempio, campioni di cellule staminali cordonali prelevate da neonati maschi, con età gestazionale inferiore a 39 settimane, nati tramite parto cesareo e con un contenuto di cellule nucleate totali (TNC) superiore a 3,44x10^8, hanno mostrato un contenuto di CD34+ significativamente più alto rispetto a campioni di neonati femmine con età gestazionale superiore a 39 settimane e nati con parto vaginale.
Questi risultati hanno permesso di definire un modello predittivo indispensabile per aumentare la disponibilità di campioni utilizzabili, un aspetto fondamentale in un periodo storico caratterizzato da un calo delle nascite. La dottoressa Fumarola sottolinea come i campioni di cellule staminali da cordone ombelicale rappresentino una fonte di speranza per numerose patologie, come evidenziato anche dal Ministero della Salute.
La creazione di una rete nazionale di biobanche, che integri settore pubblico e privato attraverso una stretta collaborazione, è considerata un punto di partenza essenziale per valorizzare al meglio i campioni disponibili, adottando un modello ibrido già in vigore in altri paesi con notevoli vantaggi.
Mobilizzazione di Cellule Staminali dal Sangue Periferico
In determinate circostanze, le cellule staminali emopoietiche possono essere mobilizzate dal midollo osseo nel sangue periferico. La chemioterapia, in particolare quella che induce moderata o severa citopenia, si è dimostrata efficace nel mobilizzare queste cellule, con un picco di progenitori emopoietici circolanti durante il recupero ematologico post-aplasia midollare.
Per ottimizzare questo processo, vengono utilizzati protocolli di chemioterapia seguiti dalla somministrazione di fattori di crescita emopoietici, come il G-CSF (Granulocyte Colony-Stimulating Factor). Il G-CSF stimola la crescita delle cellule staminali nel midollo osseo, portando a un aumento significativo dei progenitori emopoietici e delle cellule CD34+ circolanti. La raccolta di queste cellule avviene tramite procedure di leucoaferesi, utilizzando separatori cellulari a flusso continuo.
La mobilizzazione con solo fattore di crescita prevede la somministrazione giornaliera di G-CSF per 5 giorni. La raccolta delle cellule staminali è programmata intorno al quinto giorno, quando si osserva il picco di cellule CD34+ circolanti. È importante notare che la mobilizzazione tramite chemioterapia è riservata ai pazienti candidati alla raccolta di CSE per uso autologo, mentre per i donatori allogenici si utilizza esclusivamente il fattore di crescita.
La procedura di leucoaferesi richiede generalmente 3-4 ore e il prelievo di un volume di sangue periferico compreso tra 9 e 12 litri. Sebbene ben tollerata nell'adulto, la procedura può presentare criticità nei pazienti pediatrici di basso peso corporeo a causa del volume extracorporeo e dell'infusione di anticoagulante (ACD-A), che può causare ipocalcemia sintomatica. L'inadeguatezza dell'accesso vascolare rappresenta un'altra potenziale causa di effetti collaterali. In condizioni ottimali, è possibile raccogliere almeno 3-5x10^6 cellule CD34+/kg con 1-3 procedure di leucaferesi.
Conclusioni Parziali
La purificazione delle cellule CD34+ da sangue cordonale è un campo in continua evoluzione, guidato dall'innovazione tecnologica e dalla crescente comprensione del potenziale terapeutico delle cellule staminali. Dalle piattaforme a circuito chiuso alle nuove tecniche di separazione, l'obiettivo è garantire processi efficienti, sicuri e in grado di fornire un prodotto cellulare di alta qualità per applicazioni cliniche e di ricerca. Le scoperte in aree come le terapie per malattie neurodegenerative e la paralisi cerebrale ampliano ulteriormente l'orizzonte delle possibilità offerte da queste preziose cellule.
tags: #purificazione #cd34 #da #cordone #ombelicale