Il diabete gestazionale rappresenta una condizione specifica che emerge nel corso della gravidanza, caratterizzata da un aumento dei valori medi di glicemia, ovvero della quantità di zucchero nel sangue. Questa patologia endocrinologica della donna, di cui la maggiore incidenza si rileva nel secondo trimestre, è in gran parte asintomatica, motivo per cui non è infrequente che la condizione venga diagnosticata con un certo ritardo. È fondamentale distinguere il diabete gestazionale dal diabete pregravidico, ossia quando la condizione è già presente prima della gestazione, tipicamente il diabete mellito di tipo 1, il quale comporta rischi elevati, talvolta superiori, per madre e feto fin dal concepimento.
Il diabete gestazionale è un'intolleranza ai carboidrati, di gravità variabile, ad esordio o primo riscontro in gravidanza. La sua elevata frequenza, il rischio di passare misconosciuto e l'efficacia dell'intervento terapeutico nel ridurre la morbilità materno-fetale ad esso correlata, lo rendono una patologia per cui è indicato un programma di screening e diagnosi precoce. Questa condizione non è rara, con dati di prevalenza nazionali ed europei che indicano circa il 6-7% di tutte le gravidanze complicate da diabete, il che si traduce in oltre 40.000 gravidanze ogni anno solo in Italia. La sua frequenza è aumentata sensibilmente negli ultimi decenni, con un raddoppio dei tassi di incidenza in tutti i gruppi etnici. L'importanza del diabete gestazionale è legata alle molteplici problematiche ad esso correlate, che determinano un aumento della morbilità nella madre, nel feto e nel bambino a distanza di anni dal parto.

Comprendere il Diabete Gestazionale: Definizione e Meccanismi Fisiologici
Nel corso della gravidanza, si verifica il rilascio di ormoni di origine placentare che determinano un’aumentata resistenza dei tessuti all’azione dell’insulina, una condizione nota come insulino-resistenza. Questa condizione è in sé ‘fisiologica’, finalizzata al migliore utilizzo dei nutrienti necessari alla crescita fetale e si verifica soprattutto nella seconda metà della gestazione. Tuttavia, quando questa ‘resistenza’ all’insulina, in particolare se potenziata dall’eccesso di peso - causa principale dell’insulino-resistenza al di fuori dello stato gravidico -, non è sufficientemente compensata dalla secrezione di insulina, la glicemia in gravidanza tende ad elevarsi fino a sfociare nel diabete gestazionale.
Per comprendere appieno i meccanismi alla base del diabete gestazionale, è utile esaminare il processo con cui il corpo gestisce gli zuccheri. Quando consumiamo alimenti contenenti carboidrati - zuccheri semplici come nei dolci, ma anche molecole più complesse come nel caso del pane e della pasta - questi vengono frammentati a molecole di glucosio a livello intestinale per essere poi assorbite e passare così nel sangue. Questo processo determina un immediato aumento della glicemia, ossia della quantità di zuccheri nel sangue. Poiché livelli elevati possono causare danni alla maggior parte dei tessuti dell’organismo, la risposta del corpo consiste nella produzione di insulina, un ormone che stimola le cellule muscolari a prelevare il glucosio nel sangue, così da riportare rapidamente la glicemia a livelli normali, una condizione che gradualmente spegne la produzione di insulina. Questo processo, sebbene qui semplificato e scomposto in singoli passi per favorirne la comprensione, consiste in realtà in un equilibrio dinamico che viene controllato ed eventualmente corretto 24 ore su 24.
Nel contesto del diabete, possono verificarsi due scenari principali che portano all'iperglicemia. Il primo è quando la produzione di insulina è insufficiente per una disfunzione primitiva delle cellule beta del pancreas endocrino, meccanismo alla base dello sviluppo del diabete mellito di tipo 1. Il secondo si manifesta quando l’insulina prodotta non funziona più correttamente a causa di un’alterata sensibilità dei tessuti periferici alla sua azione, un fenomeno di insulino-resistenza che è il meccanismo alla base del diabete mellito di tipo 2, particolarmente rilevante in caso di obesità.
I meccanismi patogenetici alla base del diabete gestazionale sono invece per gran parte sconosciuti, ma l’ipotesi prevalente suppone che il progressivo aumento del fenomeno di resistenza all’azione dell’insulina che si osserva nel secondo trimestre di gravidanza sia conseguente ai cambiamenti ormonali che affronta la donna nel corso della gestazione, con l’obiettivo di garantire al feto una sufficiente quota di glucosio per il suo sostentamento. Per questo motivo sono state introdotte specifiche tecniche di screening per la patologia, in modo da riconoscerla e contrastarla con efficacia sin dalle prime manifestazioni. Il manifestarsi del diabete gestazionale è correlato sia a fattori genetici o ereditari, sia all’azione degli ormoni placentari che possono indurre insulino resistenza e quindi interferire con la regolazione dei livelli di glucosio nel sangue, determinando iperglicemia.
Screening e Diagnosi: Un Percorso Dibattuto e Personalizzato
La decisione di sottoporre tutte le donne in gravidanza a screening per il diabete gestazionale è oggetto di vivaci discussioni e rappresenta un argomento storicamente dibattuto. Come riportato dagli Standard italiani di cura del diabete mellito, SID-AMD 2014, la valutazione iniziale di una donna in gravidanza deve prevedere lo screening per due possibili aspetti.
Innanzitutto, lo screening per il diabete manifesto (e fino ad allora misconosciuto) e l’eventuale diagnosi devono essere effettuate alla prima visita, con la valutazione della glicemia a digiuno e dell’emoglobina glicata (HbA1c). La diagnosi viene posta in presenza di glicemia a digiuno ≥126 mg/dl, glicemia random** ≥200 mg/dl o HbA1c ≥48 mmol/mol (≥6,5%), riconfermate in un secondo prelievo ematico. È importante sottolineare che il diabete di tipo 2 include la maggior parte delle forme di diabete che derivano dalla combinazione di insulino-resistenza e deficienza insulinica, così come l'alterata tolleranza glucidica.
Per quanto riguarda il diabete gestazionale, il test diagnostico più utilizzato è l’esame del carico orale di glucosio (oral glucose tolerance test - OGTT). Questo esame consiste nell’assunzione controllata di una dose di glucosio a cui segue uno stretto monitoraggio della glicemia attraverso misurazioni seriate nei minuti successivi. Il test di screening (Oral Glucose Challenge Test) viene eseguito al mattino dopo un digiuno di circa 8 ore (in ogni caso non superiore a 12 ore). L'alimentazione, nei giorni che precedono il test, deve essere normale. La paziente beve in 5 minuti 50 g di glucosio anidro disciolto in 200 ml di acqua. Il prelievo viene effettuato dopo 60 minuti dall'ingestione della soluzione; durante il test la paziente deve rimanere seduta o sdraiata senza fumare. Il test è positivo se dopo 60 minuti la glicemia è ≥ 140 ml/dl.

Nei casi sospetti nei quali il test viene eseguito in anticipo, se risultasse negativo, va ripetuto a 28-30 settimane di gestazione. In tutti gli altri casi, se lo screening con 50g risulta positivo, è necessario effettuare la curva classica (OGTT) per la conferma diagnostica: 100 g di glucosio anidro disciolti in 400 ml di acqua da bere in 5 minuti. Si effettuano prelievi a digiuno e ogni 60 minuti per 3 ore. Un comitato internazionale (IADPSGCP) ha proposto di adottare lo screening universale e definito nuove soglie diagnostiche per GDM, basate su un OGTT con 75g di glucosio somministrato a 24-32 settimane di gravidanza, con misurazioni a digiuno, dopo 1 ora e dopo 2 ore.
Il dibattito sullo screening ha riguardato principalmente due aspetti: se sottoporre a screening tutte le gravide o solo quelle considerate a rischio, e quali criteri diagnostici utilizzare. Uno studio osservazionale, l'Hyperglicemia and Adverse Pregnancy Outcome (HAPO), ha arruolato un campione di ampie dimensioni (n =23.316) per valutare gli effetti di uno screening universale. Sulla base delle informazioni di questo studio, le soglie diagnostiche sono state poste per consenso ai valori di glucosio ai quali la probabilità di partorire un figlio con uno degli esiti avversi considerati nello studio HAPO è uguale a 1,75 volte la probabilità stimata che questi esiti si manifestino con valori medi di glucosio. È stato stimato che, applicando i criteri IADPSGCP, circa il 18% delle donne in gravidanza riceverebbero diagnosi di GDM. Diventa quindi necessario considerare gli effetti negativi, in termini di ansia materna, conseguenze sul futuro e follow-up medico, del classificare quasi una donna su cinque come una malata che necessita di un intervento, dietetico o farmacologico.
Una posizione diversa è scaturita dal panel che ha elaborato la linea guida Gravidanza fisiologica nell'ambito delle attività dell'Istituto Superiore di Sanità (ISS). Questo gruppo di esperti ha attribuito un diverso valore alla relazione lineare osservata nello studio HAPO fra aumento della glicemia materna e aumento della frequenza degli esiti primari considerati. Ha valutato gli esiti surrogati considerati nello studio di ridotta rilevanza clinica e osservato come questa strategia influenzi solo marginalmente gli esiti della gravidanza, dal momento che la maggior parte degli eventi avversi registrati nello studio si verifica nelle categorie a basso rischio. Ad esempio, il 78% delle donne con nati large for gestational age avrà un livello glicemico inferiore a quello scelto come cut-off da IADPSGCP per porre diagnosi di GDM. Questo studio, inoltre, mostra che l'indice di massa corporea pregravidico è un fattore di rischio più consistente della glicemia materna non solo per macrosomia e iperinsulinismo fetale, ma anche per pre-eclampsia. Le linee guida italiane (ISS) per lo screening del diabete gestazionale limitano la procedura diagnostica ad alcune categorie a rischio elevato.
Le condizioni di rischio per GDM, che richiedono uno screening precoce con OGTT alla 16-18 settimana (e, nel caso in cui il risultato sia negativo, l’esame va ripetuto tra la 24esima e la 28esima settimana di gestazione), sono:
- Diabete gestazionale in una gravidanza precedente.
- Indice di massa corporea (IMC) pregravidico ≥ 30.
- Riscontro, precedentemente o all'inizio della gravidanza, di valori di glicemia plasmatica compresi fra 100 e 125 mg/dl.
Qualora non sia già presente il diabete manifesto, per tutte le altre donne, deve essere eseguito un test di tolleranza al glucosio orale OGTT tra la 24esima e la 28esima settimana di gestazione. Dopo un impegnato confronto, il panel ISS, AMD e SID raccomandano ora congiuntamente uno screening universale di T2D preesistente alla gravidanza e uno screening selettivo di GDM in definiti gruppi di rischio. Queste raccomandazioni si fondano su una condivisione del razionale e del valore dell'assistenza alla gravidanza fisiologica. Screening e diagnosi di GDM costituiscono interventi di medicina preventiva, coinvolgono tutte le donne e, di conseguenza, devono dimostrare - come ogni altro intervento - di essere sicuri ed efficaci.
Gestione Terapeutica: Dieta, Attività Fisica e Farmaci
La gestione del diabete gestazionale mira a normalizzare i livelli di glucosio nel sangue per prevenire complicanze per la madre e il feto. Il primo approccio, e spesso il più efficace, è non farmacologico, basato su modifiche dello stile di vita.
La Dieta Terapeutica
L'alimentazione gioca un ruolo cruciale. La dieta deve essere personalizzata in relazione alle abitudini alimentari, culturali, etniche, allo stato economico e al BMI pregravidico. Si suggerisce pertanto di prediligere cibi a basso indice glicemico e di mantenere uno stile di vita attivo. Si dovrà raccomandare di evitare gli zuccheri semplici e di suddividere l'assunzione delle calorie calcolate in 6 pasti (3 principali e 3 spuntini). È consigliabile preferire cibi ricchi di fibre e fare largo uso di verdure, a cui va aggiunta una porzione di frutta. È importante essere consapevoli che i succhi di frutta e i frullati contengono zucchero, così come altre bevande che riportano l'indicazione "senza aggiunta di zucchero".
Inoltre, si raccomanda di prestare grande attenzione agli zuccheri nascosti, industrialmente aggiunti ad alimenti come lo yogurt o talora insospettabili come salse e anche verdure/legumi in scatola/barattolo. Fare scelte culinarie adeguate include preferire metodi di cottura salutari (come la griglia, il forno o il vapore), alimenti a basso indice glicemico (come cereali, pasta e pane integrali), carni bianche, pesce, legumi e verdure. Questi alimenti contribuiscono a controllare la glicemia. Si noti che i vegetali amidacei come le patate contano come carboidrati, ma le patate gialle tradizionali possono avere un forte impatto sulla glicemia, quindi sarebbe opportuno consumarle con la buccia e/o preferire alternative come le patate dolci americane. Ridurre il consumo di grassi, privilegiando quelli di origine vegetale (ad esclusione del pesce, che deve entrare a far parte della dieta settimanale), è un'altra raccomandazione. La scelta ideale per il condimento è rappresentata dall’olio di oliva extravergine. Nella dieta di una gestante non devono poi mancare latte e latticini, preziosa fonte di calcio, ma vengono in genere preferite le varietà magre. La riduzione dell'apporto calorico (riduzione del 30-33%) nelle pazienti con GDM obese (BMI > 30) consente di ridurre l'iperglicemia senza indurre chetosi, ed è in grado di ridurre il peso del bambino alla nascita senza aumentare la morbilità perinatale.
Attività Fisica
La pratica regolare di attività fisica moderatamente intensa, come la camminata veloce, è in grado di garantire una riduzione della quantità di zucchero nel sangue e un aumento della sensibilità all’insulina. Il medico fornirà una informazione adeguata riguardo gli esercizi che si possono praticare durante la gravidanza, ma è importante che la scelta sia condotta in accordo con il proprio ginecologo. Camminare per 30 minuti dopo il pasto può migliorare il controllo del glucosio nel sangue.
Monitoraggio Domiciliare della Glicemia
Dopo la diagnosi di diabete gestazionale, è fondamentale monitorare regolarmente i livelli di glicemia, sia a digiuno sia post-prandiali. Il diabetologo può stabilire la frequenza delle misurazioni in base alle esigenze individuali della donna. Se si ha il diabete gestazionale è possibile ricevere l'indicazione di controllare i propri livelli di glucosio nel sangue a casa, utilizzando un misuratore di glicemia detto glucometro. Il glucometro è un piccolo dispositivo che misura la concentrazione di glucosio nel sangue mediante l'uso di strisce reattive che vengono messe a contatto con una goccia di sangue ottenuta, in genere, dalla puntura del polpastrello di un dito. L'autocontrollo domiciliare della glicemia va intensificato. Ogni mattina, inoltre, va controllata la chetonuria a digiuno. Il monitoraggio continuo è necessario per valutare i livelli di glucosio nel sangue e per determinare se si raggiungono i target glicemici raccomandati dalle linee guida. Gli obiettivi del controllo glicemico sono: glicemia a digiuno fra 70 e 100 mg/dl; glicemia 2 ore dopo il pasto < 120 mg/dl.
DIABETE GESTAZIONALE: Cos'è, Cause e Cure
Terapia Farmacologica: Insulina
Quando l'approccio non farmacologico non è sufficiente, si valuta l’abbinamento di una terapia farmacologica, che comunque si rende necessaria solamente in una piccola percentuale dei casi se la dieta viene seguita con attenzione. L’utilizzo dell’insulina comporta infatti una serie di attenzioni ed una certa educazione alla paziente che rendono preferibile un primo approccio di natura non farmacologica. L'insulina è somministrata per via intradermica (gli aghi da insulina sono più corti degli aghi per le iniezioni intramuscolari) e il paziente riceverà indicazioni dal team di specialisti per fare l'iniezione correttamente. In base al tipo di insulina potrebbe essere necessario fare l'iniezione prima dei pasti o prima di andare a dormire oppure al risveglio. Recenti lavori dimostrano che l'utilizzo degli analoghi dell'insulina a rapido inizio d'azione è particolarmente efficace nel GDM per la riduzione dei picchi glicemici postprandiali. Verso la fine del primo trimestre, la richiesta di insulina può diminuire, con un rischio di ipoglicemia severa. Il trattamento insulinico potrà prevedere anche schemi atipici, personalizzati in base ai valori glicemici: solo insulina regolare ai pasti, ad esempio; l'aggiunta eventuale di insulina intermedia bed time sarà presa in considerazione in presenza di valori glicemici a digiuno non ottimali.
Il Team Multidisciplinare
La gestione e il trattamento del diabete in gravidanza rappresenta un modello di assistenza integrata in cui diverse figure professionali concorrono alla formazione del team che si prende cura della donna diabetica ambulatorialmente, già prima del concepimento e per tutta la gravidanza e il puerperio. Per raggiungere gli obiettivi prefissati è importante un'integrazione tra le varie figure e l'uniformità del linguaggio usato. I risultati migliori si ottengono quando esiste una stretta collaborazione tra diabetologo, ostetrico e neonatologo; sono altresì importanti le funzioni dell'infermiere professionale di diabetologia, dell'ostetrica e della dietista. Si raccomanda in ogni caso di fare riferimento al proprio ginecologo/endocrinologo per valutare come affrontare il proprio specifico caso. Dopo la visita iniziale, le pazienti dovrebbero essere viste ad intervalli di 1-2 mesi in base alle capacità di gestione del programma e alla presenza o assenza di condizioni patologiche preesistenti. Una volta raggiunto il controllo glicemico stabile (valutato anche mediante il test HBAc1) migliore possibile, allora possono ricevere la consulenza sul rischio di malformazioni e di aborti spontanei. L'obiettivo generale della gestione della glicemia nel periodo preconcepimento e durante il primo trimestre di gravidanza dovrebbe essere quello di ottenere il valore più basso possibile di HBA1c senza rischio di ipoglicemia per la madre. In particolare, sono auspicabili valori < 1% al di sopra del range normale.
Impatto sul Feto e Complicanze della Gravidanza
L'esposizione del feto a livelli di glucosio elevati, non adeguatamente controllati terapeuticamente da parte della madre, può determinare una serie di conseguenze cliniche rilevanti. Il feto è totalmente dipendente dalla madre nel corso della sua vita uterina; ciò significa che con essa condivide il contenuto del sangue e quindi tutte le sostanze disciolte, glucosio compreso.
Tra le principali complicanze fetali si annoverano:
- Insulino-resistenza precoce: Causata dalla prematura esposizione ad elevati livelli dell’ormone prima ancora che il nascituro inizi ad alimentarsi autonomamente.
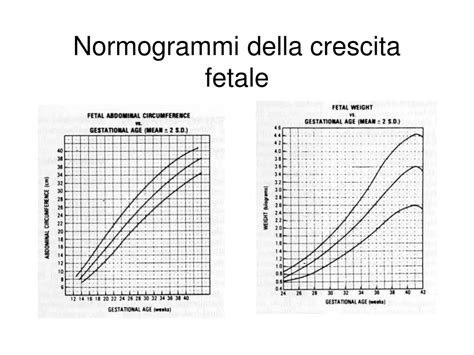
- Elevato peso alla nascita (macrosomia): Causato dall’effetto dell’insulina sul metabolismo che determina una forte deposizione di adipe nell’addome del nascituro. È per questo motivo che nel corso dei controlli ecografici viene misurata la circonferenza addominale: la crescita eccessivamente veloce può richiedere l’induzione del parto o il cesareo prima del termine previsto della gravidanza. L'errore diagnostico nei confronti della macrosomia è di circa il 10-15%. La circonferenza addominale consente di predire il peso fetale e, la crescita di questa > 1,2 cm/settimana, la differenza fra diametro traverso addominale e diametro biparietale > 2,6 cm, o la differenza fra diametro toracico e diametro biparietale > 1,4 cm, sono tutti indici di macrosomia.
- Aumento del rischio di sviluppare crisi ipoglicemiche nel primissimo periodo di vita: Ciò è spiegato dal fatto che l’elevato livello di insulina presente nel neonato in assenza di un’adeguata alimentazione abbassa eccessivamente i livelli della glicemia rendendo necessaria la somministrazione di soluzione glucosata endovena come misura correttiva.
- Rischi a lungo termine: In letteratura sono presenti una serie di studi che ipotizzano un’aumentata incidenza di obesità nel periodo che va dalla prima infanzia all’adolescenza, oltre che un rischio di sviluppare diabete mellito di tipo II superiore rispetto alla popolazione pediatrica che non ha avuto madri affette da diabete gestazionale (o madri affette, ma in buon compenso glicemico).
Il diabete gestazionale non controllato aumenta il rischio di complicanze durante la gravidanza e al momento del parto, oltre che di malformazioni fetali e/o morte intrauterina. La mortalità perinatale, intra o extra uterina aumenta progressivamente dopo la 36° settimana di gestazione specialmente in diabetiche in cattivo controllo metabolico, con macrosomia fetale, con complicanze vascolari, chetoacidosi e preeclampsia, tutte condizioni che comportano una riduzione del flusso placentare. Il rischio di sviluppare malformazioni fetali ed aborti spontanei è correlato ai livelli di HBA1c al momento del concepimento. La glicemia post prandiale sembra essere il dato più importante ai fini della comparsa del ritardo di crescita (della microsomia).
Per quanto riguarda le complicanze materne, una revisione sistematica di studi clinici controllati randomizzati non ha rilevato differenze in esiti materni rilevanti fra screening selettivo, trattamento di GDM e assistenza usuale, con la sola eccezione di una minore frequenza di pre-eclampsia nelle donne trattate.
È cruciale considerare anche il counseling pregravidanza, specialmente per donne con diabete preesistente. Andrebbe iniziato alla pubertà per le donne con diabete tipo 1 ed al primo riscontro della malattia per quelle con diabete tipo 2. La gravidanza ed il diabete si influenzano reciprocamente, determinando ciascuno effetti importanti sull'altro. La retinopatia diabetica di per sé non induce la retinopatia diabetica quando questa non è presente prima del concepimento. Tuttavia, la nefropatia diabetica conclamata, specie se associata ad ipertensione arteriosa, influenza negativamente l'evoluzione della gravidanza, aumentando ulteriormente il rischio di malformazioni congenite, ritardi di crescita intrauterina, morti perinatali e parti pretermine. Le pazienti con escrezione urinaria di proteine ≥190 mg/24h sono a rischio per disordini ipertensivi in gravidanza, e quelle con escrezione di proteine ≥400 mg/24 h corrono rischi ancora maggiori. È necessario monitorare creatinina serica ed escrezione urinaria di proteine totali e/o albumina.
Monitoraggio e Parto: Aspetti Cruciali della Gestione
La stretta sorveglianza durante la gravidanza e la gestione attenta del momento del parto sono elementi fondamentali nel percorso delle donne con diabete gestazionale. L'associazione fra iperglicemia materna, iperinsulinismo fetale e ipossia fetale giustifica il ricorso nel 3° trimestre a metodiche strumentali di stretta sorveglianza fetale.
Monitoraggio Fetale
Sono raccomandate ecografie a 28, 32 e 36 settimane di gravidanza, per monitorare la crescita del feto e la quantità di liquido amniotico presente nell'utero. Poiché nel diabete gestazionale la macrosomia fetale è frequente (20%), è importante una previsione ecografica del peso quanto più adeguata possibile. Alla gestante si insegna anche la conta materna dei movimenti fetali (che dovrebbe essere considerata a partire da 30-32 settimane) spiegando anche i cicli comportamentali del feto.
Gestione del Parto
Se si ha il diabete gestazionale, il tempo ideale per il parto è di solito tra le 38-40 settimane di gravidanza. Se i livelli di glucosio nel sangue sono normali e la salute del feto non è a rischio, è possibile aspettare che il parto avvenga naturalmente. In genere, se il parto naturale non avviene dopo 40 settimane e 6 giorni, viene consigliata l'induzione del parto o il parto cesareo.Quando ci si reca in ospedale per il parto, è opportuno portare con sé il glucometro e tutti i farmaci che si stanno assumendo. Di solito, si deve continuare a monitorare la glicemia e a prendere i farmaci fino al parto o, nel caso del parto cesareo, prima del digiuno pre-operatorio. Durante il travaglio e il parto, la glicemia sarà misurata e mantenuta sotto controllo.
Cura del Neonato Post-Parto
Dopo la nascita (entro 30 minuti) è importante alimentare il neonato il più presto possibile e poi a intervalli frequenti (ogni 2-3 ore) fino a che la glicemia del neonato non sia stabile. I livelli del glucosio nel sangue saranno misurati a partire da due o quattro ore dopo la nascita: se sono bassi, il neonato potrebbe essere alimentato mediante sondino o flebo.
Cura della Madre Post-Parto
Dopo il parto, vengono solitamente sospesi i farmaci per controllare la glicemia che la donna ha assunto durante la gravidanza e vengono controllati i livelli di glucosio nel sangue per altri uno o due giorni. È necessario che la donna continui a monitorare la glicemia fino a 6-13 settimane dopo il parto per verificare che i livelli di glicemia non si mantengano alti.
Il Diabete Gestazionale e il Rischio a Lungo Termine
Il pregresso diabete gestazionale (GDM) non è una condizione che si esaurisce con la fine della gravidanza. Sebbene si tratti fortunatamente di una patologia spesso autolimitante, che si risolve spontaneamente dopo il parto con una normalizzazione del profilo glicemico nella maggior parte delle pazienti, in una percentuale dei casi, può progredire verso una forma di diabete mellito di tipo 2. Questo rende il GDM un fattore di rischio significativo per lo sviluppo di un diabete tipo 2 negli anni successivi, motivo per cui è raccomandato un follow-up a partire da 6-12 settimane dopo il parto. L'identificazione di donne con GDM consente inoltre di individuare una popolazione ad elevato rischio per lo sviluppo di un diabete tipo 2 negli anni successivi.
Fattori Associati alla Persistenza di Alterazioni Glucidiche Post-Parto
Uno studio ha valutato i principali fattori associati alla persistenza di alterazioni della regolazione glucidica (IGR) al primo follow-up dopo il parto in donne con pregresso GDM. Questo studio ha raccolto dati clinici ed antropometrici di 523 donne afferite al Servizio di Diabetologia dell’Ospedale di Pisa da Gennaio 2011 ad Ottobre 2017 per eseguire un OGTT (75g) di screening per DM2, 6-12 settimane dopo il parto. La prevalenza di IGR era pari al 10.5% (5.5% IFG, 2% IGT, 1.5% IFG+IGT e 1.5% DM) e risultava più bassa nelle donne normopeso prima della gravidanza (IMC 18.5-25: 7.5% vs. IMC<18.5:17.6%, IMC >=25: 11%; IMC >=30: 18.1%; p<0.05). Non si era differenza nella prevalenza di IGR in relazione all’IMC al momento dello screening, all’incremento ponderale in gravidanza, al tipo di allattamento in corso.
IGR risultava più frequente nelle donne con familiarità per DM2 (14.9% vs. 6.2%; p=0.001) e nelle donne trattate con insulina durante la gravidanza rispetto a quelle trattate con dieta e attività fisica (14% vs. 7.7%; p=0.02). Le donne con IGR presentavano circonferenza vita maggiore rispetto alle NGT (99±12 vs. 94.6±12 cm; p<0.05) e livelli di pressione arteriosa sistolica più alti (121±16 vs. 116±13 mmHg; p=0.01); livelli di HbA1c (5.9±0.04 vs. 5.3±0.1%; p<0.005) e trigliceridi (230±75 vs. 163±96; p=0.01) più elevati nel III trimestre di gravidanza. All’analisi logistica rimaneva indipendentemente associata a IGR solo la familiarità (OR 2.67; 95% IC 1.39-5.14). In un sottogruppo di 70 donne con dosaggio di HbA1c nel III trimestre di gravidanza, tale parametro risultava indipendentemente associato a IGR, anche dopo correzione per altri confondenti (OR 7.67; 95% IC 1.01-58.00).
In conclusione, nelle donne con pregresso GDM, la persistenza di IGR è fortemente associata alla familiarità per DM2 e a livelli più elevati di HbA1c al III trimestre di gravidanza. Questo sottolinea l'importanza del monitoraggio post-parto, dove il diabetologo può suggerire un controllo per verificare il ritorno a valori glicemici nella norma.
Rischio di GDM in Gravidanze Successive
Il pregresso diabete gestazionale (GDM) è un fattore di alto rischio per la comparsa di GDM nelle gravidanze successive. Uno studio ha descritto l’incidenza di GDM, misurato l’insulinoresistenza (HOMA-IR) e la funzione β-cellulare (HOMA-β) in donne con pregresso GDM, antiGAD negative. Tutte le pazienti reclutate avevano ricevuto già dall’ultima gravidanza prescrizioni per un appropriato follow-up post partum e raccomandazioni sullo stile di vita per la prevenzione del diabete tipo 2 nonché del GDM nelle gravidanze successive. In accordo con le linee guida Ministeriali, le stesse donne venivano invitate a rivolgersi al diabetologo al momento della diagnosi di nuova gravidanza per valutazione clinico-metabolica precoce ed esecuzione del primo OGTT (75g per os) entro la 14-16 settimana (IADPSG criteria).
Tra il 2011 e il 2017, è stato eseguito un OGTT in 68 donne con pregresso GDM, reclutate consecutivamente, con un’età media di 35.5±4.7 anni e un BMI di 24.7 (17.5-42.2) Kg/m2, dopo 3.3±1.8 anni dalla precedente gravidanza. In gravidanza, tutte le pazienti con pregresso GDM sono state seguite ad intervalli regolari (ogni 2-4 settimane) a prescindere dal risultato dell’OGTT; 58 di 68 (85.29%) sono risultate positive all’OGTT eseguito durante la seconda gravidanza. Di queste, il 45,6% ha ricevuto diagnosi di GDM sulla base dell’OGTT precoce (16-18 settimane), mentre il 39,7% all’OGTT tardivo (24-28 settimane). Solo il 14,7% è risultato negativo ad entrambi gli OGTT. Le pazienti che risultavano positive all’OGTT precoce presentavano un HOMA-IR non significativamente più alto rispetto a quelle con OGTT negativo (OGTT+: 2.1±1.7 vs OGTT-: 1.8±0.7, ns), mentre l’HOMA-β risultava significativamente ridotto (OGTT+: 110.7±71.8 vs OGTT-: 179.6±66.7, p=0.026).
Il diabete è una malattia cronica, in parte evitabile, maggiormente frequente nelle classi socialmente svantaggiate, a larghissima diffusione in tutto il mondo e destinata ad aumentare nel prossimo futuro con il progressivo invecchiamento della popolazione e la sempre maggiore occorrenza delle condizioni di rischio che ne precedono l’insorgenza. Una corretta educazione sulla prevenzione delle patologie metaboliche è indispensabile. Una piccola parte delle pazienti con GDM (appena il 10% del totale) presenta caratteristiche cliniche, immunologiche e genetiche tipiche del diabete autoimmune, sia di tipo 1 sia del cosiddetto LADA (Latent autoimmune diabetes of the adult).
tags: #pregresso #diabete #gestazionale