La ricerca di una gravidanza è un percorso che per molte coppie può presentare sfide significative. Nell'ambito della Procreazione Medicalmente Assistita (PMA), l'avanzamento delle tecniche ha aperto nuove frontiere per aumentare le possibilità di successo e garantire la nascita di bambini sani. Tra queste, la Diagnosi Genetica Preimpianto (PGT) rappresenta una delle metodologie più sofisticate e promettenti. Questa tecnica, precedentemente nota come PGD (Diagnosi Genetica Preimpianto) o PGS (Screening Genetico Preimpianto), consente un'analisi approfondita degli embrioni prima del loro trasferimento in utero, con l'obiettivo di identificare eventuali anomalie genetiche o cromosomiche.
Negli ultimi anni, gli esperti in medicina della riproduzione ricevono sempre più spesso dai pazienti domande sulla diagnosi genetica preimpianto (PGT-DGP) o vere e proprie richieste di effettuarla a prescindere da qualsiasi indicazione. Ciò con la speranza di aumentare le percentuali di successo nei programmi di Procreazione Medicalmente Assistita (PMA). La PGT, attraverso le sue diverse declinazioni, mira a migliorare l'efficienza di ogni singolo trattamento minimizzando i rischi associati a problemi genetici. Questo approccio è particolarmente valorizzato quando l'analisi viene effettuata su embrioni allo stadio di blastocisti, un momento cruciale dello sviluppo embrionale che offre vantaggi distinti in termini di accuratezza e sicurezza.
PGT: Definizione e Distinzione tra le Sue Tipologie
Il Test Genetico Preimpianto (PGT - Preimplantation Genetic Testing) è una tecnica avanzata che permette di analizzare geneticamente gli embrioni sviluppati in laboratorio mediante un trattamento di fecondazione assistita omologa o eterologa di II livello (FIVET; ICSI; IMSI; PICSI), prima di trasferirli in utero. Questo termine ombrello racchiude diverse sotto-categorie, ciascuna con un obiettivo diagnostico specifico:
PGT-A (Preimplantation Genetic Testing for Aneuploidies): Questa è la tecnica in sostanza la ricerca di qualsiasi mutazione nell’assetto genetico di un embrione. Precedentemente nota come PGS (Preimplantation Genetic Screening), la PGT-A consente l'esame degli embrioni prima del trasferimento in termini di aneuploidie cromosomiche. Le aneuploidie sono alterazioni del numero o della struttura dei cromosomi, tenendo conto che la normale dotazione di cromosomi umani è di 46 cromosomi. Pertanto, il guadagno o la perdita di un cromosoma, così come i cambiamenti nella sua struttura, sono anomalie che possono portare a embrioni non vitali o neonati con malattie cromosomiche. Un esempio è la Sindrome di Down, definita anche Trisomia 21, caratterizzata da un cromosoma in più della coppia 21. Un altro esempio è la Sindrome di Turner, che si manifesta con un cromosoma sessuale in meno. La PGT-A permette di analizzare il corredo cromosomico dell’embrione per individuare anomalie numeriche o strutturali che pregiudicano l’impianto o il corretto sviluppo della gravidanza. Con i metodi PGT-A si controlla tutto il DNA in grandi segmenti a livello dei cromosomi o delle loro parti. Anomalie numeriche di questi cromosomi portano ad aborti oppure a difetti del nascituro.
PGT-M (Preimplantation Genetic Testing for Monogenic/Single Gene Defects): Precedentemente nota come PGD (Preimplantation Genetic Diagnosis), questa tecnica è utilizzata per analizzare i geni ed i cromosomi degli embrioni per una specifica malattia genetica. Quindi, essa è opportuna per una condizione a rischio già conosciuta dalla coppia e/o dal medico curante. Le malattie monogeniche sono quelle causate da mutazioni di un singolo gene, come la fibrosi cistica, l'emofilia, la sindrome X fragile o la distrofia miotonica (Steinert). L'obiettivo è prevenire la trasmissione di patologie ereditarie ai figli.
PGT-SR (Preimplantation Genetic Testing for Structural Rearrangements): Questa tipologia è indicata per i genitori che sono portatori di forme bilanciate di una traslocazione, ossia di un riarrangiamento cromosomico. Anche se il portatore è sano, esiste il rischio di trasmettere un riarrangiamento sbilanciato all'embrione, che può portare a gravi problemi di sviluppo o aborti. La PGT-SR permette di escludere gli embrioni portatori di mutazioni del DNA non bilanciate.
Le tecniche PGT-M/PGT-A (prima PGD/PGS) permettono di escludere gli embrioni portatori di malattie gravi (nel caso delle malattie monogene) oppure escludere gli embrioni portatori di mutazioni del DNA non bilanciate (nel caso delle traslocazioni). Poiché gli embrioni devono essere analizzati in laboratorio, sarà necessario sottoporre la coppia ad un programma di fecondazione in vitro (FIV) anche se non ci sono problemi di fertilità.
Il Ruolo Cruciale della Blastocisti nello Screening Genetico Preimpianto
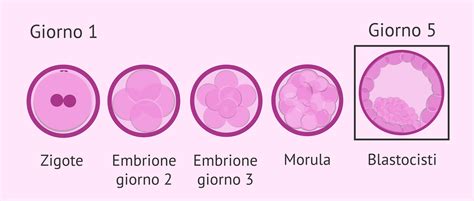
Nel nostro Centro, la PGS (o screening genetico preimpianto o stato di salute degli embrioni) viene effettuata su embrioni allo stadio di blastocisti. Le blastocisti si formano in quinta giornata dalla fecondazione e sono composte da 150-200 cellule. Questo stadio di sviluppo embrionale, che si verifica circa 120 ore dopo la fecondazione degli ovociti, è considerato il più idoneo per la biopsia genetica per diverse ragioni fondamentali.
La blastocisti è una struttura embrionale complessa e differenziata, che presenta tre parti distinte:
- Massa Cellulare Interna (Inner Cell Mass, ICM): Questa è la porzione da cui origina il futuro feto. La sua integrità è di vitale importanza per il corretto sviluppo embrionale.
- Trofoectoderma (Trophoectoderm, TE): Questo è lo strato esterno di cellule che darà origine unicamente agli annessi embrionali, come la placenta e il sacco amniotico.
- Blastocele: Una cavità interna riempita di fluido.
Il fatto che la biopsia venga fatta asportando la parte più esterna, quella destinata a formare la placenta (il trofoectoderma), è un vantaggio significativo. Poiché il trofoectoderma presenta lo stesso cariotipo della massa cellulare interna, questa analisi è sufficiente ad identificare eventuali anomalie genetiche senza prelevare cellule direttamente dal nucleo embrionale da cui si formerà il feto. È bene sottolineare che non sussistono rischi per gli embrioni quando la biopsia viene effettuata allo stadio di blastocisti, da mani esperte, e non ne vengono compromesse le possibilità di impianto nell’utero materno.
La coltivazione prolungata fino al 5° o al 6° giorno permette inoltre una selezione naturale degli embrioni. In questa fase, sopravvivono solo gli embrioni della qualità più alta, e vengono minimalizzati gli embrioni con aberrazioni cromosomiche collegate con aborti spontanei. Questo significa che, al momento della biopsia, si lavora già con embrioni che hanno dimostrato una maggiore capacità di sviluppo, potenzialmente aumentando la robustezza del campione e le probabilità di successo finale.
Il Processo di Biopsia Embrionale: Dettagli e Tecnica di Precisione
La biopsia embrionale è il processo di estrazione di una o più cellule, chiamate blastomeri, per analizzare il DNA degli embrioni alla ricerca di eventuali alterazioni genetiche. Nel contesto della PGT, la biopsia viene eseguita con estrema cura e precisione per garantire la vitalità dell'embrione e l'accuratezza diagnostica.
Esecuzione della Biopsia sul Trofoectoderma:Quando si esegue la biopsia con una blastocisti, occorre fare attenzione a fare il foro in un luogo lontano dall'ICM per evitare possibili danni. La biopsia viene fatta al microscopio con pipette speciali ed embriologi che hanno formazione ed esperienza in questo campo. La procedura richiede poco tempo e non danneggia l'embrione. Vengono prelevate poche cellule del trofoblasto (<5% della sua biomassa). Il fatto che dall'embrione si possano estrarre più cellule rispetto alla biopsia al terzo giorno è un vantaggio, poiché si otterrà un risultato più affidabile, sarà possibile individuare casi di mosaicismo e, inoltre, la vitalità dell'embrione non sarà così compromessa. È importante sottolineare che per poter eseguire la biopsia è necessario che gli embrioni abbiano un livello minimo di qualità per garantire la loro sopravvivenza.
Strumenti e Metodologia:La rimozione della cellula per l'analisi in una diagnosi preimpianto è fatta facendo una biopsia. Si deve praticare un piccolo foro nello strato più esterno dell'embrione e si deve rimuovere una delle cellule e poi si deve analizzare il DNA nel nucleo di quella cellula. In questo contesto, è più conveniente utilizzare i brevi impulsi del laser per perforare la zona pellucida rispetto all'acido Tyrodes, poiché ha notevolmente ridotto il suo spessore man mano che la blastocisti si espande e l'uso di un agente chimico potrebbe danneggiarla. Poi, una volta che è stato fatto un foro sufficiente per inserire la pipetta per biopsia, le cellule vengono rimosse per aspirazione. Per separare le cellule da rimuovere da quelle che rimangono all'interno dell'embrione, gli impulsi laser possono aiutare.
Gestione Post-Biopsia:Gli embrioni sottoposti a biopsia vengono quindi congelati individualmente utilizzando il metodo di congelamento ultra rapido, la vetrificazione. Questo è necessario perché i risultati dell'analisi genetica richiedono diversi giorni e non sarebbe possibile lasciare gli embrioni in coltura per tutto questo tempo. La vetrificazione consente di conservare gli embrioni in uno stato di sospensione vitale fino a quando non saranno disponibili i risultati delle analisi genetiche.
Contaminazione e Tecnica di Fecondazione:La biopsia embrionale può essere fatta il giorno 3 o il giorno 5. In entrambi i casi, è essenziale che la fecondazione avvenga attraverso un ICSI (Iniezione Intracitoplasmatica dello Spermatozoo). Nella FIV convenzionale (fecondazione in vitro classica), ci sono spermatozoi e cellule di granulosa attaccati alla zona pellucida dell'embrione. Ciò comporta un rischio di contaminazione dei blastomeri estratti e quindi la DGP potrebbe dare un risultato alterato. L'ICSI, iniettando un singolo spermatozoo direttamente nell'ovocita, riduce drasticamente questo rischio di contaminazione.
Embrione blastocisti: Cos’è, vantaggi, tipi e classificazione in base alla sua qualità
Metodologie di Analisi Genetica: Dalla FISH all'NGS
Una volta prelevate le cellule dal trofoectoderma, il materiale viene inviato al laboratorio di genetica che effettuerà l’analisi. Nel corso degli anni, le tecniche per l'analisi genetica preimpianto si sono evolute, diventando sempre più precise e complete.
L'Approccio Iniziale: FISH (Ibridazione Fluorescente in Situ):L'ibridazione fluorescente in situ (FISH) è stata la tecnica tradizionalmente utilizzata nello studio delle anomalie cromosomiche. Permetteva l'analisi solo di alcune regioni di 9 cromosomi (13, 15, 16, 17, 18, 21, 22, X e Y). Questi cromosomi sono spesso coinvolti in aneuploidie che possono portare a ripetuti aborti spontanei o alla nascita di bambini malati. Il processo consisteva nell'aggiunta di sonde fluorescenti per specifiche regioni dei cromosomi da analizzare, permettendo di visualizzare il segnale fluorescente attraverso uno speciale microscopio e rilevare se una delle regioni analizzate era mancante o, al contrario, se c'erano più copie di quante avrebbero dovuto essercene. Tuttavia, poiché l'analisi solo di un certo numero di cromosomi era un limite, la FISH è stata considerata un'analisi incompleta ed è stata progressivamente sostituita da tecniche più avanzate.
L'Evoluzione con Array-CGH (Ibridazione Genomica Comparativa su Array):L'Array of Comparative Genomic Hybridization (A-CGH) è una tecnica che ha segnato un importante passo avanti, permettendo di effettuare uno screening dei cromosomi completo (CCS - Comprehensive Chromosome Screening), cioè tutte le 23 coppie di cromosomi vengono analizzate contemporaneamente alla ricerca di regioni con qualche alterazione cromosomica. Per effettuare questa analisi genetica, si utilizza un DNA di controllo e il campione di DNA da studiare dalla cellula embrionale estratta. Entrambi i filamenti di DNA sono marcati con diverse sonde fluorescenti e poi ibridati nel microarray. Con questa metodologia è possibile confrontare il DNA dell'embrione con quello del campione di riferimento e identificare perdite (delezioni) o guadagni (duplicazioni) di materiale genetico, che potrebbero portare a difetti embrionali. Anche se questa tecnica è molto più determinante della FISH, fa solo confronti quantitativi, cioè rileva se c'è materiale genetico mancante o in eccesso. Pertanto, non rileva se ci sono frammenti cromosomici che non sono al posto giusto, come le inversioni o le traslocazioni. La Sindrome di Down, ad esempio, può essere rilevata con l'Array-CGH, essendo caratterizzata da un cromosoma in più della coppia 21.
La Tecnologia All'Avanguardia: NGS (Next Generation Sequencing):Nel nostro centro viene utilizzato il metodo New Generation Sequencing (NGS), che è il più avanzato tra i test di screening genetici efficaci per PGS. Attualmente si effettuano gli esami di PGT-M/PGT-A (prima PGD/PGS) con i metodi all’avanguardia NGS e PCR. Il sequenziamento di prossima generazione o NGS è la tecnica più avanzata per gli studi genetici oggi.I vantaggi che offre rispetto ad altre tecniche sono molteplici:
- Precisione Elevata: Con il metodo NGS, lo screening aneuploide dell'embrione può essere eseguito con almeno il 1% di precisione in una piccola quantità (5-95) cellule prelevate dagli embrioni mediante il metodo della biopsia dell'embrione.
- Analisi Completa: Permette lo studio di tutte le 23 coppie di cromosomi nella stessa analisi e con una risoluzione più alta, rendendo possibile fare l’analisi di tutti i cromosomi.
- Rilevazione Multipla: Permette l'analisi simultanea di oltre 500 geni associati a malattie ereditarie. È possibile studiare le aneuploidie e le malattie monogeniche separatamente o contemporaneamente in un'unica analisi, offrendo un quadro genetico estremamente dettagliato.
- Efficienza Temporale: Riduzione dei tempi di analisi, evitando di congelare gli embrioni in attesa dei risultati in alcuni scenari (anche se la vitrificazione rimane una pratica comune).
- Accessibilità Economica: Consente di analizzare un numero elevato di campioni contemporaneamente, rendendo il costo dell'analisi più accessibile nel tempo.Al giorno d'oggi, sempre più cliniche stanno optando per questa tecnologia di ultima generazione sia per lo screening dell'aneuploidia che per l'individuazione di malattie monogeniche.
PCR (Reazione a Catena della Polimerasi):La reazione a catena della polimerasi (PCR) comporta l'amplificazione di specifiche sequenze di DNA per ulteriori analisi. In questo modo, è possibile ottenere milioni di copie del gene di interesse da una singola copia presente nella cellula estratta. Una volta amplificata la sequenza desiderata, vengono utilizzate diverse tecniche di biologia molecolare per analizzarla e individuare le possibili mutazioni che danno origine a malattie monogeniche, rendendola uno strumento fondamentale per la PGT-M.
Indicazioni per la PGT-A: Quando è Raccomandata la Diagnosi Preimpianto
La decisione di sottoporsi alla PGT-A non è universale, ma è basata su specifiche indicazioni cliniche che mirano a ottimizzare le possibilità di successo della PMA e a ridurre i rischi associati a complicanze genetiche.
Età Materna Avanzata:La probabilità di avere ovociti con un numero anomalo di cromosomi è più alta in donne in età avanzata. Infatti, tradizionalmente, la PGS è proposta a donne al di sopra dei 38 anni. Anomalie cromosomiche avvengono molto frequentemente durante la normale produzione di ovociti, spermatozoi e durante lo sviluppo embrionario. È stato dimostrato che il numero delle aberrazioni cromosomiche aumenta con l’età. Questo screening è indicato per le donne over 35 che intendono sottoporsi a tecniche di fecondazione assistita, fascia d’età nella quale aumenta notevolmente la frequenza di anomalie cromosomiche negli embrioni. L'esame verifica se l'embrione ha qualche patologia cromosomica che si ritiene essere la causa principale dei fallimenti delle tecniche di PMA, consentendo di aumentare l'efficienza della fecondazione in vitro.
Storia di Poliabortività:La maggior parte degli aborti spontanei (circa l‘80%) o il non annidamento dell‘embrione nell’utero possono essere causati dalle aberrazioni cromosomiche, ossia mutazioni patologiche del DNA degli embrioni. PGT-A è inoltre indicata per le coppie con una storia pregressa di abortività. La diagnosi genetica preimpianto può aiutare a identificare embrioni cromosomicamente sani, riducendo significativamente il rischio di aborti ricorrenti. Il rischio di aborto spontaneo in donne con un’età media superiore ai 36 anni, infatti, scende sotto il 10% per concepimento grazie all'applicazione di queste tecniche.
Ripetuti Fallimenti di Impianto in Precedenti Cicli di PMA:Per le coppie che hanno sperimentato ripetuti fallimenti di impianto in precedenti cicli di fecondazione assistita, la PGT-A può essere un'opzione preziosa. Spesso, embrioni morfologicamente di buona qualità non si impiantano a causa di anomalie cromosomiche non visibili al microscopio. L'esame delle caratteristiche dello sviluppo dell'embrione al microscopio non ci fornisce l'informazione che l'embrione sia cromosomicamente normale o anormale. Queste informazioni possono essere ottenute solo mediante screening genetico con PGS. Identificare e trasferire embrioni euploidi (con corredo cromosomico normale) aumenta notevolmente le probabilità di successo.
Fattore Maschile Grave:In passato, alcune cliniche raccomandavano la PGS anche a uomini i cui spermatozoi erano a rischio di avere anomalie cromosomiche. Sebbene l'indicazione primaria per la PGT-A sia spesso legata all'età materna, la qualità dello sperma può anch'essa contribuire a un aumentato rischio di aneuploidie embrionali.
Coppie con Storia Familiare di Problemi Cromosomici o Malattie Monogeniche:Il ginecologo può anche prescrivere la PGS se è presente una storia familiare di problemi cromosomici. Per le coppie che sono portatrici di malattie genetiche specifiche (monogeniche) o riarrangiamenti cromosomici bilanciati, la PGT-M e PGT-SR sono le tecniche indicate per prevenire la trasmissione di queste condizioni alla prole. Sebbene queste siano distinzioni specifiche, rientrano nell'ampio spettro delle indicazioni per la Diagnosi Genetica Preimpianto.
Vantaggi e Benefici della PGT-A: Aumentare le Probabilità di Successo
I metodi della PGT sono di grande aiuto nella selezione dell’embrione senza le aberrazioni cromosomiche, aumentano la probabilità dell‘annidamento e dello sviluppo giusto nell‘utero. L'applicazione della PGT-A su blastocisti apporta numerosi vantaggi concreti per le coppie che si sottopongono a trattamenti di PMA.
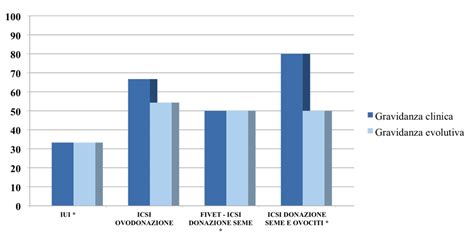
Aumento delle Probabilità di Gravidanza:Trasferire embrioni geneticamente sani, vuol dire anche aumentare in modo eccezionale la possibilità di gravidanza. Il beneficio delle tecniche PGT-M/PGT-A (prima PGD/PGS) consiste nella selezione dell‘embrione e dell’aumento della probabilità di successo. In un ciclo mestruale della donna questa probabilità è intorno al 25 %, a seconda dell’età della donna. Grazie alle tecniche usate in PGT-M/PGT-A (prima PGD/PGS) la probabilità del successo aumenta al quasi 70 % con il transfer di un embrione. I metodi di PGT-M/PGT-A (prima PGD/PGS) nel Sanatorium Helios aumentano la percentuale di successo di più del 20 %.
Riduzione del Rischio di Aborti Spontanei:Le donne sono preservate da transfer inutili e dagli aborti spontanei causati dalla mancanza o esuberanza dei cromosomi. Identificando e trasferendo solo embrioni euploidi, il rischio di aborto spontaneo dovuto ad anomalie cromosomiche viene notevolmente ridotto, offrendo maggiore serenità durante la gravidanza.
Minimizzazione dei Fallimenti di Impianto:La PGT-A permette di rilevare anomalie numeriche o strutturali dei cromosomi che pregiudicano l’impianto o il corretto sviluppo della gravidanza. Questo consente di evitare il trasferimento di embrioni che, seppur di bell'aspetto morfologico, non avrebbero probabilità di impiantarsi, risparmiando tempo, risorse emotive e fisiche. L'analisi permette di aumentare l'efficienza della fecondazione in vitro.
Diminuzione del Numero di Cicli di PMA Necessari:Un altro vantaggio di PGT-M/PGT-A (prima PGD/PGS) è il risparmio economico. Evitando il trasferimento di embrioni con scarse probabilità di successo, le coppie possono ridurre il numero totale di cicli di PMA necessari per ottenere una gravidanza, con conseguente riduzione dei costi e dello stress.
Prevenzione di Malattie Genetiche e Cromosomiche:Nel caso della PGT-A viene selezionato l’embrione senza grandi mutazioni nel corredo genetico, soprattutto senza anomalie numeriche dei cromosomi. Questo permette di rilevare, tra le altre, sindromi come quella di Down o di Turner. Nel caso della PGT-M, esiste la probabilità del 95 % che l’embrione non porta la malattia esaminata oppure non porta la traslocazione non bilanciata. Questo beneficio è di fondamentale importanza per le coppie a rischio di trasmettere gravi patologie ereditarie.
Maggiore Sicurezza e Scelte Informate:La DGP facilita il processo decisionale informato e viene sempre più inclusa come opzione nell'ambito di una corretta consulenza genetica. L'obiettivo attuale è che può raggiungere qualsiasi coppia, se liberamente scelta, e qualsiasi patologia ereditaria, a condizione che vi sia un'indicazione clinica e che sia possibile affrontare tecnicamente la sua diagnosi.
Limiti e Rischi della Diagnosi Genetica Preimpianto
Sebbene l'accuratezza del metodo PGS basato su NGS, in cui viene eseguita l'anilisi cromosomica numerica e strutturale, sia molto elevata, il test ha comunque la possibilità di non rilevare alcuni problemi e falsi positivi. È fondamentale che le coppie siano pienamente informate sui limiti e i potenziali rischi associati alla PGT.
Rischio di Mosaicismo Embrionale e Diagnosi Errata:Un altro aspetto fondamentale è che la ricerca ha dimostrato che spesso le cellule di un embrione non sono cromosomicamente identiche (mosaicismo). La PGS è una diagnosi fatta su una o poche cellule in rappresentanza dell’intero embrione. In sostanza vi è quindi il rischio di porre una diagnosi errata su un embrione sano. Ciò implica quindi che un embrione normale sia erroneamente identificato come anomalo e che non sia trasferito (falso positivo), oppure che un embrione anomalo sia identificato come normale (falso negativo). Il mosaicismo rappresenta una delle sfide più complesse nella diagnosi preimpianto, poiché la biopsia di un numero limitato di cellule potrebbe non riflettere l'intero assetto cromosomico dell'embrione.
Limiti Intrínseci della Metodica e Possibili Errori:A causa dei limiti della metodica e del rischio di errore esistente (~5%), non può essere escluso che gli embrioni ottenuti siano portatori di malattie cromosomiche o genetiche. È importante capire che la PGT non è una garanzia assoluta e non elimina completamente il rischio di avere un bambino con difetti genetici.
Impatto sulla Disponibilità di Embrioni:
- Bassa Risposta Ovarica: Una bassa risposta alla stimolazione ovarica incide sul numero di ovociti recuperati e quindi sul numero di embrioni disponibili per l’analisi genetica. Un maggior numero di embrioni da bioptizzare aumenta le percentuali di successo della procedura. Sfortunatamente non è possibile fornire una precisa percentuale di successo per i programmi con PGS. Oltre alla diagnosi errata c’è la concreta possibilità nelle donne in età avanzata di avere tutti gli embrioni anomali.
- Embrioni senza Diagnosi Conclusiva: Una piccola percentuale di embrioni potrebbe rimanere senza una diagnosi conclusiva pure essendo andata la biopsia a buon fine. Questo può essere dovuto a campioni cellulari insufficienti o a risultati ambigui.
- Arresto o Degenerazione Post-Biopsia: Nonostante esistano numerosi studi effettuati sugli animali e sull’uomo circa la possibilità di normale sviluppo embrionale successivo alla micromanipolazione per l’esecuzione della PGD/PGS, non è possibile escludere a priori che gli embrioni bioptizzati possano arrestarsi nel loro sviluppo o degenerare nei giorni successivi alla biopsia, e che quindi non ci siano embrioni disponibili per eseguire il trasferimento. Inoltre, non è possibile escludere a priori che gli embrioni bioptizzati con esito positivo (integri e vitali), anche se risultati sani all’analisi genetica, possano risultare degenerati/danneggiati al momento dello scongelamento, e che quindi non ci siano embrioni disponibili per eseguire il trasferimento. Sebbene il tasso di sopravvivenza sia molto alto, soprattutto quando la DGP viene fatta in blastocisti, la possibilità esiste.
Informazioni Limitate dall'Analisi:L’analisi PGT-A consente di ottenere solo informazioni relative alle alterazioni numeriche e strutturali dei cromosomi e non fornisce risultati riguardanti malattie genetiche ereditarie (ovvero monogeniche, causate dal difetto di un gene: es. fibrosi cistica, beta talassemia, ecc.) che potrebbero essere contemporaneamente presenti ma che non sono oggetto di questa diagnosi. Viceversa, la PGT-M consente di ottenere solo informazioni relative al disordine genetico indagato e non esclude la possibilità che siano presenti contemporaneamente altre anomalie (mutazioni genetiche; alterazioni numeriche e strutturali dei cromosomi). Per una valutazione completa, in alcuni casi, potrebbero essere necessarie entrambe le tipologie di test.
Necessità di Screening Prenatale Continuo:C’è una possibilità che durante lo sviluppo intrauterino accada un avvenimento che influenza il genoma, ovvero infiammazioni o cause fisicali. Un rischio della nascita di un bambino con difetti genetici c’è sempre. In ogni caso è necessario dedicare molta attenzione allo screening prenatale della donna, anche dopo una PGT positiva, per monitorare lo sviluppo fetale e rilevare eventuali nuove anomalie che potrebbero insorgere o quelle non identificate dalla PGT.
Il Percorso Completo della Procreazione Medicalmente Assistita con PGT: Passo Dopo Passo
La FIV con DGP è uno dei trattamenti più laboriosi nella riproduzione assistita e quindi ha diversi passaggi dalla stimolazione ovarica al trasferimento embrionale. Per le coppie che intendono intraprendere un trattamento di PGT presso il nostro Centro il primo step consiste in un colloquio preliminare con lo specialista in Genetica Medica, il quale valuterà la storia clinica della coppia, illustrerà le procedure, i limiti diagnostici, le percentuali di successo e i rischi.
Ecco i passaggi chiave di questo percorso:
FIVET (Fecondazione in Vitro con Trasferimento di Embrioni):Il processo inizia con la fecondazione in vitro, che consiste nell'eseguire la stimolazione ovarica sulla donna per produrre più ovociti. Segue il prelievo degli ovuli mediante puntura follicolare e, infine, la fecondazione degli ovuli con lo sperma del partner maschile o di una donatrice anonima. Come menzionato, la fecondazione attraverso ICSI è preferibile per ridurre il rischio di contaminazione.
Sviluppo Embrionale in Coltura Prolungata:Le caratteristiche degli embrioni in coltura sono valutate quotidianamente. Per poter eseguire la biopsia è necessario che abbiano un livello minimo di qualità per garantire la loro sopravvivenza. Gli embrioni vengono lasciati in coltura prolungata fino a che non raggiungono lo stadio di blastocisti, tipicamente il giorno 5 o 6 dopo la fecondazione. Questo permette una selezione naturale degli embrioni più vitali.
Biopsia Cellulare:Una volta che gli embrioni hanno raggiunto lo stadio di blastocisti (il giorno 5 o 6), viene eseguita la biopsia del trofoectoderma, estraendo alcune cellule. La cellula rimossa viene poi accuratamente posizionata in un tubo, un processo noto come tubing. La vitalità dell'embrione può essere compromessa da questa biopsia, poiché la perdita di una cellula può essere troppo stressante per la sopravvivenza dell'embrione. Pertanto, è necessario che questa estrazione delle cellule sia effettuata da personale di laboratorio altamente specializzato ed esperto.
Crioconservazione degli Embrioni (Vetrificazione):Dopo la biopsia, gli embrioni vengono congelati singolarmente mediante vetrificazione. Questo è un metodo di congelamento ultra rapido che preserva la vitalità degli embrioni mentre si attendono i risultati dell'analisi genetica, che richiede alcuni giorni.
Analisi Genetica:Il materiale bioptico (le cellule del trofoectoderma) viene inviato al laboratorio di genetica per l'analisi. Qui, utilizzando tecniche avanzate come l'NGS (Next Generation Sequencing) o la PCR (per PGT-M), si studiano i cromosomi e/o i geni nelle cellule biopsiate per identificare possibili alterazioni in essi. In particolare, l'analisi dei cromosomi è meglio conosciuta come screening genetico preimpianto (PGT-A) e, d'altra parte, il termine PGT-M è usato per l'analisi di specifiche mutazioni genetiche.
Selezione e Trasferimento di Embrioni Sani:Una volta ottenuti i risultati, gli embrioni sani saranno selezionati per il trasferimento nell'utero della madre o crioconservati per tentativi futuri. Gli embrioni con alterazioni genetiche vengono scartati, anche se apparentemente hanno una buona qualità morfologica.Il trasferimento di embrioni può essere effettuato in ciclo fresco o differito. Questo dipenderà dal tempo necessario per ottenere i risultati dell'analisi genetica, ed è abbastanza comune che gli embrioni debbano essere congelati. Se gli embrioni sono stati vitrificati prima dei risultati, saranno trasferiti in un ciclo sostitutivo. Per fare questo, la donna dovrà effettuare un preparato endometriale con la somministrazione di estrogeni e progesterone. Se i risultati mostrano che ci sono diversi embrioni privi di anomalie, solo l'embrione o gli embrioni con la migliore qualità morfocinetica per il trasferimento saranno scongelati, il che aumenterà la probabilità di impianto.
Questo approccio metodico e la stretta collaborazione tra specialisti in riproduzione assistita, embriologi e genetisti sono fondamentali per massimizzare le possibilità di una gravidanza di successo e la nascita di un bambino sano. La PGT, pur essendo una tecnica complessa e costosa, offre un valore inestimabile per le coppie che affrontano specifiche sfide riproduttive o genetiche, aprendo nuove speranze nel percorso della genitorialità.
tags: #pgs #su #blastocisti #step