La gravidanza rappresenta una delle sfide fisiologiche più complesse e affascinanti del corpo umano. Si tratta di un processo dinamico che trasforma radicalmente l'omeostasi materna per supportare lo sviluppo di un nuovo individuo, partendo dalla formazione dello zigote fino al complesso organismo che è il feto a termine. Comprendere la fisiologia della crescita fetale richiede un'analisi integrata dei cambiamenti sistemici della madre e dei meccanismi di regolazione placentare e fetale che ne determinano il successo.
L'avvio della gravidanza e i pilastri della cronologia gestazionale
Il primo segno di gravidanza è un mancato ciclo mestruale. Per le donne sessualmente attive che sono in età riproduttiva e hanno mestruazioni regolari, un ritardo ≥ 1 settimana è molto probabilmente dovuto a una gravidanza, anche se altri fattori possono causare amenorrea secondaria.
La data stimata del parto si basa sull'ultimo periodo mestruale. Un modo per calcolare la data stimata del parto è quello di sottrarre 3 mesi dall'ultimo periodo mestruale e aggiungere 7 giorni (regola di Naegele). Partorire fino a 3 settimane prima o 2 settimane dopo la data presunta rientra nella norma. Il parto prima delle 37 settimane di gestazione è considerato pre-termine; il parto dopo 42 settimane di gestazione è considerato post-termine.
Adattamenti cardiovascolari e ematologici materni
La gravidanza comporta in tutti gli organi e i sistemi materni una serie di modificazioni fisiologiche; la maggior parte ritorna alla normalità dopo il parto. In generale, le modificazioni sono più evidenti nelle gravidanze multiple rispetto alle gravidanze singole.
La gittata cardiaca, determinata dalla frequenza cardiaca moltiplicata per il volume di eiezione, aumenta dal 30 al 50% a partire dalla 6a settimana di gestazione e raggiunge il suo massimo tra la 16a e la 28a settimana (di solito intorno alla 24a settimana). Si prevede una lieve tachicardia materna. La gittata cardiaca resta vicino a livelli di picco fino a dopo la 30a settimana. Poi, la gittata cardiaca diventa sensibile alla posizione del corpo. Posizioni che causano compressione della vena cava da parte dell'utero aumentato di volume (p. es., la posizione sdraiata) determinano la maggiore riduzione della gittata cardiaca.
In media, la gittata cardiaca solitamente diminuisce leggermente dalla 30a settimana sino all'inizio del travaglio. Durante il travaglio la gittata cardiaca aumenta di un ulteriore 30%. Dopo il parto, l'utero si contrae e la gittata cardiaca scende drasticamente a un valore pari al 15-25% al di sopra del normale, poi diminuisce lentamente nel corso delle successive 3-4 settimane fino a raggiungere il livello pregravidico alla 6a settimana dopo il parto.
L'aumento della gittata cardiaca durante la gravidanza è dovuto prevalentemente alle richieste della circolazione utero-placentare; il volume della circolazione uteroplacentare aumenta notevolmente e la circolazione nello spazio intervilloso agisce in parte come uno shunt arterovenoso. Mentre la placenta e il feto si sviluppano, il flusso sanguigno verso la cavità uterina deve aumentare fino a circa 1 L/min (20% della gittata cardiaca normale) a termine della gravidanza. Le aumentate richieste della cute (per la regolazione della temperatura) e dei reni (per l'escrezione dei prodotti di scarto fetali) giustificano una parte dell'incremento della gittata cardiaca.
Per aumentare la gittata cardiaca, la frequenza cardiaca aumenta dal normale valore di 70 fino a 90 battiti/min; anche il volume di eiezione sistolico aumenta. Durante il 2o trimestre, la pressione arteriosa in genere diminuisce (e la pressione differenziale si amplia), nonostante la gittata cardiaca e i livelli di renina e angiotensina aumentino, perché la circolazione uteroplacentare si espande (lo spazio intervilloso placentare aumenta a sua volta) e la resistenza vascolare sistemica diminuisce. La resistenza diminuisce per via della diminuzione di viscosità del sangue e di sensibilità all'angiotensina. Durante il 3o trimestre, la pressione arteriosa può ritornare ai valori normali. Nelle gravidanze gemellari, la gittata cardiaca aumenta ulteriormente e la pressione arteriosa diastolica alla 20a settimana è inferiore rispetto a quella riscontrata nella gravidanza singola.
L'attività fisica provoca un aumento della gittata cardiaca, della frequenza cardiaca, del consumo di ossigeno e del volume respiratorio/min maggiori durante la gravidanza. La circolazione iperdinamica della gravidanza aumenta la frequenza di soffi funzionali e accentua i suoni cardiaci. Una RX o un ECG possono mostrare che il cuore è dislocato in una posizione orizzontale, ruotato verso sinistra e con un diametro trasverso aumentato. Extrasistoli sopraventricolari o ventricolari sono di comune riscontro in gravidanza. Tutte queste modificazioni sono fisiologiche e non devono indurre a una diagnosi errata di cardiopatia; si possono in genere gestire semplicemente rassicurando la paziente. Tuttavia, la tachicardia atriale parossistica si verifica con maggior frequenza nelle donne gravide e può richiedere una digitalizzazione profilattica o l'impiego di altri medicinali antiaritmici. La gravidanza non condiziona né le indicazioni né la sicurezza della cardioversione.
🔴 CARDIOPATIE E GRAVIDANZA - Diretta della Fondazione per il Tuo cuore
Il volume totale di sangue aumenta proporzionalmente alla gittata cardiaca, ma l'aumento del volume plasmatico è maggiore (intorno al 50%, solitamente di circa 1600 mL per un totale di 5200 mL) rispetto alla massa dei globuli rossi (circa 25%); pertanto l'emoglobina si riduce per diluizione, da 13,3 a circa 12,1 g/dL. Questa anemia da diluizione diminuisce la viscosità del sangue. Nelle gravidanze gemellari il volume totale sanguigno materno aumenta in misura maggiore (di circa il 60%). La conta dei globuli bianchi aumenta lievemente tra 9000 e 12 000/mcL. Una marcata leucocitosi (≥ 20 000/mcL) si verifica durante il travaglio e nei primi giorni del post-partum. Le necessità di ferro aumentano fino a un totale di circa 1 g durante l'intera gravidanza e sono più alte durante la 2a metà della gravidanza (da 6 a 7 mg/die). Il feto e la placenta utilizzano circa 300 mg di ferro e l'aumento della massa dei globuli rossi materni richiede un ulteriore apporto di 500 mg. L'escrezione corrisponde a 200 mg. È necessario un apporto supplementare di ferro per prevenire un'ulteriore riduzione dei livelli di emoglobina poiché la quantità assorbita con la dieta e quella prelevata dalle riserve di ferro (in media, 300-500 mg) è in genere insufficiente a soddisfare il fabbisogno della gravidanza.
Funzione renale e adattamenti metabolici
Le modificazioni della funzione renale vanno quasi di pace passo con quelle della funzione cardiaca. La velocità di filtrazione glomerulare aumenta dal 30 al 50%, raggiunge il suo massimo tra la 16a e la 24a settimana di gestazione e permane a tali livelli fino quasi al termine, quando può leggermente diminuire poiché la compressione dell'utero sulla vena cava spesso determina una stasi venosa alle estremità inferiori. Il flusso plasmatico renale aumenta in maniera proporzionale alla velocità di filtrazione glomerulare. Di conseguenza, l'azotemia diminuisce, solitamente fino a < 10 mg/dL (< 3,6 mmol urea/L) e i livelli di creatinina diminuiscono proporzionalmente fino a 0,5-0,7 mg/dL (44-62 micromol/L).
Una marcata dilatazione degli ureteri (idrouretere) è dovuta alle influenze ormonali (soprattutto del progesterone) e all'ostacolo rappresentato dalla pressione dell'utero aumentato di volume sugli ureteri, che può anche causare idronefrosi. La funzione renale aumenta inoltre marcatamente nel decubito laterale, in particolare quando si sta sul lato sinistro; questa posizione allevia la pressione che l'utero ingrandito esercita sui grandi vasi quando le donne gravide sono in posizione supina. Questo incremento posturale della funzione renale è una delle ragioni per cui la donna incinta ha bisogno di urinare spesso quando sta cercando di addormentarsi.
Fisiologia respiratoria e gastrointestinale
La funzionalità respiratoria cambia in parte poiché il progesterone aumenta e in parte perché l'utero ingrandito interferisce con l'espansione polmonare. Il progesterone trasmette al cervello il segnale di ridurre i livelli di diossido di carbonio (CO2). All'abbassamento dei livelli di CO2 corrisponde un aumento del volume corrente, del volume minuto e della frequenza respiratoria nonché un aumento del pH plasmatico.
Il consumo di ossigeno aumenta di circa il 20% per soddisfare le accresciute necessità metaboliche del feto, della placenta e di numerosi organi materni. Le riserve inspiratoria ed espiratoria, il volume e la capacità residui e la PCO2 plasmatica diminuiscono. La capacità vitale non subisce variazioni. La circonferenza toracica aumenta di circa 10 cm. Si verificano iperemia e edema considerevole delle vie respiratorie. A volte si verifica un'ostruzione nasofaringea sintomatica e congestione nasale, le trombe di Eustachio possono temporaneamente bloccarsi e il tono e la qualità della voce si modificano. Una modesta dispnea da sforzo è frequente e gli atti respiratori profondi diventano più frequenti.
Con il procedere della gravidanza, la compressione esercitata dall'utero in crescita sul retto e sull'ultimo tratto del colon può determinare stipsi. La motilità gastrointestinale si riduce perché gli elevati livelli di progesterone determinano il rilassamento della muscolatura liscia. La pirosi gastrica e le eruttazioni sono di frequente riscontro e sono dovute, verosimilmente, al ritardato svuotamento gastrico e al reflusso gastroesofageo dovuti al rilassamento dello sfintere esofageo inferiore e dello iato diaframmatico. La produzione di acido cloridrico diminuisce; pertanto l'ulcera gastroduodenale è poco frequente in gravidanza e le ulcere preesistenti spesso migliorano. L'incidenza dei disturbi della cistifellea aumenta leggermente. La gravidanza influisce in modo sottile sulla funzione epatica, specialmente sul trasporto della bile. I valori degli esami della funzionalità epatica di routine sono normali, ma il livello della fosfatasi alcalina aumenta progressivamente durante il 3o trimestre e può essere da 2 a 3 volte superiore rispetto a quello normale a termine della gravidanza; l'aumento è dovuto alla produzione placentare di questo enzima piuttosto che a una disfunzione epatica.
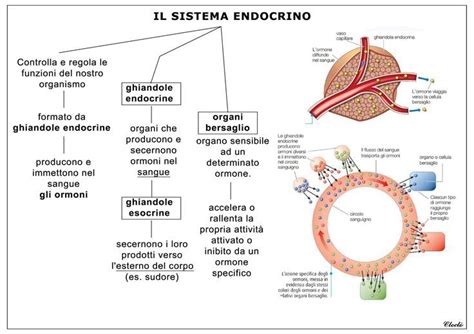
L'asse endocrino in gravidanza
La gravidanza altera la funzione della maggior parte delle ghiandole endocrine, in parte perché la placenta produce ormoni e in parte perché la maggior parte degli ormoni circola in una forma legata alle proteine e il legame alle proteine aumenta in gravidanza. La placenta inoltre produce la subunità beta della gonadotropina corionica umana (beta-hCG), un ormone trofico che, in modo analogo all'ormone follicolo-stimolante e all'ormone luteinizzante, mantiene il corpo luteo e inibisce di conseguenza l'ovulazione. I livelli di estrogeni e progesterone aumentano presto durante la gravidanza poiché il beta-hCG stimola le ovaie a produrli continuamente. Dopo 9-10 settimane di gravidanza, la stessa placenta produce elevati livelli di estrogeni e progesterone per aiutare a sostenere la gravidanza.
La placenta produce un ormone (simile all'ormone stimolante la tiroide) che aumenta la funzionalità tiroidea determinando iperplasia, incremento della vascolarizzazione e un moderato aumento delle dimensioni della ghiandola. L'estrogeno stimola gli epatociti, causando un aumento dei livelli di globulina legante la tiroide; in tal modo, sebbene i livelli di tiroxina totale possano aumentare, i livelli di ormoni tiroidei liberi rimangono normali. Gli effetti degli ormoni tiroidei tendono ad aumentare e possono simulare un quadro di ipertiroidismo, con tachicardia, palpitazioni, sudorazione eccessiva e instabilità emotiva. Tuttavia, un ipertiroidismo vero si verifica solo nello 0,08% delle gravidanze.
La placenta produce l'ormone di rilascio della corticotropina, che stimola la produzione materna di ormone adrenocorticotropo (ACTH). I livelli aumentati di ormone adrenocorticotropo (ACTH) determinano un incremento dei livelli degli ormoni surrenalici, specialmente dell'aldosterone e del cortisolo, che contribuiscono all'edema. L'aumentata produzione di corticosteroidi e l'aumentata produzione placentare di progesterone determinano una resistenza a insulina e un aumento del fabbisogno di insulina, così come lo stress della gravidanza e, possibilmente, l'aumento del livello di lattogeno placentare umano. L'insulinasi prodotta dalla placenta può inoltre aumentare il fabbisogno di insulina, cosicché le pazienti affette da diabete gestazionale sviluppano spesso forme più manifeste di diabete. La placenta produce l'ormone stimolante il melanocita (MSH), che aumenta la pigmentazione cutanea nella tarda gravidanza.
L'ipofisi si ingrossa di circa il 135% in gravidanza. I livelli plasmatici materni di prolattina aumentano di circa 10 volte. L'aumento della prolattina è correlato a un incremento della produzione di thyrotropin-releasing hormone (TRH), stimolato dagli estrogeni. La principale funzione dell'incremento della prolattina è quella di assicurare la lattazione. Il livello ritorna nella norma nel post-partum, anche nelle donne che allattano. I livelli aumentati di estrogeni, di progesterone e dell'ormone stimolante il melanocita (MSH) contribuiscono alle alterazioni pigmentarie, tuttavia l'esatta patogenesi resta sconosciuta. I nevi aranei (nevi aracniformi) sono piccoli punti rossi luminosi circondati da minuscoli capillari, che si sviluppano comunemente in pazienti in gravidanza, in pazienti che usano contraccettivi orali, e in pazienti che hanno cirrosi.
Dinamiche della crescita fetale e monitoraggio clinico
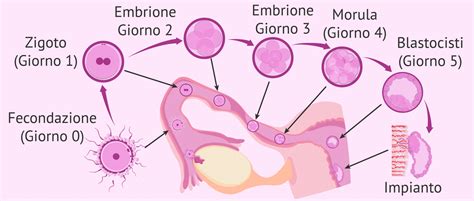
Entro le 24 ore che seguono il concepimento, lo zigote va incontro a una rapida crescita formando l’embrione. Fino all’ottava settimana circa, l’embrione si sviluppa ulteriormente dando luogo a un organismo più complesso: il feto. Lo sviluppo del feto consiste nell’insieme di fenomeni che permettono l’accrescimento e l’organizzazione delle strutture che formeranno il corpo del neonato.
La crescita del feto non è uniforme e varia in base all’età gestazionale. Nei primi mesi (dal terzo al quinto) cresce per lo più in lunghezza, guadagnando circa 5 cm al mese. Anche le proporzioni, in particolare quella tra la testa e il corpo del nascituro, si modificano nelle varie fasi di gravidanza. Si inizia a parlare di feto dalla nona settimana di gestazione. All'ottava settimana, la lunghezza del feto è di circa un centimetro e lo sviluppo del cuore è già completo. Le fattezze sono ancora abbozzate, ma sono già presenti occhi, naso e bocca. Tra la nona e la decima settimana la testa cresce più rapidamente del resto del corpo, dovendo accogliere il cervello. Alla fine del primo trimestre (tra la 9^ e la 12^ settimana) tutti gli organi e gli arti sono presenti e continueranno a svilupparsi fino a diventare funzionali. Il feto inizia in questo momento a muoversi ed esplorare ciò che lo circonda aprendo e chiudendo la bocca e i pugni, anche se la mamma non può ancora percepirne i movimenti.
Alla fine del quarto mese, il feto è lungo circa 15 cm e pesa poco più di 100 grammi. Al quinto mese iniziano a crescere sulla testa i primi capelli e la cute è ricoperta di una fine peluria che serve, insieme alla vernice caseosa, a proteggere la pelle ancora molto sottile. La madre inizia a percepire, in modo sempre più chiaro, i movimenti spontanei del feto perché iniziano a svilupparsi i muscoli. Al sesto mese le palpebre iniziano a schiudersi e gli occhi si aprono. Il sistema uditivo permette al feto di sentire i suoni, a cui risponde muovendosi e aumentando la frequenza cardiaca. Alla 24^ settimana inizia un processo molto importante, cioè la produzione di una sostanza chiamata “surfattante” che consentirà ai polmoni, dopo il primo respiro, di rimanere ben espansi e il buon adattamento alla vita extrauterina.
Al settimo mese (28^ settimana), il terzo trimestre, la fase conclusiva della gravidanza, è il momento di sviluppo finale che aiuta il feto a prepararsi per la nascita. In questi ultimi mesi il bambino prende peso velocemente e, grazie all’accumulo del grasso sottocutaneo, assume un aspetto più tondeggiante. Il cervello matura in fretta e il feto ormai vede e sente. Durante l’ultimo mese, tra la 37^ e la 40^ settimana, il travaglio potrebbe iniziare in qualsiasi momento e i movimenti fetali potrebbero ridursi, dato il poco spazio rimasto. In questa fase la posizione fetale potrebbe cambiare per prepararsi al parto, posizionandosi idealmente con la testa in basso, verso l’utero.
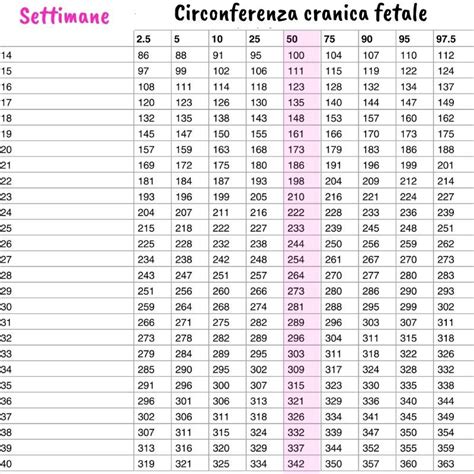
Conoscere le dimensioni del feto permette di datare in maniera abbastanza precisa la gravidanza. A tale scopo sono state studiate e messe a punto le tabelle di crescita fetale, che permettono di valutare se la lunghezza del feto, il suo peso e in generale le sue misure sono adeguate alla settimana di gestazione oppure se è necessario procedere con ulteriori approfondimenti. Durante il primo e all’inizio del secondo trimestre, la dimensione principale da tenere sotto controllo è il valore che si ottiene misurando dalla testa fino all’osso sacro (o lunghezza vertice-sacro, CRL).
Patologie della crescita e insufficienza placentare
Classicamente si parla di ritardo di crescita quando il peso fetale è pari o inferiore al 10° percentile per l’epoca gestazionale. In questa definizione sono compresi anche i feti costituzionalmente piccoli, per esempio nati da genitori di bassa statura. Con il termine ritardo di crescita intrauterino si intende più precisamente una crescita fetale rallentata rispetto ai controlli precedenti.
Il concetto di percentile o centile è fondamentale: se prendiamo 100 feti di una certa epoca gestazionale, il feto al cinquantesimo centile è quel feto il cui peso è esattamente nella media. Quinto centile vuol dire che di 100 feti di una certa epoca gestazionale, 95% sono più grandi. Novantacinquesimo centile vuol dire che di 100 feti, solo il 5% sono più grandi.
Le cause di ritardo di crescita sono molteplici ed in circa la metà dei casi non è presente un motivo ben identificabile. L’ipertensione gestazionale materna ed il ritardo di crescita fetale rappresentano diverse manifestazioni di una malattia comune: l’insufficienza placentare, a volte definita difetto di placentazione. Quando questo processo non avviene correttamente una placenta inadeguata alle necessità del feto determina un ritardo di crescita.
Per valutare il corretto sviluppo placentare è stata introdotta nella pratica clinica la valutazione della flussimetria delle arterie uterine che normalmente viene eseguita a 22-24 settimane di gestazione. Naturalmente la presenza di arterie uterine alterate non significa presenza di malattia, solo maggiore probabilità di sviluppare ritardo di crescita o pre-eclampsia. Più precisamente la presenza di arterie uterine normali a 24 settimane indicano che in meno dell’1% dei casi la gestante svilupperà preeclampsia o ritardo di crescita. Nelle arterie uterine non adeguate, il picco sistolico è molto più alto della diastole successiva; si dice che la pulsatilità dell’onda è aumentata.
La diagnosi di ritardo di crescita è esclusivamente ecografica. Tuttavia l’esame clinico è fondamentale per porre il sospetto: ad ogni visita il ginecologo esegue la palpazione dell’addome materno e la misura della distanza sinfisi-fondo (cioè la misura della lunghezza dell’utero) per avere un’idea della crescita fetale. Nei casi dubbi viene richiesta la conferma ecografica. Fondamentale è essere in possesso di un’ecografia che dia una datazione precisa della gravidanza tramite la misurazione della lunghezza vertice-sacro (CRL) nel corso del primo trimestre di gravidanza o del diametro biparietale (BPD) o del diametro trasverso del cervelletto (DTC) prima della 22° settimana. In base alla corretta datazione può essere definito ritardo di crescita una biometria inferiore al 10° centile per epoca gestazionale.
Nel caso in cui tutti i parametri biometrici (cranio, addome e femore) siano ridotti parleremo di ritardo di crescita simmetrico, mentre nel caso in cui sia presente una marcata riduzione solo della circonferenza addominale (CA) saremo di fronte ad un ritardo di crescita asimmetrico. Nella maggior parte dei casi un ritardo di crescita precoce (da cause genetiche o cromosomiche) è simmetrico, mentre un ritardo di crescita tardivo (da cause placentari) risulta asimmetrico. Nel ritardo di crescita asimmetrico, i nutrienti vengono inviati preferenzialmente verso cuore e cervello, gli organi detti “nobili”, mentre i visceri addominali, in particolare il fegato, ricevono meno nutrienti, motivo per cui la circonferenza addominale si riduce drasticamente.
Flussimetria e centralizzazione del circolo fetale
La flussimetria dell’arteria ombelicale rappresenta lo strumento più efficace per individuare tra i feti con ritardo di crescita quelli a maggior rischio di sviluppare ipossia, ovvero il ridotto apporto di ossigeno. Anche per l’arteria ombelicale, come per le arterie uterine, si valutano degli indici flussimetrici detti P.I. e R.I.: il flusso nell’arteria ombelicale è correlato al corretto sviluppo placentare sul versante fetale.
In caso di ritardo di crescita il feto ridistribuisce il flusso di sangue verso quegli organi che necessitano maggiormente di ossigeno e nutrienti per svilupparsi correttamente, come il cuore ed il sistema nervoso centrale. Tale processo è chiamato centralizzazione del circolo. Per questo motivo si assiste ad una dilatazione dell’arteria cerebrale media con aumento del flusso diastolico al fine di aumentare l’apporto di ossigeno e nutrienti.
Il dotto venoso è un vaso che porta sangue ossigenato dalla placenta in direzione del cuore. Come tutti i vasi venosi, esso presenta un flusso in direzione del cuore che in condizioni di normalità mantiene tale direzione durante tutto il ciclo cardiaco. In caso di ritardo di crescita il feto ridistribuisce il flusso di sangue verso gli organi più importanti e così aumentano le resistenze contro cui il cuore deve lavorare; in questo modo anche il flusso verso il cuore risulta alterato riducendo ed infine invertendo la parte finale del flusso nel dotto venoso chiamata onda a. Da un punto di vista clinico questa valutazione è molto importante perchè in caso di arteria ombelicale patologica un’onda a normale nel dotto venoso conferma un quadro di compenso fetale, mentre un’onda a assente o invertita mostra lo scompenso fetale.
Il dotto venoso è l’ultimo parametro che si altera nel ritardo di crescita. Un dotto venoso alterato è una condizione di altissimo rischio di esito avverso se non si interviene rapidamente. La scelta del momento del parto di un feto affetto da ritardo di crescita rappresenta una delle sfide dell’ostetricia moderna. Da una parte dobbiamo evitare di far nascere un bambino troppo presto aggiungendo al ritardo di crescita i problemi della prematurità, dall’altra non dobbiamo mantenere troppo a lungo un feto piccolo in un ambiente intrauterino che non è più in grado di ossigenarlo e nutrirlo sufficientemente.
La scelta del parto dipenderà quindi dall’epoca gestazionale, dalla gravità del ritardo di crescita e dal grado di compenso fetale. E’ necessario quindi monitorare tutti i parametri che abbiamo a disposizione: stima del peso, quantità di liquido amniotico, flussimetria fetale, epoca gestazionale e maturità polmonare. Può essere utilizzata anche la cardiotocografia che tramite la valutazione della frequenza cardiaca fetale è in grado di determinare il grado di ossigenazione fetale. Nel caso in cui il ritardo di crescita sia associato ad ipertensione e preeclampsia anche le condizioni materne devono essere prese in considerazione nella scelta corretta del momento del parto.
Una delle principali sfide globali dell’Organizzazione Mondiale della Sanità consiste nella riduzione della mortalità e della morbilità perinatale. La prevenzione di questi fattori passa anche dalla diagnosi precoce delle problematiche che possono insorgere durante la gravidanza o i primi mesi di vita. Una volta identificata una situazione di ritardo nello sviluppo è fondamentale monitorare con attenzione la crescita nelle settimane successive e studiare l’anatomia, la circolazione a livello dei vasi ombelicali e dell’arteria cerebrale fetale, il contenuto del liquido amniotico. Tuttavia non tutti i casi al di sotto del decimo percentile sono da considerarsi patologici. Alcuni feti, infatti, sono costituzionalmente più piccoli, e dunque non è necessario ricorrere a un intervento medico. Qualora si confermi un ritardo dello sviluppo fetale, si devono escludere le cause patologiche più frequenti. Inoltre, bisogna identificare eventuali problematiche fetali legate all’anatomia anomala o cause genetiche. Altre cause di crescita fetale lenta possono essere le infezioni o la sindrome da anticorpi antifosfolipidi.
tags: #fisiologia #della #crescita #fetale