L'incompatibilità del gruppo sanguigno tra madre e feto rappresenta un'area di fondamentale importanza nella medicina perinatale, con la Malattia Emolitica del Feto e del Neonato (MEFN), comunemente nota come eritroblastosi fetale, che emerge come la sua manifestazione più seria. Questa patologia si verifica principalmente quando il gruppo sanguigno della madre è Rh-negativo e il gruppo sanguigno del feto è Rh-positivo, configurando una condizione in cui il sistema immunitario materno può potenzialmente scatenare una reazione avversa contro i globuli rossi del proprio figlio. La comprensione approfondita dei meccanismi sottostanti e l'implementazione di efficaci strategie preventive, in particolare la profilassi anti-D, sono state cruciali nel trasformare la prognosi di questa condizione, da grave minaccia a patologia ampiamente controllabile. Questo articolo si propone di esplorare la natura dell'eritroblastosi fetale, i suoi meccanismi, le implicazioni diagnostiche e terapeutiche, con un'enfasi particolare sulla profilassi anti-D come pilastro della prevenzione.

Il Fattore Rh e il Complesso Meccanismo dell'Incompatibilità Materno-Fetale
Il fattore Rh è una molecola, o antigene, situata sulla superficie dei globuli rossi di alcune persone. La presenza di questo fattore determina un gruppo sanguigno Rh-positivo, mentre la sua assenza lo rende Rh-negativo. Questa distinzione, apparentemente semplice, è alla base di un complesso scenario immunologico che può sorgere durante la gravidanza. I problemi iniziano a manifestarsi nel momento in cui il sangue di un feto Rh-positivo entra in contatto con il flusso sanguigno di una donna Rh-negativa.
Il sistema immunitario della madre, trovandosi di fronte a globuli rossi fetali che esprimono il fattore Rh (considerato estraneo al suo organismo), può reagire riconoscendoli come invasori. In risposta a tale "invasione", il sistema immunitario materno produce specifici anticorpi, noti come anticorpi anti-Rh. Questi anticorpi sono proteine specializzate prodotte dalle cellule immunitarie con l'obiettivo primario di difendere l’organismo dalle sostanze estranee. La produzione di questi anticorpi in seguito al contatto con globuli rossi fetali Rh-positivi è un processo chiamato sensibilizzazione Rh. È importante notare che l'eritroblastosi fetale è una forma di anemia emolitica dovuta alla trasmissione per via transplacentare di anticorpi materni diretti contro i globuli rossi del feto o del neonato. Questa patologia è solitamente causata da un'incompatibilità del fattore Rhesus (o Rh: antigene espresso sulla superficie dei globuli rossi), che induce un'iperdistruzione eritrocitaria fetale.
In genere, la malattia emolitica del feto e del neonato non causa problemi nella prima gravidanza in cui si verifica la sensibilizzazione. Questo accade perché il primo contatto tra il sangue fetale Rh-positivo e quello materno Rh-negativo spesso non induce una risposta immunitaria immediata e massiccia da parte della madre, o comunque gli anticorpi vengono prodotti in quantità significative solo verso la fine della gestazione, spesso al momento del parto. Di solito, la sensibilizzazione materna e la produzione di anticorpi avvengono principalmente durante il parto della prima gravidanza. Tuttavia, una volta che la madre è stata sensibilizzata, il suo sistema immunitario "ricorda" l'antigene Rh. Questo significa che, in ogni gravidanza successiva in cui il feto dovesse essere nuovamente Rh-positivo, la donna sarà in grado di produrre anticorpi anti-Rh molto più rapidamente e in quantità maggiori. Gli anticorpi materni raggiungono il feto attraverso la placenta e provocano la lisi dei globuli rossi fetali.
Oltre all'incompatibilità del fattore Rh, l'eritroblastosi fetale può originare anche dal coinvolgimento di altri antigeni. Ad esempio, incompatibilità possono verificarsi anche per il sistema di Kell o di Duffy. Esiste inoltre la possibilità che la madre sviluppi anticorpi verso il feto anche per altri fattori sanguigni minori rispetto al gruppo AB0 e al fattore Rh. Le incompatibilità materno-fetali dei gruppi sanguigni AB0, pur causando fenomeni simili, sono generalmente meno gravi e meno frequenti rispetto a quelle del fattore Rh. Se la madre ha gruppo sanguigno 0 e il feto A o B, si ha incompatibilità AB0. La principale differenza tra i due tipi è che la MEFN da AB0 può colpire indifferentemente qualsiasi figlio, mentre quella da Rh colpisce indistintamente solo dal secondo figlio in poi. Tale incompatibilità può causare problemi simili a quelli della malattia emolitica del feto e del neonato, sebbene di solito con una gravità inferiore.
Sistema Rh e l'eritroblastosi fetale Zanichelli
La Malattia Emolitica del Feto e del Neonato (MEFN): Conseguenze e Manifestazioni
La Malattia Emolitica del Feto e del Neonato (MEFN), conosciuta anche come eritroblastosi fetale quando si manifesta in utero, è una condizione grave che deriva dalla distruzione dei globuli rossi del feto o del neonato da parte degli anticorpi materni. Questo processo distruttivo, noto come emolisi, può portare a una serie di conseguenze cliniche di varia entità, che spaziano da forme lievi a condizioni estremamente severe e potenzialmente letali. La patologia è causata dalla trasmissione per via transplacentare di anticorpi materni diretti contro i globuli rossi del feto o del neonato.
Quadri Clinici e Progressione della Malattia:Durante l'iniziale gravidanza in cui avviene la sensibilizzazione, le complicanze per il feto o il neonato sono improbabili o assenti. Questo perché, come accennato, la produzione di anticorpi significativi si verifica spesso tardivamente, specialmente durante il parto stesso. Tuttavia, nelle gestazioni successive, se la donna Rh-negativa concepisce un bambino con sangue Rh-positivo, gli anticorpi materni, che nel frattempo sono stati prodotti in maggiore quantità e con maggiore rapidità, attraversano la placenta in maniera più efficace. Essi raggiungono il feto molto prima, talvolta già a partire dal quarto mese di gestazione.
Il passaggio di questi anticorpi al feto innesca una distruzione accelerata dei globuli rossi fetali. Tale distruzione è chiamata malattia emolitica del feto (eritroblastosi fetale) o del neonato (eritroblastosi neonatale). Se i globuli rossi vengono distrutti più velocemente di quanto il feto ne riesca a produrre, il feto può diventare anemico, cioè avere un numero troppo basso di globuli rossi. L'anemia grave è una delle complicanze più temute, poiché può portare a insufficienza cardiaca ad alta gittata, edema generalizzato noto come idrope fetale, e, nei casi più estremi, alla morte fetale intrauterina.
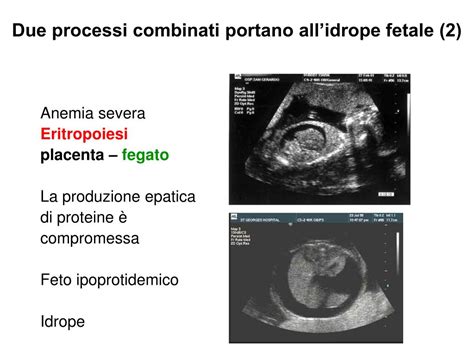
Nel tentativo di correggere l'anemia, il midollo osseo fetale intensifica la produzione di globuli rossi, rilasciando in circolazione anche forme immature, chiamate eritroblasti. È proprio da questa massiccia presenza di eritroblasti nella circolazione periferica che deriva il nome "eritroblastosi fetale". Il sistema emopoietico fetale, come risposta all’anemia, incrementa la produzione di cellule ematiche e immette in circolo forme immature di globuli rossi dette eritroblasti. Questo processo può essere talmente esagerato da provocare l'ingrossamento di organi come fegato e milza, i quali tentano di compensare la rottura dei globuli rossi attivando una produzione supplementare di emazie.
Manifestazioni nel Neonato:I neonati affetti da eritroblastosi fetale possono presentare un ampio spettro di sintomi alla nascita, a seconda della gravità dell'emolisi. I feti più gravemente colpiti che sopravvivono alla nascita possono essere estremamente pallidi e presentare edemi generalizzati, ipoproteinemia e versamenti pleurici e peritoneali, tutti segni dell'idrope fetale. Questi neonati, come quelli con idrope, sono molto pallidi, hanno edemi generalizzati, versamento pleurico e peritoneale. I neonati con anemia emolitica meno grave possono essere anemici, ma non presentano edemi o altri segni di idrope. Quelli colpiti in maniera lieve possono essere leggermente o affatto anemici alla nascita.
Subito dopo il parto, i bambini colpiti presentano, solitamente, elevati livelli di bilirubina indiretta, una pigmentazione gialla prodotta dalla distruzione dei globuli rossi. Questa condizione è nota come iperbilirubinemia e si manifesta clinicamente con l'ittero, dove la pelle e la sclera (il bianco dell'occhio) del neonato assumono una colorazione giallastra. Nei casi gravi di iperbilirubinemia, il cervello può rimanere danneggiato da un accumulo eccessivo di bilirubina, una condizione irreversibile e devastante chiamata kernittero. L'ittero nucleare, come è anche conosciuto il kernittero, è causato dal continuo effetto emolitico degli anticorpi anti-Rh che hanno superato il filtro placentare e sono rimasti nel circolo fetale. È importante sottolineare che gli anticorpi materni possono permanere nel sangue del neonato fino a 3-4 mesi dopo la nascita, continuando a causare emolisi.
Di solito, la malattia emolitica del feto e del neonato non causa sintomi nelle gestanti. Le conseguenze sono esclusivamente a carico del feto e del neonato, rendendo essenziale una diagnosi precoce e un'attenta gestione della gravidanza in donne a rischio.
Diagnosi dell'Incompatibilità Rh e Monitoraggio della MEFN
La diagnosi precoce e il monitoraggio attento sono fondamentali per la gestione efficace dell'incompatibilità Rh e della Malattia Emolitica del Feto e del Neonato (MEFN). L'approccio diagnostico si articola in diverse fasi, iniziando con lo screening materno e progredendo, se necessario, con indagini più specifiche sul padre e sul feto.
Screening Materno Iniziale:Durante la prima visita medica nel corso della gravidanza, tutte le donne vengono sottoposte a screening per determinare il gruppo sanguigno, controllare se sono Rh-positive o Rh-negative e se presentano anticorpi anti-Rh o altri anticorpi contro i globuli rossi. Questo esame comprende anche la ricerca di anticorpi irregolari mediante il test di Coombs indiretto. La verifica del gruppo sanguigno e del fattore Rh è uno degli esami che vengono offerti a tutte le donne all'inizio della gravidanza. Secondo tutte le precedenti linee guida, ogni paziente alla prima visita prenatale dovrebbe essere testata per gruppo sanguigno AB0 e lo status Rh e il test indiretto all’Antiglobulina (test di Coombs indiretto).
Valutazione del Rischio e Screening Paterno:Se il sangue della madre è Rh-negativo, il passo successivo è valutare il rischio di sensibilizzazione e produzione di anticorpi anti-Rh. In tale scenario, si procede con l'analisi del gruppo sanguigno del padre, se disponibile. Se il padre è Rh-negativo, non sono necessari ulteriori accertamenti poiché non vi è rischio che il feto sia Rh-positivo, e quindi non sussiste il pericolo di incompatibilità Rh.
Tuttavia, se il padre è Rh-positivo, o non è disponibile per le analisi ma la madre è Rh-negativa, il rischio di un feto Rh-positivo esiste. In questi casi, è possibile eseguire un test innovativo chiamato test dell'acido nucleico (DNA) fetale libero per determinare se il feto abbia sangue Rh-positivo. Questo esame consiste in un prelievo di sangue della madre da analizzare per individuare ed esaminare piccoli frammenti del DNA fetale, presenti in minuscole quantità nel sangue materno, solitamente dopo 10-11 settimane di gestazione. Tra la fine del primo e l’inizio del secondo trimestre di gravidanza, è possibile determinare il fenotipo Rh del feto sul DNA libero di origine fetale (cell free fetal DNA o cffDNA) presente nel sangue materno con il NIPT test, raccomandato in gestanti Rh(D) negativo con partner Rh(D) positivo. Le pazienti con riscontro di Rh D e test di Coombs indiretto negativi sono le candidate alla profilassi anti D a meno che non siano noti lo status Rh del padre e del nascituro e che la paternità sia certa.
Monitoraggio in Gravidanza:Se il sangue del padre è Rh-positivo e la madre è Rh-negativa (e potenzialmente sensibilizzata o a rischio di sensibilizzazione), i medici misurano periodicamente il livello di anticorpi anti-Rh nel sangue della madre. Questi accertamenti diagnostici possono richiedere anche misurazioni seriate del titolo anticorpale materno, da misurare mensilmente fino alla 24a settimana, poi ogni due settimane. Un aumento del livello anticorpale, o il raggiungimento di un determinato valore soglia, indica un aumentato rischio di anemia del feto.
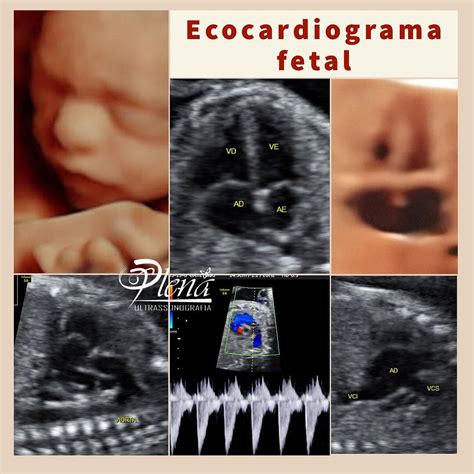
In presenza di un rischio elevato o di segni di sensibilizzazione, si ricorre periodicamente a un ecodoppler. L'ecodoppler viene utilizzato per valutare il flusso di sangue nel cervello del feto, in particolare nella arteria cerebrale media. Anomalie nel flusso sanguigno possono essere un indicatore indiretto di anemia fetale, consentendo una diagnosi precoce di questa condizione. Le carenze assistenziali sono state anche rimarcate nelle ecografie, condotte a cadenza bisettimanale proprio per il rischio di malattia emolitica del neonato, nelle quali viene chiaramente espressa la mancanza di profilassi. Questo sottolinea l'importanza di un monitoraggio costante e dell'aderenza alle linee guida.
Trattamento della Malattia Emolitica del Feto e del Neonato
Una volta diagnosticata la Malattia Emolitica del Feto e del Neonato (MEFN), l'obiettivo principale del trattamento è mitigare gli effetti dell'anemia e prevenire complicanze gravi per il feto e il neonato. Le strategie terapeutiche possono variare in base alla gravità dell'anemia, all'età gestazionale e allo stato di sensibilizzazione materno.
Gestione Prenatale: Trasfusioni di Sangue al Feto:Se il feto risulta essere Rh-negativo o se i risultati degli esami continuano a indicare che il feto non soffre di anemia, la gravidanza può continuare a termine senza la necessità di trattamenti specifici legati all'incompatibilità Rh. Tuttavia, se si giunge alla diagnosi di anemia fetale, in particolare di entità moderata o grave, si rende necessario intervenire con trasfusioni di sangue al feto prima della nascita. Queste procedure devono essere effettuate in un centro specializzato per gravidanze ad alto rischio, data la loro complessità e i potenziali rischi.
Il più delle volte, la trasfusione viene effettuata mediante un ago inserito direttamente in una vena del cordone ombelicale. In alcuni casi, soprattutto in passato o per specifiche indicazioni, si poteva intervenire con trasfusioni di eritrociti di gruppo Rh negativo al feto, iniettando direttamente nel cavo addominale fetale, sotto guida ecografica e utilizzando un mezzo di contrasto. Questa procedura, sebbene meno comune oggi, era considerata molto rischiosa in quanto poteva indurre involontarie contrazioni uterine con espulsione del prodotto del concepimento. Di norma, vengono somministrate trasfusioni supplementari a intervalli regolari, spesso fino a 32-35 settimane di gravidanza, a seconda della risposta fetale e della gravità dell'anemia. Il momento esatto delle trasfusioni dipende da quanto grave è l’anemia e dall’età del feto.
Prima della prima trasfusione, o in previsione di un parto prematuro, le donne ricevono spesso corticosteroidi se la gravidanza ha raggiunto almeno 23 settimane di gestazione. I corticosteroidi favoriscono la maturazione dei polmoni del feto e aiutano a prevenire le comuni complicanze respiratorie che possono interessare un neonato pretermine.
Tempistiche del Parto:La decisione su quando effettuare il parto dipende dalla situazione clinica individuale della donna e del feto. In alcuni casi di grave anemia fetale che non risponde adeguatamente alle trasfusioni intrauterine, o in presenza di altre complicanze, un parto prematuro può essere programmato per consentire un trattamento intensivo del neonato al di fuori dell'ambiente uterino.
Gestione Postnatale: Trasfusioni Neonatali e Exsanguinotrasfusione:Dopo la nascita, il neonato può aver bisogno di ulteriori trasfusioni di sangue per correggere l'anemia residua o per contrastare l'emolisi persistente causata dagli anticorpi materni che rimangono nel suo circolo. A volte, le trasfusioni sono necessarie solo dopo il parto, specialmente nelle forme meno severe della malattia.
In passato, l'exsanguinotrasfusione era una procedura comune e vitale per trattare l'iperbilirubinemia grave e l'anemia nei neonati affetti da MEFN. Con quest'ultima procedura, si provvede a sostituire pressoché completamente il sangue del bambino con altro sangue fornito da donatori, privo degli anticorpi specifici contro il fattore Rh. Questo processo rimuove gli anticorpi materni circolanti e la bilirubina in eccesso, fornendo allo stesso tempo globuli rossi freschi. Tuttavia, grazie all'introduzione e all'ampia adozione della profilassi anti-D in gravidanza, l'exsanguinotrasfusione per il trattamento della malattia emolitica del neonato è diventata ormai rara. Nonostante ciò, essa può ancora rendersi necessaria in casi rari o a causa dello sviluppo di altri anticorpi come anti-c, anti-E e incompatibilità AB0, per i quali non esiste una profilassi specifica. Alla nascita l'exsanguinotrasfusione, se disponibile, va attuata il più precocemente possibile in caso di necessità.
È fondamentale che, in ogni caso, il parto sia il meno traumatico possibile per minimizzare il rischio di ulteriori passaggi di sangue fetale nel circolo materno e per non aggravare le condizioni del neonato.
La Prevenzione: Pilastro della Profilassi Anti-D
La vera rivoluzione nella gestione dell'eritroblastosi fetale è avvenuta con l'introduzione della profilassi anti-D. Questa strategia preventiva ha drasticamente ridotto l'incidenza della malattia, trasformando una condizione potenzialmente devastante in una quasi completamente evitabile. Ad oggi è possibile, anzi doveroso prevenire la malattia emolitica del neonato e l'isoimmunizzazione materna con l'immunoprofilassi, cioè con la somministrazione di immunoglobuline nella madre che impediscono che ella produca anticorpi contro i globuli rossi del feto.
Il Principio della Profilassi con Immunoglobuline Rho(D):La profilassi anti-D si basa sulla somministrazione di anticorpi anti-Rh esogeni, definiti immunoglobulina Rho(D) o immunoglobuline anti-D. Questi anticorpi sono derivati dal plasma di donatori RhD negativi e sono costituiti da immunoglobuline (IgG). L'azione della somministrazione esogena di IgG per sopprimere la risposta immune, come nel caso della profilassi anti-D, è nota come soppressione immune anticorpo-mediata.
Il meccanismo d'azione è duplice: quando un piccolo volume di sangue fetale Rh-positivo entra nel circolo materno Rh-negativo, le immunoglobuline anti-D somministrate si legano rapidamente agli eritrociti fetali Rh-positivi prima che il sistema immunitario della madre possa riconoscerli e montare una propria risposta. Questo processo "maschera" l'antigene Rh, riducendo la capacità del sistema immunitario della donna di riconoscere il fattore Rh presente sui globuli rossi del bambino, eventualmente entrati nel torrente ematico della madre. In tal modo, il sistema immunitario materno non produce anticorpi per il fattore Rh. L'effetto è tale che l'esposizione susseguente all'antigene di D non provoca una risposta immune secondaria, quanto piuttosto una risposta primaria, meno aggressiva e con una produzione anticorpale minore o assente.
Quando e Come Viene Somministrata la Profilassi Anti-D:Le immunoglobuline anti-D vengono somministrate per via intramuscolare (tipicamente sulla spalla), sottocutanea o, in casi specifici come piastrinopenia materna, endovenosa. La somministrazione segue un protocollo ben definito, basato su raccomandazioni internazionali per massimizzare l'efficacia preventiva:
- Profilassi Antenatale di Routine: Come precauzione, le donne con sangue Rh-negativo non sensibilizzate ricevono un'iniezione di anticorpi anti-Rh in ciascuno dei seguenti momenti:
- Dopo 28 settimane di gravidanza (o sia a 28 sia a 34 settimane). Questa è una prassi offerta di routine a tutte le donne in gravidanza Rh(D) negative non sensibilizzate. La Society of Obstetricians and Gynecologists of Canada (SOGC) suggerisce 300 µg a 28 settimane o due dosi di 100-120 µg a 28 e 34 settimane.
- Profilassi Post-Partum: Entro 72 ore dal parto di un bambino con sangue Rh-positivo, per prevenire la sensibilizzazione causata dal massiccio passaggio di sangue fetale al momento del parto. Questa somministrazione è ripetuta entro 72 ore dal parto nel caso il neonato sia Rh positivo. In passato si eseguiva la somministrazione esogena di IgG dopo il parto, ma è stato rilevato da Bowman et al. come la profilassi antenatale migliori ulteriormente i risultati.
- Dopo Eventi Sensibilizzanti: La profilassi è indicata dopo qualsiasi episodio o procedura che potrebbe comportare un passaggio di sangue fetale nel circolo materno, come ad esempio:
- Dopo un aborto spontaneo o indotto.
- Dopo eventuali episodi di sanguinamento vaginale significativo durante la gravidanza.
- Dopo procedure diagnostiche invasive come amniocentesi, prelievo dei villi coriali (villocentesi) o funicolocentesi.
- A seguito di traumi addominali.
- In caso di minacce di aborto.
- Dopo manovre ostetriche per la versione cefalica del feto.
Talvolta, quando grandi quantità di sangue fetale entrano nel torrente ematico della donna, sono necessarie ulteriori iniezioni, o dosi maggiori, di immunoglobuline anti-D.
Linee Guida Internazionali e Importanza dell'Aderenza:L'efficacia della profilassi anti-D è ampiamente riconosciuta e supportata da diverse linee guida internazionali, tra cui quelle della SOGC (Society of Obstetricians and Gynecologists of Canada), del NICE (National Institute for Clinical Excellence) del Regno Unito, e dell'ACOG (American College of Obstetrics and Gynecology). Queste linee guida raccomandano l'implementazione sistematica della profilassi per tutte le donne Rh-negative non sensibilizzate.
L'isoimmunizzazione Rh materno-fetale è lo sviluppo di anticorpi contro antigeni del sistema Rh presenti sulla superficie dei globuli rossi che provoca incompatibilità materno-fetale causata dal passaggio, attraverso la placenta al feto, degli anticorpi anti-Rh materni. Il rispetto delle linee guida e l'immunizzazione a 28 settimane avrebbero evitato nel 99,9% dei casi l'isoimmunizzazione materna e la conseguente complicanza della successiva gravidanza. L'importanza della corretta applicazione è stata evidenziata in casi in cui la profilassi non è stata eseguita correttamente, come nel caso di una paziente la cui prima gravidanza era stata testata per il gruppo sanguigno e il test di Coombs, ma non era stata eseguita correttamente la somministrazione di immunoglobuline prevista alle 28 settimane. La negatività del test di Coombs a 30 settimane dimostrava che la signora per quell'epoca gestazionale non era ancora immunizzata; peraltro, la somministrazione di immunoglobuline come previsto alle 28 settimane sarebbe stata efficace nell’evitare la successiva isoimmunizzazione.
In conclusione, la profilassi anti-D rappresenta uno dei più grandi successi della medicina perinatale, avendo trasformato una delle più gravi minacce per la salute del feto e del neonato in una condizione prevenibile. La continua aderenza alle linee guida e l'attenzione al monitoraggio sono essenziali per mantenere questi elevati standard di cura e assicurare gravidanze più sicure per le madri Rh-negative.
Approfondimenti e Prospettive Future nella Gestione dell'Incompatibilità Rh
L'evoluzione nella comprensione e nel trattamento dell'incompatibilità Rh ha radici profonde nella storia della medicina, e la profilassi anti-D ha rappresentato un salto qualitativo inimmaginabile rispetto alle pratiche del passato. Dalla scoperta del fattore Rh alle moderne tecniche diagnostiche e preventive, il percorso è stato costellato di scoperte che hanno salvato innumerevoli vite fetali e neonatali. L’isoimmunizzazione Rh materno-fetale, intesa come lo sviluppo di anticorpi contro antigeni del sistema Rh presenti sulla superficie dei globuli rossi che provoca incompatibilità materno-fetale causata dal passaggio, attraverso la placenta al feto, degli anticorpi anti-Rh materni, è un fenomeno che è stato progressivamente svelato e combattuto.
L'Evoluzione della Diagnosi:In passato, la diagnosi di rischio si basava quasi esclusivamente sulla determinazione del gruppo sanguigno materno e paterno e sul monitoraggio dei livelli anticorpali materni. Questi accertamenti, pur essendo fondamentali, non permettevano di determinare con certezza il gruppo sanguigno del feto senza ricorrere a procedure invasive come l'amniocentesi o la cordocentesi, che comportavano un certo rischio per la gravidanza. L'introduzione del test del DNA fetale libero (cell-free fetal DNA o cffDNA) nel sangue materno ha segnato una svolta. Questo test non invasivo prenatale (NIPT) permette di determinare il fenotipo Rh del feto tra la fine del primo e l’inizio del secondo trimestre di gravidanza con un semplice prelievo di sangue materno, riducendo la necessità di procedure invasive e fornendo informazioni cruciali per la gestione del rischio. Tale innovazione è raccomandata in gestanti Rh(D) negative con partner Rh(D) positivo, permettendo una personalizzazione della profilassi anti-D basata sulla certezza del gruppo sanguigno fetale.
L'Impatto della Profilassi Anti-D sulla Terapia:Prima dell'avvento della profilassi anti-D, le opzioni terapeutiche per la MEFN erano limitate e spesso estreme. L'exsanguinotrasfusione neonatale era una pratica relativamente comune, sebbene complessa e rischiosa. Questa procedura, che comporta la sostituzione quasi totale del sangue del neonato, era essenziale per rimuovere gli anticorpi materni e la bilirubina in eccesso, fornendo globuli rossi non attaccabili. Tuttavia, con la diffusione capillare della profilassi anti-D in gravidanza, l'incidenza di casi gravi di MEFN che richiedono exsanguinotrasfusione è crollata drasticamente. L'exsanguinotrasfusione per il trattamento della malattia emolitica del neonato è ormai rara, dopo l'introduzione della profilassi anti-D in gravidanza. Questo cambiamento radicale testimonia il successo straordinario della strategia preventiva.
Nonostante il successo, la necessità di trattamenti invasivi, come le trasfusioni intrauterine, persiste in una minoranza di casi in cui la sensibilizzazione si verifica nonostante la profilassi o in situazioni di sensibilizzazione preesistente. Queste procedure, che implicano l'iniezione di sangue Rh-negativo direttamente nel feto, sono altamente specializzate e richiedono competenze e strutture ad alto rischio. I feti più gravemente colpiti sviluppano una severa anemia in utero con morte fetale intrauterina oppure nascono con idrope fetale.
Sfide e Prospettive Future:Nonostante gli enormi progressi, la ricerca continua a esplorare nuove frontiere. Una delle sfide future è l'identificazione e la gestione delle incompatibilità causate da antigeni minori diversi da Rh e AB0. Sebbene meno comuni e spesso meno gravi, possono comunque causare problemi e non beneficiano di una profilassi standardizzata. La comprensione approfondita del ruolo di questi anticorpi, come anti-c, anti-E, e altri, è un campo di studio attivo. Il sistema immunitario della mamma rimane "sensibilizzato" nel tempo contro i globuli rossi del neonato con un gruppo sanguigno incompatibile e mantiene gli anticorpi.
Inoltre, l'ottimizzazione della somministrazione della profilassi anti-D, con studi che valutano dosaggi e tempistiche più personalizzati, rappresenta un'area di continuo miglioramento. La determinazione fetale non invasiva del genotipo Rh, che consente di evitare la somministrazione routinaria di anti-D a madri Rh-negative che portano un feto Rh-negativo, è un esempio di come la medicina stia evolvendo verso approcci sempre più mirati e meno invasivi. Ciò offre anche la possibilità di evitare un trattamento non necessario per la madre.
Il successo della lotta contro la MEFN è un esempio lampante di come la collaborazione tra enti, istituzioni, medici e governi, a livello nazionale e internazionale, possa portare a risultati straordinari nella salute pubblica. Come affermato da un osservatore del settore: «Quando abbiamo dato avvio al nostro impegno in quest’ambito non avevamo idea di quanto lontano ci avrebbe portato. In pochi anni si sono uniti enti ed istituzioni nazionali ed internazionali, medici, governi, ospedali, ONG.» Questo spirito di collaborazione è ciò che continua a guidare l'innovazione e il miglioramento nelle cure perinatali.
Sistema Rh e l'eritroblastosi fetale Zanichelli
tags: #eritroblastosi #fetale #profilassi #anti #d #ppt