La vita del feto è caratterizzata da alcune particolarità che la rendono profondamente differente dalla vita successiva dopo la nascita. Negli animali vivipari, la circolazione fetale è il sistema circolatorio di un feto, un meccanismo straordinariamente adattato per sostenere lo sviluppo in un ambiente intrauterino. Questa circolazione prenatale funziona diversamente dalla normale circolazione postnatale, soprattutto perché i polmoni non sono utilizzati come organi di scambio gassoso. Il suo corretto funzionamento è vitale per l'apporto di ossigeno e nutrienti essenziali, e la sua comprensione è fondamentale per diagnosticare e gestire le patologie che possono comprometterne l'efficienza, come il ritardo di crescita fetale e le malformazioni vasculo-linfatiche.
La Circolazione Fetale: Un Sistema Unico
Nel corso della vita embrionale e successivamente nella vita fetale le condizioni anatomiche della circolazione del sangue subiscono varie modificazioni. Si distinguono una prima circolazione, detta anche circolazione vitellina, che è transitoria e di breve durata, e si effettua fra cuore, vasi dell’embrione e vasi vitellini. Segue una seconda circolazione, conosciuta come circolazione placentare, che compare già nell’embrione ma si perfeziona nel feto con la formazione e lo sviluppo della placenta e che fa capo ai vasi ombelicali, ovvero arterie e vena ombelicali. Questa seconda circolazione rappresenta il dispositivo circolatorio proprio del periodo fetale e permane fino alla nascita.
Nel feto a termine il sistema circolatorio è costituito da un apparato cardiovascolare simile a quello dell’adulto, ma con alcuni adattamenti e dispositivi anatomici peculiari della circolazione fetale, e dai vasi specifici della circolazione placentare. La placenta, che ha la forma di un disco e la struttura interna simile a quella di una spugna, gioca un ruolo centrale come organo di scambio. Per mezzo delle arterie ombelicali giunge alla placenta il sangue fetale; questo circola nelle reti capillari dei villi coriali che pescano nel sangue arterioso materno degli spazi intervillosi, cede anidride carbonica e prodotti catabolici derivanti dal ricambio dell’organismo fetale e contemporaneamente assume materiali nutritizi e ossigeno.
Percorso del Sangue e Adattamenti Anatomici
Il sangue, divenuto così arterioso, torna dalla placenta al feto per mezzo della vena ombelicale. Quest'ultima, per i suoi peculiari caratteri di vaso fortemente propulsivo e pulsante, interviene attivamente nella circolazione di ritorno. Il sangue giunge al ramo sinistro della vena porta e, da qui, in parte passa direttamente nella vena cava inferiore mediante il condotto venoso dell’Aranzio, e in parte si immette, attraverso il ramo sinistro della vena porta, nel circolo epatico.
Nella vena cava inferiore, il sangue arterioso proveniente dalla placenta si mescola dunque con il sangue venoso refluo dalla parte sottodiaframmatica del corpo, divenendo così sangue misto, prevalentemente arterioso. Questo sangue giunge quindi all’atrio destro del cuore dove, per la presenza di una piega a semiluna chiamata valvola dell’Eustachio che si estende dal suo contorno inferiore fino al margine anteriore del forame ovale, si forma una corrente diretta verso il forame ovale. Attraverso questo forame, un’apertura tra l'atrio destro e quello sinistro, il sangue passa quasi totalmente dall’atrio destro nell’atrio sinistro. Da qui, il sangue discende nel ventricolo sinistro donde viene spinto nell’aorta. Pertanto, il sangue prevalentemente arterioso convogliato al cuore dalla vena cava inferiore evita il circolo polmonare e passa direttamente nella grande circolazione per essere avviato a tutti gli organi.
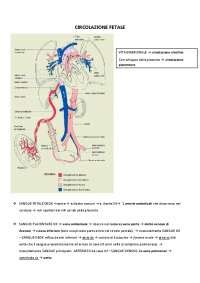
Una parte del sangue che entra nell'atrio destro, tuttavia, non passa direttamente all'atrio sinistro attraverso il forame ovale ma entra nel ventricolo destro e viene pompato nell'arteria polmonare. Il sangue venoso refluo dalla testa, dagli arti superiori e dalla parte sopradiaframmatica del tronco, che ritorna al cuore per mezzo della vena cava superiore, forma nell’atrio destro una corrente discendente in direzione dell’ostio atrioventricolare che incrocia la corrente sanguigna della vena cava inferiore senza mescolarvisi. Questo sangue discende nel ventricolo destro, si immette nel tronco polmonare e mentre in piccola quantità perviene ai polmoni attraverso le due arterie polmonari, in maggior parte, non essendo i polmoni ancora funzionanti, prende la via del condotto arterioso (del Botallo) e si riversa nell’aorta. Questa particolare connessione tra l'arteria polmonare e l'aorta, chiamata dotto arterioso di Botallo, devia la maggior parte del sangue lontano dal circolo polmonare. Le arterie ombelicali nascono dalle arterie iliache interne e, decorrendo prima sulla vescica quindi sulla superficie interna della parete anteriore dell’addome, raggiungono l’ombelico, lo attraversano, penetrano nel cordone ombelicale e con questo raggiungono la placenta dove si ramificano immettendosi nelle reti capillari dei villi coriali.
La Miscelazione del Sangue e le Sue Implicazioni
Tenendo presente che una porzione significativa del sangue che si riversa nell'aorta al di sotto dell’arco è quasi totalmente venoso, ne consegue che il sangue circolante nei rami che originano dall’aorta in questa parte del corpo è meno ricco di ossigeno e di metaboliti di quello trasportato dai rami che nascono dall’arco aortico. Il maggiore accrescimento che presentano nel feto la testa, gli arti superiori e la parte superiore del tronco, rispetto agli arti inferiori e alla parte inferiore del tronco, sarebbe da correlarsi con la differente costituzione del sangue che circola nell’aorta nella parte soprastante e in quella sottostante al condotto del Botallo. In ogni caso, nel feto non esiste quella netta separazione fra sangue venoso e sangue arterioso che è invece normalmente tipica della vita postnatale, ma gli organi sono sempre perfusi da sangue misto.
Dalla Nascita all'Adattamento: Le Trasformazioni Postnatali
Alla nascita, l’inizio della respirazione richiama ai polmoni una grande quantità di sangue che provoca un considerevole aumento di pressione nelle vene polmonari e quindi nell’atrio sinistro. Contemporaneamente, per l’obliterazione e la legatura dei vasi ombelicali, venendo a cessare la spinta impressa al sangue dalla vena ombelicale, cade la pressione nella vena cava inferiore e nell’atrio destro del cuore. Si determinano pertanto immediatamente alcuni importanti mutamenti funzionali del dispositivo circolatorio fetale che si rendono poi definitivi per successive trasformazioni anatomiche.
Si hanno, per i mutamenti di pressione instauratisi a livello degli atri, dapprima la chiusura funzionale e quindi anatomica del forame ovale per accollamento del setto primitivo (valvola del forame ovale) al setto secondario. Per il richiamo del sangue ai polmoni, si verifica l’esclusione, e quindi l’obliterazione del condotto arterioso del Botallo. Per la legatura della vena ombelicale, avviene l’esclusione del condotto venoso dell’Aranzio e la sua successiva obliterazione.
In ogni caso, la chiusura del forame ovale, del condotto arterioso e del condotto venoso, inizialmente funzionale, diviene poi anatomica tra il 30° e il 90° giorno di vita, per la trasformazione dei condotti in legamenti (legamento arterioso e legamento venoso) e per la coalescenza del lembo della fossa ovale con la parete atriale alla quale questo aderisce e si salda. La porzione intraaddominale della vena ombelicale, per un processo di obliterazione che si completa entro il 3° mese di vita, si trasforma nel legamento rotondo del fegato.
Il Ritardo di Crescita Fetale (FGR): Un'Analisi Approfondita
Il ritardo di crescita fetale, o FGR (Fetal Growth Restriction), è una condizione in cui il feto non raggiunge il proprio potenziale di crescita a causa di un fattore patologico, più comunemente la disfunzione placentare. I feti in cui si ha una vera restrizione della crescita in utero vengono definiti Feti FGR o IUGR (Intra Uterine Growth Restriction). Questi due termini sono utilizzati come sinonimi in letteratura, ma è utile considerare FGR la definizione che identifica l'incapacità del feto di raggiungere il proprio potenziale di crescita a causa di un fattore patologico. Si definisce ritardo di crescita una situazione in cui il peso fetale è inferiore al 10° percentile per l’epoca gestazionale. Naturalmente in questa definizione sono compresi anche i feti costituzionalmente piccoli, per esempio nati da genitori di bassa statura, i quali sono indicati come SGA (Small for Gestational Age). La prima sfida nel percorso diagnostico dei difetti di crescita fetali è proprio differenziare i Feti SGA (feti piccoli ma sani) dai Feti FGR (feti piccoli con vera restrizione della crescita) il cui benessere è in pericolo a causa di un ambiente intrauterino ostile.
Con il termine ritardo di crescita intrauterino si intende più precisamente una crescita fetale rallentata rispetto ai controlli precedenti. Nei feti piccoli con FGR, si verifica una riduzione degli scambi ossigenativi-metabolici con conseguente rischio di esito potenzialmente sfavorevole. L'importanza di questa patologia è infatti legata più che al basso peso del feto alla elevata morbilità e mortalità fetale e perinatale che ne consegue.
I Centili di Crescita e la Loro Interpretazione
Il concetto fondamentale è che il centile a cui appartiene un feto ha relativa importanza finché la crescita è regolare, cioè procede stabilmente sempre sulla stessa linea. Se prendiamo 100 feti di una certa epoca gestazionale, il feto al cinquantesimo centile è quel feto il cui peso è esattamente nella media (linea verde del grafico). Quinto centile vuol dire che di 100 feti di una certa epoca gestazionale, il 95% sono più grandi (linea rossa nel grafico). Novantacinquesimo centile vuol dire che di 100 feti, solo il 5% sono più grandi (linea nera nel grafico).
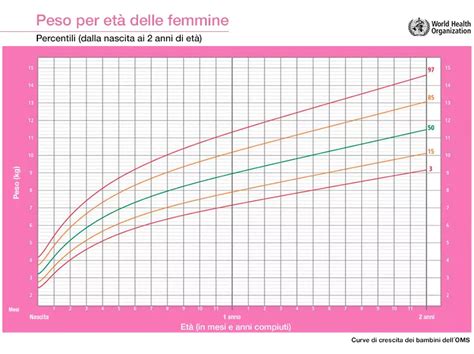
La valutazione della crescita fetale mediante l'uso di grafici consente di individuare quei feti che, deviando dalla curva, non raggiungono il loro potenziale di crescita. Normalmente si considera come ridotta velocità di crescita una deflessione di > 50° percentili della circonferenza addominale o del Peso Fetale Stimato (EFW) in esami ecografici consecutivi. Per esempio, un feto che parte dal cinquantesimo centile ma con il passare delle settimane rallenta la crescita, è indicativo di un problema, mentre un feto che si mantiene stabile sul quinto centile, con velocità di accrescimento conservata, pur essendo piccolo, potrebbe non presentare un vero ritardo di crescita patologico.
Ritardo di Crescita Simmetrico e Asimmetrico
La diagnosi di ritardo di crescita è esclusivamente ecografica. Nel caso in cui tutti i parametri biometrici (cranio, addome e femore) siano ridotti, parleremo di ritardo di crescita simmetrico. Questo tipo di ritardo di crescita precoce (da cause genetiche o cromosomiche) è tipicamente simmetrico. Nel caso in cui sia presente una marcata riduzione solo della circonferenza addominale (CA), saremo di fronte ad un ritardo di crescita asimmetrico. Nella maggior parte dei casi un ritardo di crescita tardivo (da cause placentari) risulta asimmetrico.
Questa distinzione è clinicamente rilevante. Nell’adulto succede che quando ci si mette a dieta la parte che “dimagrisce” è la pancia. Nel caso del feto, in condizioni di restrizione di crescita, i nutrienti vengono inviati preferenzialmente verso cuore e cervello, gli organi detti “nobili”, mentre i visceri addominali, in particolare il fegato, ricevono meno nutrienti. Questo meccanismo porta alla riduzione selettiva della circonferenza addominale.
Eziologia del Ritardo di Crescita Fetale
Le cause di ritardo di crescita sono molteplici ed in circa la metà dei casi non è presente un motivo ben identificabile. Le cause della restrizione della crescita fetale possono essere materne, placentari e fetali.
Insufficienza Placentare e Difetto di Placentazione
L’ipertensione gestazionale materna ed il ritardo di crescita fetale rappresentano diverse manifestazioni di una malattia comune: l’insufficienza placentare, a volte definita difetto di placentazione. Durante il proprio sviluppo la placenta invade la parete delle arterie materne che portano sangue all’utero trasformandole in vasi più grandi e meno rigidi in grado di aumentare l’apporto di ossigeno e nutrienti al feto. Quando questo processo non avviene correttamente, una placenta inadeguata alle necessità del feto determina ritardo di crescita. L’insufficienza vascolare placentare, inizialmente caratterizzata dall’aumento del PI dell'arteria ombelicale (UAPI), può peggiorare passando, nella fase terminale, da un flusso diastolico ridotto in arteria ombelicale (PED) ad un flusso assente (AED) o invertito (RED).
Cause Materne: Ipertensione e Preeclampsia
Sul versante materno, ad un iniziale tentativo di compenso con un aumento di pressione arteriosa per incrementare l’afflusso di nutrienti, può far seguito un danno vascolare non solo utero-placentare, ma multiorgano con sviluppo di gestosi o preeclampsia (ipertensione e proteinuria - proteine nelle urine- ) con rischi per la salute sia materna che fetale. Le gravidanze con FGR ad esordio precoce sono a più alto rischio di preeclampsia e morbilità e mortalità perinatali.
Cause Fetali: Anomalie Congenite e Infezioni
Circa il 10% dei feti FGR presenta anomalie congenite e dal 20 al 60% dei bambini malformati sono SGA. In presenza di un feto con restrizione della crescita bisogna eseguire un esame ecografico dettagliato comprendente anche una ecocardiografia fetale in caso di dubbi sulla normalità del cuore e, considerato il rischio di aneuploidie, è indicato anche un esame citogenetico prenatale, in particolare Array-CGH.
Varie infezioni possono essere associate a FGR, tra cui citomegalovirus, toxoplasmosi, rosolia, varicella, herpes simplex, sifilide, virus zika, e malaria (nelle zone endemiche). È interessante notare che il Covid 19 non sembra essere associato a una maggiore prevalenza di FGR. Tuttavia, una revisione sistematica e una meta-analisi di studi di qualità relativamente alta con gruppi di confronto appropriati hanno rilevato un aumento del rischio di preeclampsia, parto pretermine e natimortalità tra le persone in gravidanza con infezione da SARS-CoV-2 rispetto a quelle senza infezione da SARS-CoV-2. Tra le persone in gravidanza con COVID-19, la malattia grave è stata associata a preeclampsia, parto pretermine, diabete gestazionale e basso peso alla nascita rispetto a quelle con malattia lieve.
Insufficienza placentare
Diagnosi e Monitoraggio del Ritardo di Crescita Fetale
Il percorso diagnostico e di monitoraggio del FGR è complesso e si avvale di una combinazione di esami clinici e strumentali.
Valutazione Clinica e Datazione della Gravidanza
L’esame clinico è fondamentale per porre il sospetto: ad ogni visita il ginecologo esegue la palpazione dell’addome materno e la misura della distanza sinfisi-fondo (cioè la misura della lunghezza dell’utero) mediante un comune metro da sarta per avere un’idea della crescita fetale.
Fondamentale è essere in possesso di un’ecografia che dia una datazione precisa della gravidanza. Nel primo trimestre (tra 7 e 13 sett. + 6 gg.) il parametro biometrico più attendibile per la stima dell'epoca gestazionale è la misurazione della lunghezza vertice-sacro (CRL). Se vi è una discrepanza di 7 giorni o più tra età gestazionale anamnestica (in base all'ultima mestruazione LMP) ed età gestazionale ecografica (basata sulla misura del CRL) bisogna ridatare l'epoca gestazionale. La ridatazione dell'epoca gestazionale quando vi è discordanza LMP/CRL si effettua se viene confermata la normale crescita dell'embrione su due esami ecografici a distanza di due settimane e si può formulare diagnosi di difetto di crescita solo quando nel successivo controllo ecografico il CRL corrisponde ad una età gestazionale di almeno 5-7 giorni in meno. Nel II trimestre (da 14 + 0 a 27+ 6 settimane), in genere a > 24 settimane di gestazione, l'epoca gestazionale e nello specifico il peso fetale stimato (EFW) viene calcolato col nomogramma della formula di Hadlock che utilizza le misurazioni ecografiche del diametro biparietale (BPD), circonferenza cranica (HC), circonferenza addominale (AC) e lunghezza del femore (FL). In base alla corretta datazione può essere definito ritardo di crescita una biometria inferiore al 10° centile per epoca gestazionale.
L'Ecografia nella Diagnosi di FGR
Lo screening per la diagnosi di FGR prevede la valutazione della crescita fetale, con una circonferenza addominale (CA) o un peso fetale stimato (EFW) inferiore al 10° percentile. Allo stato attuale è ritenuto dai vari Autori che una circonferenza addominale inferiore al 10° percentile per l'epoca gestazionale è il parametro più sensibile per l'individuazione dei feti SGA/FGR. Il range di normalità è quello compreso tra il 10° e il 90° percentile per una data epoca gestazionale.
Valutazione della Quantità di Liquido Amniotico
La valutazione della quantità di liquido amniotico è di aiuto nella diagnosi di FGR. L'oligoidramnios, cioè la diminuzione del liquido amniotico, è presumibilmente dovuto alla diminuzione della minzione fetale come conseguenza della ridistribuzione del flusso sanguigno dai reni verso organi più sensibili all'ipossiemia fetale come encefalo e cuore. L'oligoidramnios è uno dei segni distintivi nella diagnosi di FGR ed è associato a un esito negativo quando l'EFW è <3° percentile per l'età gestazionale. Il polidramnios, al contrario, aumenta il rischio di aneuploidia (in particolare trisomia 18) e di sindromi genetiche. In questi casi è consigliabile una consulenza genetica e l'Array-CGH.
La Velocimetria Doppler: Uno Strumento Essenziale
La velocimetria Doppler (o Doppler-flussimetria - DF) consente di valutare la funzione utero-placentare e la risposta fetale all'ipossia attraverso lo studio dei flussi in diverse arterie e vasi specifici. La continua evoluzione delle conoscenze fisiopatologiche e la sempre maggiore applicazione della velocimetria Doppler nello studio della restrizione della crescita fetale sono oggetto di confronto scientifico e le raccomandazioni che ne conseguono sul loro utilizzo sono anch'esse in rapida evoluzione.
Arterie Uterine
La flussimetria delle arterie uterine ha validità prevalente tra la 20a e la 24a settimana di gestazione. Nel primo trimestre di gravidanza, quando le arterie spirali invadono il trofoblasto, le arterie uterine passano da vasi ad alta resistenza a vasi a bassa resistenza con conseguente aumento del flusso sanguigno; ciò permette di stabilire un flusso a bassa resistenza adeguato alla perfusione della placenta. Se questo processo, che si completa intorno alla 20° settimana di gestazione, non si verifica normalmente, la mancata trasformazione delle arterie uterine da vasi ad alta resistenza in vasi a bassa resistenza condiziona una inadeguata invasione trofoblastica delle arterie spirali con conseguente circolazione ad alta resistenza ed aumento del PI (Indice di Pulsatilità) nelle arterie uterine.
Come ogni onda flussimetrica arteriosa, anche questa presenta una fase di maggiore flusso durante la contrazione ventricolare (flusso sistolico) ed una fase di flusso a velocità ridotta durante il rilasciamento ventricolare (flusso diastolico). Nel caso di una placenta correttamente sviluppata le arterie uterine presenteranno un flusso adeguato anche durante la diastole, mentre nel caso di insufficienza placentare la differenza tra flusso sistolico e flusso diastolico sarà maggiore e potrà essere presente un’incisura nel flusso all’inizio della diastole, chiamato notch. PI e RI sono degli indici che esprimono numericamente il rapporto tra flusso sistolico e diastolico. In presenza di un difetto di crescita la persistenza di un PI medio delle arterie uterine elevato (PI medio > 95° percentile per epoca gestazionale) è associata a insufficienza placentare. L’aumento del PI nelle arterie uterine provoca un aumento delle resistenze nella vascolarizzazione placentare con conseguente riduzione della superficie placentare disponibile per lo scambio di ossigeno e nutrienti. Naturalmente la presenza di arterie uterine alterate non significa presenza di malattia, solo maggiore probabilità di sviluppare ritardo di crescita o pre-eclampsia. Più precisamente la presenza di arterie uterine normali a 24 settimane indica che in meno dell’1% dei casi la gestante svilupperà preeclampsia o ritardo di crescita. La eventuale successiva normalizzazione degli indici di velocità di flusso risulterà ancora associata ad un aumentato rischio di neonato FGR.
Arteria Ombelicale
La flussimetria dell’arteria ombelicale rappresenta lo strumento più efficace per individuare tra i feti con ritardo di crescita quelli a maggior rischio di sviluppare ipossia (=ridotto apporto di ossigeno). Anche per l’arteria ombelicale, come per le arterie uterine, si valutano degli indici flussimetrici detti P.I. e R.I.: il flusso nell’arteria ombelicale è correlato al corretto sviluppo placentare sul versante fetale, cioè ci dice come funziona la placenta. L'aumento del PI nelle arterie uterine è seguito da un progressivo aumento del PI nelle arterie ombelicali (UAPI).
Nel feto, il primo cambiamento emodinamico è una riduzione del flusso venoso ombelicale con conseguente ridistribuzione del flusso venoso dal fegato al cuore fetale; le dimensioni del fegato diminuiscono causando un ritardo di crescita della circonferenza addominale fetale che è il primo segno biometrico di Feto FGR. Il flusso diastolico invertito (reverse-flow) in arteria ombelicale rappresenta una condizione particolarmente a rischio di morte in utero e come tale deve essere gestita. L’insufficienza vascolare placentare può peggiorare passando, nella fase terminale, da un flusso diastolico ridotto in arteria ombelicale (PED) ad un flusso assente (AED) o invertito (RED). La velocimetria Doppler dell'arteria ombelicale non è raccomandata per lo screening della popolazione generale mentre è raccomandata nella popolazione ad alto rischio per l'identificazione dei ritardi di crescita e per il monitoraggio delle gravidanze complicate da ritardo di crescita. Le Linee Guida del RCOG, SOGC e CNOGF raccomandano l'esecuzione della velocimetria Doppler dell'arteria ombelicale quale modalità primaria di monitoraggio delle gravidanze complicate da ritardo di crescita intrauterino in quanto in grado di ridurre la morbilità perinatale e anche al fine di valutare la necessità di anticipazione del parto.
In un recentissimo studio effettuato su una popolazione con sospetta restrizione della crescita fetale, sono state messe a confronto l'emodinamica materna e fetale. Nei feti con restrizione della crescita è stata riscontrata una correlazione tra emodinamica materna e fetale in particolare il profilo emodinamico materno con elevata resistenza vascolare sistemica, bassa gittata cardiaca, ridotto inotropismo e circolazione ipodinamica è stato correlato con un ridotto flusso della vena ombelicale e un aumento dell'indice di pulsatilità dell'arteria ombelicale.
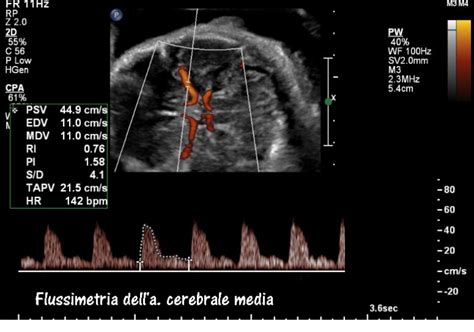
Arteria Cerebrale Media
Nelle fasi avanzate dell'insufficienza vascolare placentare il feto attua dei meccanismi di compenso all'ipossiemia con modifiche emodinamiche che interessano le arterie cerebrali, il dotto venoso e altri distretti vascolari. Il flusso nelle arterie cerebrali medie è un flusso ad alta resistenza con valori medi del PI di 1,5-1,6 ± 0,2 DS durante il terzo trimestre di gravidanza. In caso di ritardo di crescita il feto ridistribuisce il flusso di sangue verso quegli organi che necessitano maggiormente di ossigeno e nutrienti per svilupparsi correttamente, come il cuore ed il sistema nervoso centrale. Tale processo è chiamato centralizzazione del circolo. Per questo motivo si assiste ad una dilatazione dell’arteria cerebrale media con aumento del flusso diastolico al fine di aumentare l’apporto di ossigeno e nutrienti. Da un punto di vista clinico la modificazione dell’arteria cerebrale media dimostra che il feto sta cercando di compensare il ridotto apporto di ossigeno. Le arterie cerebrali, come risposta emodinamica all'ipossia fetale, vanno incontro a vasodilatazione (Brain Sparing Effect) che alla velocimetria Doppler si evidenzia come diminuzione dell'indice di pulsatilità neli'arteria cerebrale media (MCA-PI); tale meccanismo di compenso, che si realizza mediante il rilevamento della tensione di ossigeno nei vasi cerebrali, si innesca anche in altri letti vascolari come le arterie coronarie e le ghiandole surrenali. In risposta all'ipossia il surrene fetale produce catecolamine che agiscono sulle arteriole precapillari provocando vasodilatazione dei distretti coronarico e cerebrale (Brain Sparing Effect) e vasocostrizione nei distretti cutaneo, splancnico e polmonare.
Dotto Venoso
Il dotto venoso è un vaso che porta il sangue proveniente dalla placenta ricco di ossigeno e nutrienti verso l'atrio destro del cuore fetale. Come tutti i vasi venosi, esso presenta un flusso in direzione del cuore che in condizioni di normalità mantiene tale direzione durante tutto il ciclo cardiaco. In caso di ipossia fetale la stimolazione dei chemocettori per la PO2 e la PCO2 presenti nell’istmo provoca la progressiva dilatazione del dotto venoso al fine di aumentare il flusso sanguigno verso il cuore. Col perdurare dell'ipossia il cuore va incontro allo scompenso, aumenta la pressione in atrio destro per l'elevato postcarico cardiaco conseguente all’aumento della resistenza vascolare placentare e di conseguenza rallenta il passaggio di sangue nel dotto venoso con progressivo aumento della pulsatilità fino alla assenza ed inversione dell'onda "a".
Da un punto di vista clinico questa valutazione è molto importante perché in caso di arteria ombelicale patologica (flusso diastolico assente o invertito) un’onda "a" normale nel dotto venoso conferma un quadro di compenso fetale, mentre un’onda "a" assente o invertita mostra lo scompenso fetale (riduzione critica dei livelli di ossigeno). Il dotto venoso è l’ultimo parametro che si altera nel ritardo di crescita. Un dotto venoso alterato è una condizione di altissimo rischio di esito avverso (morte in utero o dopo la nascita). Fortunatamente, nella maggior parte dei casi abbiamo la possibilità di identificare le situazioni maggiormente a rischio ben prima di arrivare al dotto venoso alterato, che è un quadro che si osserva molto raramente.
Aorta Fetale
L'indice di pulsatilità (PI) in aorta è anch’esso correlato alla prognosi fetale. Il flusso in aorta, dopo la 20a settimana di gestazione, è caratteristicamente un flusso ad alta resistenza con valori di P.I. attestati intorno a 2,0. Il flusso aortico viene studiato valutando la fase telediastolica EDF (end diastolic flow): in condizioni patologiche la EDF può scomparire (EDF 0) o essere negativa (EDF -). In presenza di una condizione di ipossia cronica con iposviluppo asimmetrico del feto si ha un aumento del P.I.
Rapporto Cerebro-Placentare (CPR)
Nella diagnostica dei feti FGR ad esordio tardivo può essere utilizzato anche il rapporto cerebro/placentare (CPR) che viene calcolato dividendo gli indici di pulsatilità o resistenza dell'arteria cerebrale media per quelli dell'arteria ombelicale (CPR= MCAPI/UAPI). Sono stati proposti diversi valori soglia di CPR per predire l'esito avverso (<1, <1,05, ≤1,08, <5° percentile); un CPR basso indica una ridistribuzione del flusso sanguigno fetale (brain sparing). Nella FGR ad esordio tardivo, la riduzione del CPR può essere l'unico cambiamento Doppler presente. Studi più recenti sembrano però dimostrare che il CPR non aggiunge alcun valore predittivo per l'esito perinatale avverso rispetto ai flussi in arteria ombelicale.
È stato osservato che alcuni Feti SGA con Doppler-flussimetria feto-placentare normale vanno comunque incontro a problemi placentari come invecchiamento e fenomeni di ipovascolarizzazione, alterato flusso nella vena ombelicale, alterata emodinamica materna, sofferenza fetale e maggiore incidenza di taglio cesareo rispetto ai Feti AGA (Appropriate for Gestational Age). In questi casi è stato ipotizzato l'esistenza di un sottogruppo di feti SGA che soffrono di una crescita "stentata" e si adattano ad un ambiente nutrizionale povero.
L'utilizzo di Biomarcatori nello screening di feti FGR, allo stato, non pare dia risultati migliori rispetto all'imaging ecografico. Tra i più studiati vi sono fattori placentari come la proteina plasmatica A (PAPP-A) e il rapporto sFlt-1/PIGF (tirosin-chinasi-1/fattore di crescita placentare).
Strategie di Gestione e Tempistica del Parto
La scelta del momento del parto di un feto affetto da ritardo di crescita rappresenta una delle sfide dell’ostetricia moderna. Da una parte dobbiamo evitare di far nascere un bambino troppo presto aggiungendo al ritardo di crescita i problemi della prematurità, dall’altra non dobbiamo mantenere troppo a lungo un feto piccolo in un ambiente intrauterino che non è più in grado di ossigenarlo e nutrirlo sufficientemente.
La scelta del parto dipenderà quindi dall’epoca gestazionale, dalla gravità del ritardo di crescita e dal grado di compenso fetale. È necessario quindi monitorare tutti i parametri che abbiamo a disposizione: stima del peso, quantità di liquido amniotico, flussimetria fetale, epoca gestazionale e maturità polmonare. Può essere utilizzata anche la cardiotocografia che tramite la valutazione della frequenza cardiaca fetale è in grado di determinare il grado di ossigenazione fetale. Nel caso in cui il ritardo di crescita sia associato ad ipertensione e preeclampsia, anche le condizioni materne devono essere prese in considerazione nella scelta corretta del momento del parto.
L'Igroma Cistico: Un'Anomalia Vasculo-Linfatica
L’igroma cistico è un quadro malformativo del collo fetale costituito da un’ectasia cistica dei vasi linfatici latero-cervicali e cervico-dorsali dovuto a un alterato deflusso paravenoso dal complesso linfatico latero-cervicale a quello giugulare e da questo al dotto toracico. È una patologia che maggiormente sembra associarsi alla diagnosi ecografica di patologia linfatica del collo.
Caratteristiche Ecografiche e Forme
Per la diagnosi sono utilizzate sia la scansione assiale del collo, che quella sagittale mediana dell’estremo cefalico, possibilmente anche con approccio dorsale: in questo modo sarà possibile valutare l’estensione cranio-caudale e laterale della massa e differenziare l’igroma non settato da quello settato. La differenziazione principale riguarda la presenza o meno di setti: alcune forme non settate, specialmente se non associate ad aneuploidie né a idrope, possono regredire nel corso della gestazione o alla nascita con un outcome neonatale normale.
Associazioni Patologiche e Genetiche
Tra i segni ecografici rilevanti e patognomonici, l'igroma (soprattutto non settato) si associa alla presenza di cardiomiopatia ipertrofica, difetti interatriali e/o interventricolari ma soprattutto stenosi polmonare, che sembra essere il marker complicativo, talvolta letale, del quadro sindromico. Etiologicamente le cause cardiache sono le più frequenti (20-30% dei casi), anche se le cause cromosomiche sono prevalenti nel I trimestre. Le anomalie più frequentemente riscontrate sono la sindrome di Turner (45, X) e le tre trisomie autosomiche (trisomia 21, 18 e 13) oltre ad un’ampia gamma di arrangiamenti cromosomici rari (delezioni e traslocazioni sbilanciate).
Approccio Diagnostico e Counseling per l'Igroma Cistico
La gestione dell'igroma cistico prevede, per prima cosa, un accurato inquadramento diagnostico.
Ecocardiografia Fetale
È fondamentale eseguire un'ecocardiografia fetale alla ricerca di cardiopatie funzionali e strutturali, permettendo la diagnosi precoce delle maggiori cardiopatie congenite, anch’esse cinque volte più frequenti nella popolazione di feti affetti da igroma cistico rispetto alla popolazione generale. L’ecocardiografia fetale ha inoltre l’importante compito, in caso di non settazione dell’igroma, di identificare precocemente la stenosi polmonare, la cardiomiopatia ipertrofica e i difetti settali patognomonici della Sindrome di Noonan.
Analisi del Cariotipo
Dato l'elevato rischio di aneuploidia, che risulta sei volte maggiore rispetto alla popolazione generale, è indicata l'analisi del cariotipo, ottenibile mediante villocentesi o amniocentesi o prelievo materno per la valutazione del DNA fetale.
L'Importanza del Counseling Multidisciplinare
Una volta posta la diagnosi di certezza, la coppia (ovvero la paziente e talvolta il partner) ha il diritto di ricevere un counseling diagnostico-prognostico al fine di precisare i punti chiave della gestione ostetrica del caso, l’associazione con patologie malformative eventualmente presenti, con cromosomopatie e patologie cardiologiche fetali, e infine per illustrare l’eventualità di regressione in utero della patologia del feto, specialmente se la forma era isolata. Così è stata proposta la possibilità di precisazione diagnostica mediante accertamento del cariotipo (amniocentesi) ed ecocardiografia fetale e, in buona parte dei casi, quando questo era indicato, mediante il colloquio con un chirurgo pediatrico.
Studi Retrospettivi e Follow-up
Uno studio retrospettivo condotto sulla casistica di pazienti afferenti all’Hospice Perinatale - Centro per le Cure Palliative Prenatali, al Day Hospital (DH) di Ostetricia del Polo Salute della Donna e del Bambino - Policlinico “Agostino Gemelli” di Roma tra il maggio 1985 e il dicembre 2012, si è proposto di precisare il counseling fornito alla paziente in gravidanza a cui viene riscontrata la patologia fetale igroma cistico. Questo al fine di contenere il dubbio diagnostico e di ricercare elementi prognostici utili alla consulenza ostetrica.
237 pazienti con una diagnosi di sospetta malformazione vasculo-linfatica del collo fetale sono state valutate mediante ecografie ostetriche seriate effettuate ogni tre settimane di gravidanza. Gli studi ultrasonografici sono stati eseguiti mediante Technos MP ESAOTE High Definition System e VOLUSON E8 usando sonde trans-addominali a 3,5 MHz e sonde trans-vaginali. Il follow-up ostetrico è stato ottenuto mediante ripetute interviste telefoniche alle pazienti e mediante l’utilizzo del Sistema Informatico del Policlinico “A. Gemelli”.
Il test di Mann-Whitney è stato compiuto per valutare l’associazione tra l’esito neonatale e l’età materna, la dimensione dell’NT e dell’igroma (diametro massimo prima e ultima misurazione) e le dimensioni dell’ascite. I neonati vivi, figli delle madri sottoposte ai predetti controlli presso il DH di Ostetricia, sono stati valutati in collaborazione con i colleghi Neuropsichiatri infantili del Dipartimento per la Tutela della Salute della Donna e della Vita Nascente, del Neonato e dell’adolescente, i quali hanno visitato i pazienti e hanno somministrato loro specifici questionari scientificamente validati al fine di valutare il grado di rilevanza degli aspetti neurocognitivi e psicomotori della patologia igroma cistico sui bambini (casistica fino ai 26 anni di età) le cui madri avevano ricevuto tale diagnosi in gravidanza. A tutti i genitori dei bambini/adolescenti/adulti con riscontro ecografico di igroma in gravidanza è stata somministrata durante un’intervista il test Vineland Adaptive Behavior Scales in forma completa per valutare la percezione dei genitori rispetto alle competenze adattive dei rispettivi figli. Nei bambini di età compresa tra 4 e i 6 anni è stato somministrato il test delle matrici progressive colorate di Raven.