La medicina fetale, come raccontato dal ginecologo e ostetrico Giancarlo di Renzo nel suo libro “Il mio paziente non è ancora nato”, ha segnato la nascita di una nuova era, definita da lui stesso come uno “shock culturale”. Se in passato il feto era sovente considerato quasi esclusivamente un’appendice della madre, oggi la comprensione scientifica ha evoluto, e qualunque medico sa che durante la gravidanza i pazienti sono almeno due, con esigenze e condizioni distinte. Questa consapevolezza ha spinto la ricerca verso orizzonti inediti, focalizzandosi sullo sviluppo e sulla cura del feto prima della nascita. Al centro di molte di queste innovazioni vi sono le cellule staminali, entità biologiche con la straordinaria capacità di auto-rinnovarsi e di differenziarsi in vari tipi cellulari, offrendo prospettive rivoluzionarie in ambito diagnostico e terapeutico.
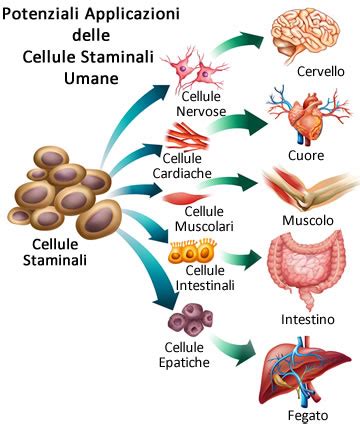
Le possibili fonti di cellule staminali sono molteplici, ciascuna con le proprie caratteristiche e implicazioni. Tra queste, quelle provenienti dagli embrioni sono attualmente considerate le più flessibili per la loro pluripotenza, ovvero la capacità di dare origine a qualsiasi tipo cellulare dell'organismo. Tali cellule vengono generalmente prelevate da embrioni prematuri, spesso "in eccesso" rispetto alle esigenze delle cliniche della fertilità che supportano le coppie nel percorso di procreazione assistita. Esiste anche la possibilità, almeno teoricamente, di ottenere embrioni attraverso la clonazione delle cellule di un paziente, un processo noto come clonazione terapeutica che non implica la crescita dell'embrione fino allo stadio di impianto nell'utero materno. Parallelamente, le cellule staminali possono essere prelevate dai feti abortiti, oppure, sebbene con maggiore difficoltà e con una minore versatilità dovuta a una parziale differenziazione, dal sangue e da vari tessuti di esseri umani adulti. L'utilizzo di cellule staminali prelevate dagli adulti, a differenza di quelle embrionali, non ha finora incontrato particolari opposizioni di natura etica, e numerosi ricercatori stanno attivamente lavorando per svilupparne le applicazioni, sebbene la loro utilità effettiva sia ancora oggetto di studio e non pienamente definita.
Organoidi Fetali: Una Nuova Frontiera dalla Ricerca Italo-Britannica
Nel panorama della medicina fetale, un progresso significativo è stato raggiunto attraverso la capacità di riprodurre una miniatura degli organi fetali, i cosiddetti organoidi, a partire da cellule staminali. Questa metodologia, che non comporta rischi né per il feto né per la madre, è stata brillantemente sviluppata da un team di ricerca italo-britannico. La squadra, guidata dal prof. Paolo De Coppi, affiliato al Great Ormond Street Institute of Child Health (GOS ICH) presso l’University College di Londra, ha pubblicato il suo innovativo studio sulla prestigiosa rivista Nature Medicine, un risultato che ha suscitato un notevole interesse nella comunità scientifica.
Per creare gli organoidi, i ricercatori hanno diverse opzioni. Possono partire da cellule staminali embrionali, che per la loro natura pluripotente sono in grado di dare origine a qualsiasi tipo cellulare. In alternativa, possono utilizzare biopsie di tessuti adulti; in questo secondo scenario, le cellule mature vengono "riportate indietro nel tempo" allo stadio di cellule staminali pluripotenti, attraverso un processo di riprogrammazione, per poi essere nuovamente indotte a differenziarsi nel tipo cellulare desiderato. I risultati ottenuti con queste tecniche si sono rivelati particolarmente rivoluzionari per lo studio e la modellizzazione di tessuti complessi come il cervello, la retina e il cuore.
Un'applicazione cruciale di questa tecnologia è la creazione di organoidi fetali. Questi modelli in miniatura consentono di studiare in profondità lo sviluppo del feto e, soprattutto, l’insorgenza di difetti congeniti. Queste condizioni rappresentano una sfida medica di vasta portata, poiché riguardano circa il 5-6% di tutti i nati. Sebbene individualmente possano essere considerate rare o molto rare, nel loro insieme interessano una popolazione significativa: si stima che 8 milioni di bambini ogni anno in tutto il mondo siano colpiti da difetti congeniti, con una stima di oltre 20.000-25.000 casi in Italia.
Il principale ostacolo nella realizzazione di organoidi a partire da cellule fetali risiede nella loro difficile reperibilità, una problematica che è spesso intrecciata con complesse questioni etiche e legali. Tuttavia, esiste un’alternativa promettente che i ricercatori conoscono da decenni: il liquido amniotico. Questa sostanza, che circonda e protegge il feto nell’utero, contiene naturalmente cellule fetali. Tale principio è alla base di pratiche diagnostiche consolidate come l’amniocentesi, utilizzata per accertare la presenza di eventuali anomalie congenite, quali la sindrome di Down, o malattie genetiche specifiche, come l’anemia falciforme o la fibrosi cistica.
Tuttavia, è fondamentale notare che la stragrande maggioranza delle cellule presenti nel liquido amniotico, circa il 95% o più, sono cellule morte eliminate dal feto. Una frazione molto più piccola e dalla composizione ancora incerta è invece rappresentata da cellule vive. Tra queste, una parte è costituita da cellule progenitrici, un tipo specifico di cellule staminali note anche come “multipotenti”. A differenza delle cellule pluripotenti, le multipotenti possono differenziare solo in un tipo cellulare specifico o in un numero limitato di tipi cellulari. Quelle presenti nel liquido amniotico, in particolare, sono del tipo epiteliale, il che significa che possono dare origine unicamente allo strato più esterno che riveste la superficie degli organi.
Il team di ricerca italo-britannico ha sfruttato proprio queste cellule progenitrici epiteliali ottenute dal liquido amniotico. Le cellule sono state prelevate da 12 gravidanze in un arco temporale che andava dalla 16esima alla 34esima settimana di gestazione. È importante sottolineare che il prelievo è avvenuto in occasione di esami programmati per le operazioni di screening e di diagnosi prenatale, garantendo l'assenza di qualsiasi danno per il feto o per la madre. Questo approccio innovativo offre numerosi vantaggi, tra cui la possibilità di realizzare organoidi da gravidanze ancora in corso. Nel giro di sole 4-6 settimane, i ricercatori possono generare l’organoide e utilizzarlo per testare farmaci o sviluppare terapie personalizzate specificamente per il feto. Un ulteriore vantaggio risiede nel fatto che le cellule progenitrici sono naturalmente programmate per differenziarsi in un tipo cellulare specifico: immerse in un gel di coltura adatto, nel giro di poche settimane, esse esprimono spontaneamente il loro potenziale, senza la necessità di ulteriori manipolazioni o complesse riprogrammazioni.
Organoidi simulano cervello, così scienziata italiana sfida malattie
Una delle applicazioni più significative esplorate nello studio è stata la ricreazione di un modello di malattia fetale. Mentre molti difetti congeniti possono essere scoperti e monitorati attraverso tecniche di imaging sempre più sofisticate, gli organoidi offrono la capacità di fornire informazioni aggiuntive e più dettagliate sulla severità della patologia e sulla funzionalità degli organi colpiti. In un esempio concreto, i ricercatori hanno ricreato un modello di ernia diaframmatica congenita (CDH). Questa condizione è un difetto embrionale caratterizzato da uno sviluppo incompleto o dal mancato sviluppo del diaframma, il che comporta che gli organi addominali premano contro la cavità toracica, comprimendo i polmoni e spostando il cuore.
Per comprendere meglio questa patologia, i ricercatori hanno creato organoidi polmonari sia da cellule di feti affetti da CDH sia da feti "sani" per un confronto. Inizialmente, i due tipi di organoidi apparivano identici, ma durante il loro sviluppo in coltura, sono emerse chiare differenze: gli organoidi derivati da feti con CDH producevano una quantità inferiore di surfattante, una sostanza fondamentale per la corretta funzionalità respiratoria, e mostravano una crescita e una differenziazione cellulare irregolare. La condizione di CDH è curabile attraverso una procedura che prevede l'inserimento di un palloncino nella trachea del feto, il quale respinge gli organi addominali nella loro posizione corretta, decomprimendo i polmoni. L'obiettivo finale di questa ricerca è "accedere al feto senza toccare il feto". Il modello di CDH, ad esempio, può fornire indicazioni preziose per capire lo stato reale dei polmoni, valutare l'effettiva necessità di un intervento chirurgico e persino monitorare l'efficacia della terapia una volta somministrata. È importante, tuttavia, evidenziare un limite attuale della tecnologia: essa permette di creare organoidi solo a partire dalle cellule epiteliali rilasciate nel liquido amniotico. Ciò significa che rimangono al di fuori delle attuali capacità di modellizzazione alcuni organi fondamentali, come il cuore o il cervello, e i difetti congeniti che colpiscono altri tipi cellulari, come quelle mesenchimali.
Terapia Genica Fetale: La Promessa dell'"Autoterapia"
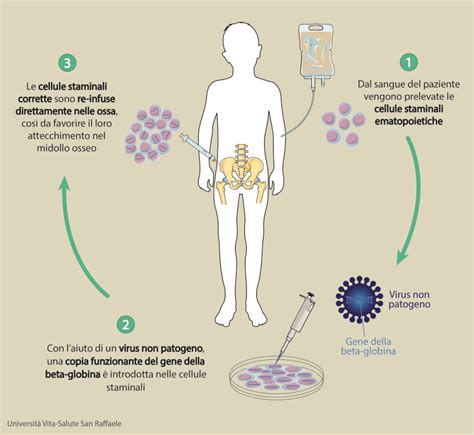
Il sangue fetale, così come il liquido amniotico, contiene cellule staminali. Questa consapevolezza apre la strada a nuove frontiere terapeutiche, in particolare nel campo della terapia genica. Queste cellule possono essere prelevate e, in un ambiente controllato, trattate geneticamente per mezzo di un virus vettore appositamente modificato per trasportare un particolare gene terapeutico. Dopo questo trattamento, le cellule non solo conservano le loro caratteristiche fondamentali, come la capacità di replicarsi in grande quantità e di differenziarsi in altri tipi di cellule, ma mantengono anche il gene inizialmente introdotto. Questo scenario paventa la possibilità di realizzare una delle grandi attese della medicina moderna: la terapia genica fetale, in una modalità che potrebbe essere definita di “autoterapia”. Tale approccio avrebbe il vantaggio cruciale di prevenire un possibile rigetto delle cellule infuse, poiché esse deriverebbero dallo stesso organismo del ricevente. In tal modo, un feto diagnosticato con una malattia genetica potrebbe potenzialmente essere curato prima ancora di nascere.
Un esperimento pionieristico in questa direzione ha coinvolto il prelievo di una piccolissima quantità di sangue fetale da un feto alla decima settimana di sviluppo, in una gravidanza che, per ragioni cliniche, sarebbe stata comunque interrotta. Trattando questo sangue con speciali fattori di crescita in laboratorio, i ricercatori sono riusciti ad ottenere cellule staminali. Queste cellule si presentavano con le stesse caratteristiche di quelle che si trovano nel sangue dell’adulto o nel midollo osseo e sono note come MSC, ovvero Cellule Staminali Mesenchimali. Successivamente, nelle MSC ricavate dal feto, è stato introdotto un virus contenente un certo gene, artificialmente inserito nel DNA del virus stesso.
Immaginando di trasferire in pratica i risultati di questo esperimento e di applicarli a una malattia come la fibrosi cistica, si potrebbe ipotizzare uno scenario terapeutico rivoluzionario. Si potrebbero creare in laboratorio una popolazione di cellule staminali prelevate direttamente da un feto malato, correggerle geneticamente utilizzando un vettore virale per inserire il gene sano, e poi indurle a evolvere in cellule dell’epitelio respiratorio, il tessuto colpito dalla fibrosi cistica. A quel punto, queste cellule geneticamente corrette potrebbero essere trasfuse nel feto ancora in uno stadio molto precoce della gravidanza, idealmente alla fine del primo trimestre o all'inizio del secondo. Questa metodologia è stata delineata in studi come quello di Chan Jerry et al. intitolato “Human Fetal Mesenchymal Stem Cells as Vehicles for Gene Delivery”, evidenziando il potenziale delle MSC fetali come veicoli per la consegna genica, con tutte le cautele legate al fatto che le affermazioni espresse in tali articoli sono unicamente quelle degli autori.
Cellule Fetali e Malattie Neurodegenerative: Il Caso Parkinson
Oltre agli organoidi e alla terapia genica, le cellule fetali hanno dimostrato un potenziale anche nel trattamento di malattie neurodegenerative. Ricercatori dell'Università di Cambridge, in una intervista rilasciata alla rivista New Scientist, hanno dichiarato di aver trapiantato cellule fetali di origine umana, specificamente derivate da feti abortiti, in un paziente affetto da malattia di Parkinson. Questo approccio non è del tutto nuovo; gli stessi ricercatori hanno ricordato che sperimentazioni simili con le cellule fetali erano già state effettuate negli anni '90.
All'epoca, tuttavia, la metodica era stata dichiarata inefficace, portando a una pausa nella ricerca in questo campo specifico. Ora, la prospettiva è cambiata, e i ricercatori di Cambridge ritengono che questa metodologia debba essere rivalutata. Il motivo di tale rivalutazione risiede nelle nuove scoperte: nel frattempo, è stato documentato che le cellule fetali impiegano diversi anni a sviluppare connessioni nervose complete e ad inserirsi pienamente nei circuiti nervosi esistenti. Questa comprensione del lungo processo di integrazione cellulare potrebbe spiegare l'apparente insuccesso delle sperimentazioni precedenti e suggerisce che risultati positivi potrebbero manifestarsi solo a lungo termine, aprendo nuove speranze per il trattamento di condizioni neurologiche complesse.
La Complessità Etica nell'Utilizzo delle Cellule da Feti Abortiti
L'utilizzo di cellule staminali, in particolare quelle derivanti da feti abortiti o da embrioni, solleva complesse questioni etiche che hanno generato un acceso dibattito e che continuano a dividere esperti e la società su posizioni spesso inconciliabili. Figure di spicco nel campo della bioetica, come D'Agostino ed Elio Sgreccia, hanno contribuito ad alimentare questa discussione. Il problema principale riguarda la fonte di queste cellule, in quanto spesso coinvolge la "tutela della vita del concepito", un principio morale e legale di grande rilevanza.
La legislazione in diversi paesi è intervenuta per dettare regole e restrizioni precise, cercando di bilanciare il progresso scientifico con le preoccupazioni etiche. Uno dei punti centrali del dibattito è la necessità di garantire che l'utilizzo di cellule staminali non derivate da fonti controverse sia almeno "equivalente per la cura del malato" rispetto a quelle embrionali o fetali, un requisito che spesso si scontra con la versatilità superiore delle cellule embrionali. La "contesa" etica si manifesta anche nel contesto della procreazione assistita, da cui provengono molti degli embrioni "in eccesso" utilizzati per la ricerca.
Organoidi simulano cervello, così scienziata italiana sfida malattie
Nonostante le difficoltà, la ricerca sulle cellule staminali promette nuove speranze per la cura di "malattie spesso inguaribili". È cruciale, tuttavia, che ogni passo avanti sia accompagnato da "una valutazione etica caso per caso", adottando un approccio che miri a "vietare il meno possibile e controllare il più possibile". Ciò implica un'attenta considerazione delle "restrizioni" necessarie per guidare la ricerca e l'applicazione clinica in modo etico.
Un interessante sviluppo in questo contesto è stato riportato da alcuni ricercatori del Wellcome Cancer Research Institute inglese. Essi hanno riferito che anche gli embrioni difettosi, quelli cioè incapaci di svilupparsi in un essere umano completo, potrebbero essere in grado di fornire cellule staminali utili. I risultati di questa ricerca, che in una fase iniziale ha riguardato solo le rane, sono stati descritti sulla rivista "Proceedings of the National Academy of Sciences". Il professor John Gurdon, che, insieme ai suoi colleghi, ha scoperto che anche gli embrioni difettosi, ottenuti per clonazione, delle rane sono in grado di produrre utili cellule staminali, ha spiegato che «Questo potrebbe essere un modo interessante di aggirare il problema». La sua scoperta è particolarmente rilevante considerando che molti degli embrioni ottenuti dalla fecondazione artificiale sono anormali e vengono solitamente gettati via dai ricercatori per timore di utilizzarli come fonte di cellule staminali. Gurdon ha dimostrato che, almeno per quanto riguarda le rane, è possibile recuperare "buone cellule che possono essere usate per la ricerca o per trapianti" anche da "embrioni destinati a morire molto rapidamente". Le cellule staminali derivate dal processo di trapianto nucleare somatico, o clonazione terapeutica, rientrano in questa categoria di fonti potenziali.
Vaccini e Dilemmi Morali: Un Esempio Concreto di Cooperazione al Male
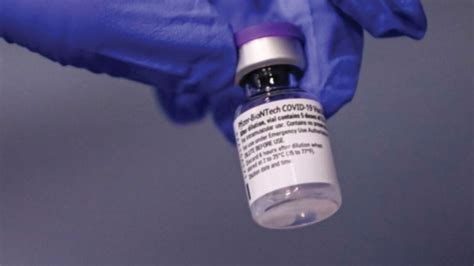
Il dibattito etico sull'utilizzo di materiali biologici derivati da feti abortiti non si limita alla ricerca sulle cellule staminali, ma si estende anche ad altre aree della medicina, come la produzione di vaccini. Questo è un tema particolarmente sentito in alcune parti del mondo dove malattie come la rosolia sono ancora endemiche. L'infezione di queste malattie, se contratta da donne gravide, può causare gravi danni e portare addirittura alla morte del feto. In questo contesto, la vaccinazione su larga scala rappresenta un mezzo irrinunciabile e universalmente riconosciuto nella lotta contro queste malattie infettive, essenziale per la protezione della salute pubblica.
Tuttavia, alcuni vaccini di ampia diffusione, utilizzati contro malattie come la rosolia e la varicella, sono stati sviluppati utilizzando ceppi di virus ottenuti da feti umani volontariamente abortiti. Questa realtà solleva un profondo problema etico. L'Autore di un articolo proveniente dall'archivio storico del manifesto, che affronta proprio questa questione, riflette sul problema etico sollevato sia dai medici impegnati nelle campagne di vaccinazione sia da coloro che necessitano dei vaccini, soprattutto dai genitori che devono vaccinare i propri figli. Essi si chiedono se l'uso di tali vaccini non sia in contraddizione con il rifiuto etico di ogni forma di aborto volontario.
Per rispondere a questo interrogativo, l'Autore analizza il problema riflettendo sulle diverse modalità e i vari gradi della cooperazione al male. Questa analisi porta a una conclusione articolata: esiste un dovere grave di usare i vaccini alternativi, laddove esistano e siano disponibili, e di invocare l'obiezione di coscienza riguardo a quelli il cui uso presenta dei problemi morali insuperabili per la coscienza individuale.
Per quanto riguarda i vaccini per i quali non esistono alternative disponibili, la situazione diventa più complessa. In questi casi, si dovrebbe ribadire con forza sia il dovere etico e scientifico di lottare affinché ne vengano approntati altri che non sollevino problemi morali, sia la liceità del loro uso nella misura in cui ciò è strettamente necessario per evitare un pericolo grave per le condizioni sanitarie della popolazione. La liceità di tale uso, tuttavia, va interpretata in un modo molto specifico: non come una legittimazione della produzione di tali vaccini, ma piuttosto come una "cooperazione materiale passiva". Questa forma di cooperazione è moralmente giustificata unicamente come extrema ratio, cioè come ultima risorsa, dal dovere superiore di provvedere al bene dei propri figli, nel caso dei genitori, e della popolazione in generale. In nessun caso tale uso può essere interpretato come una dichiarazione di liceità della loro produzione, mantenendo salda la condanna morale dell'atto originario dell'aborto. I dati disponibili su questo specifico articolo potrebbero essere limitati, e di conseguenza, l’articolo potrebbe risultare incompleto, tuttavia la problematica da esso sollevata rimane attuale e centrale nel dibattito bioetico.