Lo sviluppo embrionale dei mammiferi rappresenta uno dei processi biologici più affascinanti e complessi, una cascata finemente orchestrata di eventi che trasformano una singola cellula fecondata in un organismo multicellulare altamente organizzato. Tra le strutture fondamentali che emergono durante le prime fasi di questo sviluppo, l'aorta dorsale svolge un ruolo cruciale, in particolare come nicchia per la formazione delle cellule staminali ematopoietiche (HSC). Comprendere come si formano i tessuti durante lo sviluppo è utile per poter dedurre tale informazione nell’organismo adulto. Nonostante i progressi della scienza, molte fasi iniziali di questo viaggio sono rimaste a lungo avvolte nel mistero, soprattutto per la difficoltà di osservare direttamente e in modo continuo gli embrioni di mammifero, che si impiantano rapidamente nell'utero materno.
La ricerca moderna, tuttavia, sta compiendo passi da gigante, aprendo nuove finestre su questi processi finemente regolati. Studi recenti hanno non solo permesso di osservare con una precisione senza precedenti le prime fasi dello sviluppo embrionale, ma hanno anche condotto alla creazione di modelli embrionali sintetici in laboratorio, rivoluzionando la nostra comprensione dei meccanismi che guidano la formazione degli organi, inclusa la genesi di strutture vitali come il cuore e i precursori del sistema nervoso, e le origini delle cellule staminali ematopoietiche dalla regione dell'aorta dorsale.

Rivoluzione nell'Osservazione dello Sviluppo Embrionale Precoce: Visti da Vicino
Per anni, l'osservazione diretta dello sviluppo embrionale dei mammiferi in tempo reale e con un dettaglio cellulare così elevato era considerata una sfida quasi insormontabile. A differenza di pesci, anfibi e uccelli, il cui sviluppo è più facilmente osservabile, quello dei mammiferi sfugge ai nostri occhi dal momento che l’embrione si impianta in utero. Questa limitazione ha reso particolarmente difficile svelare i segreti della morfogenesi precoce e della differenziazione cellulare. Tuttavia, un progresso significativo è stato raggiunto grazie a tecniche di imaging innovative.
Una delle chiavi per superare questa barriera è stata l'applicazione di una particolare tecnica avanzata chiamata ‘microscopia a foglio di luce’. Questa metodologia ha permesso ai ricercatori di visualizzare in modo non invasivo e per periodi prolungati il dinamico processo di sviluppo. In pratica, il raggio laser usato per illuminare il campione viene concentrato fino a formare un foglio di luce che illumina solo un sottilissimo strato del campione per volta. Questo approccio minimizza il danneggiamento cellulare e la fototossicità, consentendo osservazioni continue per giorni interi. “È la prima volta che siamo riusciti a osservare le cellule cardiache così da vicino e per così tanto tempo, durante lo sviluppo dei mammiferi”, ha commentato Kenzo Ivanovitch, che ha coordinato uno di questi studi pionieristici. “Inizialmente abbiamo dovuto coltivare gli embrioni in laboratorio per lunghi periodi, da poche ore a qualche giorno, e quello che abbiamo scoperto è stato del tutto inaspettato”.
Le immagini ottenute attraverso questa tecnica rivoluzionaria hanno fornito intuizioni sorprendenti sul comportamento cellulare. Le immagini mostrano come le cellule che danno origine al cuore emergano molto rapidamente e si comportino in modo altamente organizzato: non si muovono, cioè, in modo casuale, ma seguono percorsi ben precisi, come se sapessero già il ruolo che dovranno svolgere. Questa osservazione diretta dell'auto-organizzazione cellulare in tempo reale è fondamentale per comprendere come le complesse strutture embrionali prendano forma con una precisione così notevole. Questo tipo di ricerca potrebbe cambiare la comprensione dei difetti cardiaci congeniti, che colpiscono quasi un neonato su 100, e il modo di correggerli, aprendo alla possibilità di intervenire in fasi molto più precoci.
L'Avvento degli Embrioni Sintetici: Un Nuovo Paradigma di Ricerca e la Formazione degli Organi
L'incapacità di osservare lo sviluppo embrionale in utero ha spinto la ricerca verso la creazione di modelli in vitro sempre più sofisticati. Un risultato straordinario in questo campo è stata la generazione di embrioni sintetici, o modelli embrionali, a partire da cellule staminali. Questo approccio rappresenta un salto qualitativo nella ricerca, in quanto fornisce un sistema controllabile e replicabile per studiare le prime fasi dello sviluppo. L’importanza di questo lavoro, pubblicato su Nature, deriva proprio dalla parola «sintetico, «artificiale»: gli embrioni vengono solitamente creati in vitro con fecondazione artificiale tra una cellula uovo e uno spermatozoo, in questo caso, però, la «partenza» dell’embrione viene dalle cellule staminali.
Il Professor Carlo Alberto Redi, di Zoologia e Biologia dello sviluppo all’Università di Pavia e membro dell’Accademia dei Lincei, ha commentato che «È un lavoro importante e interessante: fa avanzare la dissezione molecolare della conoscenza della formazione di un embrione e lo fa evitando problemi di tipo etico perché sta usando delle cellule staminali». Questi modelli non mirano a creare un embrione capace di crescere fuori dall'utero, ma a indagare le prime fasi dello sviluppo embrionale, quelle che precedono l’impianto. Si pensa che due terzi delle gravidanze umane fallisca in questa fase, prima ancora che una donna possa rendersi conto di essere incinta.
CHE COSA SONO E COME FUNZIONANO LE CELLULE STAMINALI (e anche un po' la leucemia) | #TELOSPIEGO!
Il team guidato da Magdalena Zernicka-Goetz dell'Università di Cambridge, con Gianluca Amadei e Charlotte Handford, di Cambridge e del Caltech, ha giocato un ruolo pionieristico in questo campo. Già nel 2017, lo stesso gruppo di ricerca aveva ottenuto il primo embrione sintetico a partire da cellule staminali embrionali di topo, sebbene non fosse in grado di percorrere tutte le fasi dello sviluppo. I risultati sono il culmine di oltre un decennio di studi e potrebbero aiutare i ricercatori a capire perché alcuni embrioni falliscono mentre altri si trasformano in un feto in una gravidanza sana.
Nel nuovo esperimento di Zernicka-Goetz e colleghi, è stata utilizzata una combinazione di staminali embrionali e trofoblastiche extra-embrionali di topi geneticamente modificati, fatte crescere su un'impalcatura tridimensionale nota come matrice extracellulare. Finora, i tentativi di ottenere strutture embrionali in vitro usando solo staminali embrionali ha avuto un successo limitato: anche le prime fasi di sviluppo degli embrioni richiedono infatti tipi di cellule differenti che si coordinano le une con le altre. Zernicka-Goetz e colleghi hanno perciò intrapreso una strada diversa, usando una combinazione di staminali embrionali e trofoblastiche extraembrionali di topi geneticamente modificati, fatte crescere su un'impalcatura tridimensionale nota come matrice extracellulare. Il risultato è una struttura capace di autoassemblarsi e il cui sviluppo e la cui architettura somigliano molto all'embrione naturale.
Fondamentali in queste fasi sono le diverse popolazioni di cellule staminali, le loro successive specializzazioni e le loro mutue interazioni. Lo zigote, frutto della fecondazione di una cellula uovo da parte di uno spermatozoo, va incontro a successive divisioni cellulari: quelle che inizialmente sono cellule staminali totipotenti, perché possono dare origine un organismo completo, via via si specializzano. Si distinguono così cellule staminali embrionali (ESC) pluripotenti, da cui proseguirà lo sviluppo dell'embrione, le cellule staminali trofoblastiche extra-embrionali (TSC), che formeranno la placenta, e infine le cellule staminali endodermiche che formeranno il sacco vitellino, che insieme ad altri annessi embrionali, è deputato a fornire tutto ciò di cui l'embrione necessita per il suo corretto sviluppo. In questo nuovo esperimento è stata utilizzata una combinazione di cellule staminali embrionali, cellule della struttura necessaria al nutrimento dell'embrione (trofoblasto) e cellule extra-embrionali (ETiX), tutte di topo. La grande differenza, rispetto al 2017, è nel fatto che i ricercatori sono riusciti a far dialogare le cellule fra loro, in modo che si assemblassero in modo spontaneo, senza la necessità di stimoli esterni.
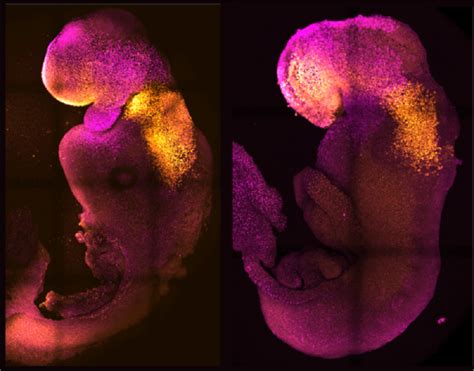
Questo "dialogo" è cruciale. “Le cellule embrionali e quelle extra-embrionali iniziano a comunicare le une con le altre e a organizzarsi in una struttura che somiglia a un embrione e si comporta come un embrione”, ha spiegato Zernicka-Goetz. “In sintesi: ha regioni anatomicamente corrette che si sviluppano nel posto giusto al momento giusto”. Zernicka-Goetz e colleghi hanno scoperto un notevole grado di comunicazione tra i due tipi di cellule staminali: in un certo senso, si "dicono" reciprocamente dove collocarsi all'interno dell'embrione. “Sappiamo che le interazioni tra i diversi tipi di cellule staminali sono importanti per lo sviluppo, ma la cosa sorprendente è che il nostro lavoro mostra ora che si tratta di una vera collaborazione, senza cui lo sviluppo anatomico e la corretta successione dei meccanismi biologici cruciali non possono avvenire in modo corretto”.
L'embrione artificiale dunque somiglia molto a quello naturale, e comprende anche staminali che si possono specializzare nel tessuto della placenta, ma è improbabile che si possa sviluppare in un feto sano, perché mancano le cellule da cui ha origine il sacco vitellino. Nonostante questa limitazione, è stato per la prima volta ottenuto un embrione di topo sintetico che ha raggiunto lo sviluppo record di 8,5 giorni, con cervello e cuore battente. L'embrione si è sviluppato per otto giorni e mezzo, dando origine a una struttura complessa e differenziata che comprende alcune regioni del cervello, il tubo neurale che dà origine al sistema nervoso, una struttura simile a un cuore in grado di battere e un'altra simile all'intestino.
Meccanismi Genetici e Molecolari che Guidano la Morfogenesi e l'Ematopoiesi
I progressi nell'osservazione e nella creazione di modelli embrionali sintetici hanno ulteriormente illuminato la comprensione dei meccanismi genetici che sottendono la morfogenesi. L'esperto Carlo Alberto Redi aggiunge che «questo studio avanza la conoscenza della genetica molecolare sullo sviluppo precoce degli embrioni, uno stadio ancora poco conosciuto dello sviluppo embrionale: riesce a dirci quali sono alcuni geni capaci di regolare come le cellule si mettono insieme per formare un embrione». I geni che guidano la formazione sono, infatti, i veri "istruttori" dello sviluppo. Finora nell’osservazione in vivo o in vitro di questo processo, erano noti solo alcuni geni. Ora, controllando questi geni, si possono mettere insieme i tre tipi di cellule che costituiscono gli organi e arrivare ad un embrione.
Ci sono tre tipi di cellule che costituiscono tutti noi (endoderma, mesoderma, ectoderma), le cellule staminali possono svilupparsi in quasi tutti i tipi di cellule del corpo: il gruppo di lavoro ha trovato i geni che regolano come le cellule si appiccicano una all’altra per formare gli organi (un cuore battente e un pezzo di cervello, nello specifico) e poi l’embrione. La complessità di questi processi è strabiliante: le cellule staminali embrionali a piccoli gruppi di trofoblasti, le cellule che vanno a formare la placenta, che nutrono l'embrione ma non partecipano direttamente alla sua formazione, sono state mescolate in un gel semisolido che ha permesso alla struttura di crescere nelle tre dimensioni. Dopo 5 giorni, l'ammasso di cellule si era già differenziato e organizzato in diverse popolazioni, come se le staminali si fossero coordinate, posizionandosi in luoghi diversi. Da una parte i trofoblasti, dall'altra le cellule embrionali una cui piccola parte era pronta a specializzarsi nel mesoderma, le cellule che di norma danno origine a cuore, ossa e muscoli.
Un'area di ricerca particolarmente rilevante, e strettamente legata allo sviluppo dell'aorta dorsale nell'embrione di topo, riguarda la genesi delle cellule staminali ematopoietiche (HSC). Le HSC sono una sottopopolazione di cellule primitive capaci di generare l’intero sistema ematopoietico e immunitario, contribuendo all’omeostasi. Si ritiene che le HSC di AGM (Aorta-Gonade-Mesonefro) vengano fuori dall’endotelio sottostante, che in tale stadio dello sviluppo possiede proprietà emogeniche. L'aorta dorsale embrionale, in particolare la regione AGM, è riconosciuta come un sito cruciale per l'emergenza delle HSC durante lo sviluppo.
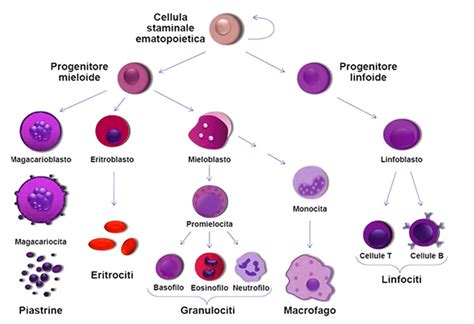
Il progetto FRINGEHE (“Uncovering the role of Notch modifiers in the generation of hematopoietic stem cells in the embryo”), finanziato dall’UE, si proponeva di studiare il ruolo della via di trasduzione del segnale Notch nella EHT (Transizione Endoteliale-Ematopoietica). Questa via di segnalazione è fondamentale in numerosi processi di sviluppo. Si sa che i ligandi Notch Jagged-1 e Delta-4 sono espressi nell’endotelio aortico e sembrano influire su destini biologici diversi. Per comprendere come la trasduzione del segnale Notch esercita tali effetti, i ricercatori di FRINGEHE hanno analizzato il profilo di espressione genica di cellule nella regione AGM, prima che diventino ematopoietiche. L’esposizione di tali cellule endoteliali a Jagged-1 e non a Delta-4 le ha spinte a divenire ematopoietiche. Questo dimostra la specificità e la potenza dei segnali molecolari nella determinazione del destino cellulare. Nel loro complesso, i risultati dello studio FRINGEHE ampliano notevolmente le conoscenze sull’ematopoiesi embrionica e la comparsa delle prime HSC, offrendo una visione dettagliata dei segnali che regolano questa transizione cruciale nell'aorta dorsale.
Implicazioni Cliniche e Prospettive Future: Dalla Ricerca al Trapianto
Le scoperte ottenute dallo studio dello sviluppo embrionale, sia attraverso l'osservazione diretta che con l'utilizzo di modelli sintetici, hanno implicazioni profonde che vanno ben oltre la biologia dello sviluppo fondamentale. Innanzitutto, questo lavoro potrebbe cambiare la comprensione dei difetti cardiaci congeniti, che colpiscono quasi un neonato su 100, e il modo di correggerli, aprendo alla possibilità di intervenire in fasi molto più precoci. Le osservazioni dettagliate delle cellule cardiache e la loro organizzazione precoce potrebbero rivelare le anomalie che portano a tali difetti.
I risultati potrebbero anche accelerare i progressi nella coltivazione di tessuto cardiaco in laboratorio, da utilizzare nella medicina rigenerativa. Se in futuro la tecnica sperimentata nei topi avrà successo anche con cellule staminali umane, dicono i ricercatori, si potranno costruire in laboratorio organi per i trapianti destinati ai pazienti in lista d'attesa. “Nel mondo ci sono tante persone che attendono anni per avere un trapianto”, osserva Zernicka-Goetz. “Quello rende il nostro lavoro così entusiasmante è che le conoscenze che ne derivano potranno essere utilizzate per coltivare in futuro organi umani sintetici per salvare vite”. Coltivare organi, conclude, “aiuterebbe anche a capire meglio come sono fatti e a curarli in modo più efficace”.
CHE COSA SONO E COME FUNZIONANO LE CELLULE STAMINALI (e anche un po' la leucemia) | #TELOSPIEGO!
Inoltre, i risultati ottenuti da questi modelli embrionali potrebbero essere utilizzati per guidare la riparazione e lo sviluppo di organi umani «sintetici» adatti al trapianto. Il passo in avanti è notevole: è stato per la prima volta ottenuto un embrione di topo sintetico che ha raggiunto lo sviluppo record di 8,5 giorni, con cervello e cuore battente. Questi risultati sono il culmine di oltre un decennio di ricerca e potrebbero aiutare i ricercatori a capire perché alcuni embrioni falliscono mentre altri si trasformano in un feto come parte di una gravidanza sana.
Il gruppo di ricerca del California Institute of Technology (Caltech) sta già lavorando a un modello di embrione umano analogo a quello di topo appena ottenuto e l'obiettivo è riuscire a comprendere passaggi cruciali dello sviluppo embrionale altrimenti impossibili da osservare in embrioni umani reali. “Riteniamo che presto sarà possibile riprodurre molti degli eventi che si verificano prima del quattordicesimo giorno usando staminali embrionali ed extraembrionali umane in un approccio simile a quello che ha avuto successo con i topi”, ha spiegato Zernicka-Goetz. Ciò permetterebbe di studiare le cause di aborti spontanei precoci e di sviluppare strategie per prevenirli.
In questo vero e proprio laboratorio vivente in miniatura, i ricercatori hanno anche dimostrato di poter riprodurre le caratteristiche osservate nei cosiddetti topi di laboratorio knockout, ossia privati di un un gene allo scopo di studiare caratteristiche fisiologiche o le cause di malattie. Questo offre una piattaforma senza precedenti per la ricerca farmacologica e lo studio delle malattie genetiche.
Tecniche Avanzate per la Coltura Cellulare e la Ricerca in 3D
La creazione di modelli embrionali sintetici e l'osservazione approfondita dello sviluppo non sarebbero possibili senza avanzamenti significativi nelle tecniche di coltura cellulare, in particolare quelle che consentono la crescita in tre dimensioni. Una tecnica di coltura cellulare in 3D potrebbe sostituire gli embrioni di topo per molte applicazioni. Cellule staminali fatte crescere in una struttura gelatinosa che imita le proprietà della matrice extracellulare e fornisce supporto e orientamento spaziale: questo è il punto cruciale del nuovo metodo di coltura cellulare sperimentale i cui dati sono stati pubblicati su Science a inizio dicembre.
I ricercatori del MPIMG sono riusciti a replicare una fase centrale dello sviluppo embrionale di topo in una capsula Petri (la banale piastra di laboratorio in cui si fanno crescere le colture cellulari di vario tipo) facendo crescere la parte centrale del tronco dell’organismo partendo da cellule staminali embrionali. Le cosiddette “Trunk-Like-Structure” (strutture simili al tronco) hanno sviluppato in soli cinque giorni i precursori per i tessuti neurali, ossei, cartilaginei e muscolari a partire da aggregati disordinati di cellule. Le strutture sono grandi circa un millimetro e possiedono un tubo neurale da cui si svilupperebbe il midollo spinale. Inoltre, hanno somiti, che sono i precursori di scheletro, cartilagine e muscolo. Alcune delle strutture sviluppano anche i precursori di organi interni come l'intestino.
Queste strutture sono un esempio di come l'ambiente di coltura possa influenzare la morfogenesi. Durante lo sviluppo embrionale, la matrice extracellulare fornisce stimoli chimici e meccanici essenziali. In vitro, il Matrigel, un surrogato della matrice extracellulare, può guidare la morfogenesi e questo ha portato i ricercatori ad utilizzarlo in varie condizioni per valutarne l’efficacia e a stabilire che il 5% di Matrigel è sufficiente per indurre la formazione di strutture organizzate. “Il gel fornisce supporto alle cellule coltivate e le orienta nello spazio; ad esempio, possono distinguere l'interno dall'esterno”, ha spiegato il primo autore dello studio Jesse V. Veenvielt.
Dopo quattro o cinque giorni, il gruppo di ricerca ha separato le strutture, isolando le cellule e analizzandole singolarmente. "Anche se non tutti i tipi di cellule embrionali sono presenti nelle Trunk-Like-Structure, sono sorprendentemente simili ad un embrione della stessa età", dice Adriano Bolondi, co-autore dello studio. Insieme alla bioinformatica Helene Kretzmer, gli autori hanno confrontato l'attività genetica delle strutture in vitro con gli embrioni di topo, rivelando somiglianze sorprendenti nel loro profilo di espressione genica.
Sebbene sia considerato abbastanza semplice isolare un embrione quando non è ancora impiantato, una volta superata la fase d’impianto nell’endometrio diventa estremamente isolato e difficile da osservare. Grazie a questa tecnica innovativa di coltura è possibile esaminare ogni fase iniziale dello sviluppo direttamente, in modo continuo e su un numero di campioni a scelta e in crescita contemporanea. Questo cambia radicalmente il modello di studio standard e permette di analizzare processi complessi come la morfogenesi. A differenza dei vari sistemi di cellule staminali tridimensionali che sono stati sviluppati per aggirare questo impedimento - i più recenti dei quali riescono a produrre i cosiddetti gastruloidi - in questo caso si formano delle strutture con l’aspetto tipico di un embrione, dimostrando un livello superiore di organizzazione e complessità.
Il Contesto della Ricerca Biomedica e le Sfide Etiche
La ricerca sullo sviluppo embrionale, e in particolare l'uso di modelli animali come l'embrione di topo, si inserisce in un contesto più ampio di dibattito etico e scientifico. Se da un lato l'avanzamento delle conoscenze offre prospettive rivoluzionarie per la medicina e la comprensione della vita, dall'altro solleva questioni importanti sull'uso degli animali nella ricerca e sulla potenziale creazione di strutture sempre più complesse in laboratorio.
I ricercatori sottolineano che l'uso di cellule staminali per creare embrioni sintetici, piuttosto che la fecondazione di cellule uovo, contribuisce a evitare problemi di tipo etico. Questo approccio basato sulle staminali riduce alcune delle preoccupazioni associate all'uso di embrioni ottenuti tramite fecondazione. Tuttavia, il progresso scientifico non è sempre esente da resistenze. Di recente, Research4Life e la comunità scientifica, rappresentata da 45 firmatari, hanno pubblicato una lettera aperta alle massime cariche della Repubblica italiana per chiedere ed ottenere risposte a favore della ricerca biomedica, osteggiata e minacciata dagli animalisti che bloccano progetti di ricerca e oggi, di fatto, i lavori parlamentari. Questo mette in evidenza la tensione costante tra l'esigenza di progredire nella conoscenza scientifica per il benessere umano e le legittime preoccupazioni etiche riguardo ai metodi di ricerca. La ricerca sugli embrioni di topo, come illustrato dal lavoro di mol. Genet. / Léo Guignard, Max Delbrück Center f. Mol., rimane un pilastro fondamentale per svelare i meccanismi più intimi dello sviluppo biologico, con la promessa di tradurre queste scoperte in benefici concreti per la salute umana.