La gravidanza è un percorso straordinario che, purtroppo, non sempre si conclude come desiderato. La perdita di una gravidanza, in particolare l'aborto spontaneo precoce, è un evento molto più frequente di quanto si pensi. Si manifesta nelle prime settimane di gestazione, talvolta ancor prima che la donna sia effettivamente consapevole di essere incinta. È sempre un’esperienza emotivamente complessa da affrontare: subentrano dubbi sulla capacità di portare avanti una gravidanza, timori per il futuro e sensi di colpa. Comprendere le cause è importante non solo per elaborare quanto accaduto, ma anche per guardare avanti con maggiore consapevolezza. La genetica gioca in questi contesti un ruolo determinante, soprattutto negli aborti precoci e in quelli che si ripetono nel tempo. Oggi, grazie ai progressi scientifici, è possibile indagare a fondo tali aspetti ed impostare eventuali percorsi di cura personalizzati, al fine di portare una gravidanza a termine e mettere al mondo un bambino sano.
Definire l'Aborto Spontaneo: Tipi e Impatto
Quando si parla di aborto spontaneo si intende l’interruzione naturale di una gravidanza entro la 20ª-22ª settimana di gestazione; la maggioranza dei casi, comunque, l’evento avviene entro il primo trimestre. Circa il 13% delle gravidanze si concludono con la perdita del feto. In alcuni casi si presenta con sintomi quali sanguinamento e dolore addominale, e se si tratta dell’inizio della gestazione, la donna può confondere questi disturbi con quelli tipici del ciclo mestruale; in altri contesti si scopre con la prima ecografia di routine. Va sottolineato: il più delle volte l’aborto spontaneo è un fatto fisiologico, dovuto ad alterazioni biologiche e genetiche che rendono impossibile il normale sviluppo dell’embrione. Non è provocato dai comportamenti della donna. È importante fare un distinguo: si parla di aborto spontaneo estemporaneo o episodico quando avviene una sola volta, mentre si definisce come ricorrente la perdita di due o più gravidanze consecutive (secondo alcune definizioni, tre). Tale distinzione è importante per definire l’approccio diagnostico e terapeutico. La perdita di due o più gravidanze si valuta come gravidanza ricorrente, un fenomeno che colpisce circa l'1-2% delle donne in età riproduttiva e comporta significative conseguenze fisiche ed emotive, come indicato dal Practice Committee of the American Society for Reproductive Medicine (2012).
La perdita di una gravidanza può essere un'esperienza molto traumatica per le coppie. Gli studi indicano che oltre un quinto delle donne che subiscono una perdita di gravidanza mostrano sintomi di ansia e depressione. Quando una singola perdita di gravidanza può avere effetti così traumatici, la perdita di gravidanza ricorrente (RPL) può avere effetti psicologici devastanti.
Il Ruolo Cruciale dei Cromosomi: Fondamenti Genetici
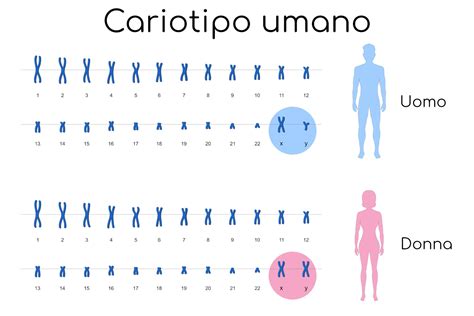
Per comprendere appieno le cause genetiche dell'aborto spontaneo, è fondamentale sapere cosa sono i cromosomi. I cromosomi sono strutture presenti nelle cellule, che contengono il DNA e, quindi, tutte le informazioni genetiche necessarie per lo sviluppo, la crescita ed alla differenziazione dell'organismo. Ogni cellula del nostro corpo contiene normalmente un determinato numero di cromosomi. Nell'essere umano, il corredo cromosomico di un individuo è costituito da 46 cromosomi, organizzati in 23 coppie. Di queste, 22 coppie sono autosomi (cromosomi non sessuali) e una coppia è di cromosomi sessuali (XX per le femmine, XY per i maschi). Gli uomini, quindi, hanno un cromosoma X e un cromosoma Y. Questi cromosomi portano i geni, le unità ereditarie che determinano le nostre caratteristiche individuali. Il patrimonio genetico degli embrioni non è altro che la somma dei cromosomi contenuti nei gameti che li originano.
Aneuploidie: La Causa Genica Predominante di Aborto Spontaneo
Tra le cause genetiche di aborto spontaneo, le anomalie cromosomiche sono la principale causa genetica, responsabili di circa il 50-60% delle perdite precoci di gravidanza che si verificano per motivi genetici. La genetica è responsabile del 50-70% degli aborti spontanei precoci. Il più delle volte si tratta di anomalie cromosomiche dell’embrione, che insorgono al momento della fecondazione o nelle prime divisioni cellulari. Almeno la metà dei casi di pazienti che soffrono di aborti spontanei ricorrenti è dovuta a cause sconosciute e questo non aiuta certo la coppia.
Che cosa sono le aneuploidie? L'aneuploidia è un numero anomalo di cromosomi, ovvero la presenza di un numero di cromosomi differente da quello tipico della specie. Si riferisce ad un'alterazione del numero di cromosomi che può consistere nella mancanza o nell'eccesso di uno o più cromosomi interi o di una coppia di cromosomi omologhi. Le aneuploidie, ovvero un numero anomalo di cromosomi, sono una delle cause più comuni di aborto spontaneo. Tali anomalie impediscono un corretto sviluppo embrionale e portano a un’interruzione precoce della gravidanza: l’aborto spontaneo è spesso un meccanismo naturale di selezione biologica.
I tipi più comuni di aneuploidie includono monosomia e trisomia completa. La monosomia si verifica quando manca un intero cromosoma (ad esempio, monosomia del cromosoma X, associata alla sindrome di Turner), mentre la trisomia implica la presenza di un cromosoma in più (ad esempio, trisomia del cromosoma 21 nella sindrome di Down). Esistono anche trisomie parziali, che implicano la copia di singoli segmenti di cromosoma e che sono causa di una sintomatologia più lieve. Le aneuploidie non sono da confondere con le poliploidie, che riguardano la presenza di uno o più interi set di cromosomi in più.
La trisomia (presenza di un cromosoma in più) è l'aneuploidia più frequente osservata, in particolare le trisomie dei cromosomi 16, 21 e 22. Le trisomie più comuni sono quelle dei cromosomi 16, 18 e 13. La trisomia del cromosoma 21 porta al bambino con la sindrome di Down. La trisomia del cromosoma 18 si associa ad una elevata abortività. La trisomia del cromosoma 13 si associa ad elevata abortività. Anche la monosomia X (sindrome di Turner) è prevalente tra gli aborti spontanei, ma è raramente vitale oltre il primo trimestre, come osservato da Hassold & Hunt (2001).
Le aneuploidie si verificano spesso a causa della non disgiunzione meiotica, un processo in cui i cromosomi non riescono a separarsi correttamente durante la divisione cellulare nei gameti, portando a embrioni con contenuto cromosomico anomalo (Nagaoka et al., 2012). Questo è un evento frequente, stimato che circa il 7,5% dei concepimenti sia affetto da malattie cromosomiche. L’età materna avanzata comporta la probabilità di ovociti “vecchi”, non di buona qualità, che più facilmente possono presentare errori nella divisione cromosomica. Il rischio di aborto spontaneo aumenta notoriamente e progressivamente dopo i 35 anni. Le donne di età superiore ai 35 anni hanno un rischio maggiore di produrre ovociti con errori cromosomici, che portano ad aborti spontanei (Hassold & Chiu, 1985).
CARIOTIPO: POLIPLOIDIA e ANEUPLOIDIA
Oltre l'Aneuploidia: Altre Anomalie Genetiche e Strutturali
Sebbene le aneuploidie siano la causa principale, altre anomalie genetiche e strutturali possono contribuire all'aborto spontaneo.
Anomalie Cromosomiche StrutturaliAnche le anomalie cromosomiche strutturali, tra cui traslocazioni, inversioni e delezioni, contribuiscono all'aborto ricorrente. Le traslocazioni si verificano quando i segmenti cromosomici vengono riorganizzati tra cromosomi non omologhi. Negli aborti spontanei ricorrenti, aumenta la probabilità che uno dei partner sia portatore di una traslocazione cromosomica bilanciata o di altre anomalie strutturali. Questo significa che il genitore è sano e fertile, ma che può produrre gameti con anomalie che danno origine ad embrioni con assetti cromosomici alterati. Si tratta di condizioni relativamente frequenti, che rimangono silenti fino a quando non si cerca una gravidanza. Le traslocazioni bilanciate, che non comportano un guadagno o una perdita netta di materiale genetico, potrebbero non influenzare l'individuo ma possono portare ad aborti se i cromosomi riorganizzati interrompono lo sviluppo dell'embrione (Stephenson et al., 2002). L'analisi del cariotipo parentale può spesso rivelare anomalie strutturali nelle coppie con aborti ricorrenti.
Mutazioni di Singoli Geni e Sindromi GeneticheSebbene le anomalie cromosomiche siano significative, anche le mutazioni di singoli geni o le sindromi genetiche possono aumentare il rischio di aborto spontaneo. Alcune riguardano geni coinvolti nella coagulazione del sangue (trombofilie ereditarie), altre interessano processi fondamentali per lo sviluppo embrionale o l’impianto. Le condizioni genetiche ereditarie, tra cui le sindromi autosomiche recessive o autosomiche dominanti, possono contribuire alla perdita della gravidanza. Mutazioni genetiche specifiche che causano trombofilia, o aumento della coagulazione del sangue, sono state collegate ad aborti spontanei. Mutazioni in geni come F5 (Fattore V Leiden) e F2 (protrombina) possono portare a una coagulazione anomala del sangue nella placenta, compromettendo il flusso sanguigno e causando infine aborto spontaneo (Rey et al., 2003). Sebbene la trombofilia sia una condizione multifattoriale, la predisposizione genetica è un fattore che contribuisce ad alcune perdite di gravidanza ricorrenti.
Cambiamenti Epigenetici e Fattori Legati all'EtàAnche i cambiamenti epigenetici, modifiche ereditarie nell'espressione genica che non comportano cambiamenti nella sequenza del DNA, contribuiscono al rischio di aborto spontaneo. L'età avanzata della madre e del padre è associata a un rischio maggiore di anomalie genetiche, principalmente a causa di un accumulo di mutazioni nelle cellule germinali nel tempo. I disturbi dell'imprinting, in cui alcuni geni sono espressi in modo specifico del genitore di origine, sono collegati al rischio di aborto spontaneo. Errori nell'imprinting possono portare a disturbi come la sindrome di Prader-Willi o la sindrome di Angelman, che possono causare aborti spontanei o esiti avversi della gravidanza (Chong & Hutchinson, 2000).
Fattori Non Genetici Contribuenti all'Aborto Spontaneo Ricorrente
A differenza degli aborti spontanei isolati, che sono spesso attribuiti ad anomalie cromosomiche casuali, gli aborti spontanei ricorrenti sono più probabilmente dovuti a patologie sottostanti. Sebbene vi siano diversi fattori accertati che possono essere collegati alle ripetute perdite di gravidanza, le cause di quasi la metà delle gravidanze ricorrenti rimangono ancora un mistero. Insieme, fattori autoimmuni, problemi ormonali e problemi di coagulazione del sangue costituiscono quasi il 70% di tutte le cause note. Quando si verificano più aborti, è importante sospettare e valutare una serie di altri motivi che possono rendere difficile il proseguimento di una gravidanza. Comprendere queste cause aiuta a guidare una gestione e un supporto efficaci per le coppie interessate.
Anomalie Anatomiche dell'Apparato RiproduttivoLe anomalie strutturali all'interno del tratto riproduttivo possono compromettere l'impianto, interrompere il normale sviluppo fetale o portare a insufficienza placentare, tutte situazioni che possono contribuire a un evento indesiderato di aborto spontaneo. È stato stimato che le anomalie anatomiche contribuiscano fino al 15% di tutti gli aborti spontanei.
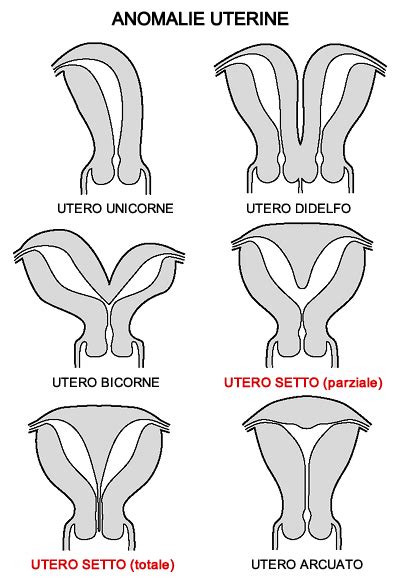
- Anomalie uterine congenite: Le malformazioni uterine, come l'utero setto, bicorne o unicorne, possono aumentare il rischio di aborto spontaneo. Un utero setto, in cui un setto fibroso divide la cavità uterina, è particolarmente associato a tassi elevati di aborto spontaneo. Il setto potrebbe non supportare un flusso sanguigno adeguato all'embrione impiantato, portando a insufficienza placentare e perdita di gravidanza (Grimbizis et al., 2001). È stato dimostrato che la correzione chirurgica del setto migliora i risultati della gravidanza.
- Anomalie uterine acquisite: Condizioni come i fibromi (in particolare i fibromi sottomucosi che deformano la cavità uterina) e le aderenze intrauterine (cicatrici all'interno dell'utero, spesso conseguenza di precedenti interventi chirurgici o infezioni) possono interferire con l'impianto o lo sviluppo fetale.
Squilibri Endocrini e OrmonaliLe anomalie endocrine sono fattori ben documentati che contribuiscono alla perdita ricorrente di gravidanza, principalmente a causa del loro impatto sull'equilibrio ormonale e sulla ricettività uterina. È noto che i problemi ormonali svolgono un ruolo nel 15-20% degli aborti spontanei ricorrenti.
- Sindrome dell'ovaio policistico (PCOS): La PCOS è un comune disturbo endocrino caratterizzato da ovulazione irregolare, iperandrogenismo e resistenza all'insulina. Livelli elevati di insulina nelle donne con PCOS possono portare a uno scarso sviluppo dell'endometrio e possono contribuire alla perdita precoce della gravidanza (Boomsma et al., 2006). Inoltre, lo squilibrio ormonale associato alla PCOS può interrompere la fase luteale (il periodo dopo l'ovulazione in cui l'endometrio si prepara all'impianto dell'embrione), portando potenzialmente a un ambiente uterino inadeguato per l'impianto.
- Difetto della fase luteale: La fase luteale, regolata dal progesterone prodotto dal corpo luteo dopo l'ovulazione, è fondamentale per mantenere un ambiente endometriale ottimale per l'impianto e il supporto precoce dell'embrione. Una carenza nella produzione di progesterone, nota come difetto della fase luteale, può portare a una preparazione endometriale insufficiente, compromettendo l'impianto e aumentando il rischio di aborto spontaneo.
- Disturbi della tiroide: La funzione tiroidea svolge un ruolo significativo nel mantenimento della gravidanza. L'ipotiroidismo (tiroide ipoattiva) può portare a una produzione insufficiente di ormoni tiroidei, essenziali per lo sviluppo fetale, soprattutto nel primo trimestre, quando il feto dipende dagli ormoni tiroidei materni. Anche nelle donne eutiroidee (funzione tiroidea normale), la presenza di autoanticorpi tiroidei, in particolare anticorpi anti-perossidasi tiroidea (TPO), è associata a un rischio di aborto spontaneo 2-3 volte maggiore (Thangaratinam et al., 2011).
Interazioni Immunitarie e TrombofilieIl sistema immunitario deve adattarsi per supportare la gravidanza, poiché il feto è geneticamente distinto dalla madre. Le interruzioni di questo adattamento possono portare all'aborto spontaneo.
- Sindrome da anticorpi antifosfolipidi (APS): L'APS è una condizione autoimmune caratterizzata dalla presenza di anticorpi antifosfolipidi, come l'anticoagulante lupico e gli anticorpi anticardiolipina. Questi anticorpi aumentano il rischio di formazione di coaguli nei vasi sanguigni, compresi quelli nella placenta. I coaguli placentari riducono l'apporto di ossigeno e nutrienti al feto, portando all'aborto spontaneo. L'APS è una causa ben documentata di aborto ricorrente e la sua gestione in genere prevede una terapia anticoagulante (Rai et al., 2005).
- Anomalie delle cellule Natural Killer (NK): Le cellule NK svolgono un ruolo nella gravidanza precoce, aiutando lo sviluppo della placenta. Si ipotizza che livelli elevati di cellule NK o una funzione anomala delle cellule NK contribuiscano all'aborto spontaneo ricorrente, poiché le cellule NK iperattive possono attaccare le cellule placentari.
- Trombofilie ereditarie: Le trombofilie ereditarie sono condizioni genetiche che predispongono gli individui a una coagulazione del sangue anomala, che può avere effetti negativi durante la gravidanza.
- Mutazione del fattore V di Leiden: Questa mutazione porta alla resistenza alla proteina C attivata, un anticoagulante cruciale, con conseguente stato di ipercoagulabilità. Durante la gravidanza, questa mutazione può portare a trombosi placentare (formazione di coaguli nella placenta), compromettendo l'apporto di ossigeno e nutrienti al feto, il che può causare aborto spontaneo, in particolare nel secondo trimestre (Preston et al., 2002).
- Mutazione del gene della protrombina: Questa mutazione promuove anche uno stato ipercoagulabile, aumentando il rischio di coaguli di sangue nella placenta. Le donne con questa mutazione hanno un rischio più elevato di aborto spontaneo, soprattutto nella fase avanzata della gravidanza.
- Carenze di proteine C e S: Le proteine C e S sono anticoagulanti naturali. Le carenze di queste proteine portano a una maggiore formazione di coaguli, che può compromettere la funzionalità della placenta.
Fattori Legati allo Stile di VitaDiversi fattori modificabili legati allo stile di vita possono influire sull'esito della gravidanza.
- Fumo: La nicotina e altre tossine presenti nel fumo di sigaretta compromettono il flusso sanguigno uterino, creando un ambiente ipossico (con poco ossigeno) che può interrompere lo sviluppo dell'embrione e aumentare il rischio di aborto spontaneo. Il fumo è associato a un rischio più elevato di anomalie cromosomiche nell'embrione, probabilmente a causa dello stress ossidativo del tabacco (Green et al., 2007).
- Assunzione di alcol e caffeina: Un consumo eccessivo di alcol è associato a tossicità fetale, che può contribuire all'aborto spontaneo. Un'elevata assunzione di caffeina (tipicamente superiore a 200-300 mg al giorno) è stata collegata a un aumento del rischio di aborto spontaneo, potenzialmente dovuto ai suoi effetti sui sistemi cardiovascolare e ormonale che supportano la gravidanza (Ford & Schust, 2009).
- Obesità: L'obesità è associata a un rischio più elevato di aborto spontaneo dovuto a squilibri ormonali, aumentata resistenza all'insulina e infiammazione cronica di basso grado.
Infezioni: Un Contributo Meno Frequente ma RilevanteAlcune infezioni possono aumentare il rischio di aborto spontaneo causando risposte infiammatorie che danneggiano i tessuti fetali o interrompono l'interfaccia materno-fetale. Mentre le cause infettive sono spesso suscettibili di indurre una perdita di gravidanza durante la fase attiva, alcune infezioni possono causare problemi cronici che possono essere un fattore per aborti spontanei ricorrenti.
- Chlamydia trachomatis e Ureaplasma urealyticum: Questi batteri possono causare endometrite cronica, un'infiammazione del rivestimento uterino, che può compromettere l'impianto o interrompere la funzione placentare, portando ad aborto spontaneo. L'infezione cronica con questi batteri è stata associata a esiti avversi della gravidanza, sebbene le prove che li collegano specificamente ad aborti spontanei ricorrenti siano contrastanti (Baud et al., 2008).
- Citomegalovirus (CMV): Il CMV è un herpesvirus che può essere trasmesso al feto se la madre è infetta durante la gravidanza. L'infezione fetale da CMV può portare ad anomalie dello sviluppo e aumentare il rischio di aborto spontaneo, in particolare quando l'infezione avviene all'inizio della gravidanza. È probabile che ciò rappresenti un problema nella fase attiva dell'infezione.
Cause Inspiegate: La Sfida DiagnosticaCirca la metà di tutti gli aborti ricorrenti rimangono inspiegati nonostante una valutazione approfondita. Gli aborti ricorrenti inspiegati possono comportare sottili anomalie nella funzione immunitaria, genetica o ormonale che gli attuali test diagnostici non sono in grado di rilevare. Inoltre, in molti casi sono probabili cause multifattoriali, in cui piccole anomalie in più sistemi contribuiscono collettivamente alla perdita della gravidanza (Coomarasamy et al., 2014). In alcuni casi, anche se non vi è una causa nota, possono essere adottate alcune misure profilattiche e osserviamo risultati positivi con queste misure, il che dimostra che anche se alcuni problemi potrebbero non presentarsi nei laboratori, potrebbero comunque rispondere ad anticoagulanti, corticosteroidi, antibiotici e altre misure profilattiche.
La Diagnosi Prenatale e Preimpianto: Strumenti per la Prevenzione e la Comprensione
I progressi nelle tecnologie genomiche hanno notevolmente migliorato la comprensione delle cause genetiche dell'aborto spontaneo.
Tecniche Diagnostiche Invasive e Non InvasiveLa diagnosi prenatale ha l'obiettivo di individuare alcune delle patologie del feto. Esistono tecniche diagnostiche sia invasive che non invasive. Le tecniche non invasive includono l'analisi del DNA fetale libero circolante e offrono la possibilità di accertamenti citogenetici. Tra le tecniche invasive troviamo la villocentesi e l'amniocentesi. È importante notare che la legislazione attuale garantisce il diritto della gestante a non essere sottoposta a tali tecniche diagnostiche se non lo si desidera. Una trasparenza ed etica medico-paziente è fondamentale per un percorso appropriato per la sua gravidanza.
La diagnosi prenatale può individuare la presenza del genoma di agenti infettivi (es. Rubeovirus, HIV), oltre a patologie genetiche.
Metodi Avanzati per l'Analisi Genetica: CMA e NGSL'analisi genetica del materiale abortito è di importanza cruciale. Poiché le aberrazioni cromosomiche sono la causa principale di aborto spontaneo è importante eseguire l’analisi genetica del materiale abortito in caso di perdita ricorrente di gravidanza. La probabilità di aberrazioni citogenetiche nel materiale abortito aumenta ogni anno.
- Analisi del microarray cromosomico (CMA): La CMA ha sostituito il cariotipo in molte cliniche come test primario per identificare anomalie cromosomiche nel tessuto dell'aborto spontaneo. Questa tecnologia rileva squilibri cromosomici submicroscopici che il cariotipo tradizionale potrebbe non rilevare, fornendo informazioni sulle cause degli aborti spontanei inspiegati (Reddy et al., 2012).
- Sequenziamento di nuova generazione (NGS): L'NGS ha facilitato l'identificazione di mutazioni monogeniche e anomalie genetiche su piccola scala che contribuiscono all'aborto spontaneo. Ha anche aiutato a scoprire nuovi geni associati alla perdita precoce della gravidanza, fornendo ulteriori approfondimenti sulle cause genetiche (Xu et al., 2020). Quando le pazienti sperimentano perdite di gravidanza multiple, un ciclo di fecondazione in vitro che prevede test NGS diventa uno strumento molto efficace.
La Diagnosi Genetica Preimpianto (PGT-A/PGS): Un Approccio PreventivoLa denominazione diagnosi genetica preimpianto raccoglie un gruppo di tecniche basate sull’analisi di alcune cellule della blastocisti per valutare l’assetto cromosomico dell’embrione, al fine di aumentare le probabilità di gravidanza per transfer e ridurre le probabilità di aborto (PGT-A o PGT-SR) o per rilevare la presenza di mutazioni genetiche causa di gravi malattie ereditarie (PGT-M). Il metodo PGS consente l'esame degli embrioni prima del trasferimento in termini di aneuploidie cromosomiche e traslocazioni. Nel nostro centro viene utilizzato il metodo New Generation Sequencing (NGS), che è il più avanzato tra i test di screening genetici efficaci per PGS.
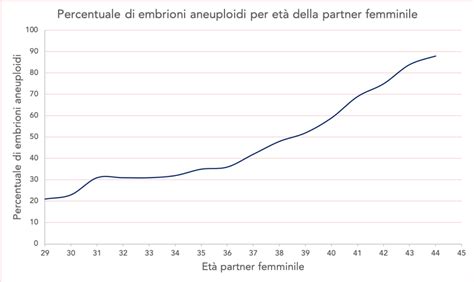
Principi Biologici della PGT-A: La PGT-A o PGS si basa sul principio che una certa percentuale degli embrioni ai primi stadi dello sviluppo porta con sé un numero anomalo di cromosomi; questo tipo di corredo cromosomico viene definito aneuploide. La percentuale di embrioni affetti da aneuploidie dipende principalmente dall’età della partner femminile. Questo è determinato dal fatto che, con l’aumentare dell’età della donna, aumenta anche la probabilità che i gameti femminili, gli ovociti, presentino un corredo cromosomico anomalo. Considerato che il patrimonio genetico degli embrioni non è altro che la somma dei cromosomi contenuti nei gameti che li originano, se l’ovocita o lo spermatozoo che originano l’embrione possiedono delle anomalie, anche l’embrione conterrà queste anomalie. Per ragioni biologiche e a meno di particolari quadri patologici, gli spermatozoi tendono a essere meno soggetti ad aneuploidie e, conseguentemente, l’origine delle aneuploidie nell’embrione è prevalentemente materna.
La Procedura di Biopsia Embrionale: La PGT-A o PGS viene eseguita prelevando 5-8 cellule dall’embrione allo stadio di blastocisti. Con il metodo NGS, lo screening aneuploide dell'embrione può essere eseguito con almeno l'1% di precisione in una piccola quantità (5-95) di cellule prelevate dagli embrioni mediante il metodo della biopsia dell'embrione. La biopsia embrionale può essere eseguita su embrioni al di sopra di una certa qualità che possono raggiungere lo stadio di blastocisti. Gli embrioni ottenuti in IVF vengono valutati secondo criteri definiti in base alle loro caratteristiche morfologiche di sviluppo e si cerca di ottenere una gravidanza sana trasferendo in utero l'embrione con le migliori caratteristiche di sviluppo. L'esame delle caratteristiche dello sviluppo dell'embrione al microscopio non ci fornisce l'informazione che l'embrione sia cromosomicamente normale o anormale. Queste informazioni possono essere ottenute solo mediante screening genetico con PGS.In questa fase l’embrione è formato da due popolazioni di cellule distinte: il trofoectoderma (o trofoblasto) e la massa cellulare interna. Mentre quest’ultima è costituita da un insieme di cellule poste internamente all’embrione che andranno a formare il feto, il trofoblasto è formato dalle cellule che si differenzieranno negli annessi embrionali (es. la placenta), e si trovano aderenti all’interno della zona pellucida. Sono proprio le cellule del trofoblasto ad essere prelevate per l’analisi. Considerato che queste cellule in futuro andranno a formare i villi coriali, si può pensare alla biopsia del trofoectoderma come una sorta di villocentesi precoce.Per poter prelevare le cellule del trofoectoderma, si effettua una biopsia utilizzando un laser ad altissima precisione e un micromanipolatore. La procedura consiste nel forare con il laser la zona pellucida che circonda l’embrione e con una micropipetta si aspirano delle cellule dal trofoblasto della blastocisti. Queste vengono poi separate dal resto dell’embrione con il laser e poste in una provetta apposita per la successiva analisi. L’embrione viene quindi vitrificato. Il metodo della biopsia embrionale viene eseguito al microscopio con pipette speciali ed embriologi che hanno formazione ed esperienza in questo campo. La procedura richiede poco tempo e non danneggia l'embrione. Gli embrioni sottoposti a biopsia vengono quindi congelati individualmente utilizzando il metodo di congelamento ultra rapido, la vetrificazione.Le cellule sono analizzate mediante Next Generation Sequencing (NGS) per valutare l’assetto cromosomico degli embrioni. Si tratta di una procedura complessa in grado di analizzare con accuratezza i cromosomi degli embrioni anche a partire da un campione ridotto come 5-8 cellule. I risultati dell’analisi vengono forniti in circa 2 settimane e definiscono lo stato di ploidia degli embrioni: per ogni embrione viene espresso il corredo cromosomico come euploide o aneuploide e in quest’ultimo caso viene specificato il tipo di anomalia specificando i cromosomi coinvolti. I risultati vengono quindi illustrati alla coppia e discussi per delineare il percorso clinico successivo.
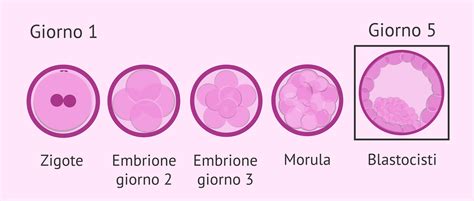
Vantaggi e Limiti della PGT-A: Rimuovere delle cellule dall’embrione ne riduce le capacità di sviluppo? Nelle prime forme di biopsia embrionaria, venivano prelevate una o due cellule dell’embrione allo stadio di clivaggio, ovvero dopo 3 giorni dall’inseminazione. A questo stadio un embrione dallo sviluppo definito regolare è formato da 8 cellule. Diversi studi hanno evidenziato che la biopsia in terza giornata può essere dannosa all’embrione e dunque ad oggi questa forma di biopsia è limitata a poche realtà cliniche. Più recentemente, è stata introdotta la biopsia embrionaria in quinta giornata, allo stadio di blastocisti, quando l’embrione è formato da 100-300 cellule organizzate già in due popolazioni cellulari (massa cellulare interna e trofoblasto). Diversi studi hanno concluso che la rimozione di 5-8 cellule del trofoblasto a questo stadio è una procedura sicura, che non ha impatto sul potenziale di sviluppo dell’embrione.La PGT-A non aumenta le probabilità di gravidanza per prelievo ovocitario, ma per transfer eseguito. Gli embrioni definiti euploidi (ovvero con un corretto numero di cromosomi) hanno una maggior probabilità sia di impianto, che di risultare in una gravidanza a termine. Il principale vantaggio di trasferire un embrione euploide è dato dal fatto che la probabilità di gravidanza per transfer eseguito diventa indipendente dall’età materna ed è compresa tra il 50 e il 60%. Allo stesso modo, trasferire un embrione euploide consente di abbassare le probabilità di aborto spontaneo dipendente dall’età, a circa il 10%.
A Chi è Indicata la PGT-A/PGS: Per i vantaggi visti sopra, tutti i pazienti possono considerare la PGT-A per aumentare le chance di gravidanza a termine per transfer eseguito. La Società Italiana di Genetica Umana (SIGU) in particolare evidenzia alcuni gruppi di pazienti che possono beneficiare di questa tecnica:
- Età materna avanzata: ovvero se la partner femminile ha una età maggiore di 35 anni, considerata la correlazione tra aumento dell’età materna e incidenza delle aneuploidie.
- Ripetuti fallimenti di impianto: definito quando siano stati effettuati >3 cicli con transfer di embrioni di buona qualità (o trasferiti in totale >10 embrioni) senza gravidanza clinica.
- Ripetuti aborti spontanei (>3) nel primo trimestre. In casi selezionati dal clinico in base a diversi fattori come età e riserva ovarica.
- Fattore maschile grave che richiede prelievo di spermatozoi per via chirurgica.
Affrontare l'Aborto Spontaneo: Percorsi di Cura Personalizzati e Supporto
La perdita precoce della gravidanza porta a una situazione di sofferenza per molte coppie. Per ciò che riguarda un aborto spontaneo estemporaneo non c’è bisogno di fare nulla. Basterà aspettare un po’ di tempo e ritentare. Diverso è il discorso se l’evento è ricorrente, anche se non necessariamente consecutivo. In questo caso, una indagine più accurata dovrebbe essere eseguita su entrambi i partner in presenza di un secondo aborto spontaneo.
È importante in tale contesto rivolgersi ad un centro specializzato, che offra un approccio multidisciplinare e cioè che sia in grado di affrontare per la diagnosi ed il trattamento eventuale, tutti gli aspetti genetici, ormonali, immunologici e anatomici, ma anche del benessere emotivo della coppia. Il primo passo è un percorso diagnostico di base che permette di individuare il fattore predominante e di evitare trattamenti inutili o inefficaci. I trattamenti dipenderanno poi dalla causa genetica identificata. In caso di anomalie cromosomiche dei genitori, la procreazione medicalmente assistita con diagnosi genetica preimpianto (PGT) può essere la soluzione ideale poiché consente di selezionare embrioni cromosomicamente sani, riducendo drasticamente il rischio di nuove perdite. Quando sono presenti trombofilie o alterazioni immunologiche, possono essere indicati invece trattamenti farmacologici specifici durante la gravidanza. Se il problema è legato a squilibri ormonali o a difetti uterini, esistono terapie mediche o chirurgiche mirate.
tags: #aneuploidie #aborto #spontaneo #precoce