Lo scopo di questa trattazione è puntualizzare alcuni dei termini e delle condizioni cliniche riferibili alla morfologia, alla struttura, alle componenti ed ai difetti della placenta, dell'amnios e del corion, considerando sia la specie bovina che quella umana. L’adozione di una terminologia comune, chiara, precisa, univoca e comprensibile nell’ambito della riproduzione permetterebbe uno scambio di conoscenze scientifiche e cliniche più efficiente tra ricercatori e medici veterinari. Questi annessi embrionali sono essenziali per il sostegno e lo sviluppo del feto, fungendo da interfaccia critica tra la madre e il nascituro.
La Placenta: Un Organo di Interfaccia Materno-Fetale
Il termine placenta si riferisce ad entrambe le componenti, materna (endometriale) e fetale. È l'organo deputato agli scambi metabolici tra la madre e il feto, collegando il feto in sviluppo alla parete uterina. La placenta consente l'assorbimento dei nutrienti, la regolazione termica, l'eliminazione dei rifiuti e lo scambio di gas attraverso la fornitura di sangue della madre; inoltre, è cruciale per combattere l'infezione interna e per produrre ormoni che supportano la gravidanza. Essa fornisce ossigeno e sostanze nutritive ai feti crescenti e rimuove i rifiuti dal sangue fetale. La placenta si attacca alla parete dell'utero, e il cordone ombelicale del feto si sviluppa proprio dalla placenta, connettendo direttamente la madre e il feto.
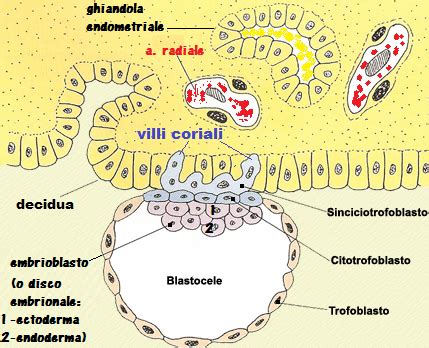
La placenta subisce continue modificazioni nel corso dello sviluppo fetale. Uno dei suoi compiti fondamentali è quello di ridurre al minimo la distanza tra il sangue materno e quello fetale; questo ruolo è principalmente svolto dai villi coriali, che compaiono a partire dal 13° giorno come citotrofoblasto. Successivamente, tra questi e l'epitelio uterino viene interposto uno stroma connettivale di derivazione mesodermica, nel quale si inseriscono capillari arteriosi e venosi. Le cellule del citotrofoblasto continuano a proliferare, tendendo verso la decidua basale dove si trovano i vasi materni, formando un disco trofoblastico parallelo, attorno a cui il sinciziotrofoblasto si contrae.
Una delle funzioni più importanti della placenta è la produzione di ormoni aventi lo scopo di regolare le attività della gravidanza. La placenta, sebbene rappresenti un potente filtro per i parassiti del sangue, è meno efficace contro virus, batteri e sostanze tossiche trasmissibili al feto dalla madre, come il treponema della sifilide e gli agenti patogeni della setticemia.
Morfologia e Classificazione della Placenta Bovina
Nella specie bovina, la classificazione attuale descrive la placenta come di tipo “cotiledonata sinepiteliocoriale”. In precedenza, era definita di tipo sindesmocoriale. L’aggettivo “cotiledonare” indica la presenza di aree specializzate di proliferazione trofectodermica chiamate cotiledoni.
L’epitelio uterino persiste nonostante sia inizialmente modificato in placche di sincizi ibridi materno-fetali, i quali si originano dalla migrazione e dalla fusione di cellule trofectodermiche - che derivano dall’epitelio esterno della blastocisti - ed epiteliali uterine (UE). Le cellule trofoblastiche binucleate giganti (TGCs) si fondono con le UE in cellule che possono possedere fino ad otto nuclei. Queste placche vengono poi sostituite da nuove UE verso il giorno 40 di gestazione, indicando che i sincizi di TGC-UE sono transitori. Il termine “sin” descrive la presenza di sincizi feto-materni, mentre “epiteliocoriale” è riferito alla semplice interdigitazione microvillare tra trofoblasto ed epitelio uterino nel resto della placenta.
Il placentoma bovino è formato dall'interdigitazione tra i villi del corion, che costituiscono i cotiledoni, e le cripte materne all’apice delle caruncole. I placentomi si presentano come strutture elevate, semicircolari, lisce e piatte; inizialmente sono individuabili solo nell’area di impianto dell’embrione ma dal giorno 60 inizia la loro espansione nel corno gravido. Essi sono distinguibili macroscopicamente a partire dal 37° giorno di gestazione e sono circondati dalla giustapposizione di tessuto ghiandolare uterino e trofoblasto, formando le aree interplacentomali.

Annessi Embrionali: Amnios, Corion e Allantoide
Gli annessi embrionali o secondine sono costituiti dalle membrane ovulari, distinte in amnios e corion, dalla placenta stessa, dal funicolo ombelicale e dal liquido amniotico. Inclusi in essi si trovano pure i residui della vescicola ombelicale con il condotto onfalo-enterico e i resti dell’allantoide; ad essi aderente all'esterno è lo strato superficiale della caduca parieto-riflessa, appartenente alla madre.
La membrana più esterna che limita l'uovo è il corion. Il corion è il "guscio" che delimita la camera gestazionale e prende anche il nome di “somatopleura”, essendo formato dal trofectoderma e dal mesoderma non vascolarizzato. Questo strato epiteliale, derivato dall'ectoderma ovulare, viene a trovarsi in immediato contatto con la decidua o caduca, ovvero con la mucosa uterina modificata per effetto della gravidanza. Dalla seconda e terza settimana di sviluppo la superficie esterna del corion risulta ricoperta da villosità arborizzate, che continuano a crescere dal lato in contatto con la primitiva sede di impianto dell'embrione nella mucosa uterina, formando il corion frondosum. Al contrario, si atrofizzano quelle villosità (corion laeve) che si trovavano in relazione con la membrana caduca che ricopriva l'ovulo (caduca capsulare o riflessa). Durante il terzo mese, contemporaneamente all’espansione del corion, i villi situati sulla parte decidua capsulare vengono stirati fino a scomparire. Alla parte opposta, sullo strato basale, i villi diventano più folti, lunghi e ramificati per compensare la scomparsa dei villi dal lato deciduale.
Internamente al corion, abbiamo la membrana amniotica o amnios, la quale è la più interna delle membrane ovulari. L'amnio è una sacca membranosa che racchiude, oltre al feto, il famoso liquido amniotico. Strutturalmente, amnios e corion sono così vicini da essere considerati come un’unica entità, formando le membrane amnio-coriali che avvolgono il feto e il cordone ombelicale. La fusione tra la membrana amniotica e quella coriale avviene durante il secondo mese di vita intrauterina, in conseguenza del fatto che la cavità amniotica (entro la quale è sospeso l’embrione) si ingrandisce molto più rapidamente del sacco coriale. Successivamente la membrana coriale si fonde con la decidua capsulare, e poi quest’ultima con la decidua parietale, così che verso la fine del 3° mese la cavità dell’utero risulta obliterata. L’amnios riveste, inoltre, aderendovi in modo lasso, la faccia fetale della placenta e costituisce la guaina amniotica del cordone o funicolo ombelicale. L'amnios è l’annesso embrionale che costituisce una sacca membranosa in grado di circondare e proteggere l’embrione prima e il feto dopo. Evolutivamente, tale membrana è presente nei rettili, negli uccelli e nei mammiferi, ovvero in tutte le classi definite Amniota, non è, invece, presente in anfibi e pesci che sono dunque definiti Anamni. Dal punto di vista istologico la cavità amniotica presenta un singolo strato di cellule di origine ectodermica, di forma appiattita, definito ectoderma amniotico, mentre il pavimento risulta costituito da ectoderma di tipo prismatico che deriva dal disco embrionale. L'ectoderma amniotico si forma anche grazie alla secrezione attiva da parte della membrana amniotica. Al giorno 35 di gestazione l’embrione con il suo sacco amniotico completamente formato viene definito “vescicola amniotica”.
Terminata la formazione dell’amnios, dalla porzione terminale dell’intestino embrionale emerge una vescicola endodermica; questa formerà l’allantoide. L’allantoide è in continuazione con il tratto urogenitale dell’embrione e raccoglie i prodotti di scarto di quest’ultimo. L’allantoide è riccamente vascolarizzato e, fondendosi con il corion a formare l’allantocorion, si espande nei cotiledoni assumendo il ruolo fondamentale di organo deputato agli scambi gassosi. Fino al giorno 45 di gestazione le due membrane, allantoide e corion, appaiono ancora ben distinguibili microscopicamente: l’allantoide è formato da cellule appiattite mentre il corion da cellule epiteliali cuboidali. “Splancnopleura” è il nome attribuito alla parete del sacco vitellino.
Componenti Cellulari della Placenta e Loro Funzioni
Come anticipato, il trofectoderma o trofoblasto è lo strato epiteliale che circonda la blastocisti. Questo ha una grande capacità di espansione, invasione, fusione cellulare, produzione ormonale, assorbimento di nutrienti, trasporto selettivo e resistenza alla risposta immunitaria materna. Durante la progressione della gravidanza le cellule uninucleate del trofoblasto (UCTs) si differenziano o in UTCs mature oppure nelle TGCs (cellule trofoblastiche binucleate giganti). Le UTCs mature possiedono granuli citoplasmatici legati alle membrane che vengono gradualmente rilasciati nella circolazione materna. La giunzione microvillare è formata dall'interdigitazione dei microvilli del trofectoderma e dell’epitelio uterino; intervallate tra le giunzioni vi sono lacune vascolari dove gli eritrociti materni sono fagocitati dalle UTCs e fungono da riserva di ferro per il feto. Le UTCs sono inoltre note per produrre interferone τ, un fattore implicato nel riconoscimento materno della gravidanza, la cui produzione raggiunge il suo massimo al giorno 17 e prosegue fino a circa 35 giorni di gestazione nei bovini. Le TGCs invece sono responsabili della secrezione di lattogeno placentare, progesterone, estrogeni e prostaglandine.
Un'altra popolazione cellulare placentare rilevante è rappresentata dai macrofagi. Il loro numero all’interno del tessuto connettivo cotiledonare incrementa fino a dieci volte verso l’ottavo mese di gravidanza. Si suppone che siano implicati nella risposta immunitaria fetale. Tuttavia, in corso di placentite micotica, batterica e da lieviti, questi macrofagi possono trasportare l’agente patogeno dalla placenta al feto attraverso le vene ombelicali. I macrofagi che risiedono nei placentomi bovini appartengono ai cluster di differenziazione CD68+CD14+MHC classe II- e spesso anche al CD11b, mentre i macrofagi caruncolari esprimono CD68+CD14+MHC classe II+ e sono privi del CD11b.
Lo Sviluppo Embrionale e Fetale in Relazione agli Annessi
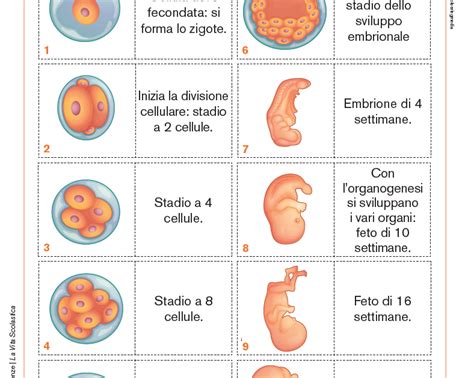
La gametogenesi è il processo di sviluppo dalle cellule germinali primordiali ai gameti maturi: oogenesi nelle femmine e spermatogenesi nei maschi. Nelle femmine e nei maschi, inizia con cellule germinali diploidi che poi vanno incontro a mitosi, meiosi e citodifferenziazione in gameti aploidi. Per la fecondazione, gli spermatozoi (gameti aploidi maschili) migrano attraverso il canale cervicale, la cavità uterina e nelle tube di Falloppio. Nell’ovaio si sviluppano i follicoli e, durante l’ovulazione, il follicolo dominante rilascia un ovocita (gamete aploide femminile). L’ovocita entra nella tuba di Falloppio attraverso l’estremità fimbriata, viaggia attraverso la tuba e poi passa nella cavità uterina. L’ovocita diventa un ovulo fecondato quando uno spermatozoo penetra negli strati esterni dell’ovocita. La fecondazione si verifica in genere quando l’ovocita si trova nella tuba di Falloppio. Solitamente, un solo spermatozoo fertilizza un ovocita; tuttavia, due ovociti possono essere rilasciati e poi fecondati da due spermatozoi, con conseguente gravidanza gemellare dizigotica (fraterna). Una gestazione multipla di ordine superiore (es. triplette, quadruplette) può verificarsi se vengono liberati e fecondati più di due ovociti, ma questo è raro. È anche possibile che più di uno spermatozoo penetri un singolo ovocita, ma questo si traduce in uno zigote anormale.
In una donna con cicli mestruali di 28 giorni, l'ovulazione si verifica circa 14 giorni dopo il primo giorno di un ciclo mestruale. Al momento dell’ovulazione, il muco cervicale diventa meno viscoso, facilitando il rapido movimento degli spermatozoi verso l’ovocita. Lo spermatozoo può sopravvivere nelle vie genitali fino a circa 3 giorni dopo il rapporto sessuale.
L’ovulo fecondato, ora uno zigote diploide, si divide ripetutamente attraverso un processo chiamato segmentazione, formando cellule identiche e totipotenti. Queste divisioni continuano mentre lo zigote migra verso il sito di impianto nell’endometrio, solitamente vicino al fondo o sulla parete posteriore dell’utero. Al momento dell’impianto, lo zigote è divenuto una blastocisti, una piccola struttura sferica delimitata da uno strato di cellule esterne che racchiude una cavità. La parete della blastocisti ha un singolo strato di cellule eccetto il polo embrionale, formato da 3 o 4 strati di cellule. Circa 6 giorni dopo la fecondazione, la blastocisti si impianta nell’endometrio; il polo embrionale, che si svilupperà nell’embrione, è il primo punto dell’impianto.
Entro 1 o 2 giorni dall’impianto, uno strato di cellule, le cellule del trofoblasto, si sviluppa intorno alla blastocisti. Le cellule progenitrici dei villi del trofoblasto, ovvero le cellule staminali della placenta, si differenziano in due linee cellulari: il Citotrofoblasto, che è un trofoblasto extravilloso non proliferativo le cui cellule penetrano nell’endometrio, facilitando l’impianto e ancorando la placenta; e il Sinciziotrofoblasto, le cui cellule producono gonadotropina corionica entro il 10° giorno e altri ormoni trofici poco dopo.
Uno strato interno (amnios) e uno strato esterno (corion) delle membrane si sviluppano a partire dal trofoblasto; queste membrane formano il sacco amniotico, che contiene il prodotto del concepimento. Quando il sacco è formato e la cavità della blastocisti si chiude, approssimativamente entro il 10° giorno, il prodotto del concepimento viene considerato un embrione. Il sacco amniotico si riempie di liquido e si espande al crescere dell’embrione, riempiendo la cavità endometriale verso le 12 settimane circa dopo il concepimento; a questo punto, il sacco amniotico è la sola cavità rimanente nell’utero. L’embrione a questo stadio misura circa 4,2 cm. Le cellule del trofoblasto si differenziano in cellule che formano la placenta. Il trofoblasto extravilloso forma i villi, che penetrano nell’utero, mentre il sinciziotrofoblasto copre i villi, sintetizza ormoni trofici e fornisce scambi arteriosi e venosi tra la circolazione embrionale e quella materna. La placenta è completamente formata entro le 18-20 settimane ma continua a crescere, fino a raggiungere il peso di circa 500 g al termine della gravidanza.
Intorno al 10° giorno circa dopo la fecondazione si possono solitamente distinguere all’interno dell’embrione 3 foglietti germinativi (ectoderma, mesoderma, endoderma). Allora inizia a svilupparsi la stria primitiva, che diventa poi il tubo neurale. Intorno al 16° giorno la porzione cefalica del mesoderma si ispessisce formando un canale centrale che darà origine al cuore e ai grossi vasi. Il cuore inizia a pompare il plasma intorno al 20° giorno e il giorno successivo compaiono i globuli rossi fetali, che sono inizialmente immaturi e nucleati, per essere poi subito sostituiti da globuli rossi maturi. I vasi sanguigni si sviluppano in tutto l’embrione, e infine si formano l’arteria e la vena ombelicale che collegano i vasi dell’embrione alla placenta. La maggior parte degli organi si forma tra i 21 e i 57 giorni dopo la fecondazione (5-10 settimane di gestazione); tuttavia, il sistema nervoso centrale continua a svilupparsi durante tutta la gravidanza.
Il feto nell'utero vive di vita propria, sebbene parassiticamente a spese dell'organismo della madre. Esso esercita funzioni della vita vegetativa, cioè nutrizione, respirazione, escrezione, circolazione sanguigna, secrezione ghiandolare e termogenesi, e funzioni della vita di relazione, come sensibilità e movimento. Il feto si nutre assorbendo dal sangue materno, attraverso la placenta, i materiali di cui necessita, quali albuminoidi, idrati di carbonio, grassi e sali inorganici. Si rifornisce d’acqua deglutendo il liquido amniotico e si provvede d’ossigeno, cioè respira, in corrispondenza pure della placenta, per effetto d’un’ossidasi placentare, capace d’attivare il distacco dell’ossigeno dall’emoglobina del sangue materno e di farsene veicolo verso il sangue fetale. Per la stessa via elimina l’anidride carbonica e le scorie del suo metabolismo organico, per cui l’asfissia fetale consegue prontamente alla cessazione degli scambi con il sangue materno o all’interruzione della circolazione ombellico-placentare.
Il feto ha una circolazione propria, detta cardioplacentare, diversa per alcune sue particolarità da quella cardiopolmonare della vita extrauterina. Nel suo cuore, i cui battiti s’avvertono anche attraverso l’addome della madre a partire dalla metà della gravidanza, esiste il foro di Botallo (o meglio di Carcano Leone, che per primo lo descrisse esattamente), che fa comunicare fra loro le due orecchiette; e nel suo albero circolatorio l’arteria polmonare comunica ampiamente con l’aorta, dopo che questa ha descritto il suo arco, per mezzo del dotto arterioso. Le due arterie iliache interne si continuano direttamente con le arterie ombellicali, che portano sangue venoso alla placenta; mentre il sangue, divenuto arterioso, da essa ritorna al feto per la vena ombellicale. Durante la vita fetale le funzioni di secrezione sono dimostrate dalla presenza della vernice caseosa, dovuta alle ghiandole sebacee e alla desquamazione cutanea, da quella del meconio e dall’accertata possibilità della secrezione urinaria, almeno a carico della funzione glomerulare.
Il feto, mentre non pare verosimile che possegga già entro l’utero le sensibilità specifiche, è provvisto certamente e precocemente di sensibilità tattile, e reagisce con movimenti riflessi agli stimoli direttamente o indirettamente su di lui esercitati (movimenti attivi). Tentativi di movimenti si possono talora provocare già su feticini trimestri, espulsi vivi in parti abortivi; ma tali movimenti, bene evidenti al quarto mese, a partire dalla metà della gravidanza diventano percepibili anche attraverso l’addome materno. Data la sproporzione che già precocemente si stabilisce fra la capacità uterina e la lunghezza del feto, questo deve adattarsi all’angustia di quella, assumendo con essa particolari rapporti che sono regolati dalla cosiddetta legge d’adattamento feto-utero-placentare, oltre che dall’influenza della gravità, esercitantesi più o meno manifestamente sul corpo fetale spostabile entro il mezzo liquido delle acque dell’amnio.
Per atteggiamento s’intendono i rapporti che le diverse parti del feto assumono tra di loro. L’atteggiamento normale del feto nell’utero è quello in flessione: cioè la testa flessa, il tronco in flessione dorsale e gli arti flessi sul tronco. Per situazione s’intende il rapporto del diametro cefalopodalico del feto con i diametri uterini. La situazione normale è quella longitudinale; mentre sono anomale la trasversale e l’obliqua. Si designa con il nome di presentazione la parte voluminosa del corpo fetale (testa, tronco, o podice), che occupa l’ingresso pelvico e regola il meccanismo del parto. Nella specie umana la presentazione più tipica e frequente è quella cefalica di vertice. S’intende per posizione il rapporto della parte presentata fetale con il contorno dello stretto superiore del bacino della madre.
Il Liquido Amniotico e la sua Importanza
Il feto non si trova annidato a diretto contatto con la mucosa uterina, ma è immerso in una cavità ripiena di liquido, la cavità amniotica, anche definita cavità ovulare, contenente il liquido amniotico. La parete che riveste la cavità è di origine fetale, differenziandosi da una porzione dell’embrione. Essa rappresenta una specie di guscio (non calcificato), formato da un duplice strato: esternamente, a contatto con la decidua materna, si trova il corion dello spessore di circa 1 millimetro (una sua parte è differenziata a formare la placenta), all’interno si trova invece una membrana più sottile, l’amnios, che tappezza la cavità, ricoprendo la faccia fetale della placenta e il funicolo ombelicale e racchiudendo completamente l’embrione.
Il liquido amniotico, presente in una quantità di circa 1000 cmc a termine, ha aspetto e consistenza acquosa, è limpido, appena lievemente opalescente, ha reazione neutra o leggermente alcalina, e un peso specifico basso, fra 1002 e 1008, con un Δ fra 0,31 e 0,496 (media 0,45). È costituito per la massima parte da acqua (98%), e contiene sali inorganici (0,60%), poca albumina (0,18%), urea (0,02-0,40), discreta quantità d'acido lattico, creatina, creatinina, non raramente glucosio, e sostanze estrattive diverse. Al microscopio presenta pelurie e squamme epidermiche, derivanti dalla cute del feto.
Le funzioni del liquido amniotico sono molteplici: protegge il feto dai traumi esterni e ne favorisce lo sviluppo regolare, impedendo che su di esso s’eserciti direttamente la pressione delle pareti uterine. Concorre agli scambi materno-fetali provvedendo d’acqua il sangue del feto. Durante il parto, facilita, con la formazione della borsa delle acque, la dilatazione della bocca uterina e deterge nella sua fuoruscita a fiotto le vie genitali materne, cooperando verosimilmente a proteggerle contro i facili inquinamenti. Per l’analisi del cariotipo fetale si può ricorrere anche al prelievo dei villi coriali, ma trattandosi di un tessuto di derivazione sia materna che fetale, si preferisce utilizzare sovente il prelievo del liquido amniotico che contiene solo cellule di derivazione fetale e rispecchia più propriamente l’assetto cromosomico del nascituro. L’analisi del cariotipo consente di diagnosticare eventuali aberrazioni cromosomiche, quali le trisomie come la più nota Trisomia del cromosoma 21 responsabile della Sindrome di Down.
Terzo trimestre di gravidanza: il controllo del liquido amniotico
Diagnosi e Monitoraggio della Gravidanza
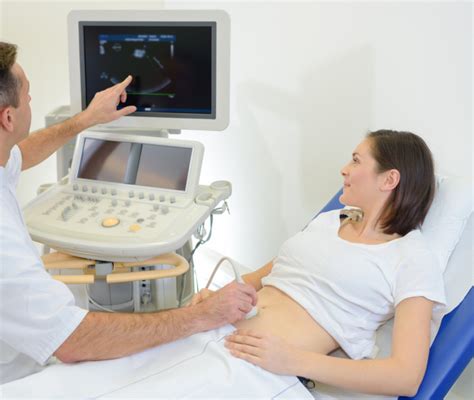
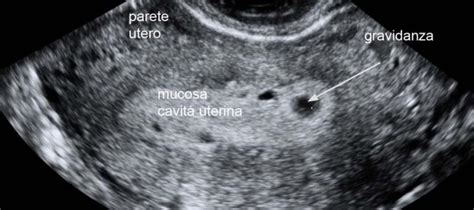
La diagnosi di gravidanza può essere effettuata tramite palpazione transrettale a partire dal giorno 35 di gestazione, con lo scopo di rilevare lo scivolamento delle membrane o “fetal membrane slip” nei bovini. Approssimativamente nello stesso periodo è possibile percepire anche la vescicola amniotica. Sebbene la bibliografia non sia concorde, gli studi più recenti negano la correlazione tra diagnosi di gravidanza eseguita tramite palpazione transrettale e morte embrionale/fetale. Una revisione sistematica pubblicata prima del 1997 afferma che una palpazione particolarmente vigorosa della vescicola amniotica può essere responsabile di un aumentato rischio di “atresia coli”, una anomalia dello sviluppo embrionale nella quale l’ultimo tratto del canale gastroenterico è assente. L’Autore indica come preferibile la tecnica dello scivolamento delle membrane piuttosto che la palpazione della vescicola amniotica durante l’esecuzione della diagnosi manuale di gravidanza.
L’uso dell’ultrasonografia permette di evidenziare il sacco allantoideo dal giorno 22 al 27; l’amnios è visibile a partire dal giorno 30 circa. In ambito umano, un’immagine di scansione ecografica di una placenta a 20 settimane di gravidanza permette di osservare l'inserzione sulla parete posteriore dell'utero e l'inserzione centrale del cordone ombelicale sul piatto coriale.
Anche il dosaggio delle PAGs (Pregnancy Associated Glycoproteins) può essere utilizzato per diagnosticare una gravidanza in atto nelle bovine tra i 28 ed i 30 giorni post inseminazione, con un valore di riferimento di 0.8 ng/mL o maggiori per una diagnosi positiva. Tuttavia, la lunga emivita di queste glicoproteine può causare falsi positivi in caso di morte embrionale o fetale.
Complicazioni e Patologie degli Annessi Embrionali
Il distacco prematuro delle membrane fetali dalle caruncole materne è una condizione che, nei bovini, è spesso responsabile di mortalità perinatale, con una stima di prevalenza del 5-10%. Tra i fattori responsabili si ipotizzano le infezioni o una sovrapposizione anormale degli invogli sull’ostio cervicale interno, nota come placenta previa. La ritenzione delle membrane fetali, invece, si verifica nel 5-10% delle bovine da latte quando gli invogli non sono espulsi entro le 12 ore dal parto. L’immaturità placentare è considerata la condizione fondamentale per la patogenesi della ritenzione. Sono stati individuati altri fattori responsabili come flogosi, edema non infiammatorio dei villi (come in caso di torsione e/o taglio cesareo, distocia), involuzione prematura dei placentomi o iperemia. Un ruolo indiretto è attribuito a stress, stagione, sesso del feto, fattori nutrizionali e patologie dell’utero o del feto. Lo sviluppo placentare è massimo nella prima parte della gravidanza e può essere influenzato negativamente dall’apporto nutrizionale, dallo stress, dall’ipotermia e da infezioni concomitanti. La vascolarizzazione e la proliferazione placentare possono essere inibite tanto da apporti nutrivi insufficienti quanto eccessivi, probabilmente a causa di un’alterata espressione di fattori angiogenetici.
L’idroallantoide è definita come la condizione bovina in cui si ha un eccessivo accumulo di liquido allantoideo, che può superare anche di dieci volte i fisiologici 8-15 litri. Il freemartinismo è una condizione di anomalo sviluppo sessuale in un feto femmina gemello di un feto maschio. La vicinanza delle membrane fetali permette la creazione di anastomosi vascolari e di una chimera XX/XY. A causa del chimerismo, lo sviluppo degli organi riproduttivi del feto femmina è inibito e/o alterato.
I Distacchi delle Membrane Amnio-coriali:Un distacco amniocoriale è una complicanza che può insorgere nelle prime settimane della gravidanza umana. È importante notare che un distacco amniocoriale non equivale a un distacco di placenta. Quest’ultimo indica, infatti, una patologia ostetrica in cui la placenta si distacca in modo prematuro dalla parete uterina, tardivamente, prima della nascita del bambino, e può insorgere nella seconda parte della gravidanza, dalla ventesima settimana di gestazione.
Le membrane amniocoriali sono due strati connettivali fibrosi, sottili e trasparenti che si sviluppano dall’embrione: il corion e l’amnios. Fino all'ottava-nona settimana il corion e l’amnios sono separati dalla cavità coriale. Con il tempo e il progredire della gestazione si avvicinano e verso la tredicesima settimana si fondono, dal momento che la cavità amniotica si espande molto più velocemente del sacco coriale. Aderiscono tra loro avvolgendo il feto e il cordone ombelicale.
Le cause del distacco amniocoriale sono ancora oggetto di studio. I sintomi possono variare; vale la pena sottolineare, tuttavia, che talvolta il distacco tra il sacco amniotico e quello coriale può essere asintomatico e presentarsi dunque senza perdite di sangue. Se le perdite sono intense, dolorose e persistenti, al contrario, devono essere un motivo per cercare immediatamente assistenza medica, recandosi al pronto soccorso. Nella maggior parte dei casi, la condizione si riassorbe in modo spontaneo, senza la necessità di ricorrere a interventi specifici. Talvolta, può essere opportuno avviare un trattamento che include un periodo di riposo, per ridurre la pressione sull’utero e facilitare l’accollamento delle membrane. A seconda delle circostanze, il riposo può essere relativo o assoluto.
Le dimensioni del distacco amniocoriale hanno un ruolo chiave nella determinazione della sua durata e gravità. La tempestività con cui viene diagnosticato e affrontato il distacco amniocoriale è cruciale. In presenza di segni e sintomi sospetti, la consultazione medica immediata è essenziale. Anche le caratteristiche individuali della paziente, come il suo stato di salute generale, la risposta al trattamento e le settimane gestazionali in cui si verifica il distacco, possono influire sulla durata complessiva della condizione. Il tipo di trattamento adottato è un altro elemento che può determinare la durata del distacco amniocoriale.
Le conseguenze di un distacco amniocoriale possono essere significative. La gravità della condizione dipende dalle dimensioni e dalla sintomatologia dello scollamento. Soprattutto quando le perdite di sangue sono abbondanti e persistenti, il rischio di aborto spontaneo aumenta in modo significativo. Un distacco amniocoriale di dimensioni considerevoli può compromettere l’apporto di nutrienti al feto attraverso la placenta, portando a un ritardo della crescita fetale. Le madri che affrontano un distacco amniocoriale possono sperimentare complicazioni a livello di salute, e la condizione aumenta anche il rischio di nascita prematura.
Un caso specifico potrebbe riguardare un distacco coriale di 19mm alla sesta settimana. In questo contesto, è importante escludere un’infezione delle vie urinarie mediante esame urine ed urinocoltura, poiché non di rado le contrazioni uterine che provocano il distacco sono causate a loro volta da un’infezione/infiammazione a carico dell’apparato genito-urinario.
Infezioni Placentari: Corionamnionite e Villite
La placenta può presentare alterazioni flogistiche in varie malattie infettive che colpiscono la madre. L’esame istologico della placenta può essere utile per dimostrare la presenza di infezioni specifiche o di quadri di flogosi amniocoriale che possono avere gravi ripercussioni sul feto (sepsi fetale, decesso, danni cerebrali permanenti) o sul neonato (distress respiratorio, polmoniti neonatali).
I germi possono arrivare a livello degli spazi intervillosi e, una volta raggiunto lo stroma del villo, provocano fenomeni più o meno evidenti. Si verifica quindi un’infezione ematogenica il cui principale effetto è la comparsa della villite. La villite, in particolare, è una reazione della componente fetale della placenta caratterizzata dalla proliferazione e dall’infiltrazione di cellule infiammatorie di origine fetale in uno o più villi. In genere si presenta con una distribuzione a focolai e solo nei casi più gravi coinvolge tutto il tessuto placentare. Nel caso della toxoplasmosi, ad esempio, la placenta macroscopicamente appare normale, di rado è voluminosa e pallida. Invece, al microscopio spesso si individuano focolai di villite ed infiltrato con prevalente composizione linfocitaria ed istiocitaria. Si può riscontrare la presenza delle pseudocisti parassitarie a livello della placca coriale o dell’amnios, più raramente a livello della decidua basale.
Batteri o virus, tramite un’infezione ascendente (vaginale) per via transamniotica, provocano un quadro diverso dalla villite, che è denominato corionamnionite. Le due manifestazioni, però, possono anche coesistere. Per corionamnionite si intende la presenza di granulociti neutrofili nel contesto del sacco amniotico e del piatto coriale. La flogosi a livello delle strutture amniocoriali può danneggiare il feto anche a membrane integre e senza il passaggio nel liquido amniotico dell’agente infettivo. È stato anche dimostrato che le sostanze proinfiammatorie prodotte dal processo flogistico possono penetrare nel liquido amniotico e danneggiare i pneumociti (cellule che fanno parte dell’epitelio degli alveoli polmonari). Un’induzione farmacologica della maturità polmonare risulterà, dunque, inefficace; anche se il neonato sarà partorito a termine, la produzione del surfactante polmonare sarà insufficiente e il neonato presenterà la sindrome da distress respiratorio.
La corionamnionite è collegabile a fattori eziologici multipli ma non sempre si riesce ad individuare una causa plausibile. Solitamente l’infezione inizia in prossimità dell’orifizio uterino interno, ma vi sono casi in cui la partenza è stata correlata al punto di penetrazione di un ago per amniocentesi. Circostanze che contribuiscono a favorire l’insorgenza della corionamnionite sono quelle in cui vi è un aumento dell’area del polo inferiore delle membrane a contatto con l’orifizio uterino interno (ad esempio in caso di gravidanza multipla, polidramnios, ecc.). Tale infezione può provocare l’inizio del travaglio di parto pretermine o a una sepsi della gestante e/o del bambino.
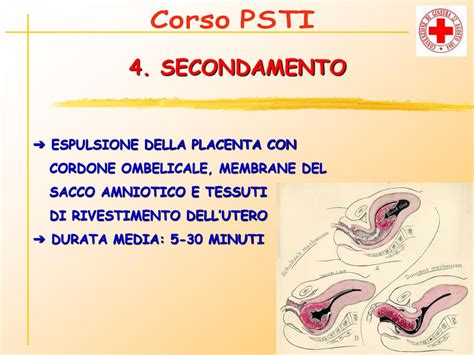
La Placenta Definitiva e il Secondamento
La placenta definitiva, verso il quarto-quinto mese di gravidanza, presenterà dai 10 ai 30 cotiledoni materni. Essi sono delle porzioni di placenta che vengono divise dalla presenza di setti connettivali che si dipartono dalla decidua basale. Al termine della gravidanza (280 giorni circa dal suo inizio) la placenta con le membrane e il funicolo pesa 500-600 gr.
Il distacco e l’espulsione della placenta dal feto avviene subito dopo il parto, in una fase detta secondamento. In quel momento l’utero attua un meccanismo di contrazione tetanica noto con il nome di globo di sicurezza che ferma l’emorragia. Un mancato distacco placentare completo può portare a perdite ingenti di sangue e quindi a shock.
Il cordone ombelicale si forma contemporaneamente all’embrione, mantenendo collegato il feto alla placenta. Si tratta di un cordone costituito da tre vasi sanguigni, i quali sono protetti da una gelatina chiamata di Wharton, che cresce con il feto, e può raggiungere fino a 60 centimetri di lunghezza, per permettere al feto di muoversi e girarsi all’interno del sacco amniotico. I vasi sanguigni di cui è costituito il cordone ombelicale servono a trasportare il sangue ricco di ossigeno e sostanze nutritive dall’utero al feto tramite la placenta, e a trasportare il sangue fetale privo di ossigeno e ricco di rifiuti metabolici dal feto al sangue materno. Attraverso il cordone ombelicale e la placenta, però, passano al feto sia nutrienti e ossigeno, sia le sostanze dannose (nicotina da fumo di sigaretta, alcol, farmaci) eventualmente presenti nel sangue della mamma.
Con il travaglio, di solito si rompe il sacco amniotico, e dalla vagina fuoriesce il liquido amniotico. Il taglio del cordone ombelicale avviene dopo la nascita, e con un parto eutocico (vaginale), si può aspettare che smetta di pulsare. Dopo questo, anche la placenta viene espulsa per via vaginale. L’azienda farmaceutica Mastelli è stata una delle prime aziende al mondo ad estrarre il PDRN (polidesossiribonucleotide) dalle gonadi di trota e a brevettarne i suoi usi farmaceutici, evidenziando l’interesse per i composti bioattivi derivanti da tessuti riproduttivi.